应用CMA产前诊断10q23缺失综合征1例
2018-12-28罗晓辉杜娜胡蓉卢建李怡黄伟伟
罗晓辉 杜娜 胡蓉 卢建 李怡 黄伟伟*
(1. 广东省妇幼保健院 医学遗传中心,广东 广州 510080;2. 广东省妇幼保健院 新生儿科,广东 广州 510080)
10q23缺失综合征(chromosome 10q23 deletion syndrome)是一种罕见的染色体微缺失综合征,缺失区域包含BMPR1A、NGR3、GRID1等致病基因。10q23缺失综合征表型复杂多样,表型可为发育迟缓、语言发育迟缓,特殊面容(眼距宽、低位耳等),有少许患者可见心脏、手脚等先天畸形[1]。染色体异常是导致新生儿出生缺陷的关键因素。10q23微缺失综合征的产前诊断目前报道较少,本文对1例10q23缺失综合征的病例进行产前诊断及遗传学分析,现将该病例报道如下。
1 资料与方法
1.1 一般资料 孕妇,32岁,G4P1A2,因“停经17+周,超声发现胎儿NT增厚(3.3mm)”来本科室就诊,孕妇孕期顺利,无特殊不适。无抽烟、嗜酒史,无胎儿畸形家族史,2018年1月3日孕妇超声提示:宫内妊娠,单活胎,胎儿NT增厚。
1.2 方法
1.2.1 标本采集 该孕妇接受检测前的遗传咨询并签署同意书,根据孕周行羊膜腔穿刺,在B 超探头引导下行羊膜腔穿刺术抽取羊水30ml进行培养以及染色体微阵列分析(chromosomal microarray analysis, CMA)。
1.2.2 CMA检测 采用美国Affymetric公司提供的高分辨全基因组CytoScan 750K芯片,实验操作严格按照Affymetric公司提供的操作流程。该芯片不仅能检测基因组缺失、重复,还能检测杂合性缺失和单亲二体。
1.2.3 CNV的判断和评价 数据分析过程分别参照本实验室内部数据库以及在线公开数据库,如DGV数据库、DECIPHER数据库、OMIM数据库等。
2 结果
CMA检测结果分析本病例胎儿羊水CMA检测发现10号染色体10q22.3-q23.2位置发生缺失arr 10q22.3q23.2(81,603,169-89,227,475)×1,片段大小约7.6Mb,该区域包含17个OMIM基因,包含BMPR1A(601299)、NGR3(605533)、GRID1(610659)等致病基因,具体见图1。
3 讨论
10q23微缺失综合征是较少见的染色体缺失综合征之一,临床表型涉及多个系统,具有较大的个体差异,由于10q23包含较多基因,基因型-表型间的联系尚未完全明确。
10q22.3-q23.2区域的特征是一组复杂的低拷贝重复序列(low-copy repeats,LCRs),它可以引起由非等位同源重组介导的基因组变化[2],本病例CMA检测发现10q22.3位置发生7.4Mb缺失,应用疾病数据库检索分析发现该片段区域缺失引起10q23微缺失综合征。10q23微缺失片段中包含42个基因,其中17个OMIM基因。其中BMPR1A、NGR3、GRID1为该综合征的主要致病基因。
BMPR1A位于染色体10q22.3范围内,全长52167bp,其编码骨形态发生蛋白1A型受体(bone morphogenetic protein receptor 1A,BMPR1A), 该
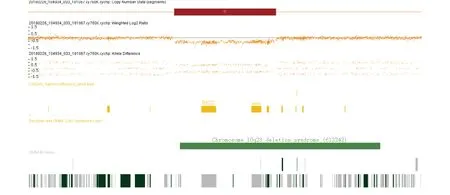
图1 本例胎儿羊水CMA分析结果图
受体属于丝氨酸/苏氨酸激酶型受体,参与骨发生和形成过程中TGF-β/BMPs的细胞核内信号传导。BMPs信号通过TGF-β依赖和-独立级联来发挥广泛的生物活性。心血管疾病如血管生成异常、动脉粥样硬化、肺动脉高压和心肌肥厚与异常BMP信号有关[3]。有学者发现BMPR1A介导的骨形态发生蛋白(bone morphogenetic proteins,BMPs)对于维持成骨细胞功能的完整性具有重要作用,BMPR1A基因在成骨细胞敲除后,会导致成骨细胞矿化减少、胶原合成能力减弱、骨质量下降[4,5],BMPR1A在调控包括心血管系统在内的各种组织和器官的细胞增殖、分化和凋亡中发挥关键作用。BMPR1A基因缺失的小鼠心脏正常形态发生改变,表现为室间隔缺损、心内膜垫缺损等[6]。有病例报道发现BMPR1A基因缺失引起身材矮小、面部畸形、先天性心脏畸形、幼儿息肉病等[7,8]。
NGR3基因主要在神经细胞中表达,其编码的神经调节蛋白3(neuregulin 3,NGR3)是酪氨酸激酶受体家族(ErBb)配体,主要分布于神经系统、心脏等组织,参与部分细胞信号传递,NGR3在神经发育、细胞增殖分化等过程发挥重要作用,NGR3基因缺陷与精神分裂等神经发育异常所导致的疾病密切相关[9]。在精神分裂患者前脑皮质中发现ErbB受体缺陷,提示NGR3信号通路参与精神分裂症发生、发展的机制[4],NGR3基因敲除的小鼠在压力应激源的共同作用下可影响小鼠内侧前额叶树突的髓鞘化,引起神经元网络中电信号传导紊乱从而引发精神病性行为,可能为精神分裂症发病机制[10]。有外文报道突变小鼠NGR3水平下降致功能不足可引起认知功能障碍,这可能是精神分裂症认知功能障碍的发病机制有关。NGR3基因是精神分裂症的一个易感基因,NGR3基因的突变或者缺失可以导致神经退行性变[11]。
谷氨酸受体1(GRID1)基因参与机体许多生理及病理反应过程,如学习与记忆、神经元的重塑、缺血缺氧的毒性作用,癫痫的形成及神经退行性病变等。GRID1基因突变或缺失与精神分裂密切相关[12]。
染色体微缺失是导致智力低下、发育迟缓、多发畸形的常见遗传因素,CMA具有通量高、分辨率高等特点,能在全基因组范围内检测染色体不平衡的拷贝数变异(copy number variant,CNV),能分辨检测染色体的微缺失微重复,也能明确染色体异常的具体位置,为产前筛选畸形的胎儿的诊断和临床遗传咨询提供依据。
