电感耦合等离子体-质谱法测定生脉注射液中14种元素含量
2018-12-25黄小琴钱保勇
黄小琴,钱保勇
(江苏省泰州市食品药品检验所,江苏 泰州 225300)
以铅(Pb)、镉(Cd)、砷(As)、铜(Cu)为代表的重金属及有害元素是中药最主要的外源性污染物之一,铅中毒可严重影响中枢神经系统,As及Cd有明确的致癌、致畸、致突变作用。中药注射剂直接进入体液,风险更大,2015年版《中国药典(四部)》明确规定了其 Pb,Cd,As,Cu残留量的限度要求[1]。此外,营养化学、毒物学和环境污染研究中公认 Pb、Cd、锑(Sb)、铬(Cr)等对生物和人体有害,其他元素虽然有一些为人体必需的微量元素,但当其蓄积一定量或价态改变时对人体亦有毒害作用。本研究中根据2015年版《中国药典》收载的 Pb,Cd,As,Cu 电感耦合等离子体 -质谱(ICPMS)测定法进行探索性研究,建立了ICP-MS法以测定生脉注射液中的硼(B)、Cd、Cu、镍(Ni)、钯(Ba)、Cr、锰(Mn)、As、铝(Al)、Pb、硒(Se)、钼(Mo)、Sn、锑(Sb)14种元素的含量,应用于其质量控制,对重金属及有害元素残留进行检测,为国家药品风险监控提供技术参数[2-14]。
1 仪器与试药
1.1 仪器
iCAP-Q电感耦合等离子体质谱仪(美国热电公司);Mars微波消解仪(美国CEM公司)。
1.2 试药
单元素标准溶液(B,批号为 16032,质量浓度为100 μg /mL),多元素标准溶液(Cd,Cu,Ni,Ba,Cr,Mn,As,批号为 15111,质量浓度为 50 μg /mL;Al,Pb,Se,批号为 15111,质量浓度为 100 μg /mL),单元素标准溶液[Mo(批号为 14113),Sn(批号为 16071),Sb(批号为16022),质量浓度均为 100 μg /mL],内标单元素标准溶液[锗(Ge),批号为 1091865,质量浓度为 1 000 μg /mL,铟(In),批号为 13051,铋(Bi),批号为 16031,质量浓度均为100 μg/mL],均由中国计量科学研究院提供;65%浓硝酸(优级纯,德国 Merk公司,批号为 UN2031);Milli-Q超纯水系统(美国Millipore公司);生脉注射液(江苏苏中药业集团股份有限公司,国药准字Z32021056,批号分别为 17030908,17031322,17031701,17031702,规格为 每支 20 mL)。
2 方法与结果
2.1 ICP-MS仪器工作条件及测定方法
射频(RF)入射功率:1.55 kW;采样深度:5 mm;冷却气流量:14 L /min;辅助气流量:0.8 L /min;载气流量:0.9 L /min;数据采集重复次数:3 次。采用在线内标法,用三通管将供试品溶液与混合内标溶液混合后进入ICP - MS 仪。测定时 B,Cu,Ni,Cr,Mn,As,Al,Se 以 Ge作为内标;Mo,Cd,Ba,Sn,Sb 以 In 作为内标;Pb 以 Bi作为内标。分别对系列混合标准溶液、空白溶液及供试品溶液进行分析,采用标准曲线法定量。
2.2 溶液制备
标准贮备液:精密量取B单元素标准溶液(100μg/mL)1 mL,置100 mL容量瓶中,用2%硝酸溶液稀释至刻度,即得 B 元素标准贮备液(1 μg/mL)。精密量取 Cd等多元素标准溶液2 mL,精密量取Mo,Sn,Sb的单元素标准溶液(100 μg/mL)各 1 mL,置同一 100 mL 容量瓶中,用2%硝酸溶液稀释至刻度,即得多元素标准贮备液(1 μg /mL)。
系列混合标准溶液:分别精密量取Cd等多元素的标准贮备液(1 μg/mL)5 mL 置 50 mL 容量瓶中,用 2%硝酸溶液稀释至刻度,得混合标准溶液(100 ng/mL)。精密量取混合标准溶液(100 ng/mL)适量,用2%硝酸溶液配制成含各元素标准溶液。
混合内标溶液:分别精密量取 Ge(1 000 μg/mL),In,Bi(100 μg /mL)的单元素标准溶液适量,用 2% 硝酸溶液稀释至刻度,配制成质量浓度为50 ng/mL的混合溶液。
样品预处理:精密量取生脉注射液2 mL,置微波消解罐中,加硝酸5 mL,密闭并消解。消解采用程序升温,20℃升温至120℃,保持5 min;再升温至150℃,保持5 min;再升温至180℃,保持20 min。消解完全后,冷却至低于60℃,然后取出消解罐,放冷,将消解后的溶液定量转移至50 mL的聚丙烯材料的容量瓶中,再用少量水洗涤消解罐5次,合并至容量瓶中,用水稀释至刻度,即得供试品溶液。同法不加生脉注射液制得空白溶液。
2.3 方法学考察
线性关系考察:取系列混合标准溶液,按2.1项下条件进样测定,仪器的内标进样管在仪器分析过程中始终插入混合内标溶液中,依次将样品管插入各个浓度的混合标准溶液中进行测定,以各元素与内标测量值的比值(Y)为纵坐标、相应质量浓度(X,ng/mL)为横坐标,分别绘制测定不同剂型样品时的随行标准曲线。结果各单元素标准溶液线性关系良好,详见表1。
精密度试验:取标准曲线第4点混合标准溶液(10ng/mL),连续进样6次,分别以各元素测量值计算 RSD。结果的 RSD均小于3%(n=6),表明仪器精密度良好。
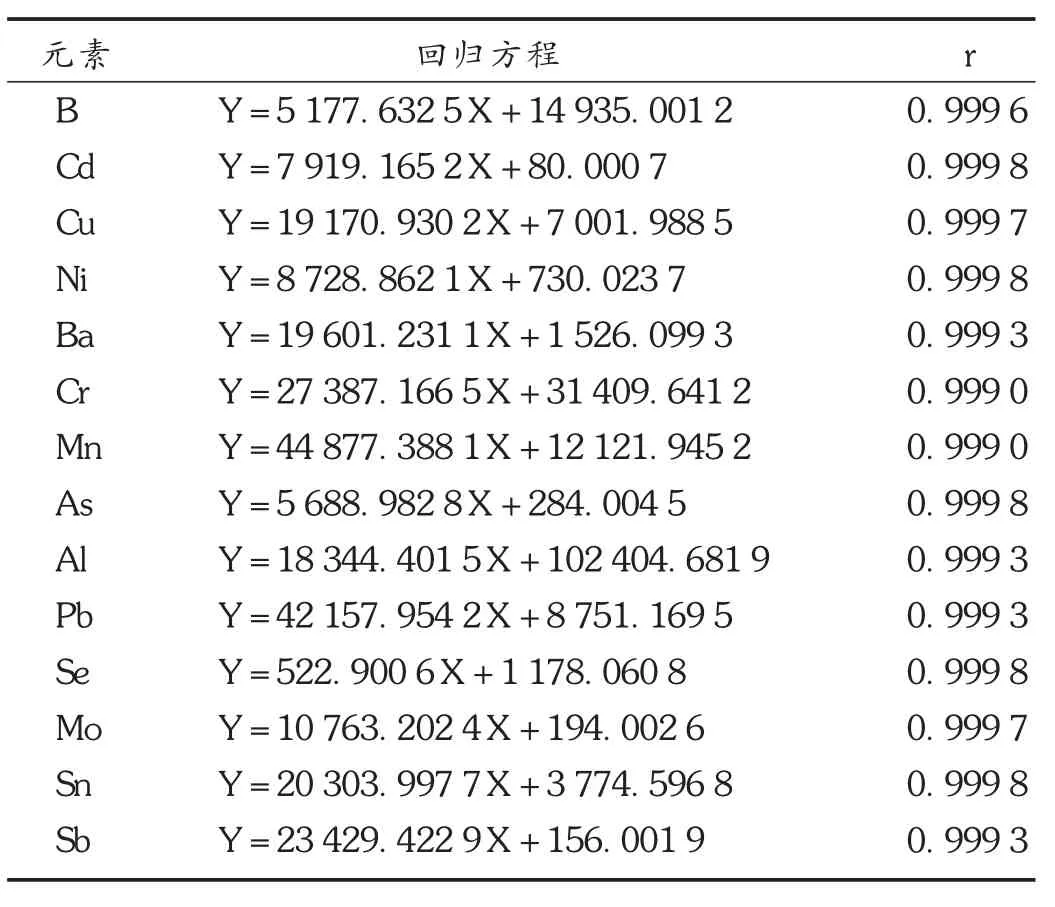
表1 线性关系考察结果
稳定性试验:取供试品溶液,在2 h内等时间间隔连续测定10次,以各元素测量值计算 RSD。结果的RSD<5%(n=10),表明供试品溶液在2 h内稳定性良好。
加样回收试验:分别精密吸取已知含量的6份生脉注射液(批号为17030908)2 mL,置微波消解罐,精密加入 B 元素标准贮备液(1 μg/mL)0.1 mL 及多元素标准贮备液(100,200 ng /mL)0.5 mL,按样品预处理项下方法处理,定容至50 mL,制得供试品溶液,测定含量并计算加样回收率。结果各元素在不同剂型中的回收率为86.5% ~ 109.2%,详见表 2。

表2 14种元素的加样回收试验结果(n=6)
重复性试验:因样品中部分元素含量低于检出限,故方法重复性用回收率及 RSD表示。结果见表2,表明该方法准确性和重复性均良好。
检出限和定量限确定:在本试验条件下,重复测定空白溶液10次,各元素信号响应的3倍标准偏差对应的元素浓度即为检出限;根据各元素信号响应的10倍标准偏差对应的元素浓度,考虑样品取样量和稀释倍数,计算定量限。结果见表3。
2.4 样品含量测定
分别取生脉注射液适量,按2.2项下方法制备供试品溶液,按2.1项下方法测定,由内标校正的标准曲线法计算含量。结果见表4。可见,4批生脉注射液中Ni,B,Ba的含量均较高,其余元素含量较低。

表3 14种元素检出限和定量限测定结果(ng/mL)

表4 样品含量测定结果( g/mL)
3 讨论
生脉注射液为澄清液体,比较了2%硝酸直接稀释和微波消解2种方法,在加样回收试验中发现,前者溶液会析出大量沉淀,影响测定结果的准确度,故舍弃该方法;采用后者,样品经微波消解后溶液澄清。本研究中也进行了其他中药注射液的重金属及微量元素的测定,认为探索方法时应结合中药注射液自身特性,如一些中药注射液易溶于酸或水,可采用直接稀释的方法;对于基质复杂、遇酸会产生沉淀或在水中溶解度低的样品,则应选用适当的消解方法以去除基质的干扰。
目前,国内外对玻璃包装容器注射液中迁移元素的研究报道较少。在注射剂中,玻璃可与药液发生化学反应。常见反应有:某些药物对酸、碱、金属离子等敏感,如果玻璃中的金属离子迁移进入药液,可催化药物成分产生催化降解作用,导致溶液颜色加深,产生沉淀,出现可见异物,药物降解加快等现象;某些毒性较大的金属离子或阳离子团迁移进入药液也会产生潜在的安全性风险。国内大多数小针剂的注射剂均采用低硼硅玻璃管制注射剂瓶作为容器,其质量直接影响药品质量。酸可能易与低硼硅玻璃发生元素迁移,造成药品中B元素含量增加,有对药品的稳定性和安全性造成影响的可能,应加强对低硼硅玻璃注射瓶的质量管理。如玻璃中的成分含有其他杂质时,玻璃的侵蚀加速,形成较深的孔洞。随着玻璃侵蚀的加剧,在受到外界振动影响时,玻璃侵蚀形成的锯齿状薄片容易脱落。美国食品药物管理局(FDA)也发布过几次因药液和玻璃容器不相容造成的药品召回事件。因此,国内在此类药品生产和研发过程中应按相关指导原则,关注药与包装容器的相容性问题,生产厂家变更玻璃容器的厂家或规格时,也要进行前期研究,保证上市产品不会产生金属离子超标的安全性问题。
本试验中采用ICP-MS法,建立了同时测定生脉注射液中14种元素的方法,操作简便快速,结果准确可靠,为中药制剂的质量评价提供了新的思路。通过对生脉注射液中 Pb,Cd,As,Cu的限度分析,生脉注射剂中的这4种常见重金属及有害元素残留基本可控。
