肺球孢子菌病误诊误治一例
2018-11-21周薇肖芃薛丽京李天义李艳刘燕熊德芳何镜荣
周薇 肖芃 薛丽京 李天义 李艳 刘燕 熊德芳 何镜荣
球孢子菌病(coccidioidomycosis,CM)是一种地方流行性真菌病。传统认为其疫区仅限于美洲部分地区,但其他国家和地区也有散发的输入性患者报道[1-2]。我国报道的数十例个案中,包括输入性及非输入性患者[3-6]。球孢子菌病又称“圣华金溪谷热”或“沙漠风湿”,是美国西南地区沙漠地带好发的、由双相粗球孢子菌引起的全身性疾病。目前已报道的球孢子菌病涉及了几乎所有的器官与系统,以肺部病变最常见[7]。笔者报道1 例肺球孢子菌病(pulmonary coccidioi-domycosis)的诊治过程,探讨其组织病理学表现及诊断和鉴别诊断,以提高临床医生对此病的认识。
临床资料
患者,男,55岁;广州市海珠区居民。因“发热、咳嗽伴胸闷15 d”于2018年3月7日收治入住广州市胸科医院。患者于2017年1月去美国加利福尼亚州探亲,在当地居住13个月,于2018年1月底回国。2月中旬因受凉后出现发热,无盗汗,体温最高39.2 ℃,高峰温度以下午出现为主;明显干咳,偶有少量白痰,无咯血,伴活动后气促、胸闷,咳嗽剧烈时有胸部隐痛。发病后于某大学附属医院门诊就诊,血常规显示:白细胞计数(WBC)26.66×109/L (正常值:4~10×109/L),中性粒细胞比率(N) 0.81(正常值:0.50~0.70);胸部X线摄影(简称“胸片”)显示右肺多发病灶,考虑“肺炎”,给予“左氧氟沙星+头孢呋辛”抗炎、对症治疗2周后,体温高峰降至38.5 ℃左右,咳嗽较前有所减少。但3月5日胸片复查显示肺部病灶较之前有增多。进一步行胸部CT检查,考虑“肺炎,不排除肺癌”,为求进一步诊治,入住我院。
一、入院初期诊治情况
入院体格检查:体温38.7 ℃,脉搏132次/min,呼吸频率21次/min,血压106/80 mm Hg(1 mm Hg=0.133 kPa)。患者发育正常,慢性病容,浅表淋巴结未及肿大,全身皮肤及巩膜无黄染,咽部及扁桃腺无充血、肿大;右肺呼吸音明显增粗,左肺呼吸音清晰,双肺未闻及干湿性啰音及胸膜摩擦音;心脏各瓣膜区未闻及病理性杂音;腹平软,无压痛、反跳痛及肌紧张,余未见异常。
实验室检查:WBC 13.12×109/L,N 0.67,血红蛋白(Hb)135.0 g/L(120~160 g/L),血小板计数(PLT) 431.0×109/L(100~300×109/L)。真菌1-3-β-D葡聚糖<10(pg/ml)(参考值<60.00 pg/ml),G-脂多糖I 7.853 pg/ml(参考值<10 pg/ml),超敏C反应蛋白(hs-CRP)88.04 mg/L(参考值0.00~10.00 mg/L),降钙素原(PCT) 0.44(ng/ml)(参考值<0.05 ng/ml)。肺炎支原体抗体1∶10 240。HIV检测阴性。痰涂片抗酸染色检查未检出抗酸杆菌;痰利福平耐药实时荧光定量核酸扩增检测技术(GeneXpert MTB/RIF)未检测到结核分枝杆菌;血γ-干扰素释放试验(IGRA):抗原A(早期分泌抗原靶6,ESAT-6)和抗原B(培养滤液蛋白10,CFP-10)孔均阴性。经纤维支气管镜冲洗液及肺穿刺活检组织抗酸杆菌培养均阴性。考虑肺部感染,给予头孢哌酮+阿奇霉素抗感染治疗1周,仍有咳嗽、持续发热等症状,以干咳为主,体温波动在37.5 ℃左右。
二、入院后对患者的进一步诊治过程
3月8日胸部CT平扫+增强扫描检查,显示右上、下肺斑片状实变影,密度不均,边缘欠清(图1);双肺见弥漫多发结节状影,边界模糊,右肺门及纵隔多发淋巴结肿大(图2)。考虑肺结核并发肺部其他细菌感染。纤维支气管镜检查(2018-03-09):可见双侧声带前联合处见溃疡样改变;右支气管黏膜充血、肿胀,大量泡沫样分泌物;右上叶黏膜红肿、粗糙,右下叶基底段开口前侧壁局部黏膜表面凹凸不平,各叶、段、亚段支气管管腔通畅,未见狭窄及出血。纤维支气管镜取活检组织标本行病理学检查:可见炎性肉芽组织增生及小灶凝固性坏死,未见肉芽肿结节及球孢子菌结构。特殊染色(抗酸染色及PAS染色)未见明确分枝杆菌及真菌结构。考虑肺部感染、结核病待除外、间质性肺病,采用头孢哌酮(2.5 g/次,2次/d,静脉滴注)联合阿奇霉素(0.5 g/次,1次/d,口服)治疗1周后,发热持续,改用亚胺培南(0.5 g/次,3次/d,静脉滴注)治疗1周,病灶持续增多(胸部CT平扫+增强扫描提示)。至此认为可排除肺部感染,调整治疗方案为诊断性抗结核药物治疗。其中,异烟肼0.3 g/次,1次/d;利福喷丁 0.6 g/次,2次/周;吡嗪酰胺 1.5 g/次,1次/d;乙胺丁醇0.75 g/次,1次/d;莫西沙星 0.4 g/次,1次/d。

图1,2 患者,男,55岁。胸部CT平扫+增强扫描检查(2018-03-08)。图1可见右上、下肺斑片状实变影,密度不均,边缘欠清;图2可见弥漫多发结节状影,边界模糊,右肺门及纵隔多发淋巴结肿大
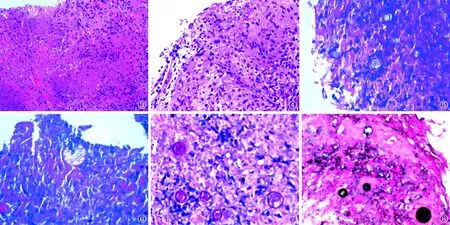
图3~6 肺穿刺活检组织病理切片检查(2018-04-06)。图3 可见小片状凝固性坏死,周边见肉芽肿结节形成 (HE ×40);图4 可见增生的类上皮细胞及少量多核巨细胞、反应性增生的成纤维细胞聚集构成肉芽肿(HE ×100);图5可见坏死物内大小不等的球状小体,厚膜孢子呈清楚的双层结构(HE ×100);图6 可见孢子体内有内生孢子(HE ×400) 图7 肺穿刺活检组织病理切片(2018-04-06)。可见孢子染色呈紫红色(PAS ×400) 图8 肺穿刺活检组织病理切片(2018-04-06)。可见孢子染色呈黑色(GMS ×400)
患者抗结核治疗10 d后仍持续发热,气促加重,影像学检查(胸部CT平扫+增强扫描)显示病变无好转且增多。为明确诊断,于3月30日行B超引导下取肺穿刺活检组织标本2条(长1.2~1.3 cm,直径0.05 cm),经4%中性甲醛固定,石蜡包埋制片。分别行苏木精-伊红染色(HE染色),光镜观察,可见肺穿刺组织内肺泡结构破坏,多发小片状凝固性坏死,周边见肉芽肿结节形成(图3);坏死周边可见增生的类上皮细胞及少量多核巨细胞、反应性增生的成纤维细胞聚集构成肉芽肿(图4),伴淋巴细胞、中性粒细胞及嗜酸性粒细胞浸润;坏死组织内可见球状小体(大而圆,直径约为30~60 μm,厚膜孢子的胞壁呈清楚的双层结构,嗜强碱性)(图5)和内生孢子,孢子体内可有内生孢子(图6)或空的细胞。特殊染色[包括过碘酸雪夫染色(PAS)和六胺银染色(GMS)]可清晰显示孢子的形态,PAS呈紫红色(图7),GMS呈黑色(图8)。病理诊断:肺球孢子菌性肉芽肿伴坏死。
结合患者曾旅居美国加利福尼亚的地域性流行病学史、组织病理学镜下特征、超过8周的病程,以及抗感染、抗结核治疗后影像学(胸部X线摄影及CT检查)检查显示病变加重的表现,诊断为进展性肺球孢子菌病。给予患者两性霉素B静脉注射(0.7 mg·kg-1·d-1)治疗,临床症状改善后(体温下降至正常,胸部CT显示病灶缩小)口服氟康唑(400 mg,1次/d,顿服)治疗(需服药1年),现随访患者,临床症状无异常、复查胸部CT显示病灶吸收。
讨 论
一、肺球孢子菌病的流行病学特点
球孢子菌病流行区多为半干旱气候,冬季温和利于真菌繁殖,夏季炎热有助于孢子的传播;这些地区的土壤具有碱性、高盐、富含有机物等特点,不利于其他微生物存活,却有利于球孢子菌的生长[8]。根据土壤样本的检出情况,传统观点认为球孢子菌的分布局限于美洲西海岸区域。美国疾病预防控制中心(CDC)一项调查显示,1998—2011年全美上报的117 717例球孢子菌病患者中97%来自亚利桑那州和加利福尼亚州[9]。此外,南美洲的一些国家,如委内瑞拉、阿根廷、巴拉圭、哥伦比亚、玻利维亚等,也有一定发病率[9-11]。
近几年,球孢子菌病的总体分布情况相对稳定,但流行病学呈现出一些新的特点。首先,球孢子菌病的发病率呈逐渐上升趋势,根据美国CDC的数据,球孢子菌的发病率在1998年为5.3/10万,随后逐年上升,至2011年已达42.6/10万,升高近10倍[12]。另一研究调查了2000—2012年美国加利福尼亚州儿童中球孢子菌病的发病率,结果提示年发病率同样呈升高趋势[12]。其次,非疫区国家输入性患者的报道增多。美洲以外的国家中,球孢子菌病输入性患者的报道也呈增多趋势。早在1967年挪威学者就报道了1例球孢子菌病输入性患者。此后,多个国家和地区,包括法国、德国、波兰、荷兰、意大利、土耳其、澳大利亚、韩国、日本、印度等,均先后报道了球孢子菌病输入性患者,这些患者在发病前均有疫区旅行或居住史[12]。最后,非传统疫区非输入性患者出现[12]。有国内学者对1958—2015年中国大陆地区报道的球孢子菌病患者进行了总结和综述,发现在纳入的30例球孢子菌感染患者中,有24例(80%)无明确疫区接触史,这一现象对我国不是球孢子菌病疫区的传统流行病学观念提出了挑战[13]。越来越多的证据表明,随着人类活动和环境的变化,球孢子菌的定植区域可能已超出以往传统认识中的北美西南沿海地域及美国其他地区(如华盛顿地区),甚至包括中国在内的其他国家,这有待后续研究做进一步证实。本例患者在发病前于美国加利福尼亚州探亲13个月,属于疫区国家输入性患者,但初期未能及时结合患者旅居史考虑到此菌的感染,以抗感染、抗结核药物治疗1个月,直到治疗效果欠佳,在肺穿刺活检组织病理检查后方确诊,故认为全面积极地收集患者发病前的流行病学史和既往史对诊断疾病意义重大。
二、肺球孢子菌病的临床分型
根据肺球孢子菌病的发生、发展,该病可分为三大类[14]:原发肺球孢子菌病、进展性肺球孢子菌病和播散性球孢子菌病。
1.原发肺球孢子菌病:一般无症状或有轻微症状,影像学检查表现为斑片状或模糊状浸润改变。偶尔患者出现结节状红斑、多形红斑和关节痛,周围血嗜酸性粒细胞增多,通常为自限性,在2~3周内消散。
2.进展性肺球孢子菌病:疾病持续久,患者的临床症状和特征超过6~8周,可有如下表现:(1)影像学检查通常表现为空洞或结节样病灶;(2)肺部空洞伴纤维化;(3)肺部播散的粟粒样病灶。缺乏典型的临床表现和影像学表现。
3.播散性球孢子菌病:较少见,约0.2%的原发性肺球孢子菌病患者可引起播散性球孢子菌病,可累及机体任何器官,常见受累部位有皮肤、骨关节系统、脑膜等中枢神经系统和泌尿生殖系统。播散形式通常以急性的方式进展,累及不同的器官或系统,诊断和治疗不及时可导致迅速死亡。
本例患者病程持久,超过8周,缺乏典型的临床表现,胸部CT检查显示为右上、下肺斑片状实变影,密度不均,边缘欠清,双肺见弥漫多发的结节状影,边界模糊;右肺门及纵隔可见多发淋巴结肿大。患者症状和特征无特征性表现,抗感染、抗结核药物治疗无效,属进展性肺球孢子菌病,容易漏诊。
三、肺球孢子菌病的诊断
本病的诊断主要依据为组织切片染色镜检,包括HE、PAS、GMS染色,因为真菌中富含黏多糖,PAS染色可显示糖原或其他多糖物质,黏多糖经过氧化后暴露醛基;而六胺银可被醛基还原为黑色的金属银,从而清晰显示真菌结构。病变组织镜下形态学表现(HE染色)为坏死性肉芽肿性炎症,肉芽肿中心见凝固性坏死或伴脓肿(病变早期),坏死内见体积大而圆的球状孢子结构,孢子菌体直径30~60 μm,部分菌体内见内生孢子,无生芽现象[5];以上描述特征本例患者均可见。文献报道的部分患者可见特征性形态改变,如孢子周围围绕嗜酸性Splendore-Hoeppli 物质(一种由抗原抗体复合物反应形成的红色放射状条纹)[15],本患者未见。
具有体积大而圆的球状孢子结构、部分菌体内见内生孢子为球孢子菌病诊断性意义孢子,在进展性和播散性病变中较多见,而在静止期则难以找到[15]。菌丝和内生孢子很少在组织中见到,而一旦在组织中找到大小、形态适合的孢子即可确诊。而仅仅发现不成熟的小球或成群的内孢子伴有菌丝壁碎片时不能作为组织学确诊的依据,需要进一步做真菌培养或放射免疫法证实,如IgM、IgG 抗体检测,结合离心沉淀法检测抗体及补体对诊断具有相对好的特异性[15]。本例患者在入院初期虽进行了支气管镜活检组织病理检查,但因送检组织内坏死灶面积极小,且未直达病灶组织,故未找到球孢子菌结构,诊断不明确。后在未进行肺穿刺组织病理学检查情况下,在尝试抗感染、抗结核药物治疗失败后方行肺穿刺组织病理学检查,检测出具有诊断性意义的孢子,有充分的依据诊断为球孢子菌病;在积极治疗后,患者病情逐渐改善。
四、鉴别诊断
1.孢子菌病与结核病鉴别:(1)球孢子菌病感染个体约60%可自愈,无临床症状或影像学表现。其他的40%可表现为急性呼吸道症状、夜间盗汗或咳嗽、胸膜炎性胸痛,可类似流感[6]。而结核病多表现为全身中毒症状,如午后低热、盗汗、疲乏无力、体质量减轻、心悸、女性患者可有月经失调或闭经。(2)球孢子菌病患者检测球孢子菌素皮肤试验阳性、血清学试验阳性;WBC升高,尤其是中性粒细胞和嗜酸性细胞比率明显增多;血红细胞沉降率持续加快。而结核菌素试验阳性,WBC基本正常,中性粒细胞和嗜酸性粒细胞比率多数正常,血红细胞沉降率加快。(3)取球孢子菌感染处脓液及穿刺液进行培养后镜检,可找到关节菌丝型孢子和孢子菌;而结核病上述标本培养可见结核分枝杆菌。(4)球孢子菌病可见肉芽肿结节、凝固性坏死或伴有脓肿形成,并见多个卵圆形或圆形样球状孢子结构,孢子菌体直径30~60 μm,部分菌体内见内生孢子。而结核病的肉芽肿结节中央可出现干酪样坏死,也可见多核巨细胞,但以郎罕细胞为主;结核分枝杆菌抗酸染色为阳性。
2.与其他疾病鉴别:球孢子菌病肉芽肿需要与其他肉芽肿性病变相鉴别,包括其他真菌感染,如新型隐球菌、芽生菌、组织胞浆菌等,以及非感染性肉芽肿性疾病,如结节病、风湿结节等。(1)新型隐球菌:直径相对较小(2~15 μm),菌体圆形,菌体壁相对较薄,淡染,菌体外有透明区,菌体繁殖方式表现为出芽,最突出特征是荚膜黏液卡红染色阳性。(2)芽生菌: 此菌感染肺的初期,为急性炎症细胞浸润及组织细胞反应,尔后形成坏死性肉芽肿,肉芽肿中心为化脓性坏死,坏死周边见上皮样组织细胞围绕;芽生菌形态较单一,平均直径8~15 μm,大者可达30 μm,具有淡棕色厚壁,内含原浆及多个核,荚膜黏液卡红染色阴性。(3)组织胞浆菌:急性组织胞浆菌肺炎,常导致坏死性肉芽肿伴有上皮样细胞肉芽肿和多核巨细胞反应,容易与肺结核混淆。慢性组织胞浆菌病肺组织病变中心见干酪样坏死伴钙化,其周围纤维化。菌体通常在细胞内,菌体小,为卵圆形或圆形的单个芽生细胞,直径1~5 μm。PAS和GMS染色可清晰见到菌体。(4)结节病:一种以上皮样细胞为主的结节,但结节内有小血管,很少有坏死,突出特征是出现多核巨细胞胞质内肖曼小体和星状小体。(5)风湿结节:可见栅栏状肉芽肿结构和坏死,尤其在使用了免疫抑制剂治疗以后导致继发感染者,需仔细寻找病原体、排除真菌感染的可能,并且要结合临床病史和血清学检测结果给予综合判断。
五、治疗与预后
球孢子菌病多数患者为自限性,无需治疗,症状多在数周内消失,但对于有免疫系统受损者,可给予抗真菌药物治疗,如口服氟康唑(400 mg/d)或伊曲康唑(400 mg/d),根据临床疗效,治疗3~6个月或更长时间;播散性球孢子菌病需要上述治疗至少1年,至症状改善并稳定;而对于出现弥漫性肺部感染的患者,无论免疫是否受损,均需药物积极治疗,给予两性霉素B脂质体(5 mg·kg-1·d-1)或两性霉素B(0.7~1.0 mg·kg-1·d-1),至症状改善后再口服氟康唑(400 mg/d)或伊曲康唑(400 mg/d)至少1年[16]。由于治疗方案不同,误诊会导致病情加重,甚至危及生命。本患者病程超过8周,病情进行性加重,最终诊断为进展性球孢子菌性肺炎,采用静脉注射两性霉素B治疗后症状明显好转。
综上所述,对发热、咳嗽、病程较长、可疑肺部感染及肺结核的患者,在初期抗感染、抗结核药物治疗过程中,应及时评估疗效,当患者病情不缓解甚至发生进展时不仅要排除药物热、耐药结核病等情况,还必须警惕误诊的可能。此时需积极寻找病理学、病原学依据,同时要重视流行病学资料的采集,扩展诊断思路,有利于对少见的传染性疾病、地方流行性疾病及时得到明确诊断。
