核黄素反应性脂质沉积性肌病一家系ETFDH基因突变研究
2018-11-14孔令恩庄顺芝李才明陈礼锟张停亭邱金华周谦武蔡春生
孔令恩, 庄顺芝, 李才明, 陈礼锟, 张停亭, 邱金华, 周谦武, 蔡春生
脂质沉积性肌病(LSM)是一组由于脂肪代谢中酶和(或)肉碱的缺陷而使异常增多的脂肪滴在肌纤维内沉积导致的肌肉疾病。多种酰基辅酶A脱氢酶缺乏症(MADD)又称戊二酸尿症Ⅱ型,是LSM 三大常见病因中的一种。MADD属于常染色体隐性遗传性疾病,是由于电子传递核黄素蛋白脱氢酶(ETFDH)基因或电子传递核黄素蛋白A/B基因发生突变所致[1]。MADD分为Ⅰ、Ⅱ、Ⅲ 3个亚型,其中Ⅲ型为青少年或成年起病,表现为核黄素反应性LSM(RR-LSM)。研究表明[2,3]ETFDH是RR-LSM的主要突变基因。截止目前,国内外已报道超过50个RR-LSM相关的ETFDH基因突变点[4],其中约1/3的突变只见于中国人的报道。本研究对RR-LSM一家系进行基因测序,探讨该家系ETFDH基因的突变方式。
1 对象与方法
1.1 临床资料 (1)RR-LSM家系 先证者为女性,75岁,广东人,因“四肢无力4 y,加重1 m。”于2017年5月收治于本科。患者于4 y前开始无明显诱因出现四肢无力,双下肢明显,下蹲后起立困难,上楼梯尤为明显,平时行走300 m后即感觉下肢酸软、费力,休息后可稍缓解,双手上抬稍费力,尚能自行完成梳头、洗脸等日常活动,3 y前开始出现抬头无力,无发热、吞咽困难、咀嚼费力、呼吸困难等。1 y前曾在外院就诊,查肌酸激酶示448 U/L,肌电图提示肌源性损害,肌肉活检提示:HE染色可见广泛存在的肌纤维内空泡,ORO染色示肌纤维内大量红染物质沉积,考虑脂质沉积性肌病可能,给予补充维生素B2治疗,患者自觉上述症状明显缓解,服用1 m后遂自行停药。近1 m以来四肢无力症状加重,症状同前,为进一步诊治收入我科。既往有高血压病史8 y,服用“络活喜”降压治疗,血压控制平稳。足月顺产,无窒息、高热惊厥史。先证者的一个妹妹现年73岁,3 y前也开始出现与先证者类似的病史,服用维生素B2治疗,效果明显。除先证者及其妹妹外,整个家系中其他成员均无类似的表现,该家系谱(见图1)。家族中无近亲婚配史。入院体格检查:先证者心肺腹查体无特殊。神经系统检查:意识清楚,查体合作,颅神经查体阴性。四肢近端肌力4级,远端5级,四肢肌张力降低,腱反射减弱,病理征未引出,感觉系统检查无异常,脑膜刺激征阴性。(2)正常对照者:100名,均为同期本院体检中心的健康体检者。入院后查先证者肌酸激酶712 U/L,3大常规、甲功5项、肿瘤4项、梅毒、HIV、乙肝两对半、离子3项、肝肾功能、风湿3项、血管炎5项、免疫8项均正常;肌电图:肌源性损害。肝胆脾胰、泌尿系、子宫附件超声检查未见明显异常。头部+颈椎MRI平扫:双侧基底节区多发腔隙性梗死灶,颈椎MR平扫未见明显异常。
1.2 方 法
1.2.1 DNA提取 经过惠州市第一人民医院伦理委员会审核通过,取得家系中4位成员(Ⅱ3、Ⅱ5、Ⅲ3、Ⅳ2)和100位健康体检者的知情同意后,用2%的EDTA抗凝管各抽取静脉血3 ml。用DNA提取试剂盒(Promega,Madison,Wi,USA)提取上述个体基因组DNA。
1.2.2 DNA扩增 参照文献[5]合成引物,扩增该家系4位成员ETFDH基因13个外显子及其侧翼系列。采用25 μl的反应体系:上、下游引物各2 μl (5 μmol/μl),DNA模板2 μl (50 ng),DreamTaqTMGreen PCR Master mix (2×)12.5 μl,加双蒸水至25 μl。PCR反应条件:95 ℃预变性4 min,然后95 ℃变性30 s,62~56 ℃退火30 s (从62 ℃开始,每个循环降低0.2 ℃,一直降至56 ℃),72 ℃延伸40 s,共30个循环,最后72 ℃延伸10 min。扩增产物用1.5%的琼脂糖凝胶电泳检查。
1.2.3 DNA测序 PCR产物经纯化后用ABI3730XL自动测序仪进行直接测序。采用基因分析软件Vector NTI 8.0比对分析测序结果。
2 结 果
基因测序显示先证者及其妹妹第7号外显子存在c.770A>G错义突变,使第257位密码子由TAT突变为TGT,导致正常的酪氨酸(Tyr)被半胱氨酸(Cys)替代(Y317C);第10号外显子存在c.1270_1273del缺失突变。先证者的儿子亦携带c.1270_1273del突变(见图2)。先证者的孙子及100名健康体检者均未见上述突变。
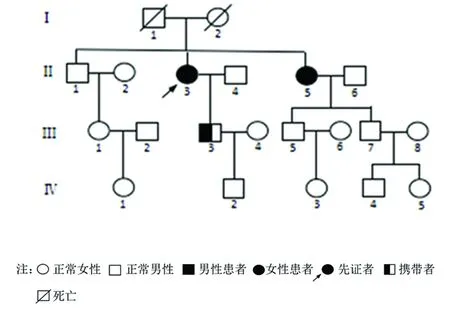
图1 核黄素反应性脂质沉积性肌病家系图
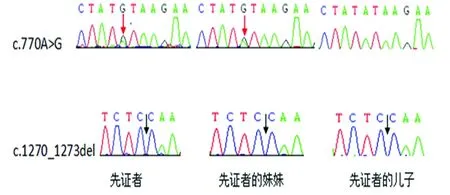
图2 先证者及其妹妹、儿子ETFDH基因测序图。先证者及其妹妹均存在c.770A>G和c.1270_1273del突变;先证者儿子存在c.1270_1273del突变。红色箭头所指为c.770A>G突变位置;黑色箭头所指为c.1270_1273del突变所在的位置
3 讨 论
本家系的先证者以四肢无力为主诉,以近端为主,严重时出现抬头无力,肌酸激酶升高,肌电图提示肌源性损害,考虑肌肉系统疾病;随后的肌活检证实为脂质沉积性肌病,对维生素B2治疗效果明显,故考虑为RR-LSM。基因检测证实先证者ETFDH基因存在突变,结合患者的发病年龄和临床表现,诊断为MADDⅢ型。RR-LSM的表现多样,常见的症状包括四肢近端无力、运动不耐受、咀嚼肌无力、颈肌无力[6~8]等,少见的可表现为呼吸困难[6]或横纹肌溶解[9]的症状。基因检测出2例患者均同时存在c.770A>G和c.1270_1273del突变,其中c.770A>G已经被诸多文献[5,10~11]证实为致病性突变。该突变使第257位密码子由TAT突变为TGT,导致正常的酪氨酸(Tyr)被半胱氨酸(Cys)替代(Y317C),从而导致蛋白功能缺失。王韵[5]等在2011年报道过中国北方地区20个RR-LSM家系,其中9个家系检测出c.770A>G突变,故提出c.770A>G可能为北方地区的热点突变,然而本家系世代久居南方地区,家系中多人出现c.770A>G突变,故本研究证实该突变并没有明显的地区差异。c.1270_1273del突变既往文献未见报道,100名健康人群中亦未筛查出该突变,结合该病的遗传方式,故我们推测该突变为新发的致病性突变,进一步拓宽ETFDH基因突变谱。该c.1270_1273del突变如何影响到蛋白功能有待功能学检测进一步研究。目前国内外虽有较多的RR-LSM的报道,但发病年龄以青少年或成年为主,本家系的2例患者的发病年龄分别为71岁、70岁,如此高龄才发病尚未见相关的文献报道,我们推测患者发病年龄晚可能与c.1270_1273del突变导致蛋白功能缺陷程度较轻,从而使得发病年龄较晚有关,不过具体的机制还有待进一步研究证实。RR-LSM为常染色体隐性遗传,本家系两姐妹先后发病,根据遗传学规律,推测2例患者的突变基因均来源于父母双方,可惜的是患者双亲已经去世,未能得到进一步证实。为进一步明确患者的子女中是否携带ETFDH基因相关突变,做好遗传咨询,我们对家系的部分成员—先证者的儿子(Ⅲ3)及孙子(Ⅳ2)进行基因检测,结果发现先证者的儿子(Ⅲ3)亦携带c.1270_1273del突变,为RR-LSM携带者,先证者的孙子(Ⅳ2)未发现上述2个突变。由于RR-LSM患者对核黄素(维生素B2)有显著的效果,口服维生素B2治疗后患者的临床症状及体征可迅速缓解或治愈,操基清[6]等提出对于临床疑似RR-LSM患者,可考虑尝试使用核黄素诊断性治疗。
