以脑梗死症状起病的主动脉夹层1例报告
2018-11-14刘代强邹慧敏郝延磊
刘代强, 邹慧敏, 郝延磊
随着中国人口老龄化的日益明显,脑卒中的发生率也不断攀升,其中缺血性脑卒中即脑梗死的发病率较高。脑梗死因为其较高的发病率、较高的致残率和较高的致死率,严重的影响着人们的生活。对于急性期的脑梗死,目前公认的有效治疗办法就是急诊溶栓,它能使部分闭塞的血管再通,从而恢复脑组织的血流灌注,也就避免了脑细胞的坏死。溶栓的利弊取决于急诊医师对于急症脑梗死的准确识别与否,准确判断是急性期脑梗死后行溶栓治疗,好处是明显的;但是如果不能除外是其他急症所致,比如说临床上致死率极高的主动脉夹层,那行溶栓治疗的预后就不好说了。可见,能够准确的识别一种急危重症是否是脑梗死,要不要予以溶栓治疗,对于每一位急诊医师而言,是何等的重要。
1 病例介绍
患者,男性,69岁。主因“左侧肢体活动不灵3 h”,于2018年3月20日入院。患者3 h前无明显诱因出现胸闷、左侧肢体活动不灵,主要表现为左手持物不稳,走路拖步,无头痛、头晕,无恶心呕吐,无意识障碍,无视物模糊。当时未在意,随后肢体无力症状持续无缓解,为求进一步治疗,今来我院就诊。急诊科行头部CT“排除脑出血”,遂以“脑梗死”收入我科。患者发病以来,精神可,未进食,一般情况可。既往有“冠心病”、“高血压病”,均未系统诊治。有吸烟史:5~6支/d×40 y,饮酒史:白酒100 ml/d×40 y。入院查体:T36.6 ℃,P45次/分,R18次/分,Bp96/64 mmHg,神志清,精神可,言语流利,左侧鼻唇沟浅,伸舌居中,左侧肢体肌力Ⅳ级,肌张力正常,双巴氏征未引出。NIHSS评分6分。考虑脑梗死,急诊排除溶栓禁忌后给予阿替普酶溶栓(0.9 mg/kg)治疗。患者在8:20突发全身不适、大汗,憋喘,血压70/43 mmHg,四肢厥冷。遂转入重症监护室,入室后评估患者病情,高度怀疑主动脉夹层,急行主动脉全层CTA检查,结果回示:(1)主动脉夹层动脉(Standford A型)并假腔内血栓形成可考虑;(2)主动脉粥样硬化性改变;(3)双肺慢性炎症、肺气肿;(4)右肺下叶小结节;(5)心包积液;(6)胰腺体部小脂肪瘤可考虑;(7)副脾可能;(8)前列腺内钙化灶(见图1~6)。
确诊为主动脉夹层伴壁间血肿形成。急查凝血常规:D-二聚体测定:240.3 mg/L,余未见异常。再次测量四肢血压:左上肢:65/40 mmHg,左下肢85/36 mmHg;右上肢67/42 mmHg,右下肢80/60 mmHg,持续中流量吸氧,血氧饱和度98%。心外科急会诊考虑诊断为急性主动脉夹层、心包填塞。 9:55患者意识突然丧失,心率下降至35次/分,心电监护示异位心律,血压测不出,无自主呼吸,考虑夹层破裂,向家属告知病情,予以抢救治疗。并立刻给予胸外心脏按压、气管插管术等抢救措施。9:58患者心率降至0次/分,血压测不出,双侧瞳孔散大固定,光反射消失,综合心电监护示等电位线,血压测不出,大动脉搏动消失,反复给予肾上腺素药物抢救治疗,于10:54宣布临床死亡。死亡原因:主动脉夹层。给予尸体料理。
2 讨 论
不同以往文献报道主动脉夹层患者常表现为胸背部疼痛,该案例较为罕见之处在于患者首先出现左侧肢体活动不灵这一脑梗死的症状,而且经神经内科溶栓治疗后因主动脉夹层抢救无效死亡。
首先,复习一下主动脉夹层的相关知识。主动脉夹层(aortic dissection,AD)属于心血管疾病中的危重急症,起病急、进展快、病死率极高,也经常被误诊和漏诊[1]。1761年Morgagni首先描述了AD,随着我国心血管疾病谱的改变,近来也有研究将AD归入急性主动脉综合征(acute aortic syndrome,AAS)[2]。AD在人群中的发病率约为每年6/10万,男性多于女性,平均发病年龄为63岁。全球疾病研究学发现主动脉夹层的病死率从1990年的2.49/10万增长到2010年的2.78/10万,其中男性比例更高[3]。免疫炎症机制在AD的发生、发展中起着重要的作用。起初,主动脉内膜发生撕裂或溃疡,主动脉腔内的血液通过内膜破口进入血管中膜或是主动脉滋养血管自发破裂在血管中膜出血,导致炎症反应,最终使得主动脉扩张或破裂。AD常累及升主动脉近端和左锁骨下动脉开口远端的降主动脉[4]。AD的危险因素有[5]:(1)获得性因素:如高血压、动脉粥样硬化、感染、自身免疫性疾病、举重、遭受外伤或车祸引起突发扭转或减速导致的损伤、吸食成瘾性药物、医源性损伤、妊娠等。其中高血压是AD最常见危险因素,65%~75%的AD患者发现有高血压并且控制不良。而妊娠是AD的一种特殊危险因素,40岁前发病的女性AD患者中近50%发生于妊娠期,且多发生在妊娠晚期和产褥早期,且有研究表明妊娠合并Stanford A型AD的院前病死率为53%。(2)遗传性因素:如马方综合征、Ehlers-Danlos综合征、主动脉瓣二叶畸形及家族性无症状性主动脉夹层分离,其中以马方综合征最常见。高达96%的AD患者起病时表现为突发、急起、剧烈、呈撕裂样或刀割样的疼痛,且疼痛很少放射至颈、肩、或手臂等部位。A型最常见的症状是前胸痛;B型最常见背痛和腹痛。发病时多伴发晕厥、主动脉瓣反流、继发性心肌缺血甚至心肌梗死、心包填塞、心功能衰竭和心源性休克等。神经系统并发症的发病率15%~40%,且多为一过性,表现为脑缺血或卒中、声嘶、急性偏瘫等[6]。并发咯血、呼吸困难、胰腺炎或急性肾功能异常、肠系膜动脉缺血所致腹痛等的发生率较低。AD的分类方法很多,常用的是根据内膜破口位置及夹层累及的范围划分为Stanford分型和De Bakey分型[7]。De Bakey I型为升主动脉及降主动脉均受累;Ⅱ型仅升主动脉受累;Ⅲ型仅累及降主动脉。Stanford分型中只要累及升主动脉而不论破口的位置如何均属于A型;仅累及左锁骨下动脉起始部远端的降主动脉的为B型。AD的临床分期一般为:急性期<14 d;亚急性期15~90 d;慢性期>90 d。本病的诊断主要依赖于影像学检查。临床上常用的检查有经胸超声心动图(transthoracic echocardiography,TTE)、CT血管造影检查(computed tomography angiography,CTA)和核磁共振成像(magnetic resonance imaging,MRI)。实验室检查中[8]D-二聚体(D-dimer,DD)胶乳凝集法(阴性<0.5 mg/L)对于AD的敏感性达100%,特异性为67%。未经治疗的AD患者预后极差,院外死亡率达25%,发病24 h和48 h内病死率高达21%和50%,1 w内病死率60%~70%;经手术干预的AD患者术后1 m内死亡率可从90%降至30%。Stanford A型AD患者最初48 h内死亡率为50%,围手术期死亡率为25%;B型AD患者术后院内死亡率为25%~50%;而接受胸主动脉腔内修复术(TEVAR)治疗的患者30 d内死亡率仅为8%[5]。
其次,分析一下该例患者最先以“左侧肢体活动不灵”这一脑梗死的症状起病,最终却因主动脉夹层而死亡的可能性及原因。已有报道指出:AD患者神经系统并发症的发病率15%~40%,其中50%为一过性,表现为脑缺血或卒中、声嘶、急性偏瘫等。可见,虽然出现神经系统并发症的发病率不是太高,但也不是不发生。可以出现急性偏瘫的情况,但此例患者特殊在是以肢体偏瘫为首发症状,极容易误诊为急性脑血管病。患者最终诊断为主动脉夹层而最先表现为左侧肢体偏瘫的很可能原因为主动脉内膜破裂、形成夹层后影响了肢体的血液供应、组织营养缺乏。而且,因为大部分正常人的心脏都位于胸腔左侧,故主动脉夹层后影响肢体的血液供应、发生肢体无力和瘫痪也多在左侧肢体。综上所述,该例患者虽然最终诊断为主动脉夹层,但是出现“左侧肢体活动不灵”这一脑梗死的症状,是可能的,也是可以的,少见的是以偏瘫为首发症状。因此,临床医生们在诊治肢体偏瘫的患者的时候,除了神经科的常见病之外,主动脉夹层也是应该考虑到的。不然极容易误诊,甚至会造成不好的预后。
最后,我们可以发现本案例罕见之处在于患者因为诊断为急性脑血管病(脑梗死)而接受了溶栓治疗,并且最终因为主动脉夹层破裂抢救无效死亡。虽然主动脉夹层是临床的急危重症,死亡率很高,但是此例患者的溶栓治疗是否加剧了夹层的破裂却很难解答。综上所述,临床医生们在进行急诊溶栓时,除了常规的识别溶栓治疗的适应证和禁忌证之外,也应该除外主动脉夹层的可能。如果诊断明确,急性脑血管病使用溶栓治疗是肯定无疑的;但是如果无法排除主动脉夹层的可能性,使用溶栓治疗则需要小心、谨慎。如何避免误诊和漏诊,这就需要临床医师们基本功要扎实,除了要掌握本科疾病,还要具备多学科的知识,尤其是对既往已明确诊断、反复就诊的患者,沿用原有方案治疗无效时,一定注意患者的临床症状群是否有变化,是否存在合并其他疾病的可能性; 多学科的发散式思维,可以帮助我们合理处理临床复杂疾病的诊疗。此外,详细的询问病史、仔细的体格检查、选择适当的辅助检查,也是必须的,可以帮助我们在复杂的临床诊疗过程中,抽丝剥茧,逐渐找到一条清晰的思路,最终避免漏诊和误诊,以免延误治疗时机。
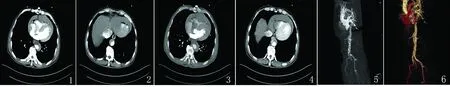
图1 主动脉CTA-胸腔段;图2 主动脉CTA-腹腔段;图3 主动脉CTA-双腔的主动脉;图4 主动脉CTA-心包填塞;图5 主动脉CTA-主动脉全程,见粥样硬化改变;图6 主动脉CTA-主动脉全程三维重建
