ALL患儿HD-MTX血药浓度对疗效及不良反应的影响
2018-11-07杨小英
杨小英,毛 凯,张 浩*
0 引言
急性淋巴细胞白血病(Acute lymphoblastic leukemia,ALL)是儿童时期最常见的恶性肿瘤,是由于原始及幼稚淋巴细胞在骨髓异常增生和聚集并抑制正常造血,导致贫血、血小板减少和中性粒细胞减少[1]。HD-MTX在治疗过程中对正常组织细胞也有杀伤作用,临床通常采用水化、碱化、亚叶酸钙(Calcium leucovorin,CF)解救等规范化治疗措施来降低相关不良反应的发生,提高治疗效果。本文通过对我院近2年来使用HD-MTX患儿的血药浓度和不良反应等资料进行回顾性统计分析,寻找宁夏地区患儿的用药特点及不良反应发生的规律,为今后临床治疗提供依据。
1 材料与方法
1.1 一般资料 2015年1月至2017年6月在我院住院且确诊为ALL并进行HD-MTX化疗的57例患儿,男35例(61.4%),女22例(38.6%);年龄1~15岁,平均(6.2±3.6)岁;体重11.0~50.0 kg,平均(22.15±10.26) kg;患儿体表面积0.45~1.43 m2,平均(0.84±0.25) m2;汉族32例(56.1%),回族24例(42.1%),满族1例。
1.2 血药浓度监测 采用高效液相色谱法测定MTX的血药浓度。
1.3 用药方法 MTX每次以总量的1/10作为突击量在30 min内均匀泵入,9/10余量在23.5 h内持续静脉滴入,亚叶酸钙(CF)在滴注MTX 36 h后开始进行解救,每次15 mg/m2,q6h,共6次;第2~4天进行水化、碱化治疗,水化4 000 ml/m2,碱化120 ml/m2,监测24、36、48、54、72 h的MTX血药浓度。本研究将48 h HD-MTX血药浓度>1 μmol/L或72 h HD-MTX血药浓度>0.1 μmol/L定义为排泄延迟,需增加 CF解救剂量及次数[2]。
2 结果
2.1 不同剂量组不同时间MTX血药浓度分布情况与排泄延迟情况分析 MTX化疗后不同时间采集静脉血,进行MTX血药浓度测定,按单位体表面积给药,其中 A组(3 g/m2) 49例次,B组(4 g/m2) 33例次,C组(5 g/m2) 153例次(总246例次中,有4例次用药剂量为1 g/m2,3例为2 g/m2,4例为4.5 g/m2,由于例次较少,未列入对比)。C组24、36 h的血药浓度高于A组、B组。通过24 h持续给药方式,三种剂量MTX平均血药浓度均达到MTXPG(甲氨蝶呤多聚谷氨酸)饱和所需稳态血药浓度。不同剂量组的排泄延迟发生率比较差异无统计学意义(χ2=1.634,P>0.05)。见表1、表2。

表1 不同剂量组排泄延迟发生率比较
2.2 MTX血药浓度在回族、汉族之间的分布情况及不同民族之间排泄延迟发生率比较 246例次MTX血药浓度监测结果中,回族109例次,汉族132例次,满族5例次。分析回族、汉族之间MTX血药浓度及排泄延迟的情况,结果显示,A组(3 g/m2)中,回族、汉族患儿36 h MTX血药浓度比较差异有统计学意义(P<0.01),而排泄延迟率差异无统计学意义(χ2=0.890,P>0.05),见表3、表4。

表2 不同剂量组血药浓度比较
注:与C组比较,*P<0.05,**P<0.01

表3 不同民族之间血药浓度比较
注:**不同民族之间比较,P<0.01

表4 不同民族组别之间排泄延迟发生率比较
2.3 MTX血药浓度与性别差异分析及不同性别之间排泄延迟发生率比较 246例次MTX血药浓度监测结果中,男童137例次,女童109例次,二者MTX血药浓度比较差异无统计学意义(P>0.05),排泄延迟发生率差异也无统计学意义(χ2=0.542,P>0.05),见表5、表6。

表5 不同性别之间排泄延迟发生率比较
2.4 使用HD-MTX化疗后不良反应发生情况 查阅患儿临床资料发现,使用HD-MTX化疗后发生不良反应主要表现为胃肠道反应(食纳欠佳、恶心、呕吐、腹痛、腹泻)、黏膜损害(口腔周围和肛周围黏膜发红、溃烂、破损等)、肝功能损害(巩膜黄染,转氨酶水平升高)、骨髓抑制(以中性粒细胞和白细胞下降为主,部分伴有血小板和血红蛋白降低)、感染(以呼吸道感染为主)。见表7。
3 讨论
MTX是抗叶酸代谢药物,是治疗儿童ALL的主要药物之一,HD-MTX在巩固治疗阶段髓外白血病的防治中发挥重要作用。但HD-MTX在抑制白血病细胞的同时也会抑制正常细胞,引起较多的全身毒副作用。36 h后,有相当量的骨髓干细胞及胃肠道黏膜的干细胞恢复进入分裂,因此大量正常细胞遭到杀伤,而此时给予四氢叶酸解救可阻断MTX的作用,可使增殖快的正常细胞不受MTX的细胞毒作用[3]。在不同时间动态监测MTX血药浓度,24 h血药浓度可预测疗效,而48、72 h血药浓度则反映MTX在体内的排泄情况[4]。本研究结果显示,3种剂量甲氨蝶呤24 h平均血药浓度均达到有效治疗浓度,高剂量血药浓度在24、36 h的平均浓度明显高于其他2个剂量组,而3个剂量组48、54、72 h的血药浓度比较差异无统计学意义,与廖静[5]报道一致,后者研究显示,不同剂量MTX输注后48 h平均血药浓度接近,推测是由于MTX剂量越大排泄越快,48 h后平均血药浓度不受剂量影响。
李秀贺等[6]研究了性别对药物消除的影响,结果显示,各时间点高浓度事件中,男性高于女性,似乎表明消除与性别有关,最终证实是由于男性单位体表面积MTX用药量显著高于女性所致,与性别无关。本研究结果排除了单位体表面积MTX用药量的影响,发现各时间点不同性别患儿血药浓度差异无统计学意义。
有研究分析了导致排泄延迟的影响因素。庞露等[7]认为,患者生理状态、药物相互作用、药物代谢酶等多方面因素均可能导致甲氨蝶呤的排泄延迟。聂艳霞等[8]认为,饮食量、呕吐、给药剂量、疾病危险度及患儿年龄是影响甲氨蝶呤治疗小儿白血病后排泄延迟发生率的重要因素。本研究246例次中,有25例次(10.2%)患儿发生排泄延迟。对比观察给药剂量、性别、民族对药物排泄延迟的影响,结果差异均无统计学意义,与Wang等[9]研究结果一致。MTX排泄延迟与患儿的个体差异及MTX在体内的药动学特点有关。
本研究中不良反应发生统计结果显示,发生率前3位分别为骨髓抑制(45.8%)、黏膜损害(19.0%)和肝功能损害(17.1%)。22例次(10.2%)发生胃肠道不良反应,而发生排泄延迟的患儿中有12例(48%)发生胃肠道反应,排泄延迟胃肠道反应的发生率显著升高。其中1例发生排泄延迟的患儿120 h的血药浓度仍高达0.364 μmol/L,同时出现恶心、呕吐、眼角糜烂、口腔黏膜糜烂、巩膜黄染、骨髓抑制、呼吸道感染等不良反应。因此,应监测MTX血药浓度,对药物排泄延迟的患儿应密切关注,积极采取有效治疗措施,减少不良反应的发生,从而保证ALL患儿化疗的安全性。
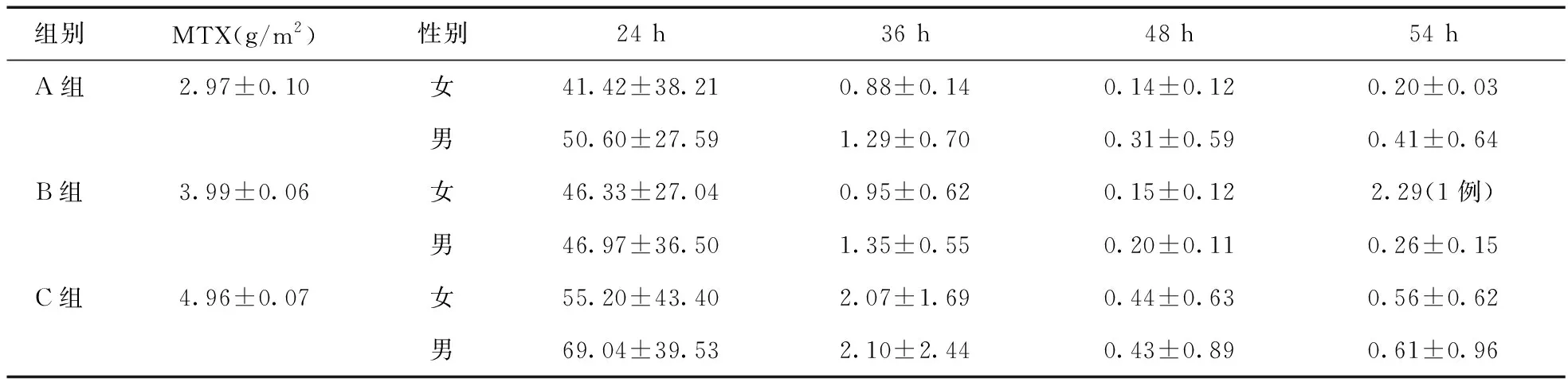
表6 不同性别之间血药浓度对比结果

表7 使用HD-MTX化疗后不良反应发生情况
4 结论
HD-MTX化疗是提高儿童ALL长期生存率的重要手段,根据血药浓度监测结果调整个体化给药方案,是提高疗效、保证用药安全的有效措施。在个体化治疗过程中,由于影响因素较多,需要综合考虑患者个体的固定效应因素及环境因素,及时进行用药干预,从而提高疗效,减少不良反应的发生。
