柯萨奇病毒B组IgM抗体检测抗原片的研制,优化及应用价值的研究
2018-10-31张晓刚金玉芬吴丽霞
常 静,张晓刚,金玉芬,吴丽霞,于 庭*
(1.吉林大学第二医院,吉林 长春130041;2.北京英诺特生物技术有限公司;3.沈阳医学院附属第二医院)
柯萨奇病毒B组(CoxB)是单股正链小RNA病毒,是呼吸道感染的主要病原体之一。根据血清型,该B组病毒可分为B1、B2、B3、B4、B5、B6六种类型,主要侵犯免疫力底下的围生儿,可引起脑膜炎,中枢神经系统感染等多种疾病,亦是引起病毒性心肌炎的主要病原体之一,占病毒性心肌炎诱因的20%-25%,病情严重者可导致死亡。CoxB传染源为病人及隐性感染者,可经口、呼吸道、肠道传播或胎儿宫内传染。多流行于夏、秋季节,一般呈散发或地区性暴发流行[1,2]。目前常规检测手段是病毒分离、血清抗体检测、核酸检测,而间接免疫荧光法被认为是除病毒分离法以外的金标准。有研究表明,在CoxB感染的早期,人体内产生的IgM抗体可持续存在数周。故此特异性抗体的出现可以作为CoxB的急性期或持续期感染诊断的重要指标之一[3]。抗原片的研制对应用间接免疫荧光法检测CoxB-IgM的特异性和灵敏性尤为重要,为了临床能够更加方便,高效的诊断CoxB感染,本文运用细胞培养技术,制备并优化CoxB抗原片,结合间接免疫荧光法对临床样本的CoxB-IgM抗体进行检测,并对其性能和应用价值进行评价。
1 材料与方法
1.1菌种
来源于北华大学生命科学研究中心提供的柯萨奇病毒B组分离株。
1.2细胞
北京协和医院提供的人源Hep-2细胞。
1.3血清
(1)沈阳医学院附属第二医院2016年9月-2017年7月收治的CoxB感染患者的血清。其中阳性血清43例,阴性血清555例。
(2)VIRION(U.S.),INC.(简称“VIRION”)的柯萨奇病毒IgG试剂盒(ELISA法),在间隔2周后检测的IgG抗体水平呈4倍升高的血清样本,确认为急性感染样本,共30例。
(3)应用北京贝尔生物工程有限公司(简称“北京贝尔”)的柯萨奇B组病毒IgM抗体检测试剂盒(酶联免疫法),按照试剂盒说明书,检测30例急性感染样本,选择应用于本试验的内控阳性血清1、2。阳性血清1:S/CO值为5.5,阳性血清2:S/CO值为1.2。再用该试剂盒检测健康人的血清,选择应用于本试验的内控阴性血清1、2。阴性血清1:S/CO值为0.08,阴性血清2:S/CO值为0.04。
(4)交叉反应血清:30份肺炎支原体(MP)阳性血清(CoxB阴性),30份肺炎衣原体(CP)阳性血清(CoxB阴性),均来自于沈阳医学院附属第二医院。
1.4仪器与试剂
Qiagen公司的病毒RNA提取试剂盒。北京贝尔的柯萨奇B组病毒IgM抗体检测试剂盒(酶联免疫法)。VIRION的柯萨奇病毒IgG试剂盒(ELISA法)。
1.5抗原片的制备
1.5.1毒株鉴定 取病毒培养的Hep-2细胞上清210 μl于1.5 ml无菌管中,按照Qiagen公司的病毒RNA提取试剂盒说明书提取基因组,并加入1 μl(40U)RNA酶抑制剂RNasin,混匀后于-70℃保存备用。作为PCR扩增反应的模板。
在NCBI上搜索该病毒序列,根据Sequence ID:gbAF160095.1序列选择保守区(301-480)设计两条引物:(F:ACAGAACCAGTTAAGGATG;R:TAAGGTAGTCGGGCCACACACC)进行PCR扩增。选用上游引物F,在全自动测序仪上进行单向测序,得到的结果与基因库比对,鉴定毒株。
1.5.2抗原片的制备 将经鉴定的毒株用含有2%胎牛血清的DMEM(细胞维持液)将病毒稀释到10-3。在生长良好的Hep-2单层细胞培养物内接种适量CoxB[4]。当细胞病变达一定程度时,用0.25%的胰酶消化细胞,制备成细胞悬液后,滴加1 ml在盖玻片上,37℃ CO2培养箱中培养后,用0.01M PBS浸洗一次,晾干,用无水乙醇-20℃过夜固定。风干后即为制备好的CoxB抗原片。
1.6抗原片制备条件的优化
1.6.1感染细胞病变程度的选择 CoxB接种到Hep-2细胞单层后,观察细胞病变的程度,分别选择细胞病变15%、25%、35%时,用0.25%的胰酶消化细胞,制成细胞悬液,分别滴到盖玻片上,每张盖玻片滴加1 ml,制成抗原片,并与吸附剂,稀释液及荧光素标记的二抗组成检测试剂,利用在不同细胞病变程度下研制的试剂分别对阳性血清1、2,阴性血清1、2进行检测。
1.6.2CoxB细胞含量的选择 当细胞病变达一定程度时,用0.25%的胰酶消化细胞制成细胞悬液,分别取浓度为105、106、107/ml的细胞悬液1 ml制备抗原片,利用抗原片制备成检测试剂,并分别对阳性血清1、2,阴性血清1、2进行检测[5,6]。
1.7间接免疫荧光法(IFA)检测
选择上述抗原片制备的最佳条件制备抗原片,与吸附剂,稀释液及荧光素标记的二抗组成检测试剂,对收集的样本进行检测。
将25 μl血清与等体积吸附剂混合后,1 000 rpm离心10 min。取吸附后血清样本40 μl加入到160 μl样本稀释液中,混匀,取15 μl血清进行检测。第二抗体使用异硫氰酸荧光素(FITC)标记的鼠抗人IgM抗体,样本在经过荧光染色后,置于荧光显微镜下观察。阳性结果显示CoxB细胞的细胞核、胞浆或胞膜出现绿色荧光,阴性结果显示CoxB的细胞呈红色。
1.8临床样本的检测
1.8.1对比试验 利用研制的试剂,与北京贝尔的柯萨奇B组病毒IgM抗体检测试剂盒(酶联免疫法)同时对收集的598例血清进行检测,操作严格按照试剂盒使用说明书执行。将两种方法检测的结果进行比对,用SPSS17.0软件对试验结果进行统计学分析。
1.8.2急性感染试验 利用研制的试剂对30例急性感染样本进行检测。
1.8.3交叉反应试验 利用研制的试剂对30份MP-IgM阳性血清,30份CP-IgM阳性血清进行检测。
2 结果
2.1毒株鉴定结果
图1是以上游引物F:ACAGAACCAGTTAAGGATG为测序引物,进行单向测序后,用NCBI-Blast进行比对的结果。因单向扩增自身的特点,扩增之初的序列不稳定,故选取稍后位置碱基序列进行比对,结果显示score为219 hits,identities值为118/118(100%),gaps为0/118(0%),表明该毒株为柯萨奇病毒B组。
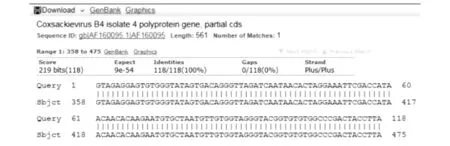
图1 单项扩增序列比对结果
2.2抗原片制备条件的优化结果
2.2.1细胞病变的选择结果 结果显示当细胞感染25%时消化细胞滴制备的检测试剂,内控血清的阳性和阴性结果的较好。见表1。
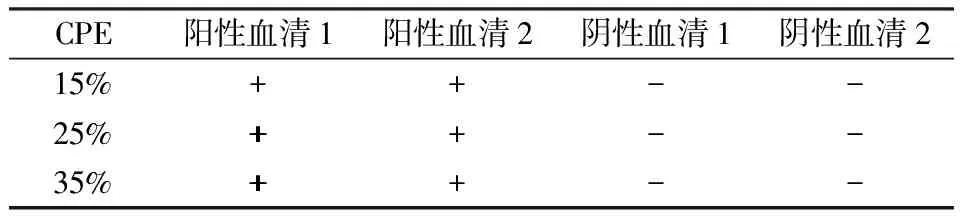
表1 CoxB感染细胞病变程度的选择
注:++:阳性;+:弱阳性;-:阴性。
2.2.2CoxB细胞含量的选择结果 见表2。试验中选择了3个细胞浓度105/ml、106/ml、107/ml,结果显示在一个盖玻片上滴加病变细胞1 ml时,病变细胞浓度为106/ml密度的检测结果较好(图2)。

表2 CoxB抗原片细胞含量的选择
注:++:阳性;+:弱阳性;-:阴性。
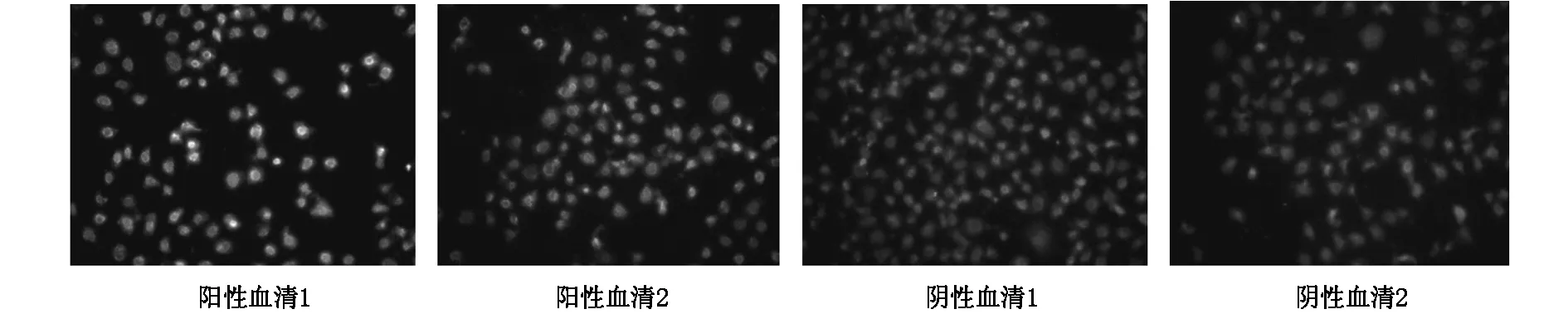
图2 CoxB细胞含量的选择结果
2.3临床样本检测结果
2.3.1对比试验结果 经对临床598例样本检测,结果显示两种方法共同检出阳性42例,阴性552例。有3例北京贝尔的试剂盒检测呈阴性,新研制的试剂检测呈阳性。1例北京贝尔的试剂盒检测呈阳性,新研制的试剂检测呈阴性。经统计学分析计算,两种方法检测的阳性符合率为97.67%,阴性符合率为99.46%,总体符合率99.33%,Kappa值为0.951。说明新研制的试剂与已上市试剂盒检测具有较高的一致性。见表3。
2.3.2急性感染试验结果 30例急性感染样本中,利用研制的试剂检测有28例呈IgM抗体阳性。说明新研制试剂盒具有较高的敏感性和特异性。见表4。

表3 598例临床样本的CoxB-IgM总体检测结果统计
注:计算方法:阳性符合率=A/(A+C)×100%;阴性符合率=D/(B+D)×100%;总符合率=(A+D)/(A+B+C+D)×100%。

表4 30例CoxB急性感染试验结果统计
2.3.3交叉反应试验结果 利用新研制的试剂分别对30例MP-IgM阳性血清, 30例CP-IgM阳性血清进行检测, 结果显示CoxB-IgM均呈阴性。说明新研制的试剂不受其他病原体干扰,具有较好的特异性。见表5。

表5 30例MP-IgM阳性血清,CP-IgM阳性血清交叉反应试验结果统计
3 讨论
柯萨奇病毒B组是呼吸道感染的常见病原体之一,病毒根据血清型可分为B1、B2、B3、B4、B5、B6,共6种类型。可引起不同疾病包括脑炎,肺炎病毒性心肌炎等。故临床早期快速诊断对CoxB感染的预防和治疗十分重要。
目前常规用于CoxB检测的手段包括病毒分离、血清检查、PCR检测等。病毒分离是最传统的诊断方法,被认为是病原学诊断的金标准,但其耗时长、操作繁琐、阳性率低,所以不适用于临床检测。PCR技术几年来被应用于CoxB感染的检测,其具有较高的特异性和准确性,但因其对设备和试剂的特殊需求使其医疗成本较高,不适合大范围推广使用[7]。
血清学常用方法是ELISA法和胶体金法,由于方法多选用基因工程抗原,其检测敏感性和特异性较差,而我们利用的是CoxB组病毒在细胞内分泌出的特异性抗原,有效的提高了检测的敏感性和特异性,是临床公认的除了分离培养以外的金标准。
抗原片的制备是应用间接免疫荧光法研制CoxB-IgM抗体检测试剂的关键步骤,若抗原片制备过程中出现细胞脱落,细胞病变程度不够等情况,都会影响抗体检测的特异性和灵敏性。本实验室研制CoxB抗原片时,经制备条件优化实验后,选细胞病变程度25%时制成细胞悬液,并取106/ml的细胞含量制作滴片为制备条件。经对临床598例样本检测,统计学分析计算,Kappa值高达0.951,说明新研制的试剂与已上市试剂检测具有较高的一致性;CoxB在30例MP阳性血清,CP阳性血清检测中均呈阴性,说明新研制的试剂具有较好的特异性;30例急性感染样本中28例被检测出CoxB-IgM呈阳性,说明该试剂对CoxB-IgM抗体检测具有较好的灵敏性和特异性。在上述试验中,对比试验中与上市试剂盒检测不相符的几例样本目前考虑为是因两种不同检测方法的区别而产生的差异,之后可经过第三方试剂进行验证。急性感染试验中,有2例未检出IgM阳性的原因可能是IgM抗体含量已经在机体内下降,转化,不易检出。亦或是该几位患者为柯萨奇B组病毒其他血清型感染。
上述结果证明本实验室研制的抗原片,可根据间接免疫荧光法的原理,与吸附剂,稀释液和FITC标记的鼠抗人IgM抗体组合成检测试剂,对CoxB感染患者的血清进行定性检测。其检出效率与上市试剂相当,且试剂的医疗成本低,操作方便,适合用于临床初级诊断,能够为CoxB感染的早期诊断和治疗提供可靠的依据。未来可考虑根据此方法制作其他呼吸道病原体抗原片,并进一步研究和优化,实现对呼吸道感染的早期诊断及筛查。
