3500例肿瘤患者中心静脉置管相关并发症及危险因素分析
2018-10-26吴永勇谢俊英杨林商卫娜薛庆月许丽娜
吴永勇,谢俊英,杨林,商卫娜,薛庆月,许丽娜
1国家癌症中心/国家肿瘤临床医学研究中心/中国医学科学院北京协和医学院肿瘤医院内科,北京100021
2北京市朝阳区桓兴肿瘤医院综合科,北京100122
中心静脉导管定义为置入静脉大血管(包括头臂静脉、贵要静脉、颈内静脉、锁骨下静脉、髂静脉、股静脉等)的导管,又称为中心血管通路装置(central vascular access device,CVAD)[1]。中心静脉导管临床可分为3类:经外周静脉置入的中心静脉导管(peripherally inserted central venous catheter,PICC)、经深静脉置入的中心静脉导管(central venous catheter,CVC)和植入式静脉输液港(implant-able venous access port,PORT)。中心静脉导管自20世纪80年代便开始在恶性肿瘤患者中使用,主要提供抽血、化疗药物输入、静脉营养和临床监测等,现已被临床广泛应用[2-3],其中CVC和PICC的应用最广泛。尽管CVAD给患者提供了便利,但在植入和长期使用过程中会不可避免地出现并发症,如感染、血栓和机械性并发症(如导管堵塞、脱落等)。这些并发症的类型和发生率与疾病过程、操作者的经验和操作设备有关[4]。本研究对于中国医学科学院肿瘤医院住院接受治疗的恶性肿瘤患者行CVC和PICC的并发症和相关危险因素进行分析,现报道如下。
1 对象与方法
1.1 研究对象
选取2012年8月至2014年9月于中国医学科学院肿瘤医院住院接受治疗(化疗、手术或支持治疗)的经细胞学或组织病理学确诊的成人恶性肿瘤患者3500例为研究对象,对所有恶性肿瘤患者进行中心静脉置管。研究期间对所有入组患者进行连续登记;患者及家属在置管前会获得清晰详尽的口头和书面通知,告知置入导管的风险、益处和操作程序;所有患者均自愿签署深静脉置管知情同意书;置管团队对患者及家属进行健康教育并建立随访手册,告知及指导带管生活注意事项,并在随访手册上详细填写相关记录,随访至深静脉置管被拔除。本研究是一项单中心、前瞻性队列研究,研究方案获得中国医学科学院肿瘤医院伦理委员会审查批准(批准文号:HCH20120530-008),并在ClinicalTrials.gov注册(编号:NCT01661218)。
1.2 置管方法
中心静脉置管严格按照美国静脉输液协会制定的《输液治疗实践标准》[3]操作,置管操作由具有专业资质的医师及护理人员在指定的置管室进行。PICC管选用法国美德公司生产的PICC包1套,管径18 G、导管总长度60 cm;CVC管采用ARROW中心静脉导管,管径16 G,长度20 cm。均连接可来福无针密闭型输液接头(型号:01CCLC2000)。置管部位:根据患者的病情、年龄、诊断、合并症、预期插入位点的近端血管条件及皮肤状况,并结合患者的偏好来选择置管部位[5]。对于慢性肾病患者,为了保护静脉,置管部位不推荐前臂、上臂和锁骨下静脉。乳腺手术侧腋窝淋巴结清扫后、放疗后、患肢淋巴水肿或脑血管意外侧应避免 PICC[6]。尽管收益与风险相当,PICC 置管时优先考虑肘正中、头静脉,CVC置管时优先考虑锁骨下静脉[7]。置管方法:用Seldinger技术或改良的Seldinger技术进行静脉置管,必要时应用超声技术提高穿刺成功率,减少穿刺相关并发症[8]。“S”形妥善固定导管,用3M透明贴固定,通过胸部正位X线检查(包含置管侧上肢和颈部)确认置管走向及导管末端位置。根据目前指南,置管后不需药物预防导管相关血栓[3]。维护方法:输液期间每天用脉冲式SAS封管法封管,治疗间歇期及院外期间保证每周由专业的护理人员更换敷料、消毒导管皮肤交界处、更换可来福接头。拔管条件:如出现不能解决的并发症或治疗停止或治疗被认为不必要时,拔除导管。如因怀疑导管相关性血流感染(catheter-related bloodstream infection,CRBSI),拔除后需进行导管细菌培养[9]。
1.3 观察指标
采集患者的人口统计学资料、恶性肿瘤相关资料(肿瘤类型、临床分期)、导管相关资料(包括置管日期、置管类型、置管部位、置管目的、置管次数、拔管日期、拔管原因、置管总天数、有无在外院维护)、症状性并发症相关资料(并发症类型、发生时间、处理措施等)。导管相关并发症发生率以每千导管日计算,计算公式:导管相关并发症发生率=并发症患者数量/中心静脉导管的留置总天数×1000。
1.4 统计学方法
原始数据标准化处理后的危险因素有10项[包括性别、年龄、体重指数(body mass index,BMI)、Charlson 共病指数(CCI)[10]评分、卡氏(KPS)[11]评分、置管部位、置管目的、有无在外院维护、肿瘤类型、肿瘤分期)。采用SPSS 19.0软件进行数据处理。计量资料以均数±标准差表示,计数资料以例数或率(%)表示,单因素分析中,两个及多个样本率的比较分别采用独立样本四格表的χ2检验及多个独立样本列联表的χ2检验;导管相关并发症危险因素分析采用二分类Logistic回归分析,纳入变量为单因素分析中有统计学意义的自变量或临床上认为与因变量关系密切的自变量,以向前逐步选择法作为自变量筛选方法。以P<0.05为差异有统计学意义。
2 结果
2.1 基本资料
3500例恶性肿瘤患者中,男性1561例,女性1939例;肿瘤类型:乳腺癌786例,肺癌553例,结直肠癌367例,宫颈癌359例,胃癌281例,食管癌217例,淋巴瘤166例,其他肿瘤771例(包括肝癌44例,胆管癌25例,胰腺癌47例,前列腺癌37例,子宫内膜癌134例,膀胱癌22例,肾癌46例,睾丸癌38例,卵巢癌78例,部位未明确恶性肿瘤300例);临床分期:I期218例,Ⅱ期567例,Ⅲ期764例,Ⅳ期1951例。
2.2 置管效果
截至随访截止日期2015年5月31日。全部患者累计置管时间195 327天,中位置管时间42天(1~403天),平均置管时间(55.8±0.83)天。其中,PICC置管1115例,包括头静脉48例,贵要静脉852例,肘正中静脉215例,累计置管时间65 598天,中位置管时间45天(2~384天),平均置管时间(58.93±1.50)天;CVC置管2385例,包括锁骨下静脉2339例,股静脉46例,累计置管时间129 729天,中位置管时间40天(1~403天),平均置管时间(54.39±0.90)天。
2.3 置管后导管相关并发症发生情况
随访期间259例患者出现导管相关并发症,导管相关并发症总发生率为7.4%(259/3500)(1.33/千导管日),其中渗漏的发生率最高,血肿、导管相关感染、导管堵塞等的发生率次之,导管破裂的发生率最低,未出现导管相关死亡事件。发生导管相关并发症的中位时间为第17天(1~183天)。发生PICC相关并发症者31例,发生率为2.78%(31/1115)(0.47/千导管日);发生CVC相关并发症者228例,发生率为9.56%(228/2385)(1.76/千导管日)。与PICC相比,CVC引起的静脉炎的发生率较低,但其余导管相关并发症的发生率均较高。(表1)

表1 3500例恶性肿瘤患者的导管相关并发症类型及发生率
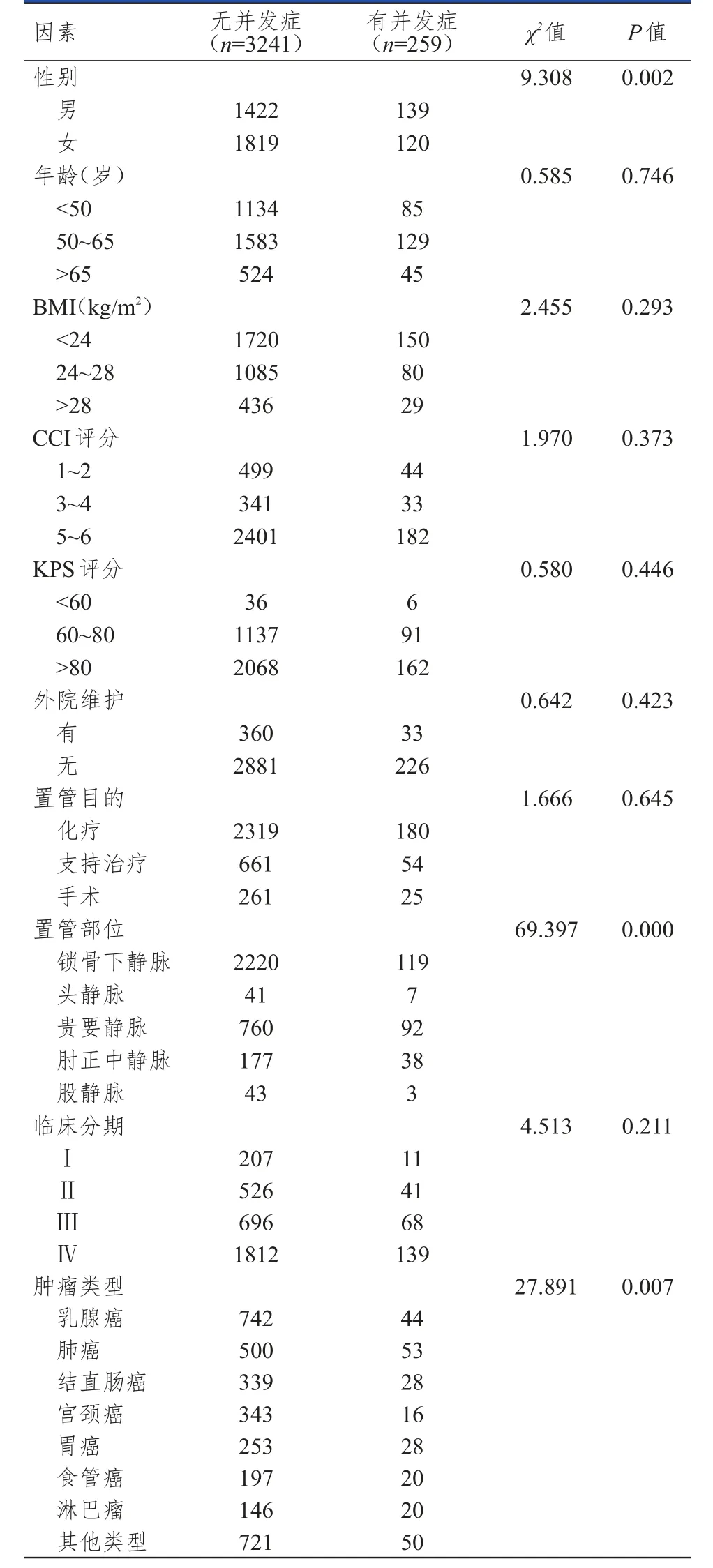
表2 3500例恶性肿瘤患者中心静脉置管后导管相关并发症影响因素的单因素分析
2.4 恶性肿瘤患者中心静脉置管后导管相关并发症影响因素的单因素分析
单因素分析结果显示:年龄、BMI、CCI评分、KPS评分、有无外院维护、置管目的、临床分期与恶性肿瘤患者中心静脉置管后发生导管相关并发症无关(P>0.05);性别、置管部位、肿瘤类型均与恶性肿瘤患者中心静脉置管后发生导管相关并发症有关(P<0.01)。(表2)
2.5 恶性肿瘤患者中心静脉置管后导管相关并发症影响因素的多因素分析
多因素Logistic回归分析显示:在调整了其他因素后,置管部位和肿瘤类型是恶性肿瘤患者中心静脉置管后发生导管相关并发症的独立危险因素(P<0.05)。其中,头静脉、贵要静脉、肘正中静脉置管相对锁骨下静脉,发生导管相关并发症的风险增加(OR=3.33,95%CI:1.44~7.68;OR=2.25,95%CI:1.65~3.04;OR=4.24,95%CI:2.81~6.41),但与股静脉置管位置无关(P>0.05)。宫颈癌患者置管后并发症风险较乳腺癌患者明显降低(OR=0.51,95%CI:0.28~0.95),淋巴瘤患者置管后并发症风险较乳腺癌患者增加(OR=1.93,95%CI:1.11~3.36),肺癌、结直肠癌、胃癌、食管癌及其他类型肿瘤患者导管相关并发症的风险与乳腺癌患者比较,差异均无统计学意义(P>0.05)。(表3)
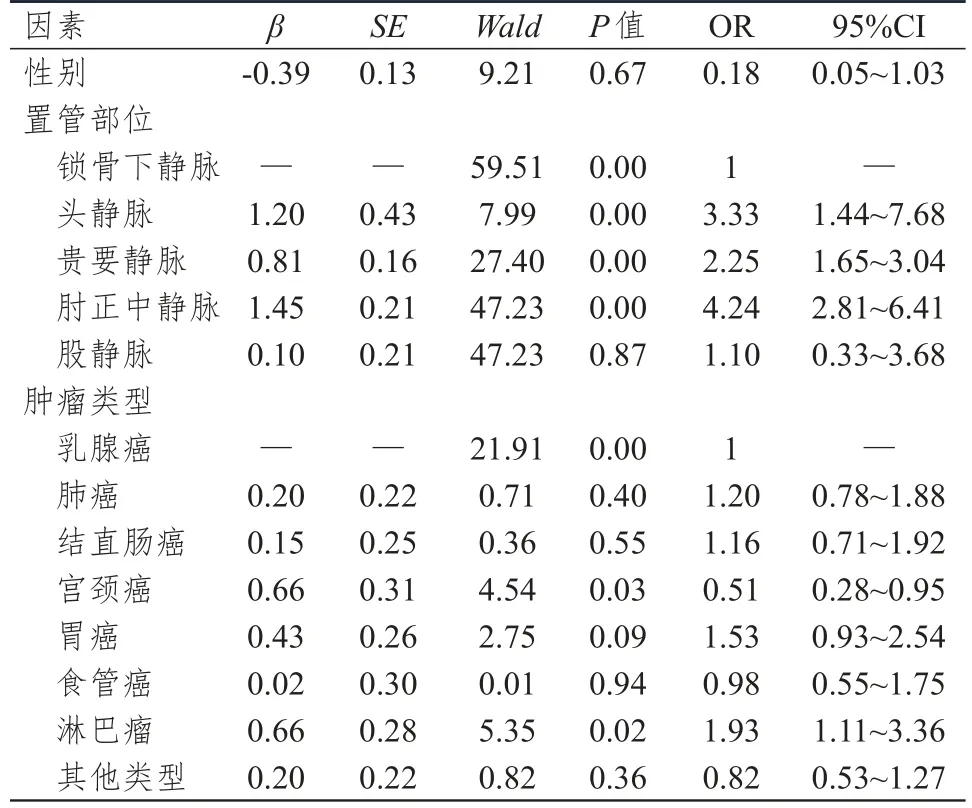
表3 3500例恶性肿瘤患者中心静脉置管后导管相关并发症影响因素的多因素Logistic回归分析
3 讨论
1953年,Seldinger[12]采用了经皮穿刺、通过导丝引导插入置管的方法成功地进行了动脉造影。自1975年Hoshal[8]首次采用Seldinger技术将硅胶管经外周静脉置入肘正中静脉以来,在导管材料、种类及置管方法上不断完善,中心静脉置管技术突飞猛进,目前在临床中的应用日趋广泛,主要适用于短期或长期持续或间断输液的解决方案,如输注抗肿瘤药物、发泡剂、刺激性药物、肠外营养、各种抗生素、任何酸碱性小于5或大于9、渗透压大于600 mosm/L的药物[13],同时可用于血液透析[14]、测量中心静脉压[15]。据统计,美国每年置管数达500万[16]。恶性肿瘤患者面临术中监测中心静脉压、术后营养支持、术后抗感染、化疗、静脉营养支持等,更需要深静脉置管[17-18]。但多数肿瘤患者免疫力低下、体质消瘦,中心静脉留置导管后可出现静脉炎、导管相关感染、导管血栓等并发症,导致住院时间延长、治疗费用增多、耽搁治疗计划,如处理不当,轻则影响治疗效果,重者甚至危及患者生命[19]。
本研究采用前瞻性调查的方法,通过建立“深静脉置管患者临床信息跟踪表”,对入组患者的置管过程及留置期间的30项指标进行跟踪调查,统计时将有临床意义并可量化的10项参数录入数据库,进行单因素及多因素Logistic回归分析,旨在明确影响中心静脉导管留置时间及并发症的相关危险因素,为降低并发症发生率、减少医疗成本、规范护理方案提供客观的循证依据和参考。
本研究3500患者的累计置管时间为195 327天,置管时间最长为403天,中位置管时间为42天,平均置管时间为(55.8±0.83)天。其中PICC置管1115例,置管时间最长为384天;CVC置管2385例,置管时间最长为403天。本研究发现,肿瘤患者选择CVC置管明显多于PICC,部位多选择锁骨下静脉,且锁骨下静脉及股静脉置管出现并发症的风险较头静脉、贵要静脉、肘正中静脉明显下降,原因可能与锁骨下静脉下后壁与胸膜仅相距5 mm有关,该静脉的管壁与颈固有筋膜、第1肋骨膜、前斜角肌及锁骨下筋膜鞘等结构相近,因而位置恒定、不易发生移位,且锁骨下静脉内径粗(1~2 cm)、血流快、较充盈,故易于穿刺且不易出现并发症。本研究还显示,PICC平均置管时间(58.93±1.50)天,CVC平均置管时间(54.39±0.90)天,两组比较,差异无统计学意义(P>0.05),提示两种置管方法的导管留置时间相似。
导管相关症状性并发症中,渗漏的发生率最高,为0.33/千导管日。渗漏指药物或溶液进入周围组织,引起大量结缔组织增生,致使血管壁增厚变硬、管腔增厚或阻塞,严重时造成组织坏死、瘢痕挛缩、关节僵直,甚至出现功能障碍。本研究全部患者的累计置管时间长达195 327天,最长保留置管403天,更易发生渗漏。一旦发生输液渗漏,应立即更换输液部位,并根据引起输液渗漏的原因、药物性质,对血管组织损伤的程度等选择不同的方法,防止其渗漏后引起组织坏死[20]。血肿的发生率仅次于渗漏,为0.20/千导管日。血肿多由于穿刺方法不当、反复多次穿刺、误穿动脉或穿刺针头不锐利等引起。形成血肿后,进行有效压迫15~30 min,尽可能将皮下瘀血挤出,血肿一般可自行吸收。血肿较大时,局部可热敷或理疗(可采用多频理疗仪),促进血肿吸收。如血肿过大,必要时行血肿清除术[21]。导管相关感染是最常见的医源性感染,具有较高的发病率和病死率。肿瘤晚期患者伴有较严重的基础疾病、营养缺乏、输液时间长、放化疗等治疗后免疫力下降、导管不容易固定、不易换药导致继发感染。本研究中导管相关感染35例(发生率为0.18/千导管日),总体感染发生率较国内外文献报道相对较低[22-23],可能原因是严格的无菌穿刺操作流程、规范化置管维护、定期随访减少了病菌沿导管扩散的概率。导管阻塞被定义为导管部分或完全的阻塞,导致无法抽到回血、冲洗导管困难、输液速度减慢或停止。本研究中导管堵塞39例(发生率为0.18/千导管日),全组发生率占比较高,可能与肿瘤患者凝血机制易出现异常、卧床较多、输高渗透压或高营养液较多有关。静脉炎可由机械性、化学性或感染引起,早期以机械性静脉炎为主,常出现在置管后1周内,主要由穿刺鞘和导管对静脉内膜、静脉瓣的机械性摩擦刺激以及外界刺激引发变态反应引起,化学性静脉炎的发生与刺激性液体有关,感染性静脉炎是由细菌引起的静脉损伤。静脉炎按美国《输液治疗护理实践标准》[24]分5级。本研究中静脉炎发生25例(发生率为0.13/千导管日),发生率低于国内外研究[25]。气胸多见于锁骨下静脉穿刺置管,往往为穿刺损伤胸膜顶和肺所致。如肺压缩不超过30%,无呼吸困难,可随访观察;如肺压缩大于30%,伴呼吸困难,可行胸腔抽气减压或胸腔闭式引流排气[26]。本研究中气胸发生16例(发生率为0.08/千导管日),肺压缩皆小于30%,自行好转,未出现相关死亡事件。导管相关静脉血栓是比较常见且易致死的并发症。本研究中导管相关静脉血栓15例(发生率为0.08/千导管日),远低于既往研究[27-28]。为降低导管相关静脉血栓的发生率,导管的置入应由经过培训的专业团队进行,置管后应尽早拔管、缩短导管留置时间,出院后需定期规范维护、严格置管护理。对于血栓患者,通过及时地治疗处理能有效控制血栓的进展,促进血栓消失、血管再通,保证患者安全。导管异位最易发生于颈内静脉,也可见于奇静脉、胸廓内静脉、胸外侧静脉、右心房或右心室。置管后胸片提示导管末端不在上腔静脉,进入其他血管或心房即为导管异位。有资料显示,导管异位多数于插管当天发生[29]。导管异位与静脉选择、置管长度的外测量方法、患者局部血管解剖变异、穿刺时患者体位、操作者送管技巧等因素有关。导管脱出多因导管固定不正确如无缝线固定、无菌贴膜覆盖不严、输液管长度不够或受压;护理人员在换药时手法不熟练,顺导管拔出方向撕下贴膜,易将导管带出;或因患者年龄大、体质弱,行动不便,穿脱衣服时导致导管脱出。导管穿刺口近端破裂可致穿刺口渗液,而破裂位置在血管深处则需胸片或拔出导管时证实[30]。
目前,国内外尚无肿瘤类型与深静脉置管并发症相关性方面的研究。本研究初次发现,在排除其他混杂因素后,宫颈癌患者中心静脉置管后发生导管相关并发症的风险较乳腺癌患者显著减少,而淋巴瘤患者中心静脉置管后发生导管相关并发症的风险较乳腺癌患者显著增加,肺癌、结直肠癌、胃癌、食管癌及其他类型肿瘤患者中心静脉置管后发生导管相关并发症的风险与乳腺癌患者无差异。
本研究表明,肿瘤患者行深静脉置管安全、有效,为临床工作带来快捷和方便。虽然少数患者有严重的并发症,但是临床应该了解深静脉置管所带来的相关问题和并发症,如果能做到置管前全面评估患者的病情,置管过程中合理选择静脉,掌握穿刺及送管技巧,置管后规范化维护,将会大大减少置管并发症的发生,有效延长导管的使用寿命,为患者造福。
据了解,本研究是国内第一个大样本、前瞻性观察肿瘤患者深静脉置管后并发症的研究。与以往的研究相比,本研究有很多独到的特点:①数据是通过临床收集而不是单纯问卷调查;②前瞻性的研究,最大限度地减少了医护及治疗因素的影响;③入组患者均为恶性肿瘤患者;④大样本的研究仅用2年就完成;⑤无患者失访。但本研究也有局限性:①本研究中观察指标如外周血常规、凝血功能、感染状态、免疫情况、化疗方案、营养支持时间、置管次数等多种因素因不易量化未纳入统计,结论可能会存在一定的局限性和分析上的偏倚;②本研究仅针对恶性肿瘤患者,并不一定适用于其他单纯长期静脉营养、外伤、烧伤等良性疾病。
志谢:感谢中国医学科学院肿瘤医院置管室团队,感谢医院及各科室对本研究的支持。
