安徽省药品批发企业飞行检查与认证检查情况分析
2018-09-22张慧席永宽魏骅
张慧 席永宽 魏骅
根据国家食品药品监管总局《关于整治药品流通领域违法经营行为的公告》[1]要求,安徽省自2016年7月组织开展全省药品批发企业飞行检查。飞行检查一般采取事先不告知、不透露检查信息、不听取一般性汇报、无需安排接待及直奔现场的方式,对被检查药品企业执行药品监管法律法规的实际情况,进行突击检查或者暗访调查[2]。而认证检查是指药品批发企业变更注册地址、仓库地址、药品经营范围(增加)、药品仓库(增减)时主动申请的检查。现将2016年安徽省批发企业飞行检查与认证检查发现缺陷情况汇总分析如下。
1 资料与方法
1.1 一般资料
自2016年7月以来,共完成59家药品批发企业的飞行检查,除1家停业企业外,其中20家存在严重缺陷,36家存在主要缺陷,仅有2家只存在一般缺陷。2016年安徽省共完成64家药品批发企业的认证检查,其中19家存在主要缺陷,45家存在一般缺陷。飞行检查与认证检查企业各地市分布情况见图1。
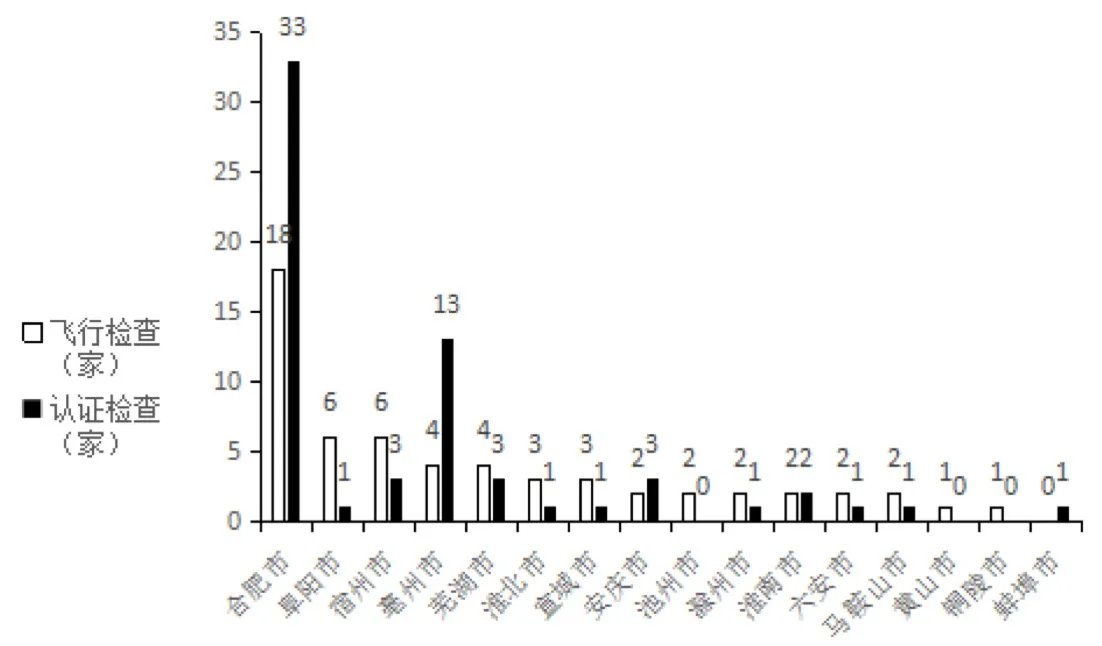
图1 2016年飞行检查及认证检查企业各地市分布对比图
1.2 方法
通过对比飞行检查和认证检查的缺陷类型及构成情况等[3],总结安徽省药品批发企业存在的问题,并分析两种不同形式的检查之间的差异。
2 结果
2.1 缺陷条款构成对比情况
58份飞行检查报告中共发现401条缺陷项,包括严重缺陷25项,主要缺陷267项,一般缺陷109项;64份认证检查报告中共发现726条缺陷项,包括主要缺陷52项,一般缺陷674项,见表1。

表1 飞行检查与认证检查缺陷类型对比
依据药品经营质量管理规范(Good Supply Practice,GSP)及附录内容对缺陷进行分类,结果如表2。从缺陷项目分类情况可以看出,飞行检查缺陷排名前3位的依次是储存与养护、 设施与设备、收货与验收, 占总缺陷项目的45.88%;认证检查缺陷排名前3位的依次是储存与养护、设施与设备、组织机构和质量管理职责,占总缺陷项目的41.6%。
2.2 严重缺陷分布情况
经对飞行检查的58份检查报告中出现的25项严重缺陷进行汇总,缺陷内容见表3。
由表3可看出,企业在日常经营中票账货款不一致、违反诚实守信是最易发生的严重缺陷,占严重缺陷总数的88%。
2.3 高频主要缺陷对比情况
经分别对飞行检查的267项主要缺陷和认证检查的52项主要缺陷进行汇总,排名前10位的主要缺陷内容如表4。
由表4可以看出,*05901、*08604在飞行检查和认证检查中同为高频缺陷,企业在日常经营中,对于库房温湿度超标和计算机授权问题上应引起重视。
2.4 高频一般缺陷对比情况
经分别对飞行检查的109项一般缺陷和认证检查的674项一般缺陷进行汇总,排名前10位的主要缺陷内容见表5。
由 表 5可 以 看 出,03401、04702、05201、06501在飞行检查和认证检查中同为高频缺陷,企业在日常经营中,设施设备管理不善、质量体系文件修订不及时和质保协议签署不规范属于共性问题,应加以注意。
3 讨论
3.1 飞行检查与认证检查的不同
一方面,由于飞行检查的突击性,面对的是企业经营最真实最直接的状态,而企业申请的GSP认证检查,通常都是经过精心准备的,因此常常会看到企业完全不同的“两面”。如58家飞行检查企业中15家出现票账货款不符、7家出现违反诚实守信经营,而64份认证检查报告中无一家发现严重缺陷;另一方面,飞行检查检查员多是经验丰富、能力出众、敢于担当的骨干检查员,而认证检查的检查员水平参差不齐,甚至有时会有刚刚加入检查员队伍中的新人。因此,人员素质的高低不同,其检查能力和水平也不同,检查的效果必会有所差异[4]。此外, 对于检查员来说,飞行检查时通常敢于“下重手”,而认证检查中却往往顾虑颇多,容易“手下留情”。
3.2 飞行检查与认证检查存在的问题
3.2.1 共性问题
通过对比飞行检查和认证检查的高频缺陷项发现企业存在着以下共性问题:一是储藏与养护方面,仓库内药品未按规定进行储存、库房温湿度超标未进行有效调控;二是在设施与设备方面,“五防”设施不全、设施设备档案不完整;三是未及时修订质量体系文件[5];四是计算机岗位授权与职责不符。
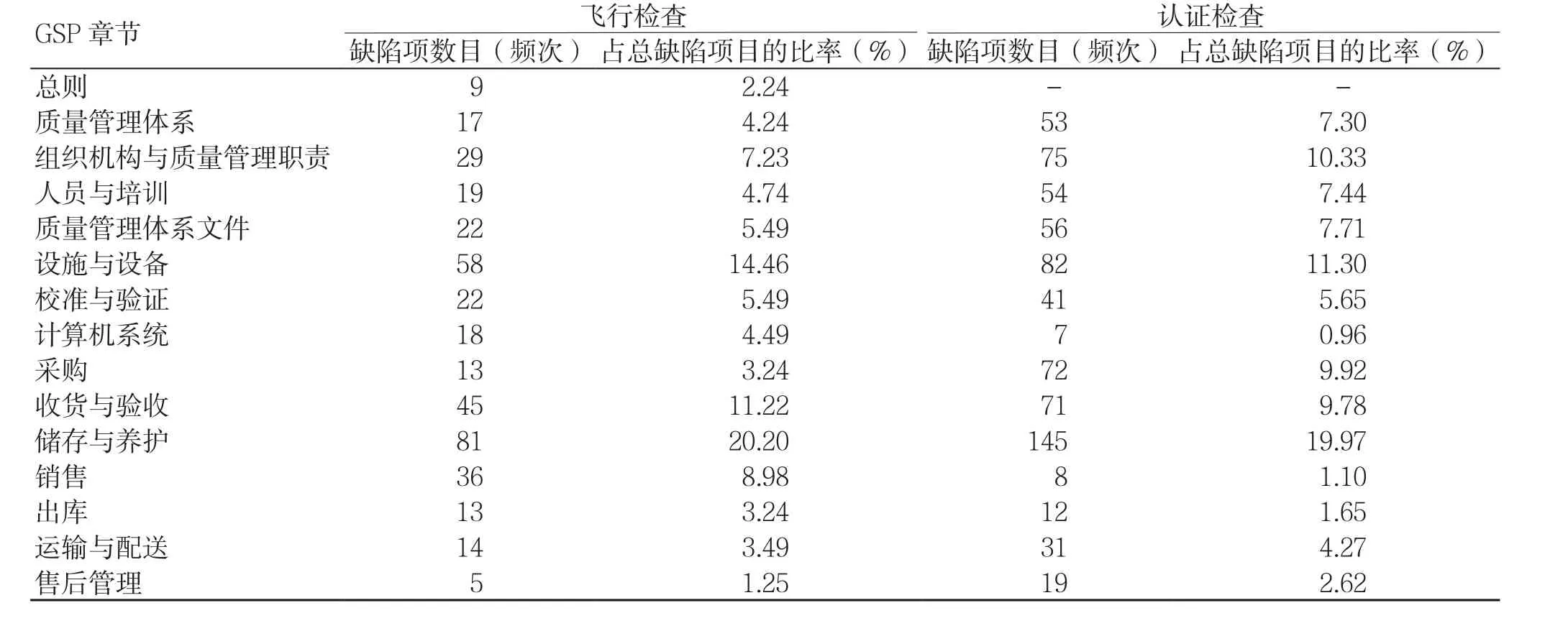
表2 飞行检查与认证检查缺陷项目构成情况对比

表3 2016年飞行检查严重缺陷项目统计
3.2.2 飞行检查问题
飞行检查中发现企业存在的严重缺陷主要集中在票、帐、货、款不一致和违反诚信守信原则。除上述共性问题外,主要缺陷集中在药品的储存不规范、冷藏药品收货未按规定和购销方资质审核不严等。
3.2.3 认证检查问题
全年认证检查均未出现严重缺陷。除上述共性问题外,主要缺陷集中在质量管理体系管理不规范和未严格按照规定进行验证。一般缺陷主要集中在培训效果不佳、质量风险点排查不全和未按规定进行养护。
3.3 原因分析
3.3.1 企业存在“回潮现象”
通过飞行检查和认证检查的情况来看,部分企业仍存在“重认证检查、轻日常”的错误思想,认为通过GSP认证检查后便万事大吉,放松管理。因此,现场检查的高频缺陷中出现库房内“五防”设施不全、在库药品堆放混乱、未及时修订质量体系文件等。这些问题并不是企业不知道应该做或者应该怎样做,而完全是由于思想意识的松懈所造成的。
3.3.2 企业存在侥幸心理
从飞行检查和认证检查的高频缺陷情况来看,部分企业存在着侥幸心理,即企业明知存在着问题,但由于这部分问题的整改通常需要花费一定的人力、物力和财力,企业侥幸地认为检查员不一定能抽查到,就不去整改。因此,会出现在飞行检查和认证检查中都属于高频缺陷的*08604库房温湿度超标未进行有效调控,会出现认证检查中反复出现未按规定开展验证相关的高频条款*05303、*05304等情况。
3.3.3 少数企业规范经营意识淡漠[6]
不可否认,当前仍有少数企业置国家总局和省局的要求于不顾,“重利益、轻管理”,规范经营意识差,这无形中成为影响企业质量管理的核心因素[7],因此,飞行检查中票、帐、货、款不一致和违反诚信守信原则的现象仍有发生,这类企业应引起监管部门高度重视。
3.4 对策与建议
一是应加强药品经营企业法人质量意识的宣传,牢固树立严格按照GSP从事经营活动的理念;二是需加强检查员能力建设,端正检查态度,不断提高检查员整体的业务素质和实战能力;三是要加大“事中、事后”监管力度,通过日常监管“严把关”和跟踪飞行检查“常态化”,督促企业的经营管理行为日趋规范。
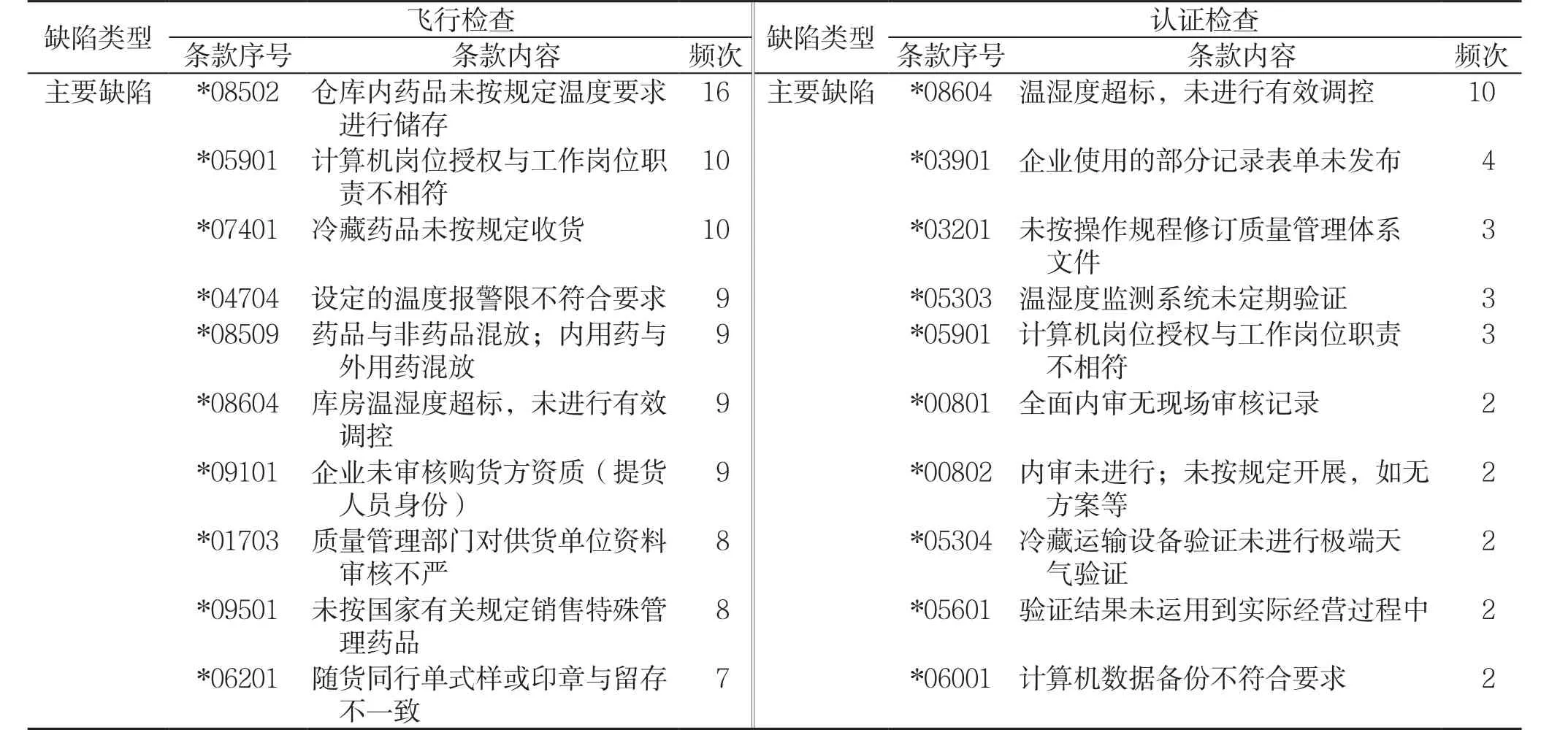
表4 排名前10位的高频主要缺陷对比情况
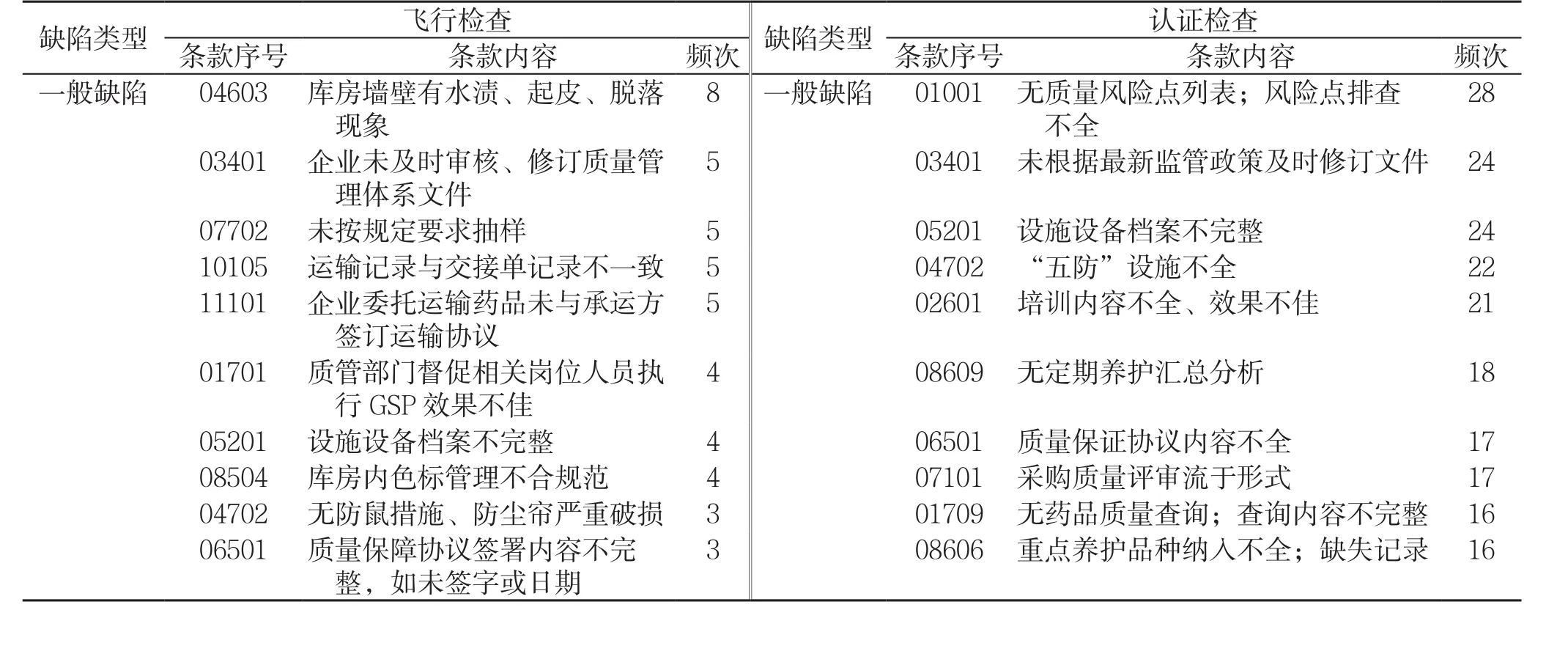
表5 排名前10位的高频一般缺陷对比情况
4 小结
药品经营质量管理规范是企业从事经营和质量管理的基本准则,从2016年的检查情况来看,认证检查促使企业主动进行自查自纠,飞行检查对企业违法违规行为起到了一定的震慑作用[8],但整体而言,目前企业执行GSP意识仍需加强,监管力度仍需加大,检查员能力和水平有待于进一步提高,只有共同努力才能使药品流通领域更加规范有序,从而有效保障人民安全用药。
