硝矾洗剂的制备工艺研究
2018-09-20皮凤娟张庆莲张世波
皮凤娟,黄 娟,张庆莲,张世波,赵 领,刘 浩
(1.泸州市中医医院,泸州 646000;2.西南医科大学药学院,泸州 646000)
硝矾洗剂是泸州市中医医院(以下简称我院)的临床协定方,是我院肛肠科根据临床经验用药组方而成。该制剂处方由大黄、黄柏和苍术等组成,具有清热解毒、消肿止痛和收湿止痒的作用[1-2],临床主治痔疮,已使用多年,疗效显著、不良反应小、安全可靠。但其中药成分复杂、药效各异,对本复方的整体提取不能只参照文献中单味药材的提取方法。为进一步开发本复方制剂,本文立足于中药复方的整体性,在保留传统中药汤剂特点的基础上,以君药大黄中的总蒽醌含量和干浸膏得率为指标,通过正交实验法对其制备工艺进行研究,为进一步开发院内制剂奠定基础。
1 仪器与试药
1.1仪器 戴安高效液相色谱仪,包括四元泵、紫外检测器和自动进样器等(美国戴安公司);FA2004型电子天平(上海安亭电子仪器厂)。
1.2试药 大黄酸对照品,大黄素对照品,大黄素甲醚对照品,芦荟大黄素对照品以及大黄酚对照品(批号分别为110757-200206,110756-200110,110758-201013,110795-201007和110796-201017),均购自中国食品药品检定研究院;大黄(批号150623)、黄柏(批号15060102)、苍术(批号150325)和白矾(批号150612)药材,均由泸州天植中药饮片有限公司提供;冰片(批号130309),由四川青神康华制药有限公司提供;芒硝(批号D1312034),由四川新荷花中药饮片股份有限公司提供;甲醇为色谱纯;水为重蒸水;其他试剂均为分析纯。
2 方法与结果
2.1单因素实验
2.1.1提取时间考察 按照处方量的1/3准确称取药材(大黄,黄柏和苍术)各4份,固定提取次数为3次,加水倍量为10倍,依次提取0.25,0.5,1和2 h,综合评分分别为60.10,80.36,95.54和99.09。结果表明,提取2 h的分数最高,但提取1 h的总蒽醌含量比2 h高,且提取2 h耗能多,故选择提取时间为1 h[3-5]。
2.1.2提取次数考察 按照处方量的1/3准确称取药材(大黄,黄柏和苍术)各3份,固定提取时间为1 h,加水倍量为10倍,依次提取1,2和3次,综合评分分别为54.63,84.86和99.96。从综合评分来看,提取3次的分数最高且与其他2个相差较大,故选择提取次数为3次。
2.1.3加水倍数考察 按照处方量的1/3准确称取药材(大黄,黄柏和苍术)各3份,固定提取时间为1 h,提取次数为3次,依次加水10,15和20倍量,综合评分分别为87.89,92.87和100.00。结果表明,当加水倍量为20倍时,综合评分最高,故选择加水倍量为20倍。
2.2正交实验 根据单因素实验结果,考虑到剂型为洗剂,故最终选定加水倍量、提取时间和提取次数作为正交实验的考察因素,将总蒽醌含量和干浸膏得率作为考察指标进行综合评定,应用L9(34)正交实验表进行实验,重复3次实验以减少偶然误差[6]。因素与水平见表1。按照L9(34)正交实验设计要求,按照处方量的1/3准确称取药材(大黄,黄柏和苍术),共27份,编为1~27号(每次实验重复3次)。每份55 g(其中大黄25 g,黄柏15 g,苍术15 g),分别置于圆底烧瓶中,加入纯化水,按照表1因素进行提取,提取液过滤,冷却,定容即得。
2.3干浸膏得率的测定 精密移取2.2项下制备的提取液50~100 mL,置于已干燥至恒质量的蒸发皿中,水浴蒸干,再置于105 ℃烘箱中干燥至恒质量,计算干浸膏得率,结果见表2。
表1水提工艺因素与水平
Tab.1 Factors and levels of the water extracting technology

水平因素A,加水量/倍B,提取次数/次C,提取时间/minD,空白118140-220260-322380-
注:-表示空白列,用于计算偶然误差。
2.4提取液中5种蒽醌的含量测定
2.4.1色谱条件 色谱柱:Kromasil C18(250 mm×4.6 mm,5 μm);流动相:1 mL·L-1磷酸∶甲醇(15∶85);流速:1.0 mL·min-1;检测波长:254 nm;柱温:30 ℃[7-9]。色谱图见图1。
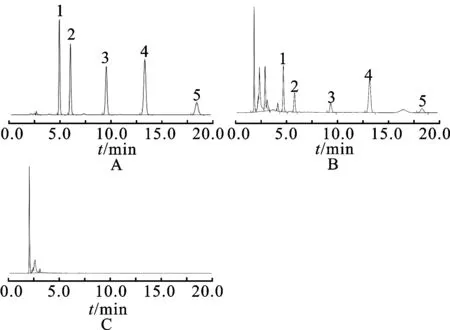
图1HPLC图
A.对照品;B.供试品;C.阴性对照;1.芦荟大黄素;2.大黄酸;3.大黄素;4.大黄酚;5.大黄素甲醚。
Fig.1 HPLC chromatograms
A.reference sample;B.sample;C.negative sample;1.aloe-emodin;2.rhein;3.emodin;4.chrysophanol;5.physcion.
表2水提工艺正交实验结果
Tab.2 Orthogonal test results of water extraction process

实验号 ABCD干浸膏收率/%总蒽醌含量/mg·g-1综合评分1111116.594.1247.872122228.358.9894.623133331.968.6897.214212320.005.1058.615223130.778.9697.556231228.397.9387.817313220.555.8564.258321325.607.5681.869332131.039.1098.81K1239.70170.73217.54244.23K2243.97274.03252.04246.67K3244.92283.83259.01237.69R1.7437.7013.822.99
注:权重系数由大黄总蒽醌含量×60%、干浸膏收率×40%来进行综合评分。
2.4.2混合对照品溶液的制备 精密称取对照品适量,加甲醇制成1 mL中含芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚质量浓度分别为20.72,24.52,21.56,22.80和11.12 μg·mL-1的溶液[10-11]。
2.4.3供试品溶液的制备 精密称取2.3项下制备的干浸膏0.25 g,置于具塞锥形瓶中,加入甲醇25 mL,精密称定,回流60 min后再次称定,若质量减少,则用甲醇补足减失的质量,摇匀,过滤,取续滤液5 mL,置于具塞锥形瓶中,水浴蒸干,加入220 mL·L-1盐酸溶液10 mL,超声处理2 min,再加入10 mL氯仿,摇匀后回流60 min,取出,放冷。分取氯仿层,酸液用氯仿提取3次,每次10 mL,合并氯仿液,挥干,残渣加甲醇溶解并定容至10 mL量瓶中,过滤,即得[12-14]。
2.4.4阴性样品溶液的制备 精密称取缺大黄的阴性干浸膏0.25 g,按照2.4.3项下方法进行制备。
2.4.5线性范围考察 在2.4.1项色谱条件下,分别取混合对照品溶液1,2,4,8,10,16和20 μL,测定不同进样量下总蒽醌的峰面积,以进样量为横坐标(x)、峰面积为纵坐标(y)进行线性回归,得回归方程:y=7.249 5x+0.429 9(r=0.999 9),结果表明,当总蒽醌进样量在72~1 440 μg范围时,进样量与峰面积呈良好的线性关系。
2.4.6精密度实验 精密吸取2.4.3项下制备的供试品溶液适量,连续进样6次,进行测定,结果表明,芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚峰面积的RSD值分别为0.29%,0.30%,0.32%,0.33%和0.35%,表明该方法精密度良好。
2.4.7稳定性实验 精密量取2.4.2项下制备的混合对照品溶液,在0,2,4,6和8 h分别进样10 μL,记录芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的峰面积,计算其RSD值分别为0.46%,0.57%,0.70%,1.06%和1.49%,结果表明,芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚均在8 h内稳定。
2.4.8重复性实验 取同一批样品6份,按照2.4.3项下方法制备供试品溶液,按照2.4.1项下色谱条件平行操作测定,记录峰面积,计算含量。结果芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的RSD值均小于2.0%,表明该方法重复性良好。
2.4.9加样回收率实验 精密量取同一批样品5 mL,6份,分别置于具塞锥形瓶中,每份均精密加入质量浓度分别为0.100 2,0.105 0,0.104 6,0.115 8和0.052 8 mg·mL-1的芦荟大黄素、大黄酸、大黄素、大黄酚以及大黄素甲醚对照品储备液9,8,3.5,7 和6 mL。按照2.4.3项下方法制备供试品溶液,依照2.4.1项下色谱条件平行操作测定,记录峰面积,计算回收率,结果RSD值均小于3%,表明加样回收率好。见表3。
表3回收率实验结果
Tab.3 The results of recovery tests

编号供试品含量/mg加入对照品量/mg测得量/mg回收率/%平均值/%RSD/%13.493 53.235 36.619 296.6199.451.6823.493 53.235 36.749 0100.6233.493 53.235 36.681 498.5343.493 53.235 36.742 1100.4153.493 53.235 36.764 2101.0963.493 53.235 36.710 499.43
2.4.10样品的含量测定 分别精密吸取2.4.2项下制备的混合对照品溶液和2.4.3项下制备的供试品溶液各10 μL,进样测定,计算样品中大黄总蒽醌的含量,结果见表4。
2.5方差分析结果 由表4可知,各因素对实验结果的重要性为B>C>A。方差分析结果表明,加水量A对总蒽醌含量和干浸膏得率影响不显著(P>0.05),提取次数B和提取时间C对总蒽醌含量和干浸膏得率影响均具有显著性(P<0.01)。故最佳工艺条件为A1B3C2,即加18倍量水,煎煮3次,每次1 h。
表4正交实验方差分析
Tab.4 Mean standard deviation analysis of the orthogonal experiment

因素离差平方和SS自由度f均方MSF显著性A5.1722.583.23B2 617.6421 308.821 638.30**C328.652164.32205.69**D (误差e)14.38180.80
注:F0.01(2.18)=5.85;F0.05(2,18)=3.49,**P<0.01表示差异具有统计学意义。
2.6验证实验 由于正交实验中9号实验综合评分最高且含量最高,故做1次验证实验[15-17]。考虑到大生产浓缩液耗能较多,且加水量无显著性影响,再做4个验证实验,每个实验平行3次:加水量15倍,提取3次,每次1 h和加水量10倍,提取3次,每次1 h。从验证结果来看,加水量22倍(9号实验)含量较高,18倍,15倍和10倍的含量差别不大,但3次提取22倍量水比10倍量水多,浓缩时耗能较大,且多出的含量有限,从大生产节约能耗考虑,最终选择的最佳工艺条件为:加水量10倍,提取3次,每次1 h。
3 讨论
大黄为本制剂的君药,故大黄总蒽醌为本洗剂的主要药理活性成分[17-19],结合相关研究资料,蒽醌既能溶于沸水也可溶于有机试剂,但考虑到本制剂为洗剂,故采用水煎煮提取,这样既保留了传统中药物质作用基础,同时也避免了有机试剂的污染。
本实验将单因素实验法与正交实验法相结合,通过单因素实验确定正交实验的方案,对影响制剂质量的主要因素包括加水量、煎煮时间和煎煮次数等进行了系统考察,以干浸膏得率和大黄总蒽醌含量的综合评分作为考察指标,优选最佳提取工艺。从正交实验结果可知,煎煮时间和煎煮次数是主要影响因素,加水量影响不显著。在验证实验中,结合工业化大生产,从降低生产成本、提高生产效率方面考虑,最终将提取工艺确定为:加水量为10倍量,煎煮时间为1 h,煎煮次数为3次。
