超高效液相色谱法测定替考拉宁血药浓度
2018-09-10王艳红任秋霞赵庆国解放军302医院药学部北京100039
王艳红,任秋霞,赵庆国(解放军302医院药学部,北京 100039)
替考拉宁(teicoplanin,TEC)是一种新型糖肽类抗生素,由5个结构相似的化合物TA2-1、TA2-2、TA2-3、TA2-4、TA2-5组成,结构复杂、组分较多含10或11个碳的脂肪链,其中TA2-2为主要成分,占各组分相对含量的40%以上[1]。测定替考拉宁谷浓度可为其在临床的合理应用提供方法学依据,其血药谷浓度可反映给药间隔期间药物暴露量是否高于细菌的MIC与持续时间,当AUC/MIC≥345 时,可达到最佳治疗效果[2]。研究表明[3],一般感染的患者替考拉宁的谷浓度应> 10 mg·L-1,重度感染时应保持在15 mg·L-1以上;血流感染、重症肺炎及感染性心内膜炎等替考拉宁血药谷浓度应维持在20 mg·L-1或更高。但由于替考拉宁成分复杂、半衰期较长,患者在常规剂量使用过程中低于目标治疗谷浓度的发生率较高。同时,替考拉宁在我国临床实际应用中普遍存在忽视起始负荷剂量或起始负荷剂量及维持剂量偏低的现象。因此,在临床使用过程中对替考拉宁血药浓度进行监测是非常必要的。
文献报道的有关替考拉宁血药浓度测定的方法主要是HPLC分析法,包括HPLC-UV检测法[4-5]、LCMS/MS检测法[6]和药典中刊载的梯度洗脱的反相HPLC检测法。本研究建立的UPLC紫外检测法采用了超高压系统和小粒径填料色谱柱,具有分离时间短、分离效率高、更加灵敏和节省试剂等优点,经方法学验证,适用于临床替考拉宁血药浓度检测。
1 仪器与试药
Agilent 1290型超高压液相色谱系统,包括G4212A型DAD检测器、G4220A型二元输液泵、G4226A型自动进样器、G1316C型柱温箱和化学工作站(美国Agilent公司);QB-600型高速振荡混合器(海门市其林贝尔仪器制造有限公司);TGL-16C型高速离心机(上海安亭科学仪器厂)。
替考拉宁标准品(纯度:1 mg相当于894 U,中国食品药品检定研究院,批号:130374-201002),甲醇、乙腈、三氯甲烷均为色谱纯,三氟乙酸为分析纯,水为纯化水。
2 方法与结果
2.1 色谱条件
色谱柱:Zorbax SB-C18柱(2.1 mm×100 mm,1.8 μm);保护住Zorbax SB-C18柱(2.1 mm×5 mm,1.8 μm);流动相:乙腈-水(含0.1% TFA)(24.2 : 75.8,v/ v);流速:0.4 mL·min-1;检测波长:220 nm;柱温:30 ℃;进样量:5.0 μL。
2.2 溶液的制备
对照品溶液:取替考拉宁标准品约50.02 mg,精密称定,用30%甲醇溶解并定容至10 mL容量瓶中,得5.02 mg·mL-1替考拉宁标准贮备液。精密量取替考拉宁标准贮备液适量,用纯化水稀释成100、400、800 μg·mL-1的标准工作液,置4 ℃冰箱保存备用。
2.3 血浆样品预处理
取血浆样品200 μL于1.5 mL的Ep管中,首先加入10 μL 10%高氯酸涡旋震荡10 s,然后加入乙腈400 μL,涡旋振荡5 min,11000 r·min-1离心5 min,取上清液400 μL至另一Ep管中,加入萃取剂三氯甲烷400 μL涡旋振荡5 min,11000 r·min-1离心5 min,取上清液100 μL至另一Ep管中,离心后取上清液5.0 μL进样分析。
2.4 方法的专属性
分别取空白血浆、空白血浆+替考拉宁标准品及患者血浆溶液200 μL,按“2.3”项下血浆样品处理方法和“2.1”项下色谱条件进行测定,结果表明血浆中内源性杂质不干扰血浆中替考拉宁的分析。同时,我们还考察了5例临床患者血浆(未用替考拉宁)+替考拉宁标准品的检测情况,结果表明未用替考拉宁的临床患者血浆内杂质及药物均不干扰替考拉宁的分析。替考拉宁各组分保留时间分别为3.2 min、4.4 min、5.2 min、8.9 min和9.9 min,理论塔板数按替考拉宁计算大于9500。如图1所示本法具有较高的专属性。

图1 高效液相色谱图A – 空白血浆,B – 空白血浆+替考拉宁标准品(30 μg·mL-1),C – 患者血浆,D – 临床患者血浆(未用替考拉宁)+替考拉宁标准品(30 μg·mL-1);1 – TA2-1,2 – TA2-2,3 – TA2-3,4 – TA2-4,5 – TA2-5Fig 1 The UPLC chromatogramsA – blank plasma; B – blank plasma + teicoplanin standard (30 μg·mL-1); C – patient plasma, D – clinical patient plasma (not used teicoplanin) + teicoplanin standard (30 μg·mL-1); 1 – TA2-1, 2 – TA2-2,3 – TA2-3, 4 – TA2-4, 5 – TA2-5
2.5 标准曲线的建立
分别取不同浓度的替考拉宁标准工作液20 μL,加入健康人空白血浆200 μL,混匀,制成相当于替考拉宁浓度为2.0、5.0、10.0、20.0、40.0、60.0、80.0 μg·mL-1的血浆样品各3份,按“2.3”项下方法处理,进样分析。以替考拉宁各组分面积(A)和对替考拉宁血浆浓度(C)作线性回归,得标准曲线方程:A= 68.85C+ 54.44(R2= 0.9998,n= 3)。结果表明,替考拉宁血药浓度在2.0 ~ 80.0 μg·mL-1线性关系良好,检测限为0.65 μg·mL-1。
2.6 回收率实验
按照标准曲线制备方法配制5.0、30.0、70.0 μg·mL-1低、中、高3个浓度的替考拉宁血浆样品各5份,按“2.3”项下方法处理后进样分析,测得替考拉宁峰面积之和与用纯化水配制的相应浓度替考拉宁标准品所得的峰面积之和进行比较,计算提取回收率;根据当日标准曲线求得实测浓度,与理论浓度进行比较得出方法回收率,结果见表1。

表1 血浆中替考拉宁的回收率和精密度. n = 5Tab 1 Recovery and precision of teicoplanin in plasma. n = 5
2.7 精密度实验
取配制的5.0、30.0、70.0 μg·mL-1低、中、高3个浓度的替考拉宁血浆样品,按“2.3”项下方法处理后进样分析,每个浓度平行5份,重复测定三批(共计45份),计算批内和批间RSD,结果如表1所示。
2.8 稳定性实验
依据标准曲线制备方法配制5.0、30.0、70.0 μg·mL-1低、中、高3个浓度的替考拉宁血浆样品,每个浓度平行27份,取3个浓度各3份按“2.3”项下方法立即处理,进样分析;剩余样品每个浓度各3份在室温放置4 h、4 ℃冰箱冷藏24 h、进样器放置24 h、– 80 ℃冰箱冷冻30 d、60 d、90 d、反复冻融2次、3次后,按“2.3”项下方法处理,UPLC进样分析,分别以当日的标准曲线计算血浆中药物浓度。结果表明,血浆中替考拉宁在常温放置4 h、4 ℃冰箱冷藏24 h、进样器放置24 h、反复冻融3次、– 80 ℃冰箱冷冻60 d条件下均保持稳定,详见表2。
2.9 临床应用
14例患者均采用静脉给药,采血时间是在给予负荷剂量3 ~ 4次,维持剂量2 ~ 3次后,下一次给药前抽取静脉血,为患者谷浓度血样(肝素抗凝)。样本3500 r·min-1离心5 min,取血浆200 μL,按“2.3”项下方法处理,根据当日标准曲线定量,测得替考拉宁血药浓度,详见表3。
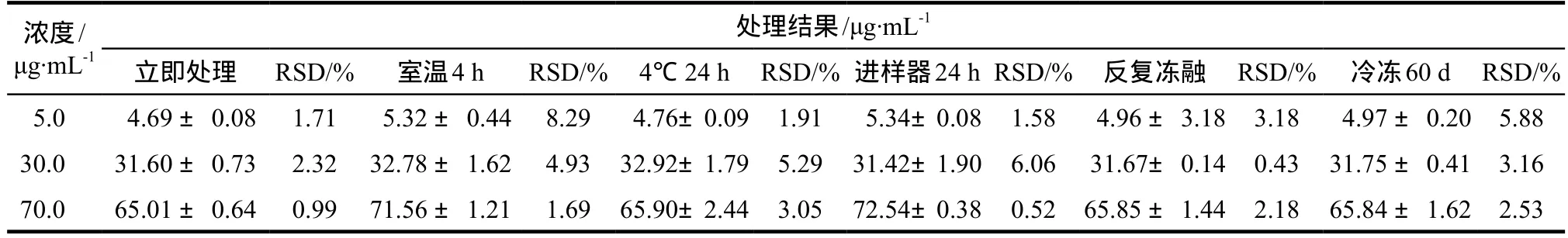
表2 稳定性实验结果. n = 5Tab 2 The results of stability test. n = 5

表3 受试者血药浓度测定结果Tab 3 Measurement results of plasma drug concentration in patients
3 讨论
3.1 流动相体系的选择
本实验首先对乙腈-磷酸缓冲盐体系进行了考察,结果发现,以磷酸盐缓冲体系作为流动相,色谱柱柱压较高,色谱柱易堵塞,样品分析后需对仪器进行长时间的清洗,工作繁琐。于是我们对流动相进行优化,考察了酸性的乙腈-水(含TFA)体系不同配比对替考拉宁5个主要成分的容量因子和分离度的影响。结果发现增加乙腈比例可缩短保留时间,适当增加三氟乙酸的含量可提高替考拉宁各组分的峰面积,消除拖尾。当乙腈-水(含0.1% TFA)(24.2 : 75.8)时,替考拉宁各组分容量因子适宜,峰形对称,保留时间在10 min内。
3.2 内标的选择
目前,文献报道的替考拉宁测定方法多为内标法。按照文献报道的条件,我们分别以哌拉西林钠和青霉素钠为内标进行了考察,但最终发现无论以磷酸盐作为流动相还是以三氟乙酸为流动相内标均不稳定,进样器放置2 h、4 h,哌拉西林钠峰面积分别降解为原来的87.8%和79.5%。同时,青霉素和哌拉西林均为临床常用药,以此为内标易出现内标受干扰现象。鉴于此,我们选择用外标法对替考拉宁进行检测。
3.3 样品处理方法的选择
单纯采用乙腈沉淀蛋白法对样品进行处理, 内源性物质干扰较大,峰形不对称,易对小粒径填料色谱柱造成阻塞,难以满足血药浓度监测的要求。结合三氯甲烷提取对样品进行处理,可将大量杂质萃取到有机相中,使样品纯化,组份浓集,但仍存在部分内源性物质干扰现象。为进一步消除内源性物质干扰,我们利用10%高氯酸加乙腈双重沉淀蛋白,然后再结合三氯甲烷萃取的方法有效避免了内源性物质干扰现象。
3.4 患者测定结果
本实验测定的14例患者谷浓度差异显著,14例患者中有4例(序号3、4、8、9)患者谷浓度低于说明书中建议的有效浓度。替考拉宁耐受性良好,但谷浓度过低易诱发细菌耐药,导致感染控制不佳,进而延长患者的治疗时间。Wang等[7]研究表明,替考拉宁是时间依赖性抗菌药物,其抗菌疗效和谷浓度密切相关。因此,我们应密切关注患者替考拉宁的血药浓度,通过监测其谷浓度及时调整用药方案以实现患者的个体化给药,保证替考拉宁的临床疗效,减少耐药的发生率。
综上,本实验建立的替考拉宁血药浓度的测定方法灵敏、准确,操作简便,回收率较高,可用于临床替考拉宁血药浓度的测定,同时对替考拉宁给药方案的调整,临床实施个体化治疗,确保用药安全、有效有一定的指导作用。
