液相色谱-串联质谱法测定鸡蛋中7种氟喹诺酮类药物的残留量
2018-08-23王桂琴
张 晶,王桂琴
(宁夏大学农学院,宁夏银川 750021)
氟喹诺酮类药物属于第3代喹诺酮类抗菌药,它是将氟原子引入喹诺酮萘啶环的6位处,哌嗪环连在7位上,因此又被统称为氟喹诺酮类[1]。氟喹诺酮类药物是一种人工合成的抗菌药物,通过对DNA回旋酶进行抑制,从而导致染色体的不可逆损害[2]。由于质粒传导耐药性并不会对氟喹诺酮类药物产生影响,因此它与许多抗菌药物之间没有交叉耐药性;同时因其有抗菌谱广、抗菌力强、组织穿透力强、不良反应少等特点,而在人类及动物感染性疾病的预防和治疗中被广泛地应用[3-5]。特别是在兽医临床方面,恩诺沙星、环丙沙星、氧氟沙星和诺氟沙星已经成为水产养殖专用的抗菌药物。由于在动物体内氟喹诺酮类药物的残留消除缓慢,过量的药物残留被人体摄入后,会损害人体健康[6]。因此,对此类药物的残留检测,各国都制定了相关的检测法规。氟喹诺酮类药物在临床上常被用作抗菌类药物,少量使用时,对动物的生长具有一定的促进作用,但如果过量使用会造成药物在动物性食品中残留,不仅会发生过敏反应,可能还会伴随其他不良反应[7]。同时使用该药物过量时,可能还会导致中枢神经系统、消化系统和肝肾等器官的病变,因此氟喹诺酮类药物必须严格控制用量,以确保家禽及其产品安全[8-9]。
建立一种快速、灵敏、准确的方法,检测动物性食品中氟喹诺酮类药物的残留量,以此对食品中氟喹诺酮类药物的含量进行监控,具有重要的现实意义。目前,国内外对氟喹诺酮类药物常用检测技术的研究报道较多[10-13],其中已有较多的文献对液相色谱-串联质谱法进行了报道[14-18],其在食品质量安全检测中的作用也越来越重要。本试验采用高效液相色谱-串联质谱法,同时检测鸡蛋中7种氟喹诺酮类药物的残留量。
1 材料与方法
1.1 材料
1.1.1 试剂 环丙沙星,购自中国食品药品研究所;洛美沙星、恩诺沙星、氧氟沙星、甲磺酸培氟沙星、诺氟沙星和恶喹酸,购自中国兽医药品监察所。柠檬酸(分析纯)、磷酸氢二钠(分析纯)、甲醇、乙腈、甲醇-乙腈溶液(体积比为40∶60)、甲酸(99%)、氢氧化钠(分析纯)、乙二胺四乙酸二钠(分析纯),科密欧试剂公司产品。
1.1.2 仪器 高效液相色谱-串联质谱仪(Waters ACQUITY UPLC/TQ-S micro),美国Waters公司产品;高速冷冻离心机CR22G,日本日立公司产品;旋涡混匀器MS3,IKA公司产品;电子天平AX-205、电子天平PL202-L、酸度计GB/T11165,梅特勒-托利多仪器有限公司产品;振荡器WSZ-100-A,上海安亭公司产品;组织匀浆机,JKA公司产品;氮吹仪N-EVAP112,美国Organomation Associates JnC公司产品。
1.2 方法
1.2.1 溶液配制 0.2 mol/L磷酸氢二钠溶液:称取磷酸氢二钠71.63 g,用水溶解后,用容量瓶定容至1 000mL;0.1 mol/L柠檬酸溶液:称取柠檬酸21.01 g,用水溶解后,用容量瓶定容至1 000 mL;Mcllvaine缓冲溶液:把1 000 mL 0.1 mol/L的柠檬酸溶液和625 mL 0.2 mol/L的磷酸氢二钠溶液混合,用盐酸或氢氧化钠调节pH为4.0±0.05;0.1 mol/L EDTA-Mcllvaine缓冲溶液:称取60.5 g乙二胺四乙酸二钠,然后将其加入1 625 mL的Mcllvaine缓冲溶液中,振荡摇匀,使其充分溶解;50 mL/L甲醇水溶液;2 mL/L甲酸水溶液。
1.2.2 储备液的配制 分别将各标准品精确称取0.010 0 g,放置于10.0 mL棕色容量瓶中,用甲醇使其溶解,并定容至刻度。标准储备液的浓度为1 mg/mL,置-20℃冰箱中保存,3个月内使用。
1.2.3 标准工作液的配制 将1.2.2配制的各标准储备液稀释,配成混合标准溶液。各组分的浓度为10 μg/mL。将此标准工作液置于4℃保存,3个月内使用。
1.2.4 样品前处理
1.2.4.1 提取 将均质试样准确称取5.00 g,置于50 mL离心管中,然后加入Mcllvaine EDTA- Na2缓冲溶液液10 mL,涡旋混匀1 min,振荡10 min,于-4℃、10 000 r/min离心5 min后,将上清液提取转移至另一50 mL的离心管中,在上清液中加10 mL的水饱和正己烷,涡旋混匀,振荡10 min后,于-4℃、10 000 r/min离心5 min,将下层备用液用吸管转移至另一50 mL的离心管中,然后再加入10 mL水饱和正己烷,涡旋混匀,振荡10 min,于-4℃、10 000 r/min离心5 min,弃去上层正己烷,下层备用液过柱。
1.2.4.2 净化 用6 mL甲醇洗涤HLB固相萃取柱(200 mg,6 mL),并用6 mL的水进行活化。然后将1.2.4.1提取的备用液过柱,过柱的速度最好为2 mL/min~3 mL/min,将滤液弃去,用2 mL 50 mL/L的甲醇水溶液进行淋洗,同样将淋洗液弃去,并把小柱抽干,再用6 mL的甲醇进行洗脱,并收集洗脱液,将洗脱液用氮气吹干后,最后用1 mL 2 mL/L甲酸水溶液进行溶解,10 000 r/min涡旋混合1 min,将溶液过膜后,用于上机测定。
1.2.5 色谱和质谱条件 色谱柱为Waters ACQUITY UPLCTMREH C18柱(100 mm×2.1 mm,粒径1.7 μm);柱温为30℃;样品室温度为室温;流速为0.3 mL/min;进样体积为10μL;流动相A为乙腈,B为1 mL/L甲酸水溶液;梯度淋洗,梯度洗脱程序见表1。
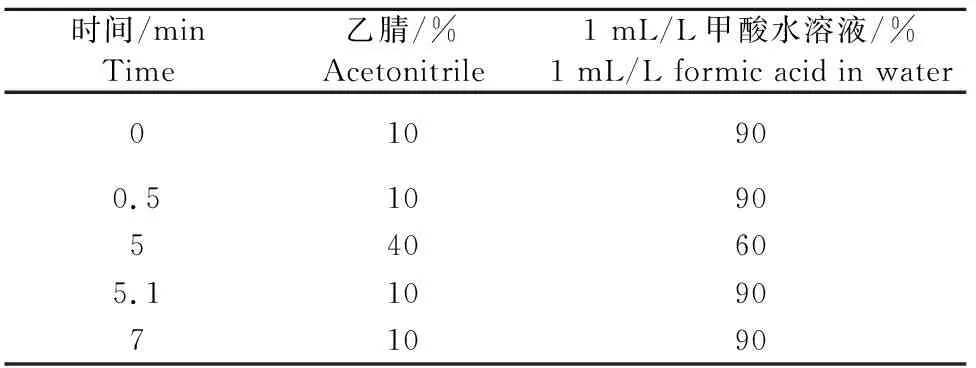
表1 梯度洗脱程序
质谱离子源:电喷雾离子源(ESI);扫描方式为正离子;毛细血管电压为1.04 kV;源温为150℃;脱溶剂温度为450℃;锥孔气流速为50 L/Hr;脱溶剂气流速为798 L/Hr;7种氟喹诺酮类药物定性、定量离子参数见表2;图1为7种氟喹诺酮类药物的定量离子流图。

表2 7种氟喹诺酮类药物的质谱条件及相关参数
2 结果
2.1 校正曲线和线性范围
称取5.00 g阴性鸡蛋样品,按上述方法处理样品,得到空白基质液,分别加入5种氟喹诺酮类药物混合标准溶液,配制成2.5、5、10、25、50、75、100 μg/L的基质标准溶液。以所得7种氟喹诺酮类药物的离子峰面积平均值为纵坐标、标准溶液的浓度为横坐标,绘制标准曲线。表3为标准曲线回归方程和相关系数。由表3可见,5种氟喹诺酮类药物的浓度在2.5 μg/L~100 μg/L时线性良好,线性相关系数R2均大于0.995 9。
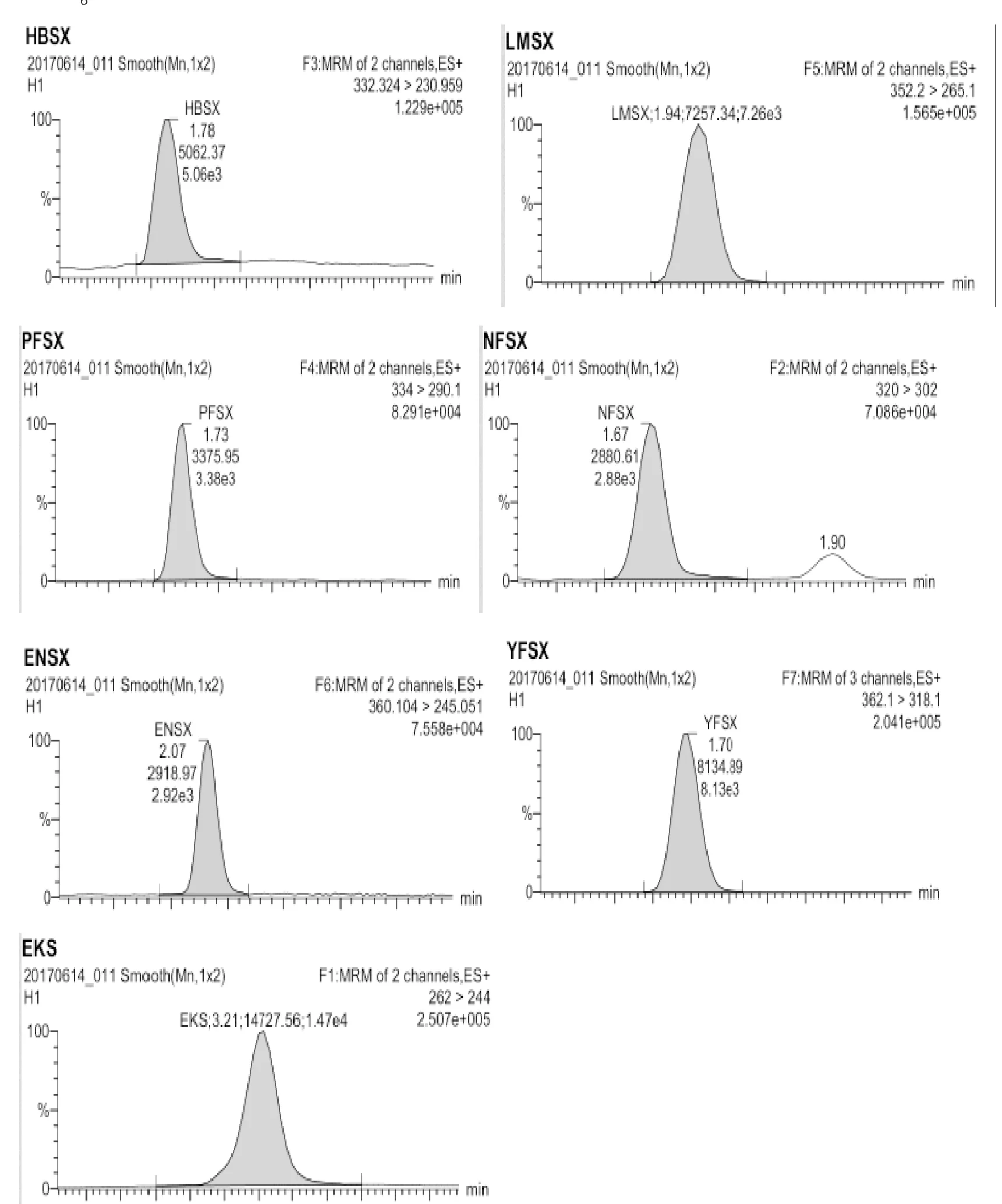
图1 7种氟喹诺酮类药物定量离子流图
2.2 检出限和定量限
样品的检出限(LOD) 是以基质标准曲线上的最低点( 2.5 μg /kg) ,取信噪比S/N=3和样品处理过程的稀释倍数计算得出;样品的定量限(LOQ) 是以基质标准曲线上的最低点(2.5 μg/kg) ,取信噪比S/N=10和样品处理过程的稀释倍数计算得出。环丙沙星和恶喹酸的检测限分别为1.2 μg/kg和0.05 μg/kg,定量限为24 μg/kg和1 μg/kg,其他5种氟喹诺酮类药物的检测限为0.5 μg/kg,定量限10 μg/kg。
2.3 准确度和精密度
将阴性鸡蛋样品称取5.00 g,进行3个水平的回收率试验,浓度分别为100、200、500 μg/kg。将每个水平重复5次,每个浓度做3批,计算相对标准偏差。按照建立的方法处理样品,测定结果见表4。7种氟喹诺酮类药物的平均回收率为36.9%~81.2%。通过测出的各组分的峰面积,计算其相对标准偏差(RSD,sr) ,对该方法的精密度进行衡量,7种氟喹诺酮类药物的批内精密度为2.2%~12.6%,批间精密度为1.8%~15.7%,说明该方法满足检测要求。
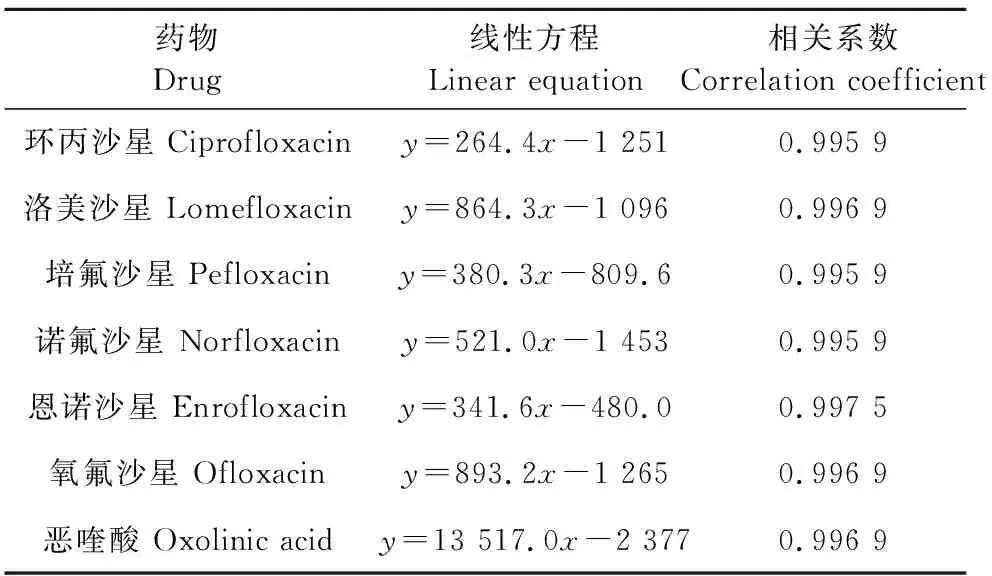
表3 7种氟喹诺酮类药物的线性方程和相关系数
3 讨论
3.1 色谱条件的优化
氟喹诺酮类药物属于酸碱两性化合物,化学结构中有羧基和哌嗪基,流动相中的酸度会对化合物的峰型和响应值产生一定的影响。本试验在流动相中加入甲酸来控制流动相的pH并提高灵敏度,试验中用1 mL/L甲酸水和乙腈进行梯度洗脱。
3.2 提取条件的优化
试验参照国家标准GB/T21312—2007《动物源性食品中14种喹诺酮药物残留检测方法 液相色谱-质谱/质谱法》中加入40 mL EDTA-Mcllvaine提取液,超声提取10 min,10 000 r/min离心10 min。由于鸡蛋中含有大量的蛋白质、脂肪、脂蛋白和色素,以上操作并不能很好的去除脂肪等杂质,因此在固相萃取时提取的上清液很容易阻塞萃取柱,导致试验无法进行。经过试验,在提取的上清液中加入水饱和正己烷去脂后,有利于固相萃取的进行,从而提高净化效率,缩短分析时间。经过多次试验,
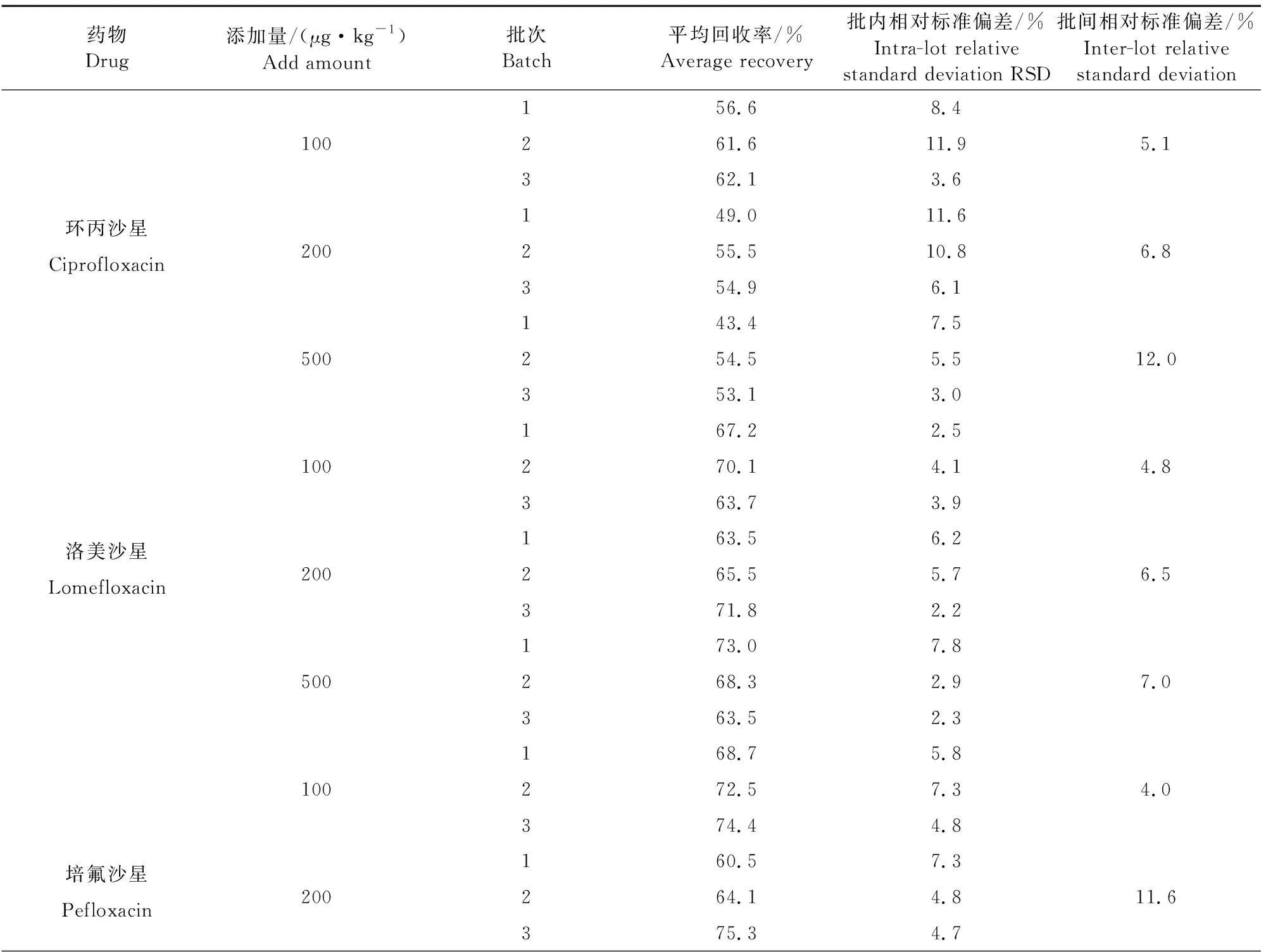
表4 空白添加回收率
续表4

药物 Drug添加量/(μg·kg-1) Add amount批次Batch平均回收率/%Average recovery批内相对标准偏差/%Intra-lot relative standard deviation RSD批间相对标准偏差/%Inter-lot relative standard deviation培氟沙星168.36.8Pefloxacin500267.44.04.1363.23.4156.85.4100258.99.64.5362.112.6诺氟沙星145.78.4Norfloxacin200252.77.67.3351.09.2136.97.3500249.24.215.7349.13.0171.96.0100273.59.01.8374.57.9恩诺沙星162.18.6Enrofloxacin200264.75.914.9381.24.2172.012.2500266.24.27.7361.73.8175.45.05100279.32.92.5377.14.2氧氟沙星166.17.4Ofloxacin200271.95.57.0376.05.1170.36.0500268.84.42.7366.64.0157.33.8100254.110.67.1349.76.9恶喹酸147.48.5Oxolinic acid200245.12.83.4344.510.9140.94.6500248.610.010.7340.33.1
每次加入10 mL的水饱和正己烷,在进行了2次去脂后,达到了很好的去脂效果。试验还比较了不同体积的提取液对回收率的影响,分别加入5 mL、8 mL和10EDTA-Mcllvaine缓冲溶液后进行重复提取1次,结果图2所示,除恶喹酸外其他药物加入10 mL提取液的回收率比较高。同时对加入10 mL提取液提取1次和提取2次进行试验,结果如图3所示,加入10 mL提取液提取1次的回收率较高。因此,确定本试验的提取方法为加入10 mL EDTA-Mcllvaine缓冲溶液提取1次。
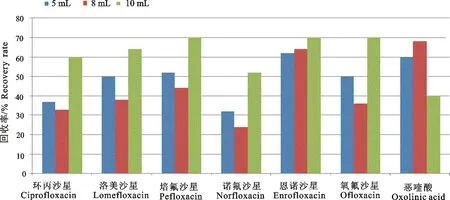
图2 提取液体积对7种氟喹诺酮类药物回收率的影响
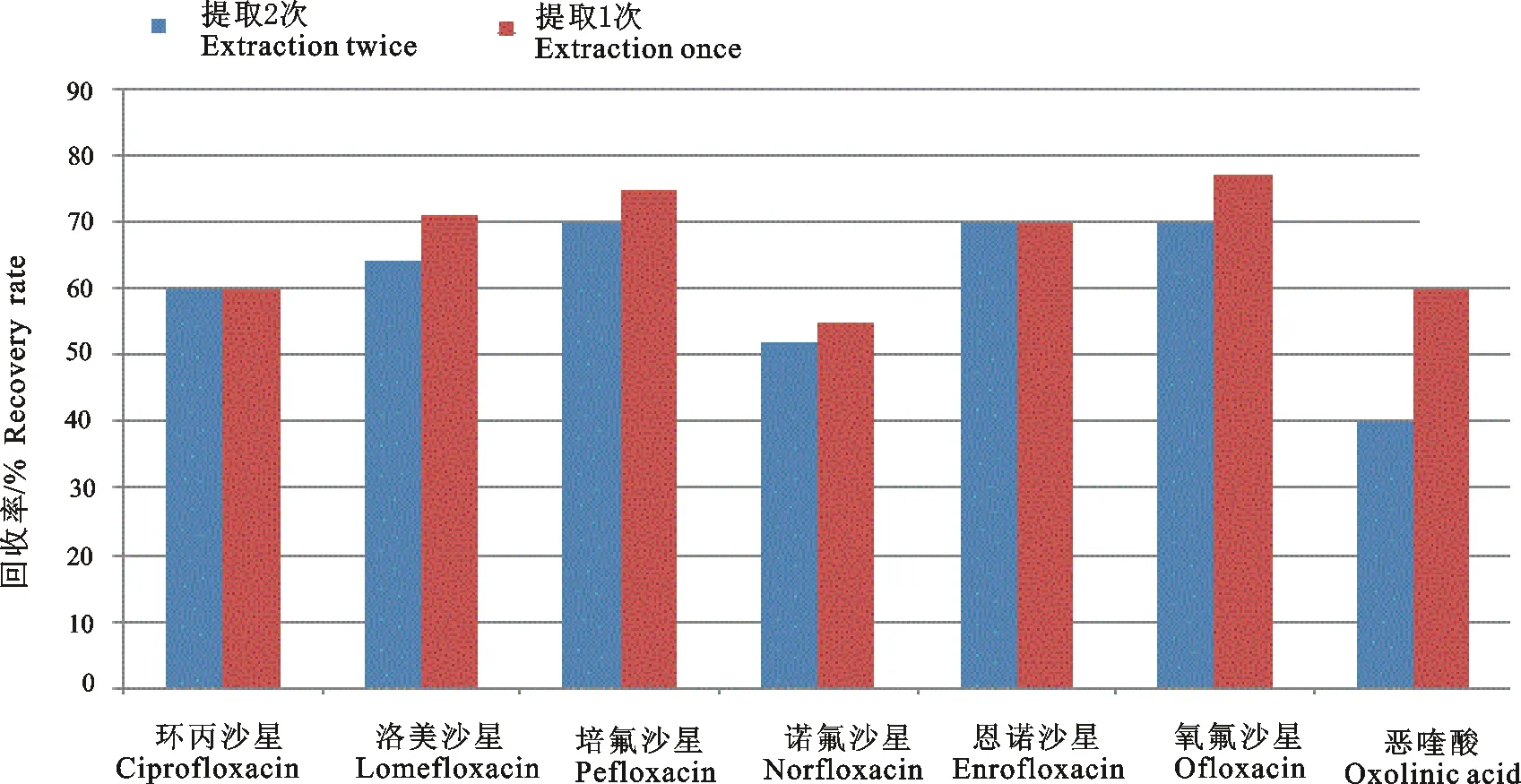
图3 提取次数对7种氟喹诺酮类药物回收率的影响
3.3 纯化条件的优化
鸡蛋中油脂含量较高,如果处理不干净,会影响方法的准确度和结果的稳定性。EDTA-Mcllvaine缓冲溶液中含有许多共萃取物,以脂肪为主,采用高速冷冻离心辅以正己烷脱脂的除脂法,可以有效地去除样品中的脂肪类干扰物。在低温状态下,脂肪粒以固体状态从溶液中析出,未分离的油脂则被正己烷除去,以达到纯化分离的目的。本方法建立中比较了4℃离心和冷冻离心(-4℃)对7种氟喹诺酮类药物回收率的影响,结果在冷冻离心条件下,药物的回收率较高。因此,本方法建立中选择高速冷冻离心辅以正己烷脱脂的除脂法。
3.4 样品的检测
按照上述建立的方法,分别对2017年宁夏地区抽取的51份样品进行检测,结果表明,此次抽取的样品中均未检出含有7种氟喹诺酮类药物残留。
本次建立了一种用高效液相-串联质谱快速检测鸡蛋中氟喹诺酮类药物残留的方法,能满足鸡蛋中7种氟喹诺酮类药物检测的要求。本次建立的方法在国家标准GB/T21312—2007《动物源性食品中14种喹诺酮药物残留检测方法 液相色谱-质谱/质谱法》的基础上,对样品前处理的过程进行了优化,使样品的处理快捷便利,灵敏度高,选择性好,且能高效、快速地检测多种抗生素,可有效应用于鸡蛋品质的监控。
