贵阳市植物饮料中过敏源性检测调查
2018-08-20孙端方
◎ 董 睿,孙端方
(1.贵州中烟工业有限责任公司技术中心,贵州 贵阳 550009;2.贵州省产品质量监督检验院,贵州 贵阳 550016)
过敏源性成分是食品生产和检测领域的重要预防和研究对象之一,欧美在数十年间已建设并具备了一定数量的生产规范和检验方法;而在我国,随着近年来疾控医学逐渐深入食品领域及人们物质生活需求的快速提升,近期相关部门在食品领域也陆续开展了食品中过敏源性成分的监抽排查。为调查贵阳市售植物饮料中过敏源性成分的分布和标识情况,本研究安排专业抽样人员对相关产品进行随机抽样,再通过ELISA方法检测过敏源性蛋白,面向省内开展实践相关检测技术,结果分析如下。
1 材料与方法
1.1 取样、制样
样品均为市场随机抽样,配料表中未含有花生的植物饮料9批次、未含有大豆的植物饮料16批次,包括核桃露、豆奶、花生乳、椰汁等。
1.2 ELISA检测
按照Biopharm的花生、大豆过敏源性试剂盒说明书进行,基本原理为以某花生蛋白或某大豆蛋白为抗原的双抗夹心显色法,用酶标仪BiotechEpoch在450 nm进行检测,用Biopharm软件Raidwin绘制标曲并计算样品中过敏源性成分含量。
2 结果
2.1 标准曲线
如图1所示,花生标曲r2>0.995、大豆标曲r2>0.999。此外,试剂盒标明,花生源性检测限1.5 mg/kg、定量限2.5 mg/kg,大豆源性检测限0.31 mg/kg、定量限2.5 mg/kg。
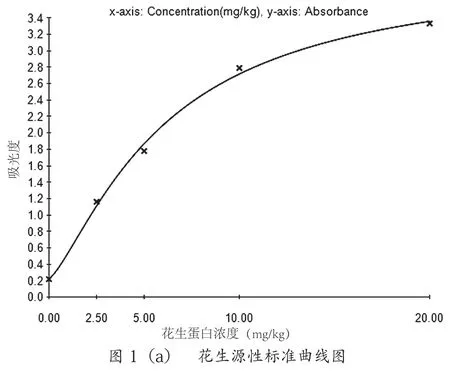
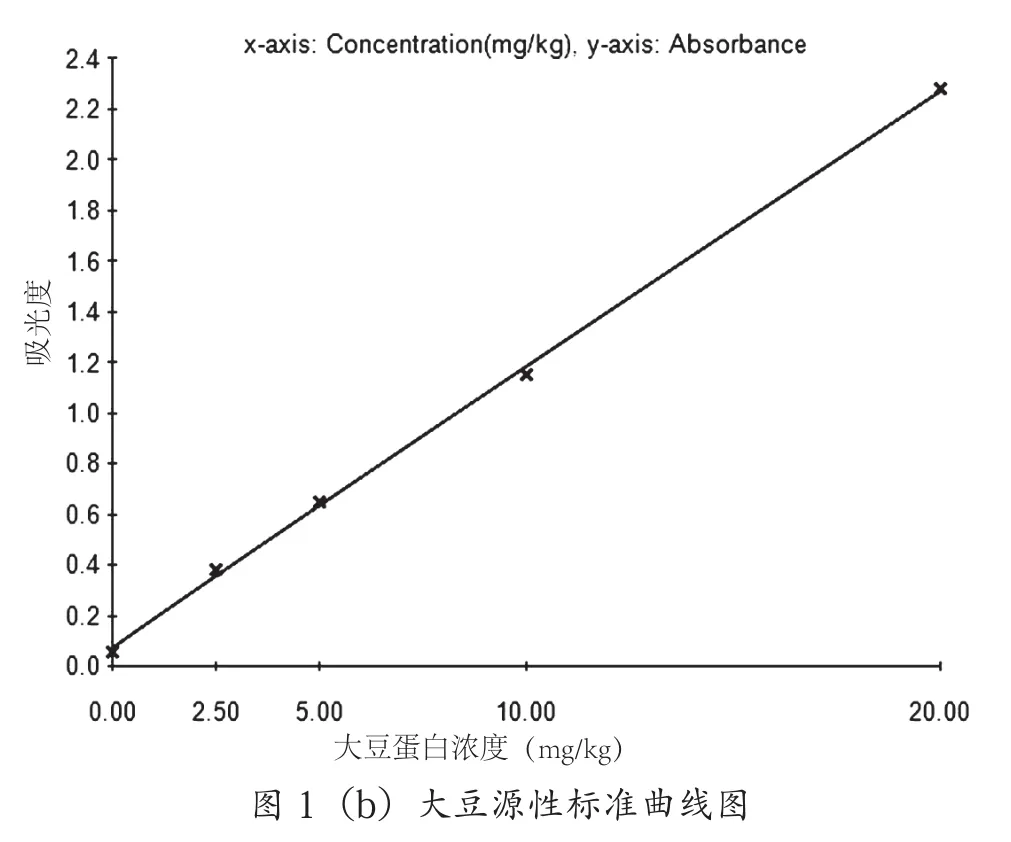
图1 源性标准曲线图
2.2 检测结果
如表1所示,未检出大于检测限的花生源性批次;检出大于检测限但小于定量限的大豆源性3批次(样品号1、2、13),检出大于定量限的大豆源性2批次(样品号5、9);阳性对照、阴性对照、空白对照符合试剂盒要求,数据略。
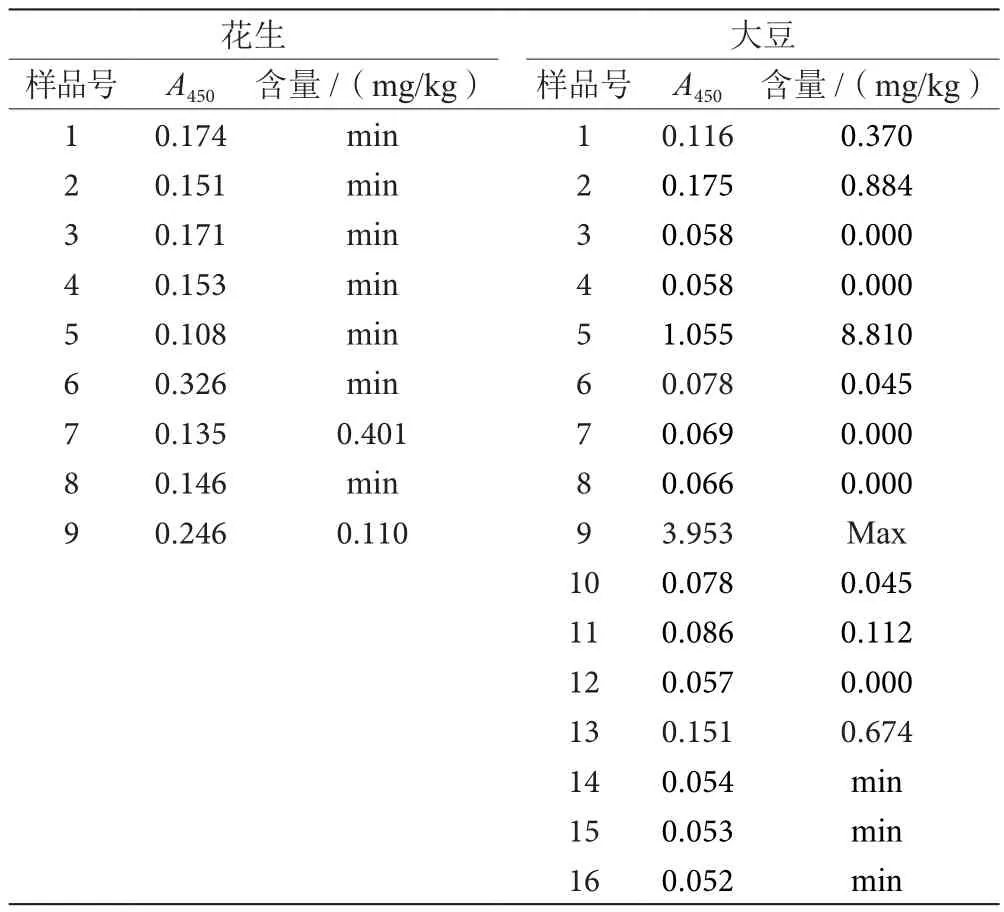
表1 花生源性和大豆源性ELlSA检测数据表
3 讨论
3.1 检测方法
目前,相关检测方法主流技术手段为荧光PCR,具有检测效率高、准确性高等优点。但在过敏源性成分检测的对象上,ELISA方法所检测的过敏蛋白相对荧光PCR所检测的特异基因更为直接。此外,ELISA方法的检测限和定量限通常低于荧光PCR,即标称灵敏度更高:如本研究所用试剂盒标称花生源性检测限1.5 mg/kg、定量限2.5 mg/kg,大豆源性检测限0.31 mg/kg、定量限2.5 mg/kg,而相关标准SN/T 1961.2-2007《食品中过敏成分检测方法第2部分实时荧光PCR法检测花生成分》未规定检测限、SN/T 1961.19-2013《出口食品过敏原成分检测第19部分:实时荧光PCR方法检测大豆成分》检测限为1‰,均为定性方法。但样品本底干扰对ELISA方法的影响通常较荧光PCR法大,如当检测对象为深色固体时,残留至样品提取液中的色素可能会对分光度值造成偏差。由于本次检测对象均为淡白色、乳白色植物饮料,其色泽在检测过程中有1/20稀释,加样至96孔板时已成完全透明液体,因而对显色结果应无干扰。
3.2 检出率
未发现无标识但检出花生源性成分的植物饮料,表明贵阳市售的植物饮料含有无标识的花生源性过敏成分风险较小。发现有大于检测限但小于定量限的无标识但检出大豆源性的植物饮料3批次,无标识但检出大于定量限的植物饮料2批次,表明贵阳市售的植物饮料含有无标识的大豆源性过敏成分,该风险应引起重视。
