大蒜挥发油提取工艺优化及GC-MS分析
2018-08-13刘阳李莎莉吴琦王丽虹许悦段金辉
刘阳,李莎莉,吴琦,王丽虹,许悦,段金辉
(武昌理工学院 生命科学学院,生物多肽糖尿病药物湖北省协同创新中心,湖北省生物多肽糖尿病药物工程技术研究中心,武汉 430223)
大蒜(AlliumsativumL.)为百合科(Liliaceae)葱属(Allium)草本植物的地下鳞茎,别名胡蒜、葫、独蒜、独头蒜等,其作为调味食材和药物使用已有四千多年的历史[1]。大蒜性温、辛、甘,以其鳞茎入药,被誉为天然的“药用植物黄金”[2]。研究表明,大蒜的主要生物活性物质为含硫化合物,即“蒜素”[3],不仅具有杀菌、抗炎等作用,对消化系统、肿瘤和乳腺癌、肝癌等恶性肿瘤也具有积极的效果[4,5],被美国国家癌症研究所称为“具有潜在抗癌特性的蔬菜”。
大蒜挥发油富含含硫化合物[6],是大蒜多种药理活性的物质基础。近年来,关于大蒜挥发油提取工艺的研究报道较多,但研究结果和挥发油品质差别较大。为满足临床对大蒜挥发油药用价值的研究开发,本试验以水为溶剂,在单因素基础上采用正交试验确定了挥发油提取的最佳工艺,并通过GC-MS进行成分分析。本法具有绿色环保、挥发油中含硫化合物含量高的特点,可为大蒜挥发油的工业化生产提供技术参考,为大蒜资源药食两用价值的深度利用提供试验依据。
1 材料与方法
1.1 材料与试剂
新鲜白皮大蒜:购于武商量贩江夏店(产地:湖北);乙醚:AR,上海国药集团化学试剂有限公司。
1.2 主要仪器
GC7890N-MSD5975C气质联用仪 美国Agilent公司;SB-3200DT超声仪 宁波新芝生物科技股份有限公司。
1.3 方法
1.3.1 挥发油提取
新鲜大蒜→去皮称重→捣碎→加纯化水均浆→室温超声→浸泡30 min→水蒸气蒸馏→乙醚萃取→收集挥发油→称重→计算提取率[7]。
1.3.2 GC-MS分析
19091J-433HP-5色谱柱(5% Phenyl Methyl Siloxan,30 m×250 μm×0.25 μm);柱温:50 ℃(保持1 min,以5 ℃/min升温到280 ℃,保持10 min);进样口温度:250 ℃;载气流速:1 mL He/min;分流比10∶1;进样量:1.0 μL。电子轰击离子源,温度230 ℃;四极杆温度:150 ℃;接口温度:280 ℃;电子能量:70 eV;电压:1976 V;扫描质量范围:30~500 amu;溶剂延迟:4 min。
2 结果与分析
2.1 正交试验
单因素试验结果显示,超声时间、浸泡温度、料液比、蒸馏时间对大蒜挥发油提取率影响较大。按L9(34)设计正交试验,以提取率为评价指标,结果见表1。
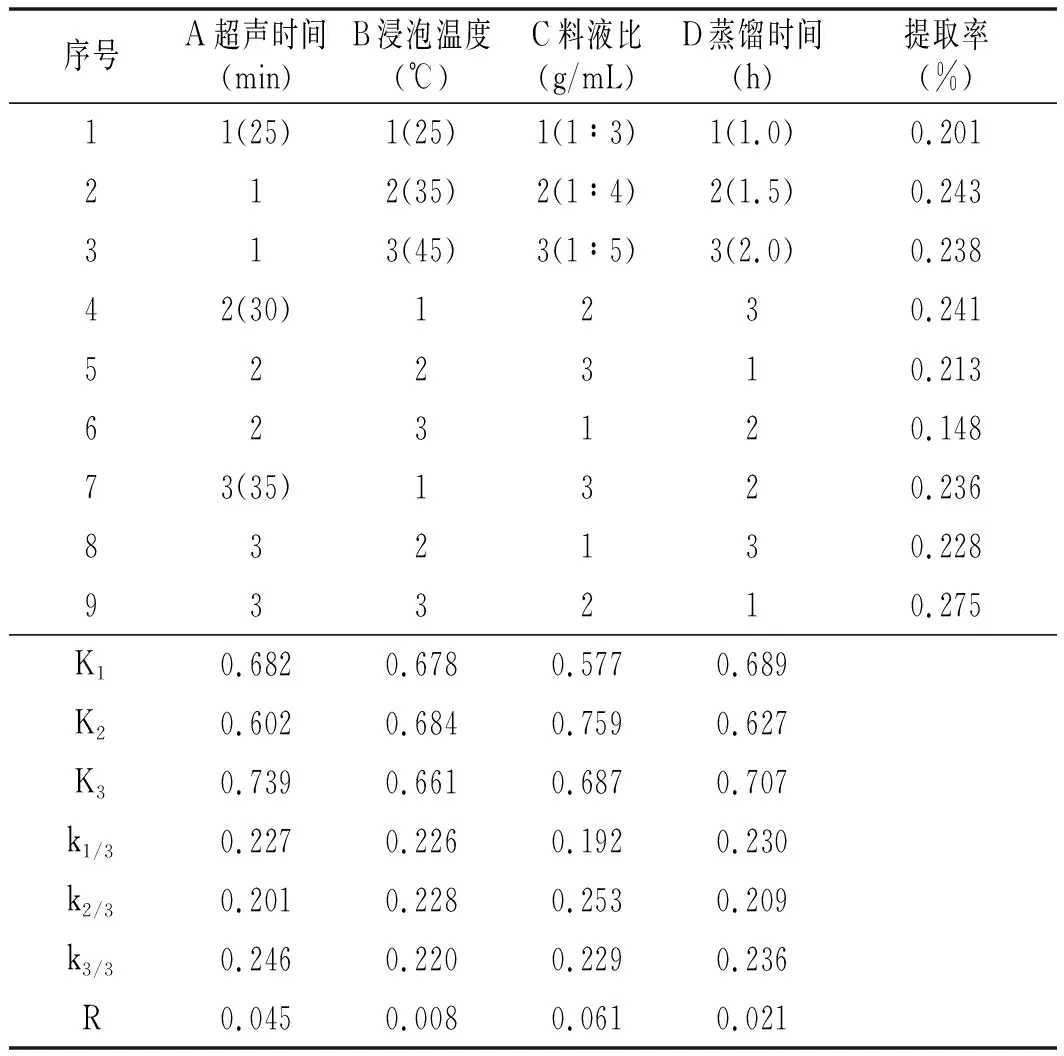
表1 大蒜挥发油提取正交试验结果Table 1 The orthogonal test results of garlic volatile oil extraction
由表1可知,料液比对提取率的影响最大,其次是超声时间和蒸馏时间,而浸泡温度的影响最小。结果表明:大蒜挥发油提取工艺的最佳组合为A3B2C2D3,即超声35 min、浸泡温度35 ℃、料液比1∶4、蒸馏2 h。
2.2 放大验证试验
在最佳工艺条件下,将大蒜取用量放大5倍进行验证性试验,提取率结果见表2。

表2 大蒜挥发油验证试验结果Table 2 The verification test results of garlic volatile oil
由表2可知,超声辅助水蒸气蒸馏法提取大蒜挥发油得率为0.280%,与正交试验结果相符,与文献[8]接近而高于文献[9]的结果,收集的挥发油为具有大蒜刺激性气味的淡黄色澄明液体。
2.3 挥发油化学成分分析
大蒜挥发油用色谱纯正己烷按1∶2(V/V)稀释,进行GC-MS检测,其总离子流图见图1。用峰面积归一化法从总离子流图中计算出各成分的相对质量分数,并利用NIST11.LIB 标准库进行成分分析,结果见表3。

图1 大蒜挥发油总离子流图Fig.1 Total ion chromatogram of garlic volatile oil

序号保留时间(min)化合物分子式相对质量含量(%)14.3682-甲基腺苷C11H15N5O40.0127.6303,4-二甲基噻吩C6H8S0.1238.052烯丙基二硫醚C4H8S24.6448.5541,3-二硫杂环己烷C4H8S20.4258.878烯丙基甲烷硫代磺酸盐C4H8O2S20.8769.910二甲基三硫醚C2H6S31.42713.891二烯丙基二硫醚C6H10S235.11814.264 2-亚乙基-1,3-二噻烷C6H10S24.69914.685 甲氧基羰基甲基二磺酰基乙酸甲酯C6H10O4S20.021014.912 四氢噻吩C3H6S20.021115.263 硫代二乙酸二甲酯C6H10O4S0.131215.669 甲硫基乙腈C3H5NS9.841315.998 1-环己基-3-甲氧基-丁烷-2-酮C12H22O20.041416.468 1-甲氧基甲硫醚C5H12OS0.221517.095 3-乙烯基-1,2-二硫环己-4-烯C6H8S20.351617.851 3-乙烯基-1,2-二硫环己-5-烯C6H8S20.321717.948 2,2'-二硫二乙醇C4H10O2S20.021818.802 亚硫酸二乙酯C4H10O3S0.011919.812 3-羟基葵酸C10H20O30.092019.996 亚硫酸二乙酯C4H10O3S0.01
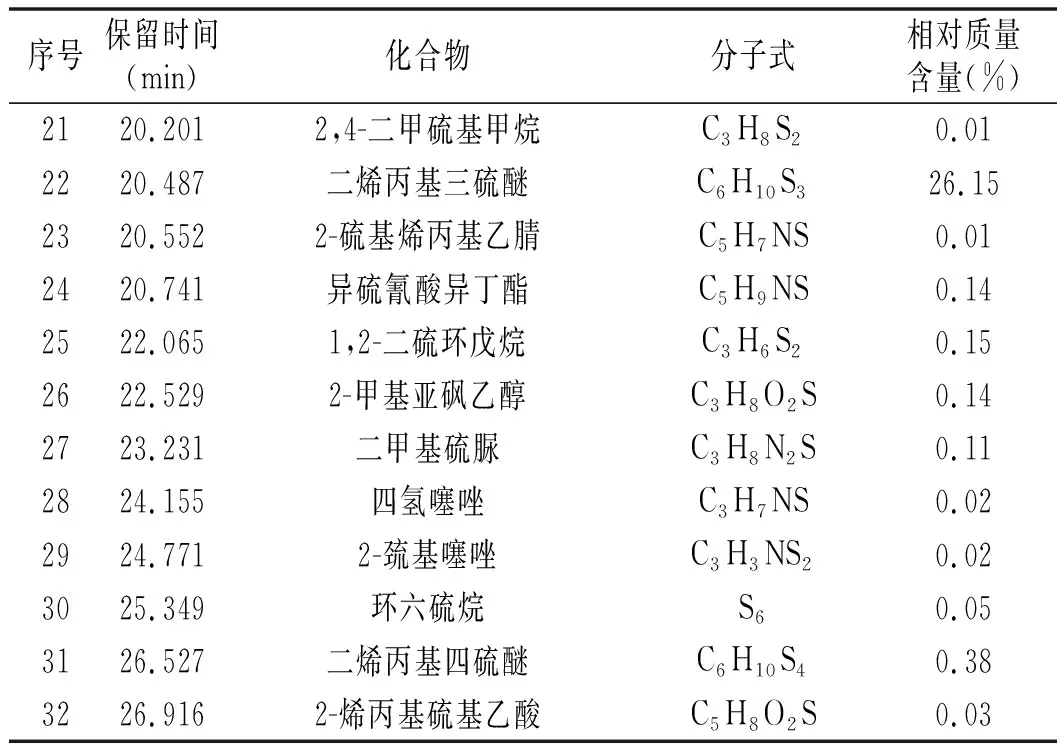
续 表
由表3可知,从该法提取的大蒜油中鉴定出了32种成分,其中含硫化合物29种,其结构主要为醚、酯、羧酸、腈、醇类以及烷烃、烯烃等,其含量占挥发油总量的88.15%,远高于文献[9]采用乙醇提取法制备大蒜油的结果。大蒜挥发性成分中含量最高的为二烯丙基二硫醚(35.11%,diallyl disulfide, DADS),其次是二烯丙基三硫醚(26.15%, diallyl trisulfide, DATS),二者含量总和占挥发油总量的69.46%,与文献[10]的结果一致。在大蒜挥发油中,除DADS、DATS外,还含有甲基烯丙基二硫醚、二烯丙基硫醚、二烯丙基四硫醚等,其中烯丙基硫醚有机物占硫醚化合物的97.68%,亦远高于文献[9]的结果。
3 讨论
3.1 挥发油制备
水蒸气蒸馏具有操作简单、成本低廉、适合工业化生产的特点[11],是提取挥发油的常用方法。近年来,大蒜挥发油的生理作用及其在食品、医药等领域的应用引起了人们的广泛关注,并进行了大量的研究[12,13],但由于大蒜的品种、产地、处理方法的差异,挥发油提取工艺相差较大。本研究通过正交试验确定了大蒜挥发油的最佳提取条件:超声时间35 min、浸泡温度35 ℃、料液比1∶4、蒸馏时间2 h,该条件下大蒜挥发油提取率为0.280%,与理论值一致[14],稍低于孟宪锋等[15]利用乙醇提取及张郁松等先进行酶解再蒸馏提取的研究结果。
主要的原因可能是:①大蒜产地来源和品种不同;②乙醇等有机溶剂提取效率更高,但成本和对后续研究有一定影响;③酶解可能比超声波的辅助效果好,更能有效提高大蒜油提取率,具体的原因尚需进一步深入研究。同时,本试验采用超声辅助以水为溶剂进行提取,避免了有机溶剂提取的残留问题和对其生物活性的影响。
3.2 挥发油成分分析
大蒜为药食两用植物,其挥发油中含有多种强烈刺激性气味的有机硫化物,是大蒜主要的生物活性物质,具有抗菌消炎、抗肿瘤、抗病毒、提高机体免疫力、缓解疲劳、促进糖代谢、预防和治疗心血管疾病等多种药理作用[16,17]。由表3可知,该法提取的大蒜挥发油主要为含硫化合物,占总量的88.15%,其中的DADS和DATS约占挥发油总量的70%,二者为大蒜素中的脂溶性含硫化合物,具有较强的抗肿瘤、降血脂、抗氧化等活性。大量研究结果显示,大蒜经多途径抑制肿瘤细胞与其亲水性或亲脂性作用靶点有关,蒜素中所含硫取代或巯基取代的数目多少与其抗肿瘤的效果呈现一定的相关性。
因此,该法制备的大蒜挥发油具有丰富的含硫化合物,保持了大蒜原有的主要生物活性成分,为临床合理利用大蒜素治疗恶性肿瘤提供了物质基础,可满足新药研发需求,有利于进一步提高其药用价值。
