择期肾下型腹主动脉瘤腔内修复术后并发截瘫2例
2018-07-30郑继行邓超频符伟国
艾 鹏, 潘 浩, 陈 魁, 郑继行, 邓超频, 陈 聪, 符伟国
临床资料
病例1 男,82岁。因“右侧腹部胀痛2周”入院。CTA发现右侧髂总动脉夹层动脉瘤,右侧髂总动脉起始部瘤样扩张,直径2 cm,腔内见双腔征。髂总动脉夹层动脉瘤直径二倍于正常值,存在瘤体破裂风险,转入血管外科。既往慢性支气管炎病史12年[1年前慢性阻塞性肺疾病(COPD)急性加重住院治疗]、肺结核病史50余年,10年前行前列腺手术史。术前评估肺功能示重度混合性通气功能障碍(MVV∶30),提示手术行全身麻醉风险极大,遂决定于局麻下行腹主动脉腔内修复术。在局麻下行双侧股总动脉穿刺,置入先健科技公司Ankuar分体型覆膜支架主体22 mm×12 mm×120 mm及右侧髂支14 mm×12 mm×120 mm准确定位于肾下腹主动脉至双侧髂总动脉髂内外动脉分叉近端因瘤体位置较高,接近腹主动脉分叉,行直筒型覆膜支架难以完全修复,遂决定选择腹主动脉分体型覆膜支架,另由于器材选择有限,不得已选择的主体长达肾动脉下缘。结束手术前造影示腹主动脉、右髂总动脉瘤隔绝满意,未见内漏,肾动脉、双侧髂外动脉通畅,双侧髂内动脉显影良好(图1)。术中因麻醉效果欠佳患者短时不配合导致创口出血(约 800 mL)并出现低血压,收缩压最低达 55 mmHg(1 mmHg=0.133 kPa),持续时间约50 min。术毕患者双下肢血运、肌力均正常。术后生命体征平稳,血压维持在120~140/60~80 mmHg,SaO2>95%,血红蛋白未低于100 g/L。次日清晨(术后18 h)发现患者双下肢不能抬举或移动,大小便障碍,腰部束带感,双下肢肌力0级,肌张力减退,脐平面以下痛触觉减退,腹股沟平面以下痛触觉消失。急症MRI示T10~L1水平脊髓缺血性病变(图2)。肌电图报告:EMG双下肢L2以下支配肌肉无MU无CMAP,静息时未见失神经电位;MCV双侧胫神经MCV轻度减慢,NAP未能诱发;下肢腓浅神经SNAP消失。因患者家属拒绝行脑脊液引流术故予药物保守治疗。遂予小剂量间羟胺(因患者难以耐受多巴胺)提升血压至140/80 mmHg左右;激素冲击治疗(甲泼尼龙400 mg/d×5 d),扩张动脉血管,那屈肝素抗凝,甲钴胺针营养神经治疗。治疗2周后双下肢肌力无明显改善,左下肢触觉恢复至足背。转至康复专科医院进一步高压氧及康复治疗。患者康复治疗半月后自动放弃继续治疗出院自行康复治疗。患者12个月后门诊复查,双下肢肌力仍0级,感觉减退平面升至乳头平面,双下肢肌肉萎缩,大小便不能自理。
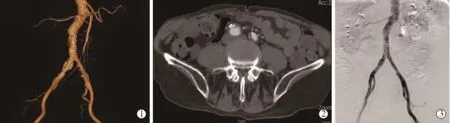
图1 髂总动脉夹层动脉瘤患者术前主动脉CTA图像
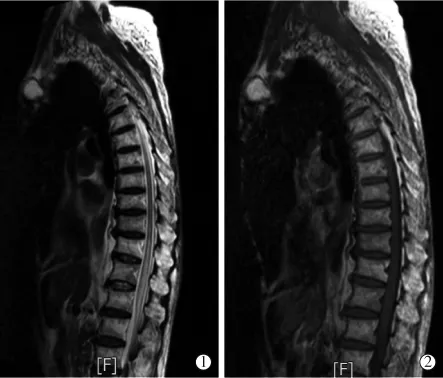
图2 胸椎矢状面T2WI图像
病例2 男,87岁。因“摔伤致腰背部疼痛2 d”入院诊断“T12椎体骨折,高血压”。既往高血压史10余年,20 d前行颈动脉支架植入术。骨科行术前检查发现腹主动脉下段、两侧髂总动脉及左侧髂内动脉动脉瘤形成,腹主动脉下段最大直径37 mm,右侧髂总动脉最大直径65 mm,左侧髂总动脉最大直径32 mm,左髂内动脉瘤样扩张,最大直径53 mm,双侧髂内动脉均累及(见图3)。完善相关术前准备后择期于全麻下行腹主动脉瘤及双侧髂动脉瘤腔内修复术(EVAR)。术中植入先健科技公司Ankuar分体型覆膜支架主体24 mm×12 mm×120 mm,加入左侧髂支支架 14 mm×12 mm×120 mm、14 mm×12 mm×80 mm, 右侧髂支 14 mm×20 mm×120 mm、14 mm×12 mm×100 mm,覆盖双侧髂内动脉开口至髂外动脉术前造影见左侧髂内动脉瘤已完全闭塞,手术方案为左髂内动脉未行栓塞直接予以封闭,同时拟保留右侧髂内动脉;术中发现右髂内动脉瘤I型内漏,即与患方沟通后再予隔绝右髂内动脉且未行栓塞术,期待此举能降低盆腔缺血的发生。术毕即刻造影示:腹主动脉瘤、双侧髂总动脉瘤、髂内动脉瘤隔绝满意,未见内漏,双肾动脉、髂外动脉显影通畅。麻醉成功后血压即降至70/40 mmHg左右,经补液纠正至100/60 mmHg才开始手术。手术全程约150 min,出血30 mL。术中监护生命体征平稳,未发生急性低血压。手术结束后留置气管插管转至重症监护室监护,期间药物维持血压为90~150/50~90 mmHg。于术后24 h发现双下肢上抬受限(肌力2级),患者诉麻木感,查体:双侧L1水平以下浅感觉略减退,马鞍区感觉存,双下肢肌力2+级,大小便无障碍。行胸腰椎MRI未见异常信号。予以加用激素冲击治疗(甲泼尼龙80 mg/d,3 d),扩张动脉血管,那屈肝素抗凝,甲钴胺针营养神经治疗。1周后患者截瘫症状明显好转,双下肢上抬明显改善,应患者要求予出院回家继续康复锻炼。1个月后门诊复诊患者双下肢肌力恢复正常水平,肢体感觉功能无障碍。
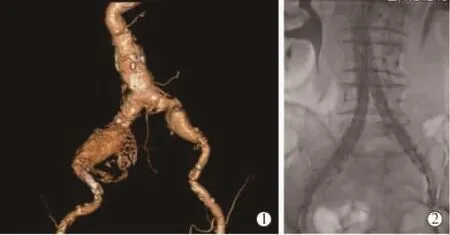
图3 腹主动脉、双侧髂动脉瘤患者术前CTA图像
讨论
腹主动脉瘤是最常见的主动脉病变之一。随着医疗器具和技术的进步,腔内修复术(EVAR)已逐渐成为腹主动脉瘤的主流治疗方案[1-2]。截瘫并发症在择期腹主动脉瘤腔内修复术后很少见,发生率0.21%~0.38%[3],且多见于破裂型腹主动脉瘤术后,急诊腔内修复术后发生率高达11.5%[4]。
腹主动脉瘤术后发生截瘫并发症的原因极为复杂,可归结为脊髓灌注压的变化造成的脊髓缺血(spinal cord ischemia,SCI)。目前认为其发生的机制可能是多方面的[5],其可能的原因包括以下。
1、开放或腔内手术中脊髓供血血管(如肋间动脉、腰动脉、髂内动脉、变异的前根大动脉等)的阻断、覆盖或血栓栓塞。如Mehta等[6]报道的在107例EVAR术中封堵髂内动脉的患者中,并没有观察到截瘫等神经功能受损症状的发生,并且Freyrie等[3]在重建1例患者的单侧髂内动脉后仍发生了脊髓缺血。本组病例1并非典型的腹主动脉瘤患者,管壁不存在严重的附壁血栓等栓塞因素,且EVAR术中双侧髂内动脉均得以保留,同时EVAR术中主动脉的阻断时间不可能很长(实际3~5 min),手术在局麻下进行亦不存在损伤脊髓的可能,但术后患者仍出现严重且不可逆的脊髓缺血;与之相反,例2为腹主动脉瘤及双侧髂动脉巨大瘤,术中腔内操作更为复杂,并且术中双侧髂内动脉均行覆盖,不出所料地患者术后出现双下肢轻瘫的症状,但1个月后完全康复,质疑该论点的可靠性。由于临床实际操作的受限,例1采用了全程覆盖肾下腹主动脉而未重视可能截瘫发生风险,其原因在于平素行腹主动脉瘤EVAR术的习惯思维。当我们反思该病例无腹主动脉管壁变形的特性,是否可猜测正常管壁的腹主动脉存在重要脊髓滋养血管的可能性更大。这一点有待我们在日后基础研究或临床中进一步验证。
2、围手术期周围循环血压低。行腹主动脉瘤EVAR术后发生脊髓缺血的概率极低,而急症行破裂型腹主动脉瘤EVAR的发生率高达11.5%[4]。其差异在于腹主动脉瘤破裂、阻断动脉时控制性降压时易出现严重的低血压。有实验研究表明,严重低血压(平均动脉压在55 mmHg)超过脊髓血供的安全范围,大脑和脊髓血供的自我调节丢失,增加中枢神经系统缺血可能性[7]。 Chiesa 等[8]认为围手术期低血压(平均动脉压<70 mmHg)是导致主动脉术后脊髓缺血的重要因素。本组例1手术过程中,因患者肺功能差而行局麻下手术导致术中患者因难以耐受疼痛而欠配合导致创口急性失血,并且术前准备不足静脉通路不畅(未行深静脉置管),因此出现较长时间(50 min)的低血压,最低时血压55/40 mmHg左右。病例2因容量不足出现全麻后血压一过性下降,时长15~30 min,血压约60/40 mmHg,经及时补液纠正后才开始手术。此后手术过程顺利,患者血压水平维持稳定。结果病例1术后出现严重的脊髓缺血,1年随访症状仍未能改善,甚至病情有进展迹象;而例2出现双下肢轻瘫症状,1个月后自行康复。总结这2例患者的病程特点,手术过程中均出现了不同程度的低血压,术后相应地出现不同程度的脊髓缺血。由此我们更有理由相信围手术期循环低血压在脊髓缺血的病因中扮演着相当重要的角色。
3、基础静脉压高具有潜在脊髓缺血风险。因慢性阻塞性肺病(COPD)患者静脉压力高,直接造成脊髓血供流出道的压力升高,间接造成脊髓流入道压力的不足,导致脊髓缺血。如再因手术引起动脉灌注压下降,脊髓缺血明显加重[9]。本组病例1患者有明确COPD病史,系主动脉术后并发脊髓缺血的高危人群,且术中突发血压下降。虽然不存在长节段主动脉隔绝、重要分支血管阻断等常见危险因素,但术后患者仍出现严重的脊髓缺血并发症,充分证明围手术期脊髓灌注压的变化与脊髓缺血的发生存在重要影响。
