水热法协同处置不同垃圾焚烧炉飞灰及其机理
2018-07-26陈志良张汉威黄群星陆胜勇严建华浙江大学能源清洁利用国家重点实验室浙江杭州3007光大绿色环保研究所江苏南京00
阮 煜,宗 达,陈志良,张汉威,黄群星*,陆胜勇,池 涌,严建华 (.浙江大学能源清洁利用国家重点实验室,浙江 杭州 3007;.光大绿色环保研究所,江苏 南京 00)
垃圾焚烧能大幅度减容,无害化程度高,可利用废热,符合垃圾处理的“三化”(减量化、无害化、资源化)原则.因此,焚烧技术成为我国垃圾处理技术的主要研究和发展方向[1-3].垃圾焚烧过程会产生飞灰,根据2016年3月30日由环保部会议修订通过《国家危险废物名录》,生活垃圾焚烧飞灰被列为危险废物,垃圾焚烧飞灰中富含易浸出的重金属以及较多的二噁英、多氯联苯(PCBs)和多环芳烃(PAHs)等有机污染物[4-6],在填埋之前需对其进行处理,防止对环境的二次污染.飞灰的产生量约占焚烧总重的 3%~5%[7],而流化床焚烧技术产生的飞灰产生量较多,高达 10%~20%[8],如此大量的生活垃圾焚烧飞灰如不妥善的处理将是一个潜在的安全隐患[9-10].
水热法有利于快速生成晶格缺陷少的晶体,粉煤灰中的Al、Si源在碱激发剂条件下能够水热合成硅铝酸盐矿物[11-14].水热法用于垃圾飞灰的固化与稳定同样有很大的潜力,可将重金属稳定于矿物中而不易浸出,对环境负担小[15-16].生活垃圾焚烧飞灰合成沸石最早是由台湾国立中山大学的Yang等[17]率先加入氢氧化钠溶液作为矿化剂合成了钠菱沸石、斜方钙沸石.中国科学院生态环境研究中心的Fan等[18]采用先熔融再水热的方法,合成了X型沸石和羟基方钠石,阳离子交换能力、比表面积和孔隙体积高于煤灰合成的沸石.
之前的研究中飞灰水热反应都需要外加碱性物质作为激发剂,且尚未对炉排炉和流化床这两种不同生活垃圾焚烧炉型的飞灰进行过协同处理,对于水热合成过程的机理分析以及雪硅钙石的重金属吸附机理解释并不明确,本文通过混合两种不同垃圾焚烧炉的飞灰,在不外加碱激发剂的情况下直接水热合成硅铝酸盐,降低飞灰中重金属的浸出毒性.根据飞灰水热产物的晶体类型和表面形貌,分析了结晶机理,并借助雪硅钙石的晶体结构解释了其重金属吸附机理,开展了飞灰稳定重金属的基础性研究.
1 材料与方法
1.1 飞灰的采集
实验中所用到的生活垃圾焚烧飞灰,一部分来自杭州萧山锦江绿色能源有限公司(记为 F),该公司采用流化床焚烧技术,日处理量 1300t,一部分来自光大环保能源宁波有限公司(记为 G),该公司采用炉排炉技术,日处理量 1000t.飞灰均取自烟气处理系统的袋式除尘器.所用的飞灰在反应之前均置于 105℃的烘箱中烘干处理24h.
1.2 水热反应
将上述流化床飞灰和炉排炉飞灰共 20g,分别按照质量比 7:3、6:4、5:5、4:6、3:7混合均匀,依次命名为F7G3、F6G4、F5G5、F4G6、F3G7,按照固液比1:10加入去离子水,置于容积为250mL带搅拌的高温高压反应釜中,在200 ℃、150r/min转速下搅拌反应24h.反应结束后,用真空抽滤装置过滤反应后的飞灰,收集抽滤过程的溶液置于冰箱 5℃下冷藏待测,固体在105℃的烘箱中干燥24h待测.
1.3 重金属浸出毒性
飞灰及其水热产物重金属毒性浸出实验按照国家标准《固体废物浸出毒性浸出方法 醋酸缓冲溶液法》(HJ/T 300-2007)[19]进行,模拟生活垃圾焚烧飞灰在填埋场的渗滤特性,浸出毒性标准参照《生活垃圾填埋场污染控制标准》(GB16889-2008)[20].
1.4 飞灰重金属含量
取 0.1g飞灰,加入氢氟酸(沪试,优级纯)、硝酸(沪试,优级纯)、过氧化氢(沪试,分析纯)各 2mL,放入微波消解仪(WX-8000,上海屹尧科技发展有限公司),在200℃下保温 2h,飞灰完全溶解在消解液中,将消解液用稀硝酸溶液稀释定容至 10mL容量瓶中待测.飞灰重金属含量计算公式如下:

式中: H为飞灰重金属含量,单位为mg/kg;c为消解液稀释定容至 10mL溶液的重金属离子浓度,单位为mg/kg.
1.5 分析测试
采用 X射线粉末衍射仪(X-pert Powder,荷兰PANalytical B.V.公司)测定粉末的衍射图谱,测量后的数据直接用OriginPro 2017作图,借助MDI jade 6软件分析原始飞灰以及反应产物中的主要晶体;X 射线荧光光谱分析仪(ARL ADVANT’X IntelliPowerTM 4200,美国Thermo公司)分析飞灰化学元素组成;场发射扫描电镜(SIRION-100,美国FEI公司)观测固体表面形貌结构;电感耦合等离子体发射光谱仪(iCAP6300,美国 Thermo公司)分析溶液中重金属离子浓度.
2 结果与讨论
2.1 飞灰的理化特性分析
飞灰的理化特性主要包括元素组成、晶体组成、表面形貌、重金属含量和重金属浸出特性.
X射线荧光光谱分析仪(XRF)测得两种飞灰的化学元素组成如表1所示,由于采用半干法脱酸,两种飞灰中的 CaO含量都很高,炉排炉飞灰中高达48.45%,流化床飞灰为 26.29%,流化床飞灰中含有大量的Si、Al元素,而炉排炉中两种元素含量很少.
对两种飞灰全量消解,然后用电感耦合等离子体发射光谱仪(ICP)测定其重金属含量如表2所示,原始飞灰中主要的重金属有 Zn、Pb、Cu、Cr、Cd、Ni. Zn、Pb的含量高且浸出量较高,Ni的含量最低且浸出量极少.在飞灰填埋时,Zn、Pb、Cu、Cr、Cd这些重金属极易渗滤,对周边土壤及地下水造成严重污染.两种飞灰的重金属浸出毒性如表3所示,流化床飞灰的Cd、Pb分别超标5.1倍和5.8倍,而炉排炉的Pb更是超标达 34倍.飞灰倘若不能妥善处置,不仅占用大量土地,还将对环境造成极大的二次污染.

表1 飞灰的化学组成(%)Table 1 The chemical composition of fly ash(%)
飞灰的主要晶体由 X 射线粉末衍射仪(XRD)测 定,采用MDI jade 6软件分析测试结果(图1),炉排炉飞灰中主要含有Ca(OH)2、CaClOH、CaCO3、NaCl、KCl,而流化床飞灰主要含有 SiO2、KCl、NaCl,未检测出Ca(OH)2.
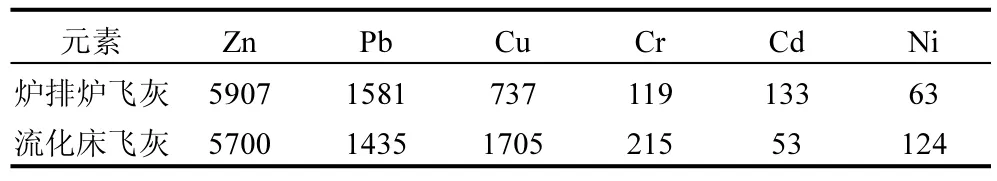
表2 飞灰的重金属含量(mg/kg)Table 2 The heavy metal content of fly ash (mg/kg)
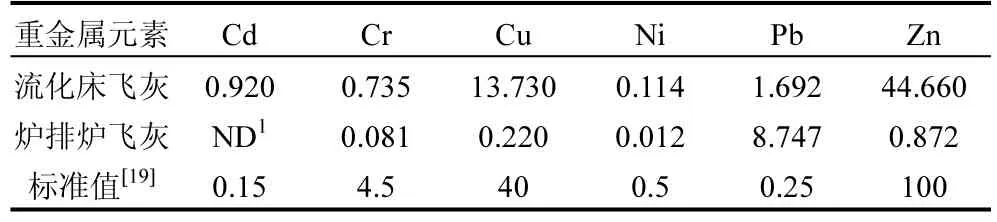
表3 飞灰的重金属浸出毒性(mg/L)Table 3 The heavy metal leaching toxicity of fly ash(mg/L)
CaClOH是Ca(OH)2和CaCl形成的一种中间体化合物,在水中可以溶解OH-和Cl-呈现碱性,反应方程式如下:
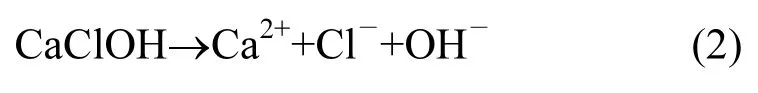
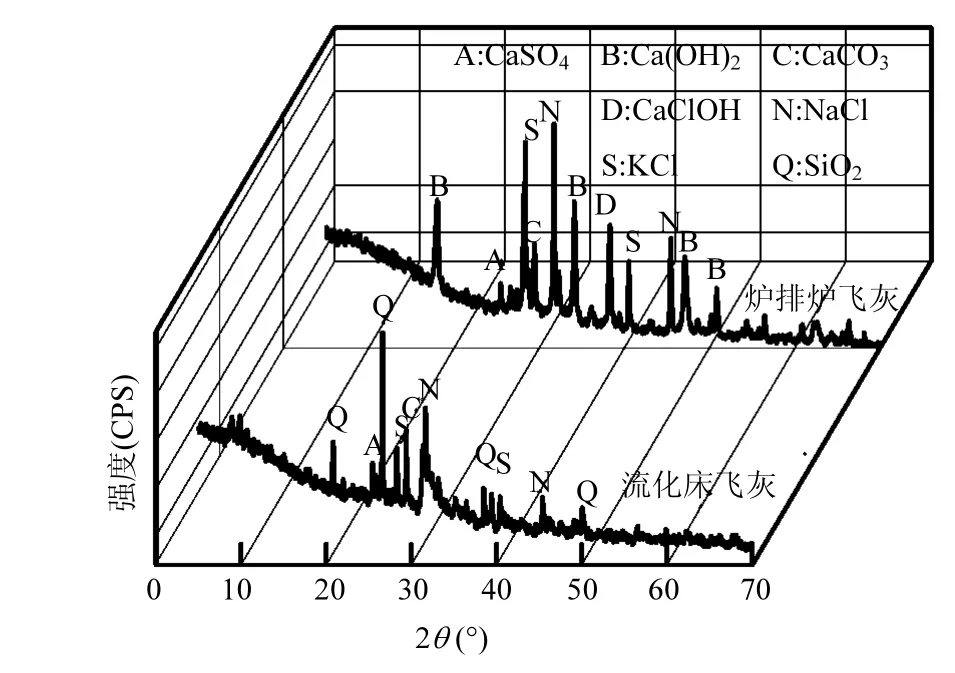
图1 原始飞灰的X射线衍射(XRD)分析Fig.1 X-ray diffraction (XRD) analysis of the original fly ash
炉排炉垃圾焚烧飞灰采用半干法脱酸,喷洒了较多的 Ca(OH)2,碱性较强,流化床飞灰由于掺了 5%的煤混烧,硅铝含量偏高.故将这两种飞灰掺和一起水热,其中炉排炉飞灰作为碱激发剂,流化床飞灰作为硅铝源,在水热条件下不需要添加剂即可合成硅铝酸盐,从而降低重金属浸出毒性.
飞灰的表面形貌如图 2所示,图 2(a)中流化床飞灰颗粒较小,由各种形状各异的矿物晶体堆叠形成,孔隙较多,表面极其不规则.图2(b)中炉排炉飞灰的颗粒团聚更加明显,主要为较大粒径球状结构.飞灰的形貌与已有的研究结果一致[9,21].这与2.2中飞灰水热产物的形貌有明显的不同.

图2 原始飞灰的扫描电镜(SEM)图像Fig.2 Scanning electron microscopy (SEM) images of the original fly ash
2.2 飞灰水热产物分析
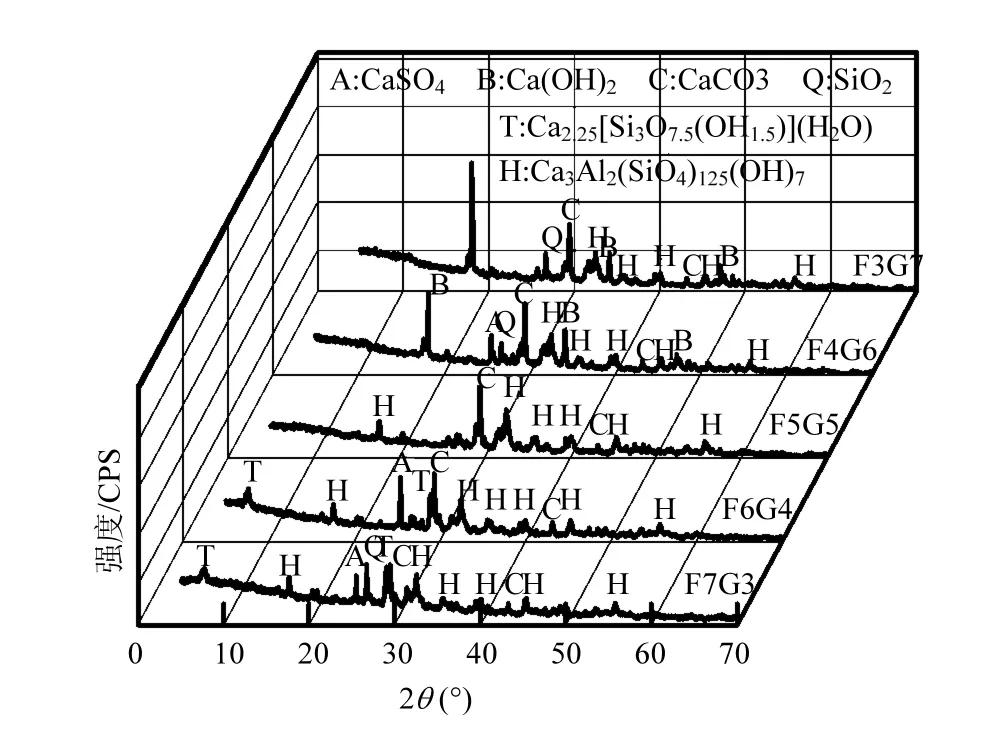
图3 飞灰水热产物的XRD分析Fig.3 XRD analysis of fly ash hydrothermal products
根据图3中水热后飞灰的XRD分析结果,所有的掺比均有水钙铝榴石生成(H,Ca3Al2(SiO4)1.25(OH)7),F7G3与F6G4中有雪硅钙石(T,Ca2.25(Si3O7.5(OH)1.5)(H2O))晶体峰位.F7G3水热产物中存在明显的石英峰位,而不存在Ca(OH)2,是由于在无添加剂的情况下,掺混的炉排炉飞灰量过少导致碱性不足无法继续水热反应;F3G7与 F4G6中也有石英峰位,但是也有Ca(OH)2存在,二者并未发生反应,可能是因为溶液中铝含量不足,导致水钙铝榴石无法继续合成,故两种飞灰直接水热合成硅铝酸盐的最佳掺比在 F:G=7:3~3:7之间.两种飞灰中的可溶性盐类(如KCl、NaCl)在水热反应后在固相中消失,在水热反应产物中也并未发现有Na、K、Cl元素存在,这些可溶性盐必然存在于水热反应后的液相中.
如图4(a)(b)所示,F7G3与F6G4水热后的飞灰呈现有纳米晶须包裹的椭球体,生活垃圾飞灰合成这样的球形颗粒尚未见其他文献报道,椭球体表面的纳米晶须较为密集,且形貌与雪硅钙石的微观结构吻合[22-23],并且只在F7G3、F6G4 2种组合中才存在,应该是雪硅钙石结晶后附着飞灰表面形成.这种结构能够大大增加其表面积,有利于雪硅钙石吸附重金属.而在图4(c)(d)(e)中,F5G5、F4G6、F3G7只有小部分区域形成纳米线,大部分都还是大颗粒的形态存在,并且随着流化床飞灰的增加,Si、Al含量增加,飞灰表面结晶更加明显.水热后的飞灰相比于图 2(a)(b)的原始飞灰,晶粒更小,表面结构更加粗糙,比表面积更大.

图4 飞灰产物SEM图像Fig.4 SEM images of fly ash hydrothermal products
2.3 雪硅钙石固化重金属机理
雪硅钙石是硅酸钙水化产物的一种,具有容重小、导热系数低、耐高温和强度大等特点[24-25],大量研究表明,雪硅钙石有稳定重金属的效果[22,26].Li等发现硅酸钙水化产物能够很好的固化Pb、Cd等重金属[27].雪硅钙石的晶胞结构如图5所示,雪硅钙石是一种层状晶体,上下两层为硅氧四面体组成的链状结构,晶胞边界上的Ca原子与硅氧四面体形成离子键而极难被重金属离子置换,而夹层中间存在着游离的 Ca2+和水分子[28-30],随着水分子的进出,外界的重金属离子能够进入雪硅钙石晶格内部,将Ca2+置换出来,从而吸附重金属[31].

图5 雪硅钙石晶体结构[29]及其重金属吸附机理Fig.5 The structure of the tobermorite crystal[29] and its heavy metal adsorption mechanism
2.4 飞灰水热产物形成机理
根据 2.1的结果分析,两种飞灰掺杂后形成CaO-Al2O3-SiO2体系,根据 2.2中的 XRD分析结果(图3),这5组水热反应后均形成了水钙铝榴石,F7G3、F6G4有雪硅钙石形成,在CaO-Al2O3-SiO2体系下Al会替代雪硅钙石中的 Si原子而形成 Al型雪硅钙石[32-33],在本实验中,并未形成Al型雪硅钙石,认为是在水热过程中先形成水钙铝榴石,由水钙铝榴石结构式可知,形成水钙铝榴石时所需 Al2O3比 SiO2要多,而由表1可知原始飞灰中的Al2O3比SiO2少,生成水钙铝榴石后飞灰中的 Al2O3消耗殆尽.另外,F7G3、F6G4中的雪硅钙石以纳米晶须的形式包裹在飞灰外部,也可佐证先形成水钙铝榴石最后生成雪硅钙石.据此,对这一微观过程进一步分析,高温下,飞灰中的Al2O3和 SiO2会缓慢溶解于碱性溶液中,经过缩合反应形成水钙铝榴石凝胶[34],由于水钙铝榴石的溶解度很小,其凝胶很快达到饱和析出形成水钙铝榴石晶核凝结于飞灰表面,凝胶的析出又促进了Si、Al的溶解,不断重复这一过程最后形成水钙铝榴石晶体.剩余的CaO与SiO2,二者在适当条件下能够继续合成雪硅钙石,生成雪硅钙石理想的 Ca/(Si+Al)值为 0.85[35],在F5G5、F4G6、F3G7中,由于掺杂的炉排炉飞灰较多而流化床飞灰较少,所以CaO含量较多而Si较低,导致 Ca/Si过高,无法继续合成雪硅钙石;而在 F7G3、F6G4中,Ca/Si的比值较为合适,溶解的SiO2会形成非晶态水化硅酸钙,进而合成雪硅钙石晶核[36],形成晶核后,雪硅钙石凝胶会选择在晶格能最大的晶面沉积,晶核沿着该晶面径向生长,最后在飞灰表面均匀的形成雪硅钙石晶须,流程如图6所示.
2.5 水热反应对重金属浸出毒性的影响
水热反应主要关注的是滤液中重金属含量以及水热后固体物中的重金属浸出特性.主要以Pb、Zn、Cu、Cd、Cr这5种飞灰中重金属作为研究对象.
水热反应后液相中的重金属含量如表 4,除F3G7与F4G6中有大量的Pb溶解于液相中,重金属在水热反应后均能很好沉淀在固相中.根据2.2的分析,飞灰中的可溶性氯盐溶解于液相中,废液中虽然重金属浓度低,但固液比 1:10所产生的大量的高盐废水如何处理是难题.合理增加固液比是一个较为可行的应用方案,但固液比过高会影响重金属浸出毒性,还需考虑固液比、相应的浸出毒性和高盐废水处理成本等问题.

图6 飞灰水热产物形成机理Fig.6 Mechanism of hydrothermal synthesis from fly ash
水热产物的重金属浸出毒性结果如表 5所示,F7G3、G6G4与F5G5对重金属Pb、Cr的固化效果很好,但是 Cd浸出量仍然超标,而 F4G6与 F3G7中Pb由于已经向液相中转移,故浸出量也很小,而F3G7的掺比下重金属浸出毒性都符合填埋标准.
为考察水热反应对飞灰中的重金属浸出毒性的影响,将表5中水热反应后飞灰重金属浸出毒性与表2中原始飞灰浸出毒性进行对比,由于 F4G6、F3G7这两组的水热反应滤液中均含有较高浓度的Pb以及少量的Zn、Cu,故不进行比较,F7G3、G6G4与F5G5反应后的液相中重金属浓度极低,重金属均保留在反应后的固相中,为了浸出毒性的比较更加直观,采用浸出率衡量水热反应对重金属浸出毒性的影响,浸出率计算公式如下:

式中:n为浸出率,%;t为浸出毒性,mg/kg; H为飞灰重金属浓度,mg/kg.

表4 飞灰水热反应后液相中的重金属含量(mg/kg)Table 4 Heavy metal content in liquid phase of fly ash after hydrothermal reaction (mg/kg)

表5 飞灰水热反应产物的重金属浸出毒性(mg/kg)Table 5 Heavy Metal Leaching Toxicity of Fly Ash Hydrothermal Reaction Products (mg/kg)
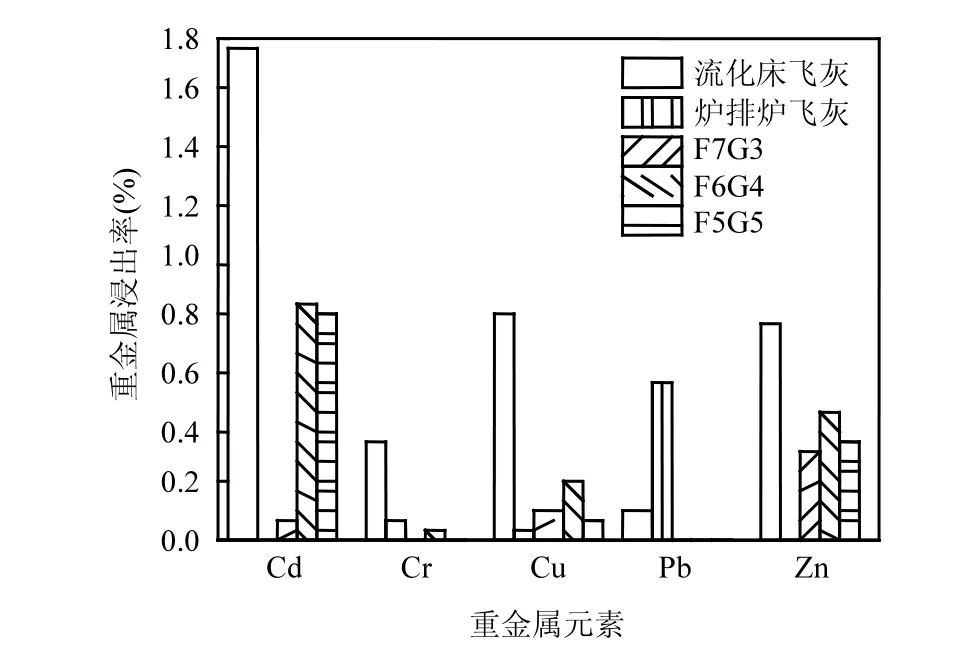
图7 原始飞灰及其水热产物的浸出率Fig.7 Leaching rate of raw fly ash and its hydrothermal products
所得结果如图7所示,与炉排炉飞灰相比,水热反应后的飞灰除了Pb的浸出率有了明显的降低, Cd、Cr、Cu、Zn的浸出率都有小幅度增大,这是因为,根据图1,炉排炉飞灰中含有较多的Ca(OH)2、CaClOH而呈现碱性, Cd、Cr、Cu、Zn等会与羟基结合沉淀,炉排炉飞灰 Cd、Cr、Cu、Zn的浸出率接近零.与流化床飞灰的重金属浸出率相比,水热反应后的飞灰 5种重金属的浸出率均有明显的降低,其中 F7G3组合的浸出率相较于F6G4、F5G5有明显的降低,其对Cd、Cr、Cu、Pb、Zn的浸出率分别为0.073%、0.006%、0.107%、0.006%、0.326%,说明水热反应过程中合理的掺入炉排炉飞灰对降低流化床飞灰的重金属浸出毒性有显著效果.
3 结论
3.1 两种飞灰直接混合不需要外加任何添加剂的情况下就合成了水钙铝榴石和雪硅钙石,合成的雪硅钙石以纳米晶须的形态包裹住飞灰.
3.2 根据雪硅钙石晶体结构,夹层中间存在着游离的Ca2+和水分子,随着水分子的进出,外界的重金属离子能够进入雪硅钙石晶格内部,将Ca2+置换出来,从而吸附重金属.
3.3 飞灰在水热反应过程中,会先形成水钙铝榴石,在Ca/Si适宜的条件下,会继续反应形成雪硅钙石.
3.4 采用重金属浸出率对飞灰浸出毒性进行量化评估,水热反应后的飞灰重金属浸出率相比流化床飞灰均有明显的降低,当水热反应添加的流化床飞灰与炉排炉飞灰的质量比为7:3时,水热后的Cd、Cr、Cu、Pb、Zn的浸出率最低,浸出率分别为0.073%、0.006%、0.107%、0.006%、0.326%.
