香兰素在大孔吸附树脂上的吸附平衡、动力学及动态吸附过程
2018-07-24季迎春吴菁岚周精卫应汉杰
季迎春,吴菁岚,周精卫,庄 伟,应汉杰
(南京工业大学 生物与制药工程学院 江苏先进生物与化学制造协同创新中心,江苏 南京 211800)
香兰素(vanillin),又称香兰醛、香草醛,是一种广谱型高档香料[1]。在香料中,香兰素系列化合物是使用量最大的品种之一,同时,它还是一种重要的化学中间体和工业原料,用于制造L-多巴、甲基多巴等,也用作镍和铬金属电镀光亮剂[3-5]。目前,香兰素的主要生产方法为乙醛酸法和木质素法[2]。木质素法已经受到了越来越多的人关注,是因为此法具有原料廉价易得且可再生、操作工艺简单、操作方便及条件易于控制等优点。但木质素法生产香兰素会产生大量的副产物[6],这些副产物极大地增加了香兰素后分离的成本和难度。因此,如何采用低能耗、绿色环保的手段分离获取香兰素产品,成为目前研究的重点。
近几年,国内外研究香兰素分离提取方法主要有:溶剂萃取法[7]、超临界CO2萃取法[8]、膜技术提取法[9-10]和离子交换法及吸附法[11-12]等。比较上述几种分离方法发现:溶剂萃取法虽然具有提取纯度高、费用低廉等优点,但其操作过程中引入大量有机溶剂,污染环境,不利于工业化放大生产。超临界CO2萃取法的设备一次性投入较大,且实验需在高压下进行。采用膜技术从木质素氧化废液中分离提取香兰素,氧化液中悬浮物会堵塞膜孔道,减少膜使用寿命,且膜需要频繁清洗。离子交换法提取香兰素具有交换容量大、吸附选择性好等优点,但离子交换树脂再生困难,并产生大量废酸废碱。吸附法被认为是一种低能耗且绿色环保的方法[13],该法具有操作方便、成本低、效率高和吸附速率快等优点。Soto等[14]采用活性炭吸附香兰素,结果发现,虽然活性炭对香兰素有较大的吸附量,但其解吸再生较困难,并不适用于实际操作。Zabkova等[15]采用SP206树脂吸附分离香兰素,并研究了pH对香兰素上柱穿透曲线的影响,该树脂对香兰素最大吸附量为114.6 mg/g。Samah等[16]采用大孔树脂H103吸附香兰素,并研究香兰素在H103树脂上的吸附热力学和动力学,树脂对香兰素最大吸附量为73 mg/g。这两种树脂对香兰素的吸附量均较小。
因此,本文中,笔者的主要目的是筛选出一种对香兰素吸附量大、吸附速率快的树脂(大孔吸附树脂LX-02),并研究香兰素在LX-02树脂的吸附平衡和吸附动力学以及动态吸附和解吸过程。
1 材料与方法
1.1 试剂与仪器
香兰素(99%)、NaOH(98%),阿拉丁试剂(上海)有限公司;大孔吸附树脂(LX-02、MR-06、AX-10、AX-16和AX-10,前2个为非极性树脂,后3个为极性树脂),南京工业大学国家生化中心(LX-02树脂骨架为苯乙烯-二乙烯苯,比表面积为971.94 m2/g,孔容为1.714 cm3/g,树脂表面以疏水性官能基团为主);Agilent 1200型高效液相色谱仪(HPLC),美国安捷伦公司;欧洲之星20型悬臂式搅拌机,德国IKA公司;MQD-A2型振荡培养箱,上海旻泉仪器有限公司;自动滴定仪,瑞士万通有限公司;BSZ-100型自动部分收集器,上海沪西分析仪器厂有限公司;DC-2010型低温恒温槽,南京文尔仪器设备有限公司;玻璃夹套色谱柱,中国药科大学玻璃仪器厂。
1.2 树脂筛选
称取0.4 g不同型号的树脂于50 mL三角瓶中,分别加入25 mL初始质量浓度为1.5 g/L的香兰素溶液。将三角瓶放置于恒温摇床中,转速设定为150 r/min,时间24 h,温度为298.15 K。待吸附平衡后,采用HPLC测定香兰素溶液的平衡浓度,根据式(1)计算不同型号树脂对香兰素的吸附量。
(1)
式中:qe为平衡吸附量(mg/g);ρ0为香兰素溶液的初始质量浓度(g/L);ρe为香兰素溶液的吸附平衡质量浓度(g/L);V为溶液的体积(mL);m为树脂的质量(g)。
1.3 pH对香兰素吸附的影响
称取0.4 g LX-02树脂于50 mL三角瓶中,分别加入25 mL初始质量浓度均为1.5 g/L的不同pH的香兰素溶液。采用NaOH调节香兰素溶液的pH分别为5.01、6.04、7.02、8.04、9.04、10.07、11.02、12.01和13.01,(香兰素溶液初始pH为4.52)。将三角瓶放置于恒温摇床中,转速设定为150 r/min,时间24 h,温度为298.15 K。待吸附平衡后,采用HPLC测定香兰素溶液的平衡浓度,根据式(1)计算不同pH下香兰素的平衡吸附量。
1.4 香兰素吸附平衡实验
香兰素吸附等温线[17]分别在温度为298.15、313.15和328.15 K条件下测定。配制不同初始质量浓度的香兰素(ρ0,0.5~5.0 g/L)水溶液,精确称取湿树脂0.4 g,置于50 mL锥形瓶中,采用移液管加入25 mL不同浓度的料液,封口膜封紧瓶口。锥形瓶置于摇床,摇床转速150 r/min,时间24 h。空白样也被制备并分析。采用高效液相色谱仪(HPLC)检测香兰素浓度,考察树脂平衡吸附容量qe。
1.5 香兰素吸附动力学试验
精确称取湿树脂4.0 g,置于500 mL三口烧瓶中,加入400 mL料液。将三口烧瓶置于恒温水浴槽中,搅拌转速为250 r/min,进行吸附动力学试验。样品每隔一定时间通过注射器取出,树脂吸附量通过式(2)计算。以时间t为横坐标,不同时刻的吸附量为纵坐标,绘制香兰素动力学曲线。本文研究不同香兰素初始质量浓度(0.5、1.5和3.0 g/L)以及不同温度(298.15、313.15和328.15 K)对香兰素吸附动力学的影响。
(2)
式中:qt为t时刻香兰素吸附量(mg/g);ρt为t时刻香兰素溶液的质量浓度(g/L)。
1.6 动态柱吸附和解吸实验
吸附实验:精确称量18 g湿树脂,采用湿法装柱,将树脂加入带有夹套的玻璃吸附柱中,吸附柱内部直径1.46 cm,长度20 cm,夹套内可通过循环水进行控温。利用蠕动泵在色谱柱出口控制流出液流量,并采用分布收集器定量收集样品流出液。待树脂对香兰素吸附达到平衡时,即柱出口香兰素浓度ρv(ρv(g/L)表示流出液体积为V时的香兰素浓度)等于香兰素溶液初始浓度,吸附试验结束。不同时间(体积)段流出液浓度可通过HPLC测定。以流出体积V(mL)为横坐标,香兰素流出液浓度与初始溶液浓度的比值ρv/ρ0为纵坐标,绘制香兰素在树脂柱上的穿透曲线。考察温度、流速对香兰素动态柱吸附实验的影响。
解吸实验:流量和香兰素质量浓度分别为0.5 mL/min和0.5 g/L。部分收集器于色谱柱出口收集解吸流出液,采用HPLC检测解吸流出液中香兰素浓度。以流出体积V为横坐标,香兰素流出液与初始溶液浓度ρv/ρ0为纵坐标绘制解吸曲线。考察NaOH(0.05 mol/L,pH=12.45)和热水(温度为328.15 K)两种解吸剂对香兰素解吸效率的影响,并根据解吸剂的解吸速率和使用量,筛选出一种合适的解吸剂。
1.7 香兰素分析检测方法
香兰素分析检测方法由文献[18]改进而得。采用高效液相色谱仪(Agilent 1260)检测香兰素浓度。色谱柱为Agilent ZORBAXSB-Aq柱(250 mm×4.6 mm,5 μm),流动相为0.3%醋酸-甲醇(体积比为70∶ 30),柱温323 K,流速0.8 mL/min,进样量10 μL,紫外检测波长280 nm,等梯度洗脱。
2 结果与讨论
2.1 香兰素吸附介质筛选
考察各种型号的树脂对香兰素的吸附情况,结果如图1所示。由图1可以看出,疏水性树脂(LX-02、MR-06)对香兰素的吸附量大于亲水性树脂,这是由于香兰素结构中含有疏水性的苯环,易与疏水性树脂通过疏水作用力相结合。此外,LX-02树脂对香兰素的吸附量大于MR-06树脂,这是因为LX-02树脂比表面积比MR-06树脂(比表面积为750.1 m2/g)大,从而有更多的活性吸附位点可以吸附香兰素。因此,接下来的香兰素吸附平衡和吸附动力学以及动态吸附和解吸试验均在LX-02树脂上进行。

图1 不同树脂对香兰素的吸附量Fig.1 Adsorption capacity of vanillin onto different resins
2.2 pH对香兰素吸附的影响
考察在不同pH条件下香兰素在LX-02树脂上的吸附量,结果见图2。由图2可知:树脂对香兰素的吸附量与溶液pH成反比,其原因在于,随着pH增加,分子型香兰素逐渐转化为离子型香兰素,而离子型香兰素在LX-02树脂上基本不吸附,当pH调至13时,香兰素在LX-02树脂上的吸附量仅为1.46 mg/g。因此,树脂吸附香兰素的最适pH为4.5。

图2 pH对香兰素在LX-02树脂上吸附量的影响Fig.2 Effect of pH on adsorption capacity of vanillin onto resin LX-02
2.3 香兰素吸附等温线
2.3.1 吸附等温线模型
考察不同温度下香兰素吸附等温线[19-20],并采用Langmuir和Freundlich模型进行拟合。
Langmuir吸附等温线模型如式(3)所示。
(3)
式中:qe为平衡吸附量(mg/g);qm为饱和吸附量(mg/g);KL为Langmuir方程参数(L/g),与吸附自由能相关;ρe为吸附平衡时溶质的质量浓度(mg/mL)。
Freundlich吸附等温线模型如式(4)所示。
qe=KFρe1/n
(4)
式中:KF为Freundlich常数((mg/g)(mL/mg)1/n),表明吸附质的吸附能力;n是Freundlich指数,表明吸附质与吸附剂间的亲和力,当n>1(1/n<1)表明该吸附过程是优惠性吸附过程。
2.3.2 温度对香兰素吸附等温线的影响
采用Langmuir和Freundlich模型对香兰素的吸附等温线实验数据进行拟合,结果如图3所示,模型参数和相关系数R2列于表1。由图3及表1拟合结果可以看出,Freundlich模型能够更好地拟合不同温度下香兰素在LX-02树脂上的吸附等温线(R2=1)。

图3 不同温度下香兰素在LX-02树脂上的吸附等温线Fig.3 Adsorption isotherm of vanillin onto resin LX-02 at different temperature
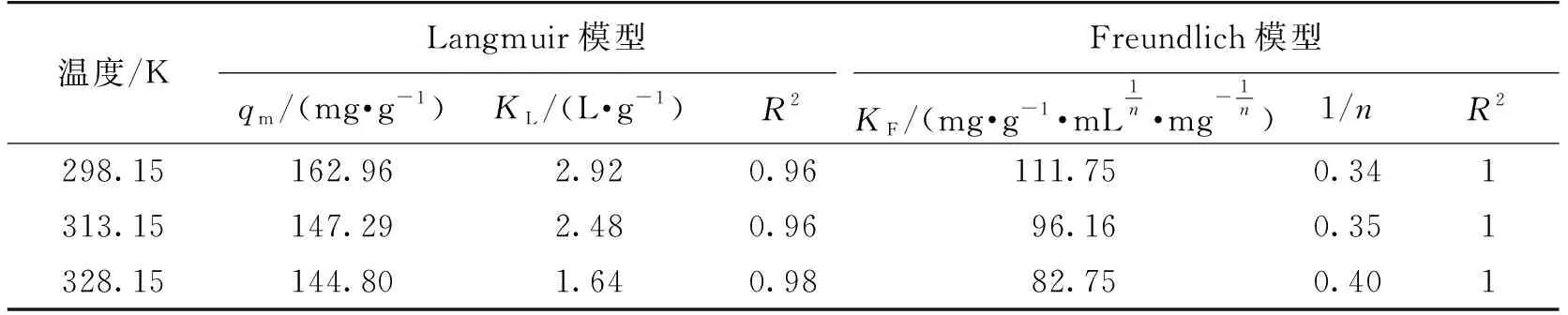
表1 香兰素在LX-02树脂上的吸附平衡参数
由图3可知:LX-02树脂对香兰素的吸附量随着温度的升高而降低,表明香兰素在树脂上的吸附是放热过程[21-22]。由表1可知,LX-02树脂对香兰素最大吸附量为162.96 mg/g,比文献中所报道的大孔吸附树脂H103高出1.2倍。Freundlich模型的常数KF值也随着温度的升高而减小,表明树脂对香兰素的吸附能力随着温度的升高而降低。此外,在不同温度下,Freundlich指数1/n值均小于1,表明香兰素在LX-02树脂上的吸附是优惠性吸附过程[23-24]。
2.4 香兰素吸附动力学
2.4.1 吸附动力学模型
吸附动力学描述了时间t与树脂吸附量的关系。考察不同温度、不同初始浓度条件下香兰素吸附动力学,并通过准一阶动力学模型(pseudo-first model)与准二阶动力学模型(pseudo-second model)对香兰素的吸附动力学进行拟合[17]。
准一阶动力学模型如式(5)所示。
qt=qe(1-e-k1t)
(5)
式中:k1为准一阶速率常数(min-1);qe为达到吸附平衡时的香兰素吸附量(mg/g);qt为t时刻香兰素的吸附量(mg/g);t为吸附所用时间(min)。
准二阶动力学模型如式(6)所示。
(6)
式中,k2为准二阶速率常数(min-1)。
2.4.2 温度、浓度对香兰素吸附动力学的影响
采用准一阶与准二阶动力学模型拟合香兰素在树脂LX-02上的吸附动力学,并研究不同温度和初始浓度对香兰素吸附动力学的影响,结果如图4所示,模型参数和相关系数R2列于表2。由图4和表2的拟合结果可以看出,准二阶动力学模型可以更好地与香兰素吸附动力学数据相吻合(R2>0.99)。
由图4可以看出,树脂对香兰素的吸附在20 min左右即可达到吸附平衡,表明香兰素在树脂上的传质速率较快。图4(a)可以看出,树脂对香兰素的吸附量随着香兰素初始浓度的增加而增加。由表2可知,吸附速率常数k2也随香兰素浓度的提升而增加。这是因为香兰素初始浓度的提高,增大了香兰素在树脂上的传质推动力[21],导致吸附速率变快。由图4(b)可以看出,树脂对香兰素的吸附量随着温度的升高而降低,这与上述的香兰素吸附等温线结果相一致。此外,由表2还可知,吸附速率常数k2随着温度的提升而增加。这是因为,温度升高促进了香兰素分子运动加快,并降低了溶液相和树脂相的黏度,从而导致树脂对香兰素的吸附速率加快[25]。

图4 不同初始浓度和温度条件下香兰素在LX-02树脂上吸附动力学Fig.4 Adsorption kinetics of vanillin onto resin LX-02 at different initial concentration(a)and temperature(b)

温度/K初始质量浓度/(g·L-1)准一阶动力学模型准二阶动力学模型k1/(102min-1)R2k2/(102min-1)R2298.150.50.350.950.007 70.99298.151.50.430.970.0830.99298.153.00.60.970.008 70.99313.151.50.650.970.014 70.99328.151.50.910.970.0240.99
2.5 香兰素动态吸附与解吸过程研究
2.5.1 香兰素动态吸附过程
考察不同温度和不同流量条件下,香兰素(0.5 g/L)在LX-02树脂上的动态吸附过程,采用穿透曲线进行描述,结果如图5所示。由图5可以看出:香兰素穿透曲线随着温度的升高而提前,这是由于香兰素在树脂上的吸附是一个放热过程,温度升高会使树脂对香兰素的吸附量下降,从而导致香兰素穿透曲线提前[25]。同时,可以发现流量对穿透曲线的影响是流速增加、穿透点提前,但流速对香兰素在树脂上的吸附量并没有显著的影响,这是因为吸附量是由吸附等温线决定的,不受流速影响[11]。在实际生产中,总是希望树脂对香兰素的吸附量尽可能大,吸附时间尽可能短。因此,筛选出香兰素最佳上柱条件为温度298.15 K,流量2 mL/min。

图5 温度(a)和流量(b)对香兰素在LX-02树脂上穿透曲线的影响Fig.5 Effects of temperature(a)and flow rate(b)on the breakthrough curves of vanillin onto resin LX-02
2.5.2 香兰素动态解吸过程
在研究了香兰素动态解吸过程的基础上,考察不同解吸剂对香兰素解吸曲线的影响,根据前面不同温度下香兰素吸附等温线实验和pH对香兰素吸附的影响可知,通过提升温度和采用NaOH调节pH的方式,均可以降低香兰素在树脂上的吸附量。因此,选用0.05 mol/L NaOH和328.15 K热水对香兰素进行解吸实验,流量为0.5 mL/min,结果如图6所示。由图6可以看出,0.05 mol/L NaOH解吸效果明显优于328.15 K热水。NaOH完全解吸所需体积为300 mL,其最高提浓倍数可达17倍,而328.15 K热水最高提浓倍数只达到香兰素原始浓度的2倍。采用NaOH解吸回收香兰素,收率为99.8%,而328.15 K热水解吸回收香兰素,收率仅为90%。且采用328.15 K热水解吸回收香兰素,耗时长,耗水量大。因此,选用0.05 mol/L NaOH作为最适解吸剂[15]。

图6 不同解吸剂对香兰素在LX-02解吸性能的影响Fig.6 Effects of eluents on the desorption performance of vanillin onto resin LX-02
3 结论
本文中,笔者筛选了一种合适的大孔吸附树脂LX-02用于香兰素的吸附分离。结论如下:
1)香兰素在树脂上的吸附随着pH增加而减少,最适pH为4.5。
2)香兰素吸附平衡实验表明,Freundlich模型可以更好地拟合香兰素吸附等温线,香兰素在树脂上的吸附量与温度成反比;动力学结果表明,香兰素吸附动力学曲线符合准二阶动力学模型,香兰素在树脂上的吸附速率较快,20 min内即可到达吸附平衡。
3)温度升高不利于香兰素在树脂上的动态吸附,而流量增加对香兰素的吸附影响不大,因此,选择最佳上柱实验温度和流量分别为298.15 K和2.0 mL/min,以0.05 mol/L NaOH为最适解吸剂。
