TCX化疗方案在进展期胃癌围手术期的应用研究
2018-07-10卢晓霞
卢晓霞 安 锋
胃癌是最常见的恶性肿瘤之一,其病死率居所有肿瘤的首位。以进展期胃癌(advanced gastric Cancer,AGC)为主,其比例高达80%。目前其治疗主要是胃癌根治术,但其术后5年生存率仅为30%~60%[1]。由于病灶转移范围广或浸润程度深,大部分患者术后容易复发,术后化疗对于延长患者生存时间也很有限。近年来提出局部可以切除或者潜在可以切除的进展期胃癌先给予术前化疗,在保证安全的前提下,通过术前化疗使原发病灶缩小、降低术前分期、减少肿瘤对周围组织的侵润,从而提高手术切除率、降低复发率、减少了术中出血量,缩短了手术时间,还可以为术后选择辅助化疗方案提供依据。目前局部进展期胃癌围手术期化疗的Ⅱ期、Ⅲ期临床研究还比较少,样本量小、研究终点短,对多种常用胃癌一线治疗方案也缺乏相互比较。本研究拟用大样本来研究围手术期化疗对局部进展期胃癌患者无病生存(DFS)和总生存(OS)的影响,比较直接接受手术和给TCX方案的新辅助化疗后其手术切除率、手术并发症、手术死亡率、无病生存、总生存和安全性,为以后胃癌病人如何进行正规化疗提供循证医学依据。
资料与方法
一、一般资料
本研究经我院医学伦理委员会批准,选取2012年9月至2014年9月我院手术前应用新辅助化疗的进展期胃癌患者98例为研究对象。诊断标准参照文献[2],同时满足以下入组标准:①经胃镜下活组织病检诊断胃癌;②根据术前胃镜、病检结果及CT等检查证实为进展期(Ⅲ、Ⅳ期)胃癌;③既往未行抗肿瘤治疗;④心、肝、肾及血液学检查大致正常,无化疗禁忌证;⑤Kamofsky评分>70分,预计生存期 >3个月;⑥年龄18~70岁;⑦已签署知情同意书。
所有患者均完成B超、CT、胃镜等辅助检查,胃镜确定肿瘤性质、部位,B超、CT观察病灶浸润范围、邻近脏器或其他部位淋巴结有无转移。98例患者随机分成两组,各49例。观察组男性38例,女性11例;年龄28~73年,平均(53.8±9.4)岁;病程 0.5 ~ 3.0 年,平均(0.7 ± 0.4)之间;肿瘤病理类型:印戒细胞癌2例,粘液腺癌4例,中分化腺癌26例,低分化腺癌17例;TNM分期:Ⅲa期14例,Ⅲb期26例,Ⅳ期9例。对照组男性35例,女性14例,年龄26~74岁,平均(51.3±9.5)岁;病程 0.5~2.0年,平均(0.6±0.3)年;肿瘤病理类型:印戒细胞癌3例,粘液腺癌4例,中分化腺癌27例,低分化腺癌15例;TNM分期:Ⅲa期26例,Ⅲb期20例,Ⅳ期3例。两组性别、年龄、病理分化程度、TNM分期等相比较,差异均无统计学意义(P>0.05),具有可比性。
二、治疗方法
1.观察组
观察组患者采用TCX方案:注射用盐酸吡柔比星40 mg/(m2·d) Ⅳ d1;顺铂 50 mg/(m2·d)静脉滴入,第 1 天;卡培他滨1 000 mg/m2早饭和晚饭后各口服1次,共服用14天;每3周为1周期。化疗2疗程后行肿瘤疗效评价,若符合手术条件者行胃癌根治术,术后行6周期化疗。
2.对照组
对照组若术前检查无禁忌,直接行胃癌根治术后行采用TCX方案化疗8周期。一般建议化疗前给予格拉司琼,可预防化疗时出现的恶心、呕吐症状,化疗期间要定期复查肝功、肾功、血常规等,如化疗期间出现白细胞明显下降,可给予重组人粒细胞集落刺激因子对症治疗。
三、评价标准
采用WHO实体瘤疗效标准[3],将疗效评价分以下四个等级:①完全缓解(CR),复查后瘤体完全消失,且>1个月无复发;②部分缓解(PR),瘤体最大直径和瘤体最大的垂直径之间的乘积减小>50%,且>1个月;③疾病稳定(SD),瘤体最大直径和瘤体最大的垂直径之间的乘积减小<50%或增大<25%,且>1个月;④疾病进展(PD):瘤体最大直径和瘤体最大的垂直径之间的乘积增大>25%。其中治疗有效率(RR)=(CR +PR)/n×100%;疾病的控制率(DCuR)=(CR+PR+SD)/n×100%。
化疗过称中出现的副作用参照WHO抗癌药物急性以及亚急性毒性反应分度标准[4]进行判断,可将其分为0、Ⅰ、Ⅱ、Ⅲ、Ⅳ度。
四、统计方法
运用统计软件SPSS19.0对数据进行处理。计量资料以x±s表示,采用t检验;计数据资料以%表示,采用χ2检验或Fisher精确检验。P<0.05为差异有统计学意义。
结 果
一、两组总疗效比较
观察组中CR 2例,PR 30例,SD 11例,PD 6例,治疗总有效率为65.3%,临床总控制率为87.8%,稍高于对照组,但差异无统计学意义,见表1。
二、观察组各期疗效对比
观察组49例患者中,有效率和控制率均Ⅲa期>Ⅲb期>Ⅳ期,见表2。
三、两组相关指标比较
观察组手术时间、术中出血量、术后6 d的白蛋白含量均优于对照组(P<0.05)。两组拆线时间、出院时间、住院费用比较,差异无统计学意义(P>0.05)。见表3。
四、两组不良反应对比
两组患者出现的毒副反应主要包括恶心、呕吐、白细胞降低、血小板降低、神经毒性、腹泻、黏膜炎、肝肾损伤,多为Ⅰ、Ⅱ级,Ⅲ级较少,未出现Ⅳ级不良反应,化疗过程中无化疗致死病例。两组不良反应发生率比较,差异均无统计学意义(P < 0.05),见表 4。
讨 论
近年来新辅助化疗受到国内外学者的密切关注,在2010年的《NCCN胃癌临床实践指南》中,建议对T2及高于T2的胃癌实施新辅助化疗,从而可提高进展期胃癌的手术切除率,达到根治效果,延长患者根治术后生的存时间。通过上述研究发现,胃癌术前给予新辅助化疗,TCX方案组治疗后其总有效率达到65.3%,临床的疾病总控制率达到87.8%,故可说明该化疗方案的总有效率较高,可以在手术前缩小瘤体与其邻近脏器及组织的侵犯范围,降低了组织与肿瘤反应性水肿,进而降低瘤体的分期,也可将手术前微小的转移灶的肿瘤负荷降低,提高术后化疗敏感度,明显降低了术后肿瘤的复发[6]。观察组患者在进行术前化疗后其根治性手术切除(RO切除)均明显高于对照组,说明术前化疗可提高进展期胃癌患者的根治性切除率、临床缓解率,与其他国内报道相符和[6-7]。对于TCX方案治疗过程中不敏感的患者,可以及时调整其化疗方案,从而避免术后的无效化疗。

表1 两组临床疗效比较 [n(%)]
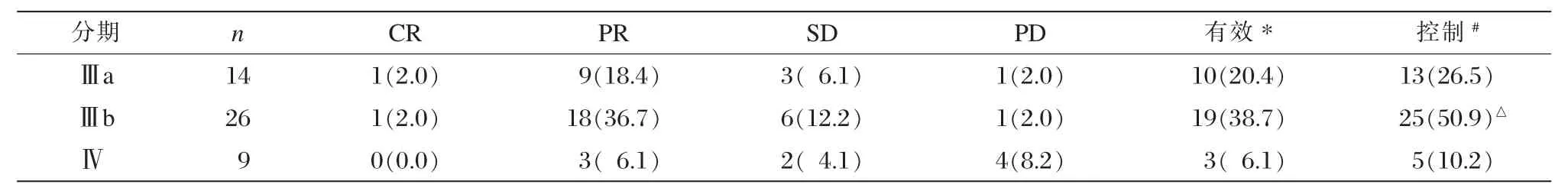
表2 观察组各分期患者临床疗效比较 [n(%)]
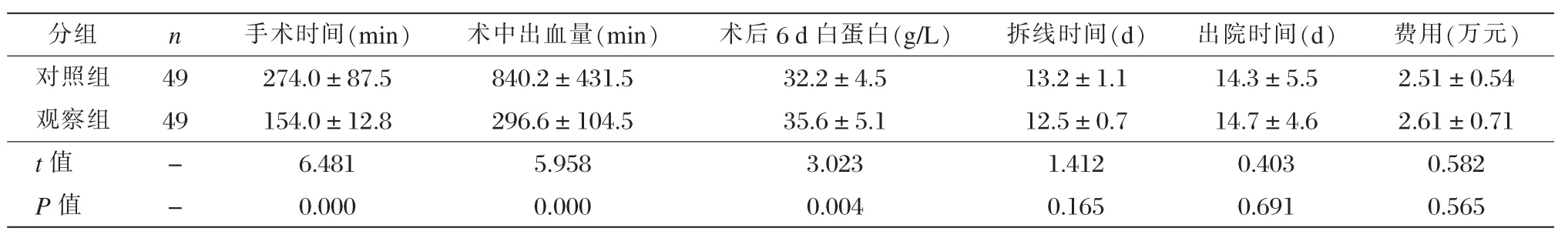
表3 两组相关指标比较 (x±s)
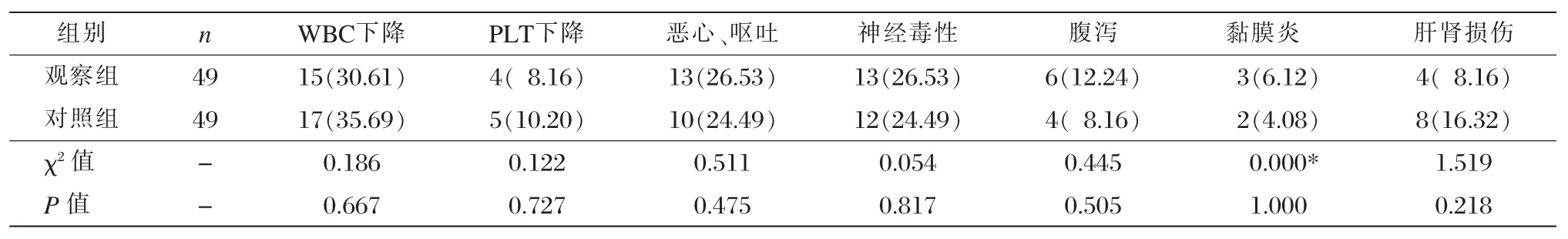
表4 两组不良反应发生情况比较 [n(%)]
目前,临床上对予晚期胃癌患者的化疗尚缺乏标准化的治疗指南,化疗药物的联合运用缺少规范。TCX方案组治疗总有效率为65.3%,临床总控制率为87.8%,也证实了该TCX方案的成效,同时患者出现的毒副反应也以Ⅰ、Ⅱ级为主,Ⅲ级较少,未发现Ⅳ级,各项不良反应在停药后均可恢复,这充分说明了其副反应轻的特点。
TCX方案在中晚期胃癌患者病情控制方面具有较为理想的效果,而且行TCX治疗的患者在手术并发症、住院时间和费用方面与单纯手术组比较无显著差异,而手术各项指标均明显优于对照组,说明新辅助化疗有利于减少手术损伤,改善患者的预后,值得临床推广应用。
[1]李子禹,季鑫,季加孚.新辅助化疗对胃癌手术并发症的影响[J].中国实用外科杂志,2013,33(4):275-278.
[2]所剑,王大广,何亮.胃癌的诊断进展[J].腹腔镜外科杂志,2012,17(9):641-645.
[3]Cunningham D,Okines A F,Ashley S.Cap ecitabine and oxaliplatin for advanced esophagogast ric cancer[J].N Engl JMed,2010,362(9):858-859.
[4]梁毅超,卿三华,丁卫星,等.全职场系膜切除术对比传统手术治疗直肠癌荟萃分析[J].中华胃肠外科杂志,2007,10(1):43-48.
[5]宋荣峰,万以叶,程楚.多西紫杉醇联合奥沙利铂及氟尿嘧啶治疗晚期胃癌的疗效分析[J].江西医药,2010,45:205-206.
[6]汪劭婷,朱朝晖,李小毅.胃癌新辅助化疗疗效临床评价方法及进展[J].中国普外基础与临床杂志,2010,17(2):200-204.
[7]Dugo D,Persiani R,Zoccali M,et a1.Surgical issues after neoadjuvant treatment for gastric cancer[J].Eur Rev Med Pharmacol Sci,2010,14(4):315-319.
