广西产多花黄精不同炮制工艺研究
2018-06-26
广西中医药大学药学院,广西 南宁 530000
黄精为合百科植物滇黄精(PoιygonatumkingianumCoLL.et HemsL.)、黄精(PolygonatumsibiricumRed.)或多花黄精(PolygonatumcyrtonemaHua.)的干燥根茎。黄精属于药食两用中药材,其化学成分主要为低聚糖、单糖和多糖,多种氨基酸、多种甾体皂苷和人体必需微量元素、生物碱等[1]。黄精历代入药生制兼用,但传统以黄精生用“刺人咽喉”,故多炮制后入药[2]。黄精炮制渊源已久,历代以来黄精炮制方法有:九蒸九曝法、蔓荆子水蒸法、酒熬法、焙制法、黑豆煮法、酒蒸法、乳浸晒法、熟地制等[3]。目前对黄精的研究大多数为黄精及滇黄精,炮制方法为酒制法,而主产在广西的多花黄精的研究还处于空白,据笔者调查,广西民间百姓多用黑豆炮制法炮制生黄精,而黑豆制法也分为黑豆汁制、黑豆、蜜、酒制,黑豆、生姜、蜜制等。笔者主要研究广西产多花黄精的酒制、黑豆制、清蒸、蔓荆子制、熟地制等不同炮制工艺,旨在为广西产多花黄精炮制工艺提供理论参考,为今后黄精黑豆制法规范化研究提供参考依据。
1 仪器与材料
1.1 仪器 UV-L5紫外可见分光光度计(上海仪电分析仪器有限公司),KQ5200B型超声波清洗器(昆山市超声仪器有限公司),DFT-200C万能高速粉碎机(温岭市林大机械有限公司),HH-S6数显恒温水浴锅(金坛市医疗仪器厂),SHB-B95型循环水式多用真空泵(郑州长城科工贸有限公司),分析天平(赛多利斯科学仪器(北京)有限公司)。
1.2 材料 人参皂苷Rb1(批号:wkq16060402,四川省维克奇生物科技有限公司),无水葡萄糖(批号wkq16082202,四川省维克奇生物科技有限公司),其余试剂均为分析纯。
2 方法与结果
2.1 样品的炮制与制备
2.1.1 生黄精 取黄精500 g,除去杂质,洗净,切厚片,晒干[4]。
2.1.2 九蒸九曝法制黄精 取黄精500 g,除去杂质,洗净。①拌黄酒:与适量(约10 %用量)黄酒与净黄精拌匀,并闷润至酒吸尽。②第1次蒸制、晒干:要求第1次“蒸至黄精中央发虚为度”(蒸制过程中注意收集黄精汁),取出“晒至外皮微干”,然后将黄精拌入黄精汁和适量黄酒,并“闷润至辅料吸尽”。③反复蒸制、晒干:按第1次蒸制、晒干方法;再蒸,晒至外皮微干,再拌入黄精汁,适量黄精,如此反复,蒸制晒8次。第2次至第8次制需要使用黄酒的70 %用量。④第9次蒸制、晒干:最后将剩余(20 %用量)黄酒及黄精汁一起拌入,“蒸至外表棕黑色,有光泽,中心深褐色,质柔软,味甜为度”;最后晒至八成干,然后切成片状[5-6]。
2.1.3 黑豆制黄精 取黄精500 g,除去杂质,洗净,加米泔水泡透心,淘净,取黑豆100 g熬取浓汁,与黄精共入锅中,加水与药平;煮沸后,用微火煮至微干,取出,筛去黑豆,晒至半干,又入蒸锅蒸至上气,取出日晒夜露,隔天又蒸至上气,再晒再露,每次蒸前,加入前次的蒸出液于盛装器皿中与黄精一起蒸,反复5次,晒干[7]。
2.1.4 黑豆、蜜、酒制黄精 取黄精500 g,除去杂质,洗净,浸泡2 d,每日换水1次,取出。取黑豆50 g水煮,取汁,与黄精合煎12 h,取出,晒至半干,再加熟蜜25 g及白酒25 g,共兑化拌匀后,蒸24 h,蒸至黑色,无麻味,晒干,即可[7]。
2.1.5 黑豆、生姜、蜜制黄精 取黄精500 g,除去杂质,洗净,加水泡透后,再加水煮沸,去水,加生姜250 g,黑豆50 g煮2 h,晒半干,加蜂蜜75 g与水拌匀,蒸至黑亮为度,取出,晒干[7]。
2.1.6 熟地制黄精 取黄精500 g,除去杂质,洗净,切厚片,蒸至略带黑色,晒半干,露一夜。如此反复3次,至第4次与熟地膏120 g拌匀,润一夜,次日蒸至里面黑透,再晒、露一次,晒干[7]。
2.1.7 酒制黄精 取黄精500 g,除去杂质,洗净,加酒拌匀,置蒸笼内,密闭,隔水加热蒸至黑透,取出,稍晾,晒干[7]。
2.1.8 清蒸黄精 取黄精500 g,除去杂质,洗净,蒸6 h,晒八成干,加蒸出液浸润,再蒸6 h,至内心成黑色,晒半干,再加蒸出液拌匀,晒至六成干,在闷润均匀。蒸格上垫编织袋,蒸一夜,闷一夜(12 h),次日取出剖视,以内外发黑为度,切片,晒干[7]。
2.1.9 蔓荆子制黄精 取黄精500 g,除去杂质,洗净,置适宜的容器内,加入蔓荆子汁及适量水拌匀,浸润过夜,置蒸制容器内蒸24 h,取出,晒干[7]。
2.2 浸出物的含量测定 取粉碎过筛后的黄精样品4 g,精密称定,按2015版《中国药典》四部附录通则2201项下热浸法[8],用稀乙醇、蒸馏水作溶剂,测定醇溶性浸出物、水溶性浸出物,结果见表1。
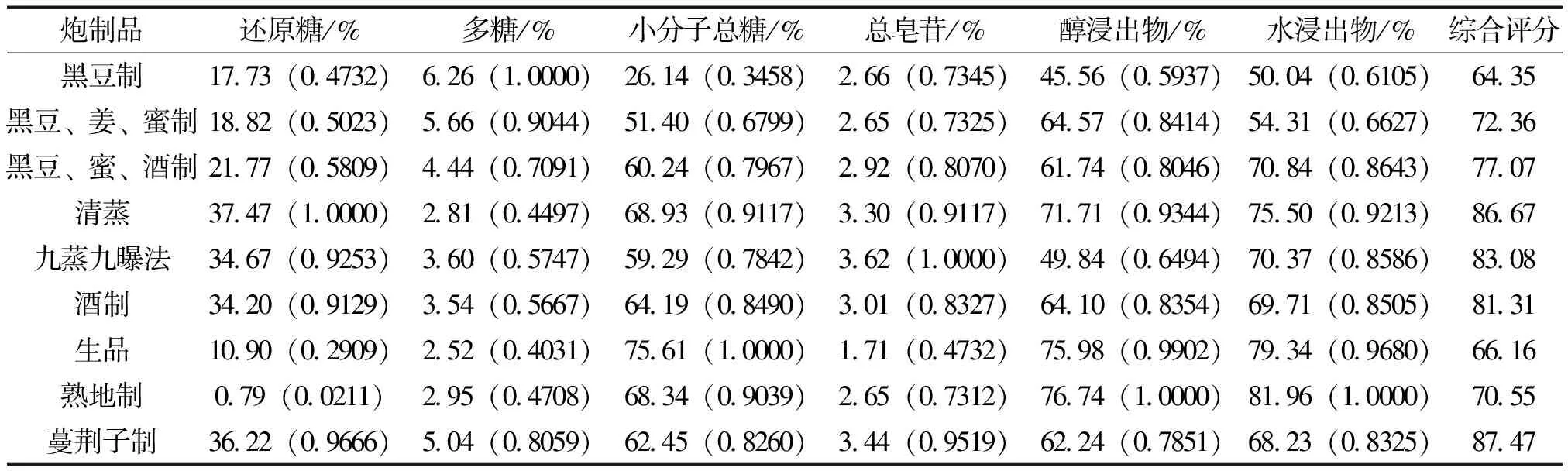
表1 多花黄精不同炮制品糖类成分含量测定结果 (n=3)
注:括号内为归一化处理。
2.3 供试品溶液的制备 取黄精样品各200 g,60℃干燥至恒重,粉碎,过80目筛,备用。取黄精样品粉末各1.00 g,精密称定,置圆底烧瓶中,加80%乙醇100 mL,水浴回流提取1 h,趁热过滤,滤渣用80 %乙醇洗3次,每次10 mL,取滤液,挥尽乙醇,转移至250 mL容量瓶中,加水至刻度,摇匀后用于小分子总糖和还原糖含量测定[1]。将药渣与滤纸置圆底烧瓶中,加蒸馏水100 mL,水浴加热回流提取1 h,趁热过滤,滤渣用水洗3次,将滤液转移至250 mL容量瓶中,加水至刻度,用于总多糖的含量测定[1]。
2.4 还原糖的含量测定
2.4.1 葡萄糖对照溶液的制备 取经105℃干燥至恒重的无水葡萄糖对照品55.0 mg,精密称定,置50 mL容量瓶中,加水稀释至刻度,摇匀,即得[1]。
2.4.2 DNS溶液的配制 取0.650 g 3,5-二硝基水杨酸,精密称定,加水50 mL溶解,转移至100 mL棕色容量瓶中,加入32.5 mL的2 mol/mL的NaOH溶液,再加入4.5 g丙三醇,加水至刻度,摇匀,即得[9]。
2.4.3 还原糖标准曲线的制备 精密量取葡萄糖对照品溶液0.2、0.4、0.6、0.8、1.0、1.2 mL,分别置10 mL具塞刻度试管中,各加水至4 mL,再各加入5 mL DNS溶液,摇匀后置沸水浴中加热6 min,冰浴冷却至室温,加水至刻度,以空白管为对照,照紫外-可见分光光度法(通则0401),在540 nm处测定吸光度[9-10]。以吸光度(A)为纵坐标,浓度(μg/mL)为横坐标进行回归处理,得回归方程:Y=0.0067X+0.0353(r=0.9997),表明无水葡萄糖对照品溶液在22~132 μg/mL范围内具有良好的线性关系,用于DNS法测定还原糖含量。
2.4.4 样品的测定 精密量取“2.3”项下方法制备的供试品溶液各1.0 mL稀释到50 mL,精密量取4 mL,分别置10 mL具塞试管中,按照“2.4.3”项下方法自“再加入5 mL DNS溶液”起操作,测定吸光度,计算还原糖含量。结果见表2。
2.5 多糖、总糖的含量测定
2.5.1 苯酚溶液的制备 取2.5 g苯酚,精密称定,加水溶解并定容于50 mL棕色容量瓶中[10]。
2.5.2 多糖、总糖标准曲线的制备 精密量取葡萄糖对照品溶液1.0、2.0、3.0、4.0、5.0、6.0 mL,分别置于50 mL容量瓶中,加水至刻度,摇匀,然后分别精密量取上述稀释后的葡萄糖对照品溶液各1 mL,置10 mL具塞试管中,加水至2mL,摇匀,再加1 mL的5%苯酚溶液和7 mL浓硫酸溶液,混匀,静置5 min,水浴加热20 min,并与冷却至室温,以空白管为对照,照紫外-可见分光光度法(通则0401),在490 nm处测定吸光度[9-10]。以吸光度(A)为纵坐标,浓度(μg/mL)为横坐标进行回归处理,得回归方程:Y=0.0696X-0.0223(r=0.9998), 表明无水葡萄糖对照品溶液在2.2~13.2 μg/mL范围内具有良好的线性关系,用于苯酚-硫酸法测定多糖、总糖含量。
2.5.3 样品的测定 精密量取2.3项下方法制备的供试品溶液各0.5 mL,置10 mL具塞试管中,按照“2.5.2”项下方法自“加水至2 mL”起操作,测定吸光度,计算多糖含量,结果见表1。
精密量取2.3项下方法制备的供试品溶液各1.0 mL稀释到50 mL,精密量取1 mL,置10 mL具塞试管中,按照“2.5.2”项下方法自“加水至2 mL”起操作,测定吸光度,计算小分子总糖含量,结果见表2。
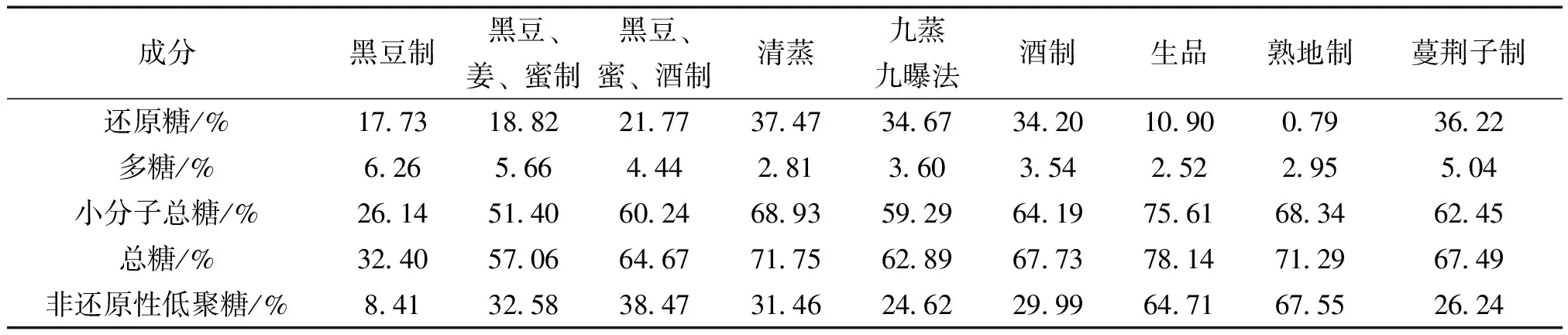
表2 多花黄精不同炮制品糖类成分含量测定结果 (n=3)
注:总糖=多糖+小分子总糖,非还原性低聚糖=小分子总糖-还原糖
2.6 总皂苷含量测定
2.6.1 标准曲线的制备 取人参皂苷Rb1对照品11.3 mg,精密称定,加甲醇溶解并定容于10 mL容量瓶中。取人参皂苷Rb1对照品溶液40、80、120、160、200 μL,置10 mL具塞试管中,挥尽溶剂,加0.2 mL 5%香草醛-冰醋酸溶液(新鲜配制),冰浴时加0.8 mL高氯酸,混匀,60℃水浴加热15 min,再冰浴2 min,加5 mL冰醋酸,混匀,静置5 min,照紫外-可见分光光度法(通则0401),在550 nm处测定吸光度[9]。以吸光度(A)为纵坐标,人参皂苷Rb1的质量(μg)为横坐标进行回归处理,得回归方程:Y=0.0039X+0.0305(r=0.9997),结果表明人参皂苷对照品溶液在45.2~226 μg范围内具有良好的线性关系。
2.6.2 样品的测定 取黄精样品粉末各1.00 g,精密称定,加14倍量水饱和正丁醇,40℃超声提取50 min,过滤,滤渣再提取1次,合并两次滤液,置25 mL容量瓶中,加水饱和正丁醇至刻度,摇匀[11]。取上述供试品溶液各100 μL,按照“2.6.1”项下方法自“置10 mL具塞试管中”起操作,测定吸光度,计算总皂苷含量。结果见表1。
2.7 数据处理及综合评分 以多花黄精不同炮制品的浸出物、还原糖、多糖、小分子总糖、总皂苷含量为指标,采用综合评分法评定。评分时以各指标的实验最大值作为参照,将数据进行归一化处理,再根据各指标的炮制工艺特性和成分重要性,给予糖类成分含量加权系数为0.4,总皂苷含量加权系数为0.3,浸出物加权系数为0.3,以行归一化处理后的数值加权求和,即得综合评分,其关系式为:(还原糖含量/还原糖含量最大值+多糖含量/多糖含量最大值+小分子总糖含量/小分子总糖含量最大值)/3×40+(总皂苷含量/总皂苷含量最大值)×30+(醇溶性浸出物含量/醇溶性浸出物含量最大值+水溶性浸出物含量/水溶性浸出物含量最大值)/2×30[1],结果见表1。
3 讨论
糖类是多花黄精中含量最高的成分,历代以来黄精炮制方法有九蒸九曝法、蔓荆子水蒸法、酒熬法、焙制法、黑豆煮法、酒蒸法、乳浸晒法、熟地制等,研究不同炮制工艺对广西产多花黄精成分含量的影响,优选出最佳炮制工艺,为广西产多花黄精制法规范化研究提供参考依据。且在2015版《中国药典》中对黄精药材及饮片检查项皆有要求“含黄精多糖以无水葡萄糖(C6H12O6)计,不得少于4.0%”[4]。不同炮制品与生品对照,多糖含量均有所增加,还原糖含量除熟地制多花黄精有所降低外,其它炮制品还原糖含量均有所增加;而不同炮制品的总糖、小分子总糖、非还原性低聚糖含量均比生品低。不同炮制工艺炮制的多花黄精之间的含量有所不同,其质量也存在一定差异,其功效是否也存在一定的差异,有待于进一步的深入研究。甾体皂苷是多花黄精的主要活性成分之一,初步研究表明,不同炮制工艺炮制的多花黄精之间的总皂苷含量差异不大,但与生品总皂苷含量对比,均比生品总皂苷含量高,其中以蔓荆子制多花黄精含总皂苷量最高。
采用多指标综合评价,蔓荆子制多花黄精得分最高为87.47,其它炮制品依次为:清蒸(86.67)>九蒸九曝法(83.08)>酒制(81.31)>黑豆、蜜、酒制(77.07)>黑豆、姜、蜜制(72.36)>熟地制(70.55)>生品(66.16)>黑豆制(64.35)。根据多花黄精有效成分及综合评分考察,蔓荆子制法为广西产多花黄精的最佳炮制工艺,其次为清蒸、九蒸九曝法,酒制。
广西产多花黄精经不同炮制工艺炮制后,其水溶性浸出物、醇溶性浸出、糖类、总皂苷等成分含量均与生品有所差异,其中以水溶性浸出物、醇溶性浸出物及非还原型低聚糖尤甚;且黑豆制多花黄精取自《现代中药炮制手册》记载,但其结果与生品比较,差异尤甚,故有待于对多花黄精炮制工艺做进一步的深入研究。
[1]戴万生,赵声兰,朱智芸,等.不同辅料蒸制对滇黄精化学成分含量的影响[J].云南中医中药杂志,2015,36(7):70-72.
[2]钟凌云,龚千锋,张的凤,等.黄精炮制研究现状分析[J].中药材,2007,30(12):1618-1621.
[3]吴建华,张涓,崔於.黄精炮制工艺的研究进展[J].川北医学院学报,2013,28(1):27-30.
[4]国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社.2015:306-307.
[5] 孟洗.食疗本草[M].北京:人民卫生出版社,1984.
[6]王怀隐.太平圣惠方(下)[M].北京:人民卫生出版社,1958:3022-3024.
[7]冉懋雄,郭建民.现代中药炮制手册[M]. 北京:中国中医药出版社,2002:428-429.
[8]国家药典委员会.中华人民共和国药典(四部)[S].北京:中国医药科技出版社,2015:202.
[9]张志军,孙伟,李永亮,等.3,5-二硝基水杨酸联合苯酚-浓硫酸法测定不同产地黄精中多糖含量[J].中国实验方剂学杂志,2012,18(6):106-109.
[10]蓝松.苯酚-硫酸法测定黄精多糖含量研究[J].广东化工,2013,40(80):132-133.
[11]秦枫,刘靖,陈玉勇,等.三七总皂苷含量测定方法及超声提取工艺研究[J].安徽农业科学,2008,36(8):3062-3064.
