过表达RSK4m1对人乳腺癌细胞MDA-MB-231生长和侵袭的影响
2018-06-20郇雪洁姬逸男杨宁伍越朱玲钰杨华伟
郇雪洁 姬逸男 杨宁 伍越 朱玲钰 杨华伟
核糖体S6蛋白激酶4(ribosomal protein S6 kinase 4,RSK4)位于X染色体q21区域,是一类丝氨酸/苏氨酸蛋白激酶[1]。研究表明,RSK4基因是抑癌基因,能抑制乳腺癌细胞增殖、迁移、侵袭及转移[2-3]。本课题组前期研究表明RSK4相关表达与乳腺癌细胞体外侵袭能力呈负相关,且在MDA-MB-231细胞系中表达最低[4]。可变剪接是指通过不同的剪接方式或在不同的剪接位点进行剪接,同一个前体mRNA可剪接成不同的基因表达亚型。RSK4通过可变剪接作用形成三种变异体[5]。可变剪接可产生蛋白质异构体调节胚胎发育、细胞分化和凋亡等重要过程[6]。前期研究发现部分RSK4变异体的相互作用蛋白还涉及肿瘤细胞的迁移和侵袭,推测RSK4的可变剪接变异体1(ribosomal protein S6 kinase 4 variant 1,RSK4m1)可能与RSK4有同样的生物学功能。本研究在人乳腺癌MDA-MB-231细胞系中过表达RSK4m1,观察该细胞系的增殖、迁移及侵袭等变化,探讨过表达RSK4m1对乳腺癌细胞MDA-MB-231功能学的影响,为明确RSK4m1对乳腺癌的作用机制提供实验依据。
1 材料与方法
1.1 主要试剂和仪器
人乳腺癌细胞株MDA-MB-231购于中国科学院典型培养物保藏委员会细胞库(上海);阴性对照病毒LVCON145及RSK4m1慢病毒表达载体LV-RPS6KA6由上海吉凯基因技术有限公司构建包装;RSK4m1及GAPDH引物由广州艾基生物技术有限公司合成;抗RSK4、GAPDH单克隆抗体购于美国Abcam公司;Transwell小室(孔径8.0 μm)购于美国Corning公司;倒置相差显微镜购于OLYMPUS公司;酶标仪实时荧光定量PCR(qRT-PCR)仪购于美国Thermo公司;凝胶成像系统购自美国Bio-Rad公司。
1.2 细胞培养与转染
将MDA-MB-231细胞置于37℃、5%CO2恒温培养箱中,用含10%胎牛血清的DMEM高糖培养基培养。细胞密度长到90%左右,吸去培养基,PBS冲洗,胰酶消化2 min后常温离心,吸上清液,加入新鲜培养基吹打均匀后计数,将细胞悬液接种于6孔板中,每孔细胞数约为1×105个。细胞密度达70%左右时转染。将细胞设置为3组:以MDA-MB-231亲本细胞为空白对照组(Con组)、转染空载病毒的MDA-MB-231细胞为阴性对照组(Mock组)、转染过表达RSK4m1的MDA-MB-231细胞为实验组(OE组)。在MOI=15条件下,OE组加入LV-RPS6KA6病毒稀释液,Mock组加入LVCON145病毒稀释液,每组均设置3个复孔,每孔均加入终浓度为5 g/mL的Polybrene及感染增强液,终体积为1 mL。放入培养箱培养,12 h后观察细胞状态,更换新鲜培养基。分别于感染24 h、48 h和72 h后在倒置荧光显微镜(×40)下观察感染效率。
1.3qRT-PCR检测mRNA表达量
用Trizol提取总RNA,逆转录为cDNA。RSK4m1上游引物序列为5'-ATATGGACCCACATCAGCGG-3',下游引物序列为5'-AGCAGCTACAGGCTCTAGGA-3'。内参GAPDH上游引物序列为5'-AGAAGGCTGGGGCTCATTTG-3',下游引物序列为5'-AGGGGCCATCCACAGTCTTC-3'。按照SYBR Premix Ex Taq试剂盒说明,每组为20 μL的Real-time PCR体系,每孔设3个复孔。反应条件:预变性95℃30 s,变性95℃5 s,退火60℃ 30 s,共40个循环。RSK4m1的mRNA相对表达量采用2-△△Ct计算,计算公式如下:△Ct=Ct平均值(RSK4m1)-Ct平均值(GAPDH),△△Ct=△Ct(Mock组或OE组)-△Ct(Con组)。实验重复3次。
1.4 Western Blot法检测蛋白表达量
收集对数期生长的细胞,RIPA裂解液提取细胞总蛋白,BCA法测定每组蛋白浓度。每孔蛋白上样量为25 μg,根据所测蛋白浓度,计算相应的上样体积。以10%SDS-PAGE电泳分离蛋白后转至PVDF膜,室温下5%脱脂牛奶封闭2 h,分别加入特异性抗体RSK4m1(1∶1 000)、GAPDH(1∶10 000)4 ℃ 摇床过夜。TBST洗涤30 min后二抗室温孵育1 h。ECL显影,凝胶成像系统拍照并进行灰度值分析。蛋白相对表达量为RSK4m1与GAPDH蛋白条带灰度值的比值。实验重复3次。
1.5 CCK-8法检测细胞增殖
每组细胞以3×103个/孔接种于96孔培养板中,加入含10%FBS培养基使每孔液体总量为100 μL,每组设 6 个复孔,分别于 0 h、24 h、48 h、72 h 和 96 h取3个复孔行CCK-8法检测,每孔加入10 μL CCK反应液,置于37℃培养箱继续培养1 h,测定450 nm处吸光度值(OD值)。以时间为横坐标,OD值为纵坐标绘制细胞生长曲线。记录各组0 h、24 h、48 h、72 h和96 h的OD值。实验重复3次。
1.6 划痕实验检测细胞迁移能力
以标记笔于6孔板背面笔直划3或4条直线,每条直线间隔1 cm。取对数生长期细胞消化并接种于6孔板,3×105个/孔。待细胞基本长满时,用 20 μL 移液枪头垂直背面的直线划3条宽度一致的直线,直线间隔1 cm。PBS洗涤3次,去除划下的悬浮细胞,加入不含血清的培养基继续培养。分别在光学显微镜下观察0 h和24 h的细胞迁移情况,细胞迁移率(%)=(迁移距离/划痕距离)×100%。实验重复3次。
1.7 Transwell小室实验检测细胞侵袭能力
将各组细胞置于37℃、5%CO2恒温培养箱中,用不含胎牛血清的DMEM高糖培养基培养12 h。用50 μg/mL Matrigel(1∶8)稀释液包被Transwell小室底部膜的上室面,每孔约100 μL,每组设3个复孔,37℃下放置1 h。各组细胞消化后离心,细胞计数,调整细胞密度为 2×105个/mL,每孔加入细胞悬液200 μL(4×104个细胞),下室加入10%FBS培养基600 μL,37℃、5%CO2培养24 h。擦去上室面未穿过膜的细胞,4%多聚甲醛固定30 min,风干后用1%吉姆萨染色30 min,PBS涤洗3次,200倍倒置显微镜下记数膜下面5个不同视野的肿瘤细胞数,结果取平均值。实验重复3次。
1.8 统计学方法
采用SPSS 17.0统计软件进行数据分析,计量数据以均数±标准差(±s)表示,组间比较采用单因素方差分析(one-way ANOVA),若组间差异有统计学意义,进一步的两两比较采用LSD-t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 慢病毒转染MDA-MB-231细胞的效率
在MOI=15条件下,用慢病毒转染MDA-MB-231细胞48 h后,绿色荧光蛋白表达率稳定增强,倒置显微镜下观察,荧光转染效率>90%。见图1。

图1 慢病毒转染MDA-MB-231细胞48 h后的转染效率(×40)
2.2RSK4m1 mRNA在MDA-MB-231细胞中的表达
qRT-PCR检测结果(图2)显示,Con组、Mock组、OE组中RSK4m1 mRNA的相对表达量分别为1.00±0.09、1.25±0.11、3.73±0.38,组间差异有统计学意义(F=126.879,P<0.001);经两两比较,OE 组 RSK4m1的mRNA相对表达量高于Con组(P<0.001)和Mock组(P<0.001),Con组与Mock组比较,差异无统计学意义(P=0.246)。
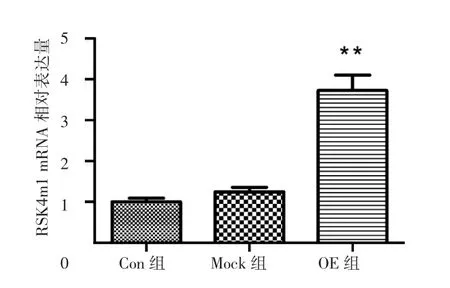
图2 RSK4m1 mRNA在MDA-MB-231各组细胞中的表达
2.3 RSK4m1蛋白在MDA-MB-231细胞中的表达
Western Blot法检测结果(图3)显示,Con组、Mock组、OE组中RSK4m1蛋白的相对表达量分别为0.35±0.02、0.34±0.01、0.79±0.02,组间差异有统计学意义(F=937.122,P<0.001);经两两比较,OE 组RSK4m1蛋白相对表达量高于Con组(P<0.001)和Mock组(P<0.001),Con组与 Mock组比较,差异无统计学意义(P=0.908)。
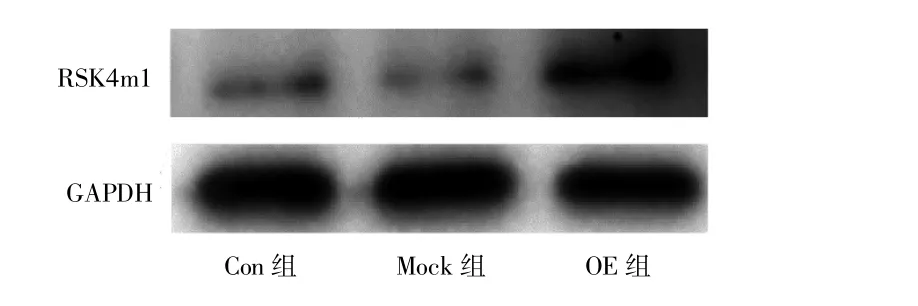
图3 RSK4m1蛋白在MDA鄄MB鄄231各组细胞中的表达
2.4 过表达RSK4m1对MDA-MB-231细胞增殖能力的影响
CCK-8法检测各组MDA-MB-231细胞在不同时间点相对应的OD值,结果显示,与Con组和Mock组相比,OE组除0 h未见明显差异(P=0.611)外,在24 h、48 h、72 h、96 h细胞的OD值均明显降低,差异具有统计学意义(P<0.05)。见图 4。
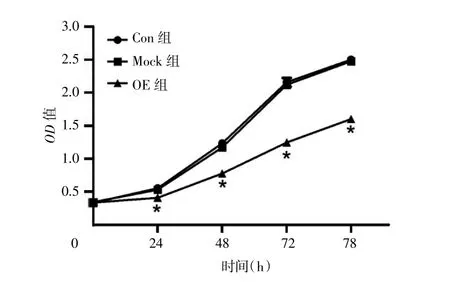
图4 过表达RSK4m1对MDA鄄MB鄄231细胞增殖能力的影响
2.5 过表达RSK4m1对MDA-MB-231细胞迁移能力的影响
细胞划痕实验检测各组细胞的迁移能力变化,结果显示,24 h后Con组、Mock组和OE组的细胞迁移率分别为(25.67±2.44)%、(24.47±2.25)%、(14.53±0.64)%,组间差异具有统计学意义(F=29.379,P=0.001);经两两比较,OE组细胞迁移率明显低于Con组(P<0.001)和Mock组(P=0.001),Con组与Mock组比较,差异无统计学意义(P=0.480)。见图5。
2.6 过表达RSK4m1对MDA-MB-231细胞侵袭能力的影响
Transwell小室检测各组细胞侵袭能力的变化,结果显示,Con组、Mock组和OE组细胞穿过Transwell小室膜的数量分别为(66.70±5.86)个、(58.67±4.16)个、(35.00±5.57)个,组间差异具有统计学意义(F=29.520,P=0.001);经两两比较,OE组细胞穿过Transwell小室膜的数量明显低于Con组(P<0.001)和Mock组(P=0.001),Con组与Mock组比较,差异无统计学意义(P=0.111)。见图6。
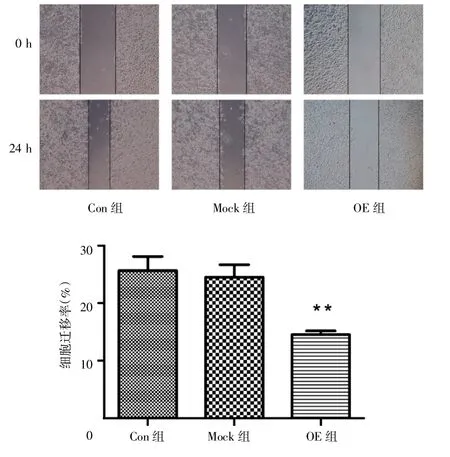
图5 过表达RSK4m1对MD A鄄MB鄄231细胞迁移能力的影响

图6 过表达RSK4m1对MDA鄄MB鄄231细胞侵袭能力的影响
3 讨论
p90核糖体S6蛋白激酶(ribosomal protein S6 kinase,RSK)是一组高度保守的丝氨酸/苏氨酸激酶,可使40S核糖体亚单位S6蛋白发生磷酸化而促进某些mRNA翻译,在调节细胞生长和增殖过程中起重要作用[7-8]。RSK 家族包括 RSK1、RSK2、RSK3和RSK4[9]。本课题组前期研究发现,人乳腺癌组织中RSK4基因表达阳性率明显低于癌旁正常乳腺组织及乳腺良性病变组织[10]。在过表达RSK4的乳腺癌细胞中,细胞的增殖和侵袭能力下降[11]。干扰RSK4基因在乳腺癌细胞株MCF-7的表达后,能明显促进裸鼠原位移植瘤生长及转移[12]。研究发现,RSK4可被MAPKs磷酸化激活,通过底物磷酸化抑制FGFR2-RASERK信号通路,进而调控细胞的生长、增殖和分化。以上研究表明,RSK4可能是重要的肿瘤抑制基因,并有抑制细胞生长、增殖及侵袭的能力。
可变剪接是真核细胞基因表达多样性的重要机制之一,同一个前体mRNA可剪接成不同的基因表达亚型。可变剪接在受体多样性、控制细胞生长发育等方面起着决定性作用,来源于单一基因的不同蛋白亚型,通过与其他蛋白结合可产生不同的亚细胞定位、酶催化活性等[13]。可变剪接可产生蛋白质异构体调节胚胎发育、细胞分化和凋亡等重要过程[6]。
Sun等[5]研究发现,RSK4除野生型外,由于第19外显子发生15个碱基的缺失突变(-15nt)和第21外显子的缺失突变(-E21),形成了三种变异体。该研究还发现RSK4对细胞生长、死亡和化学反应的影响取决于mRNA变体或表达的蛋白质异构体、细胞系的特异性及贴壁生长条件等。RSK4及其变异体常被发现在同一细胞内表达,但产生的作用可能部分相同,也有部分相反。本研究CCK-8实验表明过表达RSK4m1可显著抑制乳腺癌细胞的增殖能力;细胞划痕实验及Transwell小室侵袭实验分别提示过表达RSK4m1可显著抑制乳腺癌细胞的迁移、侵袭能力。从一定程度上验证了RSK4m1可能与RSK4有同样抑制乳腺癌细胞增殖、迁移、侵袭及转移的能力。有研究显示RSK4或RSK4m的相互作用蛋白参与tRNA代谢、氨基酸活化、蛋白折叠等多种细胞生理活动,且部分RSK4m相互作用蛋白还涉及肿瘤细胞的迁移、侵袭,如环化酶相关蛋白1(cyclase-associated protein 1,CAP1)、α-辅肌动蛋白 4(alpha-actinin 4,ACTN 4)等[14]。可变剪接引起转录组多样性的方法学已成为一种有效工具,不仅可用于改善肿瘤的生物学基础,还可用于寻找对诊断、治疗和预后更准确的分子标志物[15]。
综上所述,上调RSK4m1基因在乳腺癌细胞株MDA-MB-231的表达可显著抑制MDA-MB-231细胞的增殖、迁移和侵袭能力,为RSK4m1可能作为乳腺癌治疗新靶点提供实验依据,但其具体作用机制仍需进一步研究。
[1] Anjum R,Blenis J.The RSK family of kinases:emerging roles in cellular signalling[J].Nat Rev Mol Cell Biol,2008,9(10):747-758.
[2] Thakur A,Sun Y,Bollig A,et al.Anti-invasive and antimetastatic activities of ribosomal protein S6 kinase 4 in breast cancer cells[J].Clin Cancer Res,2008,14(14):4427-4436.
[3] Dummler BA,Hauge C,Silber J,et al.Functional characterization of human RSK4,a new 90-kDa ribosomal S6 kinase,reveals constitutive activation in most cell types[J].J Biol Chem,2005,280(14):13304-13314.
[4] 张晓丽,刘剑仑,杨华伟,等.抑癌基因RSK4的表达与乳腺癌细胞体外侵袭力的相关性研究[J].中国肿瘤临床,2011,38(6):308-311.
[5] Sun Y,Cao S,Yang M,et al.Basic anatomy and tumor biology of the RPS6KA6 gene that encodes the p90 ribosomal S6 kinase-4[J].Oncogene,2013,32(14):1794-1810.
[6] Ferreira EN,Rangel MC,Galante PF,et al.Alternative splicing enriched cDNA libraries identify breast cancer-associated transcripts[J].BMC Genomics,2010,11(Suppl 5):S4.
[7] 陈祖舜,刘剑仑.X染色体连锁基因RSK4在乳腺癌中的表达及进展[J].中国癌症防治杂志,2009,1(2):167-169.
[8] Romeo Y,Zhang X,Roux PP.Regulation and function of the RSK family of protein kinases[J].Biochem J,2012,441(2):553-569.
[9] 杨华伟,刘剑仑.p90核糖体S6蛋白激酶家族与恶性肿瘤[J].中国癌症防治杂志,2013,5(2):177-180.
[10]刘剑仑,杨华伟,陈祖舜,等.核糖体S6蛋白激酶4在乳腺癌中的异常表达及临床意义[J].中华肿瘤杂志,2011,33(6):452-456.
[11] Thakur A,Xu H,Wang Y,et al.The role of X-linked genes in breast cancer[J].Breast Cancer Res Treat,2005,93(2):135-143.
[12]朱佳,刘剑仑,韦薇,等.RNA干扰RSK4基因表达对裸鼠移植瘤生长与转移影响观察[J].中华肿瘤防治杂志,2013,20(24):1865-1868.
[13] Nilsen TW,Graveley BR.Expansion of the eukaryotic proteome by alternative splicing[J].Nature,2010,463(7280):457-463.
[14] Liu R,Liu T,Wei W,et al.Novel interacting proteins identified by tandem affinity purification coupled to nano LC-MS/MS interact with ribosomal S6 protein kinase 4 (RSK4)and its variant protein(RSK4m)[J].Int J Biol Macromol,2017,96:421-428.
[15]Brinkman BM.Splice variants as cancer biomarkers[J].Clin Biochem,2004,37(7):584-594
