医院制剂补骨脂酊的质量考察
2018-06-07牟致平梁莹莹张淑君马秉智
牟致平,梁莹莹,张淑君,马秉智,刘 晓,赫 军
(中日友好医院 药学部,北京 100029)
补骨脂酊为中日友好医院院内制剂,是由补骨脂加工制成的酊剂,主要指标成分为补骨脂素和异补骨脂素。外用补骨脂酊可增加皮肤对紫外线的敏感性,促进黑色素的生化合成和转运,对白癜风治疗效果明显[1,2]。同时补骨脂酊可活血化瘀,促进局部血液循环,营养毛发,治疗斑秃、牛皮癣等疾病[3]。我院补骨脂酊在临床上使用多年,疗效显著,临床医师与患者对其评价良好。本着保障医院制剂质量的原则,根据《医疗机构制剂注册管理办法》相关要求,本研究参照《北京市医疗机构剂制规程》2014年(征求意见版)等质量控制方法[4~6],对留样观察的3批样品进行定性鉴别和指标成分的含量测定考察,为我院补骨脂酊生产及临床用药提供参考。
1 仪器与试剂
Agilent 1260 series型高效液相色谱仪,CPA225D电子天平(德国赛多利斯仪器系统有限公司),KQ-300DE型数控超声波清洗器(昆山市超声仪器有限公司)。硅胶G薄层板(青岛海洋化工厂)。补骨脂酊为中日友好医院中药制剂室自制,规格为 100ml/瓶,批号分别为:20170214、20170628、20170801;补骨脂素、异补骨脂素为对照药材,均购自中国药品生物制品检定所,批号分别为:110739-201617、110738-201614。试验中所用甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。
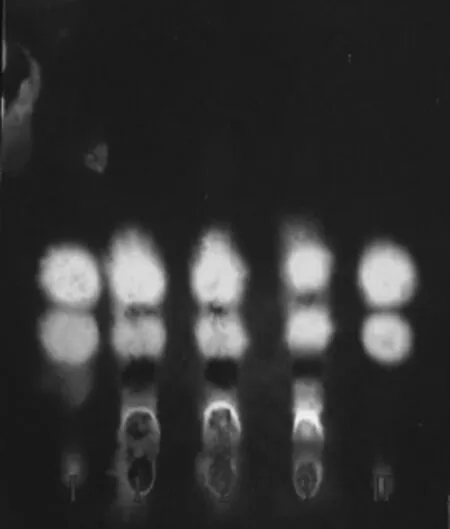
图1 薄层色谱图
2 方法与结果
2.1 定性鉴别[4]
取补骨脂素、异补骨脂素对照品,加乙酸乙酯制成每1ml各含2mg的混合溶液,作为对照品溶液,另取本品作为供试品溶液。照薄层色谱法实验,吸取上述两种溶液各5μl,分别点于同一硅胶G薄层板上,以正乙烷-乙酸乙酯(4:1)为展开剂,展开,取出,晾干,喷以10%氢氧化钾甲醇溶液,置紫外灯(365nm)下检视。供试品色谱在与对照品色谱相应的位置上,显相同颜色的荧光斑点,见图1。
2.2 含量测定[6]
2.2.1 色谱条件色谱柱
为 Symmetry C18 (4.6×250mm); 流动相为甲醇-水(50:50,V/V),流速为 1.0ml/min,检测波长为 246nm,带宽为 4nm,柱温为 40℃,进样量为 10μl。
2.2.2 溶液的制备
(1)对照品溶液的制备。精密称取补骨脂素、异补骨脂素对照品适量,加甲醇溶解,得浓度分别为0.1100mg/ml、0.1176mg/ml的补骨脂素、异补骨脂素对照品储备液。分别从上述对照品储备液精密量取10ml置50ml容量瓶中,加甲醇至刻度即得浓度为 22.0000μg/ml、23.5200μg/ml的补骨脂素、异补骨脂素对照品溶液。(2)供试品溶液的制备。取供试品5ml,置于100ml容量瓶中,用甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
2.2.3 系统适应性试验
取“2.2.2”项下对照品溶液、供试品溶液各 10μl,按照“2.2.1”项下方法进样测定。在相应保留时间上,供试品色谱与对照品色谱有相同的色谱峰。理论板数以补骨脂峰计应不少于3000,且补骨脂素、异补骨脂素分离度>1.5,见图2。
2.2.4 含量测定
按外标法以峰面积计算含量,3个批次补骨脂酊中补骨脂素和异补骨脂素的总含量见表1。
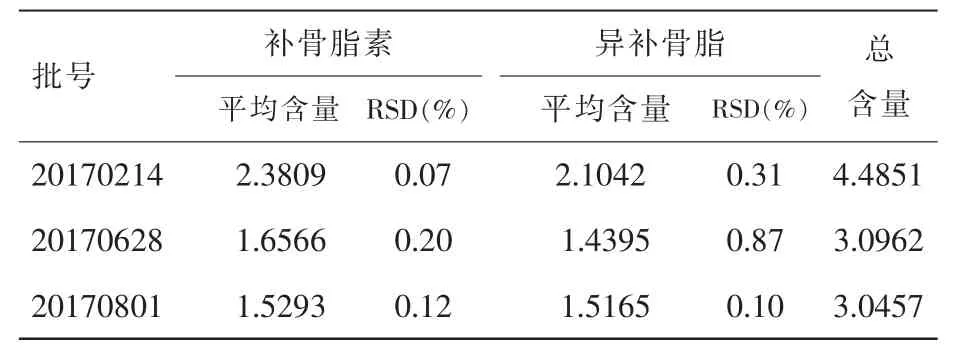
表1 样品含量测定结果(mg/ml,n=3)
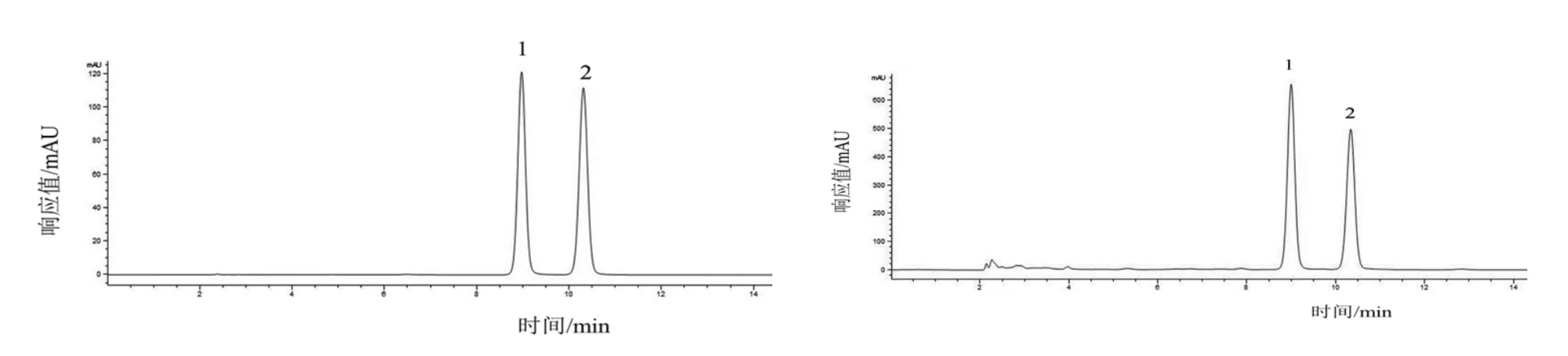
图2 高效液相色谱图
3 讨论
目前我院补骨脂酊质控执行的是《北京市医疗机构制剂规程》1984年版的规定,距今已有30余年,该标准中没有含量测定检查项,然而其唯一的原料药补骨脂的指标成分明确,补骨脂素和异补骨脂素的含量直接影响制剂的有效性[7],因此本文采用HPLC方法对3批样品进行含量测定。文献中对该成分的规定为每1ml补骨脂酊中含补骨脂素和异补骨脂素的总量须≥1.2mg[5,6],结合中国药典中对补骨脂的含量限度要求及3批样品的测定结果[8],暂定我院自制制剂补骨脂酊含量检测限度要求为每1ml补骨脂酊含补骨脂素和异补骨脂素总量≥1.2mg。
通过本次质量考察可以得出,我院补骨脂酊符合现行相关质量标准,且通过本次研究制定出高于现行质量标准的内部控制标准,为生产稳定有效的医院制剂提供了依据,以保证自制制剂的有效性。
[1]朱小兰,盛国荣,杨永美.补骨脂酊对实验性白癜风模型的影响[J].中药药理与临床,2014,30(6):115-117.
[2]王晓燕,吕月桂,张丽.外用补骨脂酊联合窄谱中波紫外线治疗白癜风的临床观察及护理干预[J].中国医药导报,2016,13(14):146-149.
[3]李恒,程孝顶,刘兰.综合治疗法治疗斑秃39例临床观察[J].中医药导报,2013,2:74-75.
[4]北京市食品药品监督管理局.北京市医疗机构制剂规程(征求意见版)[M].北京:中国商业出版社,2014.9-10.
[5]解放军总后勤部卫生部.中国人民解放军医疗机构制剂规范[M].北京:人民军医出版社,2002.279-280.
[6]徐兰,陶晓璇,王丹辉.补骨脂酊质量标准的建立[J].中国药师,2015,2:329-331.
[7]曹金一,刘京晶,黄文华.补骨脂药理作用与临床应用研究进展 [J].中药药理与临床,2008,24(6):89-92.
[8]国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2015.305.
