不同质量麦冬药材醇溶性浸出物与相关成分研究
2018-06-02干建伟钱广生
干建伟 钱广生△ 胡 敏 韦 婷
[1.四川大学华西药学院,四川 成都 610000;2.华润三九(雅安)药业有限公司,四川 雅安625000]
参麦注射液是由红参和麦冬两味药材提取而成[1],其中不同外观性状的麦冬药材会直接影响参麦注射液的质量。本文研究的麦冬药材选用百合科植物麦冬Ophiopogon japonicus(L.f) Ker-Gawl的干燥块根,主产于四川,习称川麦冬。麦冬始载于《神农本草经》,列为上品,具有养阴生津,润肺清心之功效[2],主要含有麦冬多糖、黄酮类、皂苷类、挥发油类、蛋白质、氨基酸、微量元素等有效成分,其中麦冬多糖、总皂苷、总黄酮的含量与采收期有较大的相关性[3-6]。麦冬主要为川麦冬和浙麦冬,其中的化学成分有较显著差异,主要通过指纹图谱、皂苷、黄酮类成分评价麦冬质量,与相关制剂的关联分析较少[7-14]。麦冬由于栽种、炮制、储存等问题,主要出现红锈、泛油的问题[15-16],该类麦冬在市场中混杂在符合规定的麦冬中出现,可能对参麦注射液的质量产生影响。由于不同厂家购买的麦冬品质不同,因此导致产品中糖含量的差异[17]。本研究主要是通过醇溶性浸出物、果糖等指标研究正常麦冬、红锈麦冬、泛油麦冬质量差异,进而明确参麦注射液用麦冬药材的醇溶性浸出物控制范围。
1 仪器与试药
1.1 药材
麦冬,购于雅安三九中药材科技产业化公司麦冬GAP 种植基地,共 6 批(批号:130401、130402、130403、130404、130405、130406),按照 2015 年版《中华人民共和国药典(一部)》麦冬质量标准检测均符合规定,以上药材经四川大学华西药学院钱广生教授鉴定,其中批号为 130401、130402、130403、130404 的麦冬为性状正常麦冬,批号为130405的麦冬为红锈麦冬,批号为130406的麦冬为泛油麦冬。
1.2 试剂及仪器
果糖对照品购自中国食品药品检定研究院(批号:100231-200904);鲁斯可皂苷对照品购自中国食品药品检定研究院(批号:111909-201204)。电子天平(德国赛多利斯);水浴锅;乙醇为AR级。
2 方 法
2.1 醇溶性浸出物测定[2]
将麦冬(批号:130401、130402、 130403、130404、130405、130406)按照 2015 年版《中国药典(四部)》通则2201项下醇溶性浸出物测定法测定,用乙醇作溶剂,即得。
2.2 果糖含量测定
2.2.1 供试品溶液制备 取麦冬药材(批号:130401)低温烘干(40℃),打粉后,过6号筛。取麦冬粉末约0.35 g,精密称定,置具塞锥形瓶中,精密加入50 mL纯化水,密塞,称定质量,超声提取15 min,取出冷却后用水补足减失的质量,摇匀,过滤取续滤液,作为供试品溶液。其他批次麦冬(批号:130402、130403、130404、130405、130406)按照同法制备,即得。
2.2.2 对照品溶液制备 精密称取果糖对照品适量,加5%甲醇溶解,配成约0.5 mg/mL的对照品溶液,即得。
2.2.3 色谱条件 色谱柱:Prevail Carbohydrate ES(250 mm×4.6 mm,5 μm)。 流动相:水∶乙腈=25∶75。流速:1 mL/min。柱温:35℃。检测器:蒸发光散射检测器(Alltech ELSD 2000ES),分流模式,漂移管温度:50 ℃,氮气流速:1.5 L/min。理论板数按果糖峰计算不得低于5000。
2.2.4 精密度试验 见表1。取“2.2.2”项下果糖对照品溶液,连续6次进样,分别为10 μL。计算果糖峰面积的RSD%值,结果仪器精密度良好。
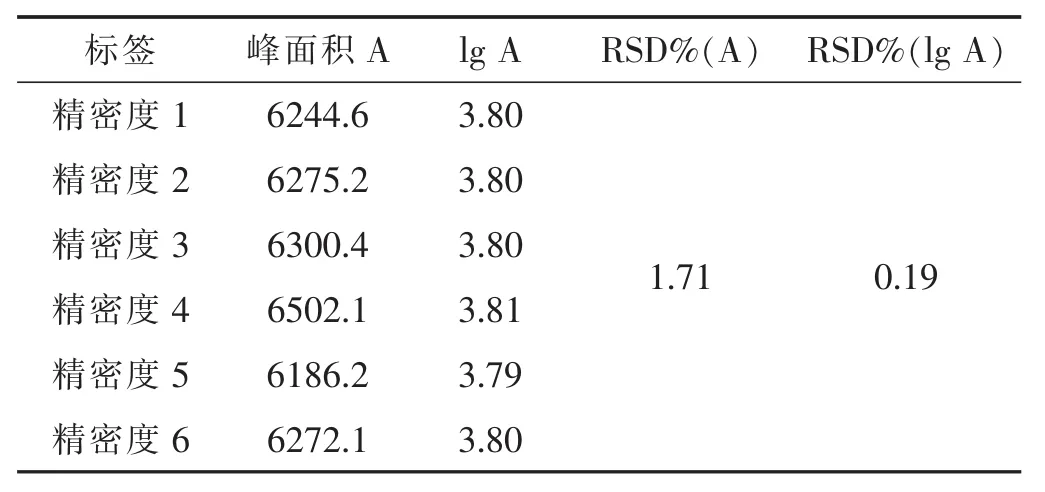
表1 精密度试验结果(n=6)
2.2.5 重复性试验 见表2。精密称取麦冬粉末6份,每份0.35 g,依法提取,作供试品溶液。分别用高效液相色谱仪检测,麦冬果糖提取稳定,重复性好。
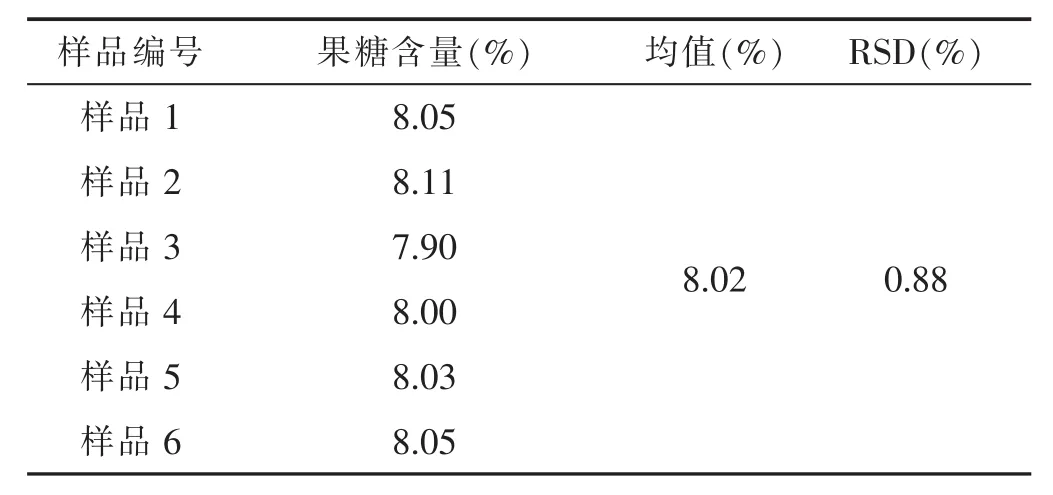
表2 麦冬药材果糖含量(n=6)
2.2.6 稳定性试验 见表3。精密称取麦冬药粉0.3792 g,依法制备成供试品溶液,分别在 0、4、8、16、24、36、48 h进样测定果糖的含量,样品中果糖含量在48 h内稳定。

表3 样品稳定性试验结果
2.2.7 线性关系考察 分别精密吸取“2.2.2”项下果糖对照品溶液 1、2、4、8、16、24、32 μL 依次进样, 测定峰果糖面积。再分别以果糖峰面积-果糖进样量取对数做图,回归线性见图1,线性方程为y=1.408734x+5.171397,R=0.9998(y:面积取对数 lgA;x:浓度取对数lgC),果糖进样量在 0.35585~8.5404 μg 时,双对数呈良好的线性关系。

图1 lgC-lgA线性回归方程图
2.2.8 加样回收率试验 见表4。精密称取麦冬粉末350 mg,供6份,每份加入果糖对照品27.53 mg,按方法提取,检测并计算回收率为112%,RSD%达1.50,回收率稳定。
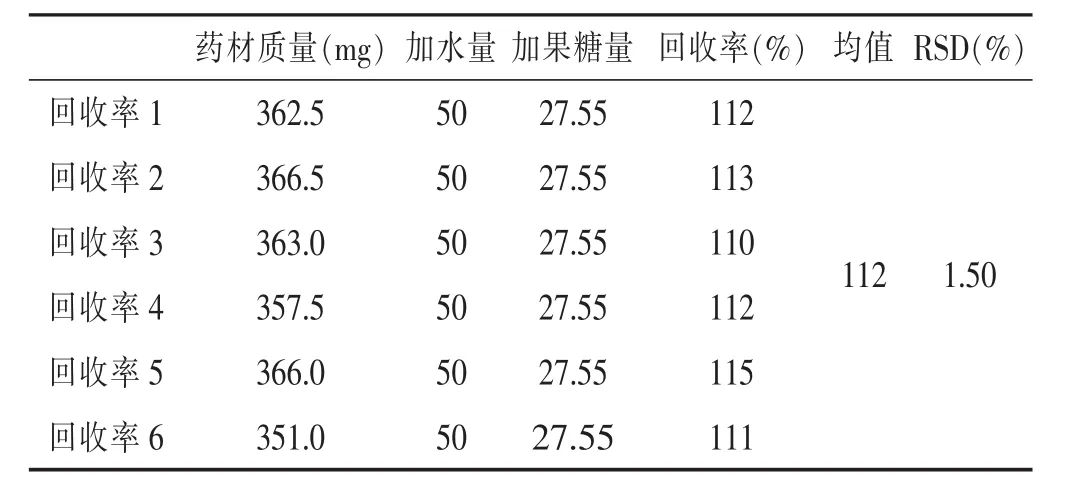
表4 麦冬果糖加样回收率试验
2.3 水溶性浸出物测定[2]取麦冬(批号:130401、130402、130403、130404、130405、130406)按照 2015 年版《中国药典(四部)》通则2201项下水溶性浸出物测定法中的热浸法测定,即得。
2.4 鲁斯可皂苷元测定[2]
2.4.1 对照品溶液制备 取鲁斯可皂苷元对照品适量,精密称定,加甲醇制成每1 mL含50 μg的溶液,即得。
2.4.2 标准曲线制备 精密量取对照品溶液0.5、1、2、3、4、5、6 mL,分别置具塞试管中,于水浴中挥干溶剂,精密加入高氯酸10 mL,摇匀,于热水中保温15 min,取出,冰水冷却,以相应的试剂为空白,照紫外-可见分光光度法(《中国药典》2015年版)测定,在397 nm波长处测定吸光度,以吸光度为纵坐标,浓度为横坐标,绘制标准曲线。
2.4.3 含量测定 取2.2.1项下麦冬(批号:130401、130402、130403、130404、130405、130406) 细粉约 3 g, 精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,称定质量,加热回流2 h,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,精密量取续滤液25 mL,回收溶剂至干,残渣加水10 mL使溶解,用水饱和正丁醇振摇提取5次,每次10 mL,合并正丁醇液,用氨试液洗涤2次,每次5 mL,弃去氨液,正丁醇液蒸干。残渣用80%甲醇溶解,转移至50 mL量瓶中,加80%甲醇至刻度,摇匀。精密量取供试品溶液2~5 mL,置10 mL具塞试管中,照“2.4.2”项下的方法,自“于水浴中挥干溶剂”起,依法测定吸光度,从标准曲线上读出供试品溶液中鲁斯可皂苷元的量,计算,即得。
3 结果与分析
3.1 果糖标准曲线
见图2。分别精密吸取2.2.2项下果糖对照品溶液2、5、8、10 μL,注入液相色谱仪,以果糖峰面积-果糖进样量取对数做图,建立标准曲线,其中R2=0.999相关性较好。

图2 果糖标准曲线
3.2 鲁斯可皂苷元标准曲线
见图3。精密量取2.4.1项下对照品溶液0.5、1、2、3、4、5、6 mL, 按照 2.4.2 项下制备标准曲线,R2=0.999相关性较好。
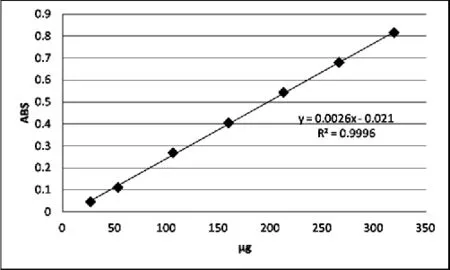
图3 鲁斯可皂苷元标准曲线
3.3 测定结果
不同麦冬药材(批号:130401、130402、130403、130404、130405、130406)按照醇溶性浸出物、水溶性浸出物、鲁斯可皂苷、果糖检测方法测定含量,见表5。

表5 不同麦冬浸出物、鲁斯可皂苷及果糖含量
3.4 结果
3.4.1 麦冬原料中,水溶性浸出物按照T检验,P>0.05,无显著差异,采用中国药典标准检测水溶性浸出物不能区别不同麦冬原料品质差异。通过对比,区别正常麦冬与红锈麦冬、泛油麦冬,可通过醇溶性浸出物、鲁斯可皂苷元及果糖含量的差异来判断。
3.4.2 红锈麦冬醇溶性浸出物与正常麦冬醇溶性浸出物基本无差异,只是略微偏高,但果糖含量明显升高。泛油麦冬醇溶性浸出物、鲁斯可皂苷、果糖含量均显著高于正常麦冬。分析认为主要是麦冬在较高水分时,通过堆置或密闭导致自发热,淀粉等有机物降解转化导致指标差异。
4 讨 论
虽然参麦注射液质量标准中没有麦冬的含量检测,现有指纹图谱中也未体现麦冬药材的色谱峰,但通过对麦冬药材的醇溶性浸出物、鲁斯可皂苷元、果糖的数据分析,针对参麦注射液质量而言,麦冬原料各指标应建立内控质量标准,指标范围应控制在正常麦冬检测范围内。
参麦注射液用麦冬药材应选用性状符合要求的原料,避免类似红锈类的麦冬原料大量混入,虽然红锈麦冬醇溶性浸出物在正常麦冬范围内,但是从颜色、鲁斯可皂苷元来说是显著异常的,给产品质量带来较高的安全风险。
建议麦冬药材增加醇溶性浸出物的检测项目,加强对麦冬药材的质量控制,同时进一步研究不同采收期麦冬药材的醇溶性浸出物,以便有效获得需要的控制范围。
企业应根据具体品种的具体要求制定适用的中药材进厂内控检验标准,避免劣质药材进入生产环节。
[1]国家食品药品监督管理总局.国家药品标准·参麦注射液[S].WS3-B-3428-98-2010.
[2]国家药典委员会.中华人民共和国药典(四部)[M].北京:中国医药科技出版社,2015.
[3]王远,秦民坚,戚进,等.不同采收期及加工条件对川麦冬多糖含量的影响[J].现代中药研究与实践,2009,23(2):3-6.
[4]姜国志,孙胜斌,刘铁军,等.参麦注射液用麦冬药材不同采收期的研究[J].现代中药研究与实践,2013,27(6):24-27.
[5]蒋畅,王远,秦民坚,等.不同采收期及加工条件对川麦冬总黄酮和总皂苷含量的影响[J].中国中药杂质,2010,35(7):821-823.
[6]徐建中,李振丰,俞旭平,等.浙麦冬不同生长周期及不同采收期研究[J].中国现代中药,2014,16(6):466-472.
[7]蒋慧莲.麦冬特征性成分及其质量标准研究[D].杭州:浙江中医药大学,2013.
[8]王永毅.参麦注射液组方药材浙麦冬的质量控制方法研究[D].杭州:浙江大学,2012.
[9]王玉霞.麦冬药材质量评价及道地性初步研究[D].北京:北京协和医学院,2014.
[10]李正,陈勇,马临科,等.浙麦冬质量标准的制定及探讨[J].中国现代应用药学,2016,33(6):795-799.
[11]王进,刘汉清,刘霖,等.HPLC定量指纹图谱法评价川麦冬质量研究[J].中药材,2013,36(5):721-725.
[12]金虹,王化东,何礼,等.川麦冬及其须根组织学与麦冬皂苷量的对比研究[J].中草药,2014,45(7):1002-1005.
[13]吴发明,杨瑞山,李敏,等.麦冬主流品种药材质量对比研究[J].中国药学杂志,2017,52(6):447-451.
[14]吴发明,杨海燕,杨瑞山,等.四川麦冬质量评价研究[J].中药材,2016,39(8):1803-1808.
[15]李敬安.贮藏与加工对麦冬品质影响的实验研究[D].成都:西南交通大学,2009-5-16.
[16]雷飞益,马留辉,吴海军,等.干燥方法对川麦冬药材品质的影响[J].中药材,2017,40(5):1078-1083.
[17]许妍,吴毅,赵雯,等.参麦注射液中糖类成分含量测定研究[J].齐鲁药事,2011,30(11):636-638.
