慢性胰腺炎体外震波碎石后内镜取石最佳时机的临床分析
2018-05-07孙晖辛磊钱阳阳胡良皞陈辉叶博廖专李兆申
孙晖 辛磊 钱阳阳 胡良皞 陈辉 叶博 廖专 李兆申
Fundprogram:National Natural Science Foundation of China(81422010,81770636,81770632,81770635);Guiding Medical Project of Shanghai Science and Technology Committee(17411971500 )
胰管结石是慢性胰腺炎(CP)特征性的病理改变[1],近50%~90%的CP患者合并胰管结石[2-4]。结石可导致胰液排出受阻、胰管高压,进而引起胰腺萎缩、胰腺功能受损,并导致患者腹痛等症状[5-6],故消除胰管结石、通畅胰液引流是CP治疗的关键[7-8]。自1987年首次报道体外震波碎石术(extracorporeal shock wave lithotripsy,ESWL)用于治疗胰管结石至今[9],ESWL联合内镜取石已成为目前CP治疗的一线方案[10-12],多项研究证实其疗效好、安全性高[13-14]。但ESWL治疗过程中冲击波会对波的传导通路及结石周围组织造成机械性损伤,部分患者可出现胃肠道及十二指肠乳头水肿,不利于后续ERCP插管和结石清除。ESWL后适当延长内镜取石时机可能有利于水肿缓解及后续的内镜取石,但目前对ESWL后何时进行内镜取石尚未形成共识。本研究回顾性分析长海医院内镜中心临床资料,探讨ESWL后内镜取石的最佳时机。
资料与方法
一、临床资料
回顾性纳入2014年2月至2015年2月长海医院内镜中心收治的接受ESWL联合内镜取石的CP患者。ESWL碎石标准为主胰管(main pancreatic duct,MPD)内存在直径>5 mm的阳性结石。排除标准:(1)不能除外恶性肿瘤者;(2)有胰腺手术史或影响ERCP操作的手术史。根据既往治疗情况将患者分为既往接受过ERCP治疗的A组和未接受过ERCP治疗的B组。
二、治疗方法
ESWL设备为第3代体外震波碎石系统(Compact Delta Ⅱ,多尼尔医疗技术公司,德国)。单次疗程最大震波5 000次,能级6级(16 000千伏),频率90~120次/min,每次治疗时间60~90 min。ESWL术后如无并发症,则连续行下一次ESWL,直至结石粉碎后行ERCP取石,如出现ESWL后并发症,则待其恢复后再行ERCP取石。
ESWL后内镜取石时机分为ESWL当日(<12 h)行ERCP组、次日(12~36 h)行ERCP组、隔日(>36 h)以后行ERCP组。ERCP由高年资内镜医师完成。根据术中情况予以胰管括约肌切开术、胰管取石术、胰管支架置入术等操作。
三、研究指标
主要研究终点为ERCP插管成功率和MPD结石成功清除率。插管成功定义为完成选择性胰管深插管[15]。90%以上结石被清除定义为完全清除,50%~90%结石被清除定义为部分清除,震波破碎的结石直径>3 mm或50%的结石未清除定义为清除失败。参考既往研究[16-17]将MPD结石完全及部分清除定义为成功清除。
次要研究终点为ERCP相关并发症,并发症的定义参照Cotton等[18]的研究;ESWL后并发症的定义参照ERCP术后并发症标准[19],将其划分为轻度、中等和重度;ESWL术后碎石成功终点定义为震波破碎的胰管结石最长径≤3 mm,或X线下结石密度减小、结石表面积增加、结石形态改变、充满主胰管和邻近分支胰管[20]。
四、统计学处理

结果
一、一般资料
研究纳入170例患者,其中男性127例(74.7%),女性43例(25.3%),平均年龄(47±14)岁。CP病因:特发性96例(56.5%),酒精性59例(34.7%),胰腺解剖异常10例(5.9%)。107例(62.9%)既往接受ERCP治疗,归为A组,63例(37.1%)既往未接受ERCP治疗,归为B组。
二、ESWL治疗情况
170例患者共进行376次ESWL治疗,其中96例(56.5%)接受1次碎石,37例(21.8%)接受2次碎石,15例(8.8%)接受3次碎石,22例(12.9%)接受4次或以上碎石,平均每例碎石(1.8±1.2)次,震波(9 235±6 081)次。ESWL术后不良事件多为一过性,包括3例高淀粉酶血症、1例血尿、1例大便隐血阳性,均在术后48 h内自行恢复。7例(4.1%)ESWL后出现并发症,均为轻度急性胰腺炎,通过药物治疗后好转。无严重并发症,无1例转外科手术。
三、ESWL后ERCP治疗情况
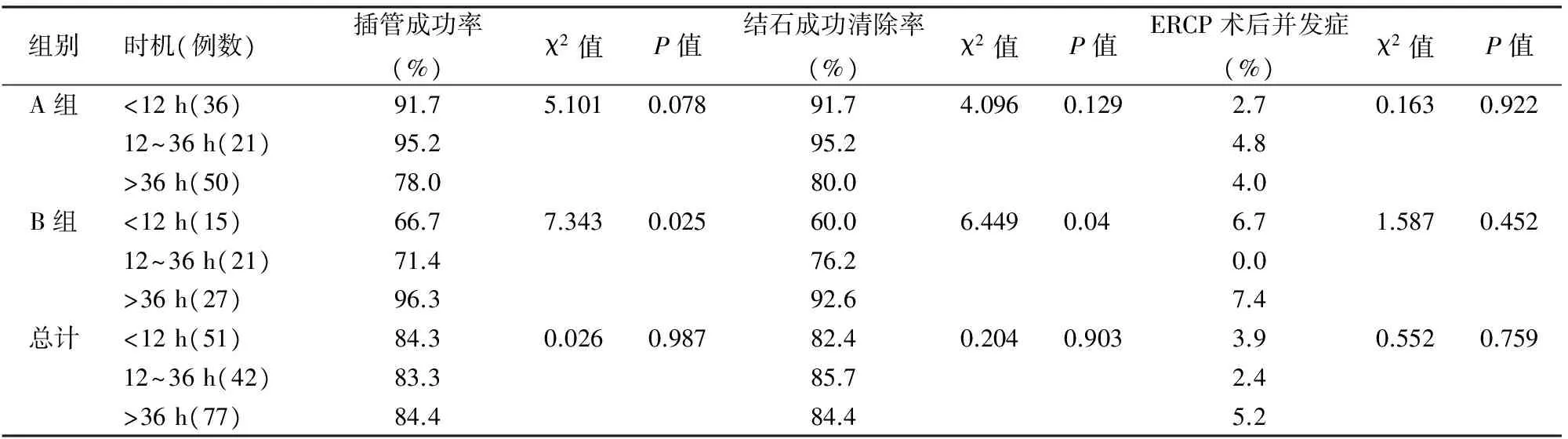
ERCP治疗情况见表1。总体上分别有51例(30.0%)、42例(24.7%)、77例(45.3%)患者在ESWL后12 h内、12~36 h、>36 h行ERCP取石。各时段插管成功率、结石成功清除率差异均无统计学意义。A组的107例患者在不同时机取石的插管成功率、结石成功清除率差异也无统计学意义; B组的63例患者中27例在ESWL后>36 h行ERCP,
插管成功率为96.3%,结石成功清除率为92.6%,均显著高于ESWL后12 h内和12~36 h行ERCP(表1)。部分患者碎石后早期行ERCP时十二指肠乳头肿胀明显(图1),若未行胰管括约肌切开,则插管较为困难;延迟ERCP时乳头肿胀一般可消退(图2),有利于插管,且在肠腔中可见自发排出的碎石,有利于提高结石清除率。7例(4.1%)患者发生ERCP后胰腺炎,均为轻度或中度,均通过药物治疗后治愈,无穿孔、出血、感染以及不良事件的发生。各组间并发症发生率差异无统计学意义(表1)。
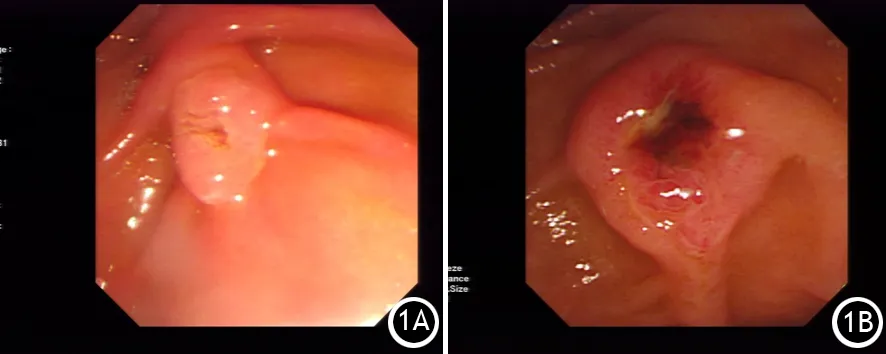
图1 既往未接受ERCP治疗的患者ESWL后(1A)至ERCP前(1B)乳头情况对比(期间间隔12~36 h)

图2 既往未接受ERCP治疗的患者ESWL后(2A)至ERCP前(2B)乳头情况对比(期间间隔超过36 h)
组别时机(例数)插管成功率(%)χ2值P值结石成功清除率(%)χ2值P值ERCP术后并发症(%)χ2值P值A组<12h(36)91.75.1010.07891.74.0960.1292.70.1630.92212~36h(21)95.295.24.8>36h(50)78.080.04.0B组<12h(15)66.77.3430.02560.06.4490.046.71.5870.45212~36h(21)71.476.20.0>36h(27)96.392.67.4总计<12h(51)84.30.0260.98782.40.2040.9033.90.5520.75912~36h(42)83.385.72.4>36h(77)84.484.45.2
讨 论
胰管结石可导致患者腹痛等症状,故清除胰管结石是CP的重要治疗目标。较小的结石多可在内镜下直接清除[21],而较大的结石则需ESWL联合内镜取石[22]。作为一种安全、有效的治疗方法,ESWL联合ERCP目前已被多国指南推荐为CP胰管结石治疗的一线方案[23]。
总体上ESWL相关并发症发生率较低,但其治疗过程中的冲击波仍会对其传导通路及周围组织造成机械性损伤,引起术后胰腺炎、出血、穿孔、石街等并发症,并可导致急性胃肠黏膜损伤等一过性不良事件。冲击波还可导致十二指肠乳头水肿,增加后续ERCP插管难度[24],影响ERCP取石疗效。目前对ESWL后ERCP最佳时机尚无定论。有观点认为,延长ESWL后ERCP时机,有利于乳头和胰腺组织水肿消退,提高内镜取石的成功率及安全性[25];也有观点认为,在ESWL和十二指肠乳头水肿形成之间存在“窗口期”,在这一时间段进行ERCP对插管等操作影响较小[26-27]。仅有的一项临床研究回顾性纳入30例接受ESWL联合ERCP取石的患者,分为早期ERCP组(ESWL后2 d内行ERCP)和延迟ERCP 组(ESWL后超过2 d行ERCP),两组MPD结石清除率分别为16%和82%,延迟ERCP组成功率显著高于早期ERCP组(P=0.001)[25]。但该研究样本量小、异质性强(未区分既往内镜治疗史、ESWL后ERCP时机在2~43 d不等),结论未被广泛采纳,且过分延长ERCP取石时机会延长住院时间,增加医疗成本。
本研究结果显示,不同时机进行内镜治疗的插管成功率、结石清除率及ERCP后并发症发生率差异无统计学意义。根据既往是否接受ERCP治疗进一步进行亚组分析则显示,既往未接受ERCP治疗的63例患者,超过36 h行ERCP其插管成功率、结石成功清除率显著高于ESWL后12 h内和12~36 h行ERCP。因此,本研究结果支持对既往未接受ERCP治疗的CP患者在碎石后延迟取石时机。
本研究中既往接受过ERCP治疗的107例患者,ESWL后不同时机行ERCP的插管成功率和结石成功清除率的差异不明显,且早期行ERCP治疗效果似乎更佳。其原因可能是既往已行ERCP的患者多数已接受十二指肠乳头括约肌切开、胰管结石取石、胰管支架置入等操作,不同程度地降低了二次ERCP插管和取石的难度。如十二指肠乳头括约肌切开等操作使原有的解剖结构产生变化,胰管开口较大,胰液引流较通畅,对细小结石的冲刷作用增强,有利于自发性排石;胰管支架的置入有利于胰管狭窄的改善,更有利于碎石后胰管结石顺利排出。因此,对既往已接受ERCP的CP患者早期进行碎石后取石亦可取得较好效果,无须延迟取石。
本研究仍存在一定局限性。首先,本研究为回顾性分析,存在一定偏倚,无法对具体结石和胰管形态、既往插管困难程度等因素进行分析。其次,对同一患者未在碎石后不同时机进行十二指肠乳头和胰腺组织肿胀程度的内镜或影像学评估,故无法准确确定ESWL及乳头水肿形成之间的窗口期。本组当日取石患者在ESWL术后接受ERCP的时机范围为30 min~12 h,延迟取石患者的时机范围为2~9 d,有待于今后研究确定更具体的最佳时机。
[1] Khanna S, Tandon RK. Endotherapy for pain in chronic pancreatitis[J]. J Gastroenterol Hepatol, 2010, 23(11):1649-1656. DOI: 10.1111/j.1440-1746.2008.05660.x.
[2] Tandan M, Reddy DN, Santosh D, et al. Extracorporeal shock wave lithotripsy and endotherapy for pancreatic calculi-a large single center experience[J]. Indian J Gastroenterol, 2010, 29(4):143-148. DOI: 10.1007/s12664-010-0035-y.
[3] Rösch T, Daniel S, Scholz M, et al. Endoscopic treatment of chronic pancreatitis: a multicenter study of 1000 patients with long-term follow-up[J]. Endoscopy, 2002, 34(10):765-771. DOI: 10.1055/s-2002-34256.
[4] Ammann RW, Muench R, Otto R, et al. Evolution and regression of pancreatic calcification in chronic pancreatitis. A prospective long-term study of 107 patients[J]. Gastroenterology, 1988, 95(4):1018-1028. DOI:10.1016 / 0016-5085(88)90178-3.
[5] Ebbehøj N, Borly L, Bülow J, et al. Evaluation of pancreatic tissue fluid pressure and pain in chronic pancreatitis. A longitudinal study[J]. Scand J Gastroenterol, 1990, 25(5):462-466. DOI: 10.3109/00365529009095516.
[6] Widdison AL, Alvarez C, Karanjia ND, et al. Experimental evidence of beneficial effects of ductal decompression in chronic pancreatitis[J]. Endoscopy, 1991, 23(3):151-154. DOI: 10.1055/s-2007-1010645.
[7] Greenlee HB, Prinz RA, Aranha GV. Long-term results of side-to-side pancreaticojejunostomy[J]. World J Surg, 1990, 14(1):70-76.DOI: 10.1007/BF01670548.
[8] Nealon WH, Townsend CM Jr, Thompson JC. Operative drainage of the pancreatic duct delays functional impairment in patients with chronic pancreatitis. A prospective analysis[J]. Ann Surg, 1988, 208(3):321-329.DOI: 10.1097/00000658-198809000-00009.
[9] Sauerbruch T, Holl J, Sackmann M, et al. Disintegration of a pancreatic duct stone with extracorporeal shock waves in a patient with chronic pancreatitis[J]. Endoscopy, 1987, 19(5):207-208.DOI: 10.1055/s-2007-1018284.
[10] Li ZS, Wang W, Liao Z, et al. A long-term follow-up study on endoscopic management of children and adolescents with chronic pancreatitis[J]. Am J Gastroenterol, 2010, 105(8):1884-1992. DOI: 10.1038/ajg.2010.85.
[11] Liao Z, Li ZS, Wang W, et al. Endoscopic placement of a covered self-expandable metal stent in the minor papilla in patients with chronic pancreatitis and pancreas divisum[J]. Endoscopy, 2009, 41(Suppl 2):E302-E303. DOI: 10.1055/s-0029-1214851.
[12] Wang W, Liao Z, Li ZS, et al. Chronic pancreatitis in Chinese children: etiology, clinical presentation and imaging diagnosis[J]. J Gastroenterol Hepatol, 2010, 24(12):1862-1868. DOI: 10.1111/j.1440-1746.2009.05967.x.
[13] Kozarek RA, Brandabur JJ, Ball TJ, et al. Clinical outcomes in patients who undergo extracorporeal shock wave lithotripsy for chronic calcific pancreatitis [J]. Gastrointest Endosc, 2002, 56(4):496-500. DOI: 10.1067/mge.2002.128105.
[14] Sauerbruch T, Holl J, Sackmann M, et al. Extracorporeal lithotripsy of pancreatic stones in patients with chronic pancreatitis and pain: a prospective follow up study[J]. Gut, 1992, 33(7):969. DOI: 10.1136/gut.33.7.969.
[15] Testoni PA, Testoni S, Giussani A. Difficult biliary cannulation during ERCP: how to facilitate biliary access and minimize the risk of post-ERCP pancreatitis[J]. Dig Liver Dis, 2011, 43(8):596-603. DOI: 10.1016/j.dld.2011.01.019.
[16] Ong WC, Tandan M, Reddy V, et al. Multiple main pancreatic duct stones in tropical pancreatitis: safe clearance with extracorporeal shockwave lithotripsy[J]. J Gastroenterol Hepatol, 2006, 21(10):1514-1518. DOI: 10.1111/j.1440-1746.2006.04224.x.
[17] Mchenry L, Watkins JL, Kopecky K, et al. Extracorporeal shock-wave lithoptripsy for pancreatic calculi: A 10-year experience at a single U.S. center[J]. Gastrointestinal Endoscopy, 2004, 59(5):P205-P205. DOI: 10.1016/S0016-5107(04)00942-3.
[18] Cotton PB, Lehman G, Vennes J, et al. Endoscopic sphincterotomy complications and their management: an attempt at consensus[J]. Gastrointest Endosc, 1991, 37(3):383-393. DOI: 10.1016/S0016-5107(91)70740-2.
[19] Hu LH, Ye B, Yang YG, et al. Extracorporeal shock wave lithotripsy for Chinese patients with pancreatic stones: A prospective study of 214 cases[J]. Pancreas, 2016, 45(2):298-305. DOI: 10.1097/MPA.0000000000000464.
[20] Dumonceau JM, Delhaye M, Tringali A, et al. Endoscopic treatment of chronic pancreatitis: european society of gastrointestinal endoscopy (ESGE) clinical guideline[J]. Endoscopy, 2012, 44(8):784-800. DOI: 10.1055/s-0032-1309840.
[21] Tringali A, Boskoski I, Costamagna G. The role of endoscopy in the therapy of chronic pancreatitis[J]. Best Pract Res Clin Gastroenterol, 2008, 22(1):145-165. DOI: 10.1016/j.bpg.2007.10.021.
[22] Braganza JM, Lee SH, Mccloy RF, et al. Chronic pancreatitis[J]. Lancet, 2011, 377(9772):1184-1197. DOI: 10.1016/S0140-6736(10)61852-1.
[23] Lehman GA. Role of ERCP and other endoscopic modalities in chronic pancreatitis[J]. Gastrointest Endosc, 2002, 56(6 Suppl):237-240. DOI: 10.1067/mge.2002.129008.
[24] Li BR, Liao Z, Du TT, et al. Risk factors for complications of pancreatic extracorporeal shock wave lithotripsy[J]. Endoscopy, 2014, 46(12):1092-1100. DOI: 10.1055/s-0034-1377753.
[25] Merrill JT, Mullady DK, Early DS, et al. Timing of endoscopy after extracorporeal shock wave lithotripsy for chronic pancreatitis[J]. Pancreas, 2011, 40(7):1087-1090. DOI: 10.1097/MPA.0b013e3182207d05.
[26] Dumonceau JM, Costamagna G, Tringali A, et al. Treatment for painful calcified chronic pancreatitis: extracorporeal shock wave lithotripsy versus endoscopic treatment: a randomised controlled trial[J]. Gut, 2007, 56(4):545. DOI: 10.1136/gut.2006.096883.
[27] Seven G, Schreiner MA, Ross AS, et al. Long-term outcomes associated with pancreatic extracorporeal shock wave lithotripsy for chronic calcific pancreatitis[J]. Gastrointestinal Endoscopy, 2012, 75(5):997-1004. DOI: 10.1016/j.gie.2012.01.014.
