CLSI EP9-A3在两种不同方法测定糖化血红蛋白结果比对及偏倚评估中的应用
2018-04-25胡军红谢建红邓灼斌黄燕莉曹证福毛文杰
胡军红,谢建红,邓灼斌,黄燕莉,曹证福,毛文杰
(佛冈县人民医院,广东 清远511600)
糖化血红蛋白(HbA1c)是人体血液中红细胞内的血红蛋白与血糖进行非酶结合的产物,其反应的是一段时间内病人的血糖控制水平,是用来判断糖尿病患者血糖控制效果的理想指标。但在目前临床应用过程中,由于仪器不同、方法不同以及实验室的检测能力不同,导致HbA1c检测结果间仍有较大差异[1-3],因此探讨不同方法之间HbA1c结果的可比性显得非常重要。我院之前的HbA1c一直是用深圳普门的高效液相色谱法(HPLC)方法进行测定,由于只有一台仪器,除了在仪器发生故障时会影响工作开展,还有碰到可疑的测定结果时,也无法用其他方法去验证,所以最近我们又准备引进宁波美康的免疫比浊法HbA1c测定试剂盒组建新的检测系统,为了了解这两套检测系统测定HbA1c结果的可比性,我们根据2013年8月CLSI发布的EP9-A3《用患者样本进行方法学比对及偏移评估——批准指南;第三版》文件[4],对普门的高效液相色谱法(HPLC)和宁波美康的免疫比浊法这两套HbA1c检测系统测定HbA1c结果进行了系统间的方法比对和偏移评估,现报告如下。
1 材料与方法
1.1 材料
1.1.1 全血样本 收集40例本院住院及门诊病人新鲜全血标本,全血标本采用乙二胺四乙酸二钾盐(EDTA-K2)抗凝,采样后在2-6℃冰箱储存,并在24h内完成测定,标本HbA1c浓度在测量线性范围(3%-18%)内均匀分布,其中在3.0%-6.7%浓度范围内样本13例,在6.9%-9.9%浓度范围内样本13个,在10%-18%浓度范围内样本14例。
1.1.2 仪器与试剂 普门H9高效液相色谱仪及其配套试剂 (批号:H9V1700702)、校准品 (批号:H9V1700702)、质 控 品(批 号 :H9V1700702);日 立7600生化分析仪及美康HbA1c试剂 (批号:17031401)、校准品(批号:17031401)和质控品(Level l:170038;Level 2:171089)
1.2 方法
1.2.1 比对系统 (1)普门H9高效液相色谱仪及其配套试剂组成的HbA1c测定系统为参比系统(X),美康免疫比浊试剂与日立7600生化分析仪组成HbA1c测定系统为待评系统(Y)。
1.2.2 标本测定 按照EP9-A3文件要求,收集的40例糖化血红蛋白标本分别用这两套检测系统随机测定,每套系统对每份标本进行一次测定,并对结果进行记录。测定之前仪器已按相关要求进行了校准,当天的质控数据也在控制范围内。如发现离群值,则应舍弃其结果并补充浓度水平相近的标本再进行测定。
1.2.3 离群值检查 按照EP9-A3文件要求,用目测散点图和ESD方法对40例标本的HbA1c测定结果进行离群值检查。
1.2.4 结果比对与偏倚评估 绘制差值偏差图、百分比差值偏差图、差值排序偏差图和百分比差值排序偏差图和散点图,根据不同检测系统间测定结果的散点图和4种偏差图的具体特征,选择最适合的回归模型进行拟合,并计算医学决定水平处的比例偏移及偏移95%的CI,以偏移值在95%CI范围内和比例偏移≤1/2允许总误差(±4%)作为它的可接受标准。
1.3 统计学软件及方法 采用微软公司Excel 2010和SPSS 19.0软件处理测定数据。计量资料用(x±s)表示,通过分析测定数据的4种偏差图和散点图的具体特征,选取最合适的回归模型进行计算,显著性检验采用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 离群值检验结果
2.1.1 目测分析:从图1的散点图可以发现,两种不同系统检测的40例标本HbA1c结果有非常好的相关性(R2=0.9982),目测分析没有发现离群值。
2.1.2 ESD法检验:根据广义极端学生化偏差ESD计算公式:ESD=max(|dj-d|)/SD,第31号样本差值最大,经计算,ESDmax=2.35,根据实验统计的样本量n=40,设定α=0.05的情况下,查询ESD临界值表,λ=3.04,故当 i=1 时,ESD1<λ1,此 2 种方法 HbA1c检测结果具有非常好的相关性,ESD法检验没有发现离群值。
2.2 结果比对与偏倚评估
2.2.1 方法间差值的偏差图特征分析及相应的回归模型选择:按照EP9-A3文件要求对此40份血清标本的HbA1c结果绘制数值偏差图 (图2A)、百分比差值偏差图(图2B)、差值排序偏差图(图2C)、百分比差值排序偏差图(图2D)等。普门高效液相色谱法与美康免疫比浊法比较,两者差值变化为恒定值,两种方法测定结果总体呈现线性变化趋势,相关系数R2≥0.95,故选择OLR回归分析模型进行拟合。
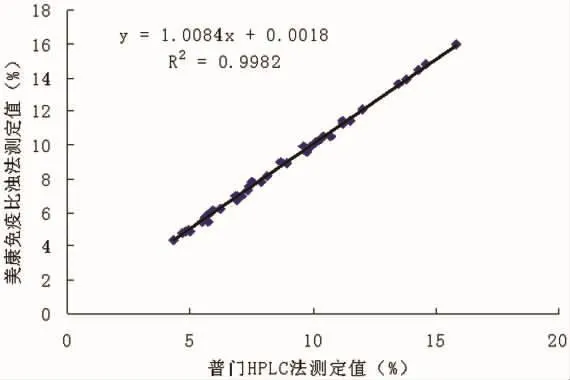
图1 2种不同方法测定HbA1c结果散点图
2.2.2 回归方程选择及偏移评估结果:EP9-A3虽然提供了 4种模型进行回归分析(OLR、WLS、Deming、Passing-Baklok),但根据这2种方法测定结果的上述4张偏差图和散点图表现出来的数值变化特点-各数据点差值变化相对一致(恒定SD),相关系数R2≥0.95,我们选取OLR作为最佳回归模型进行拟合,其回归方程为Y=1.0084X+0.0018。将10%、16%这两个HbA1c医学决定水平值分别代入拟合方程,其在医学决定水平处的偏移值分别为0.086%和0.136%,均在偏移的95%的CI范围内,其比例偏移分别为0.85%、0.84%,均小于±4%的可接受标准。(见表1)。
3 讨论

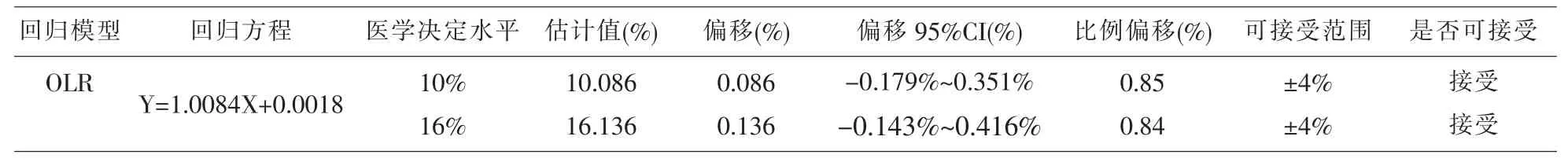
表1 HbA1c比对OLR回归模型在医学决定水平处的偏移结果
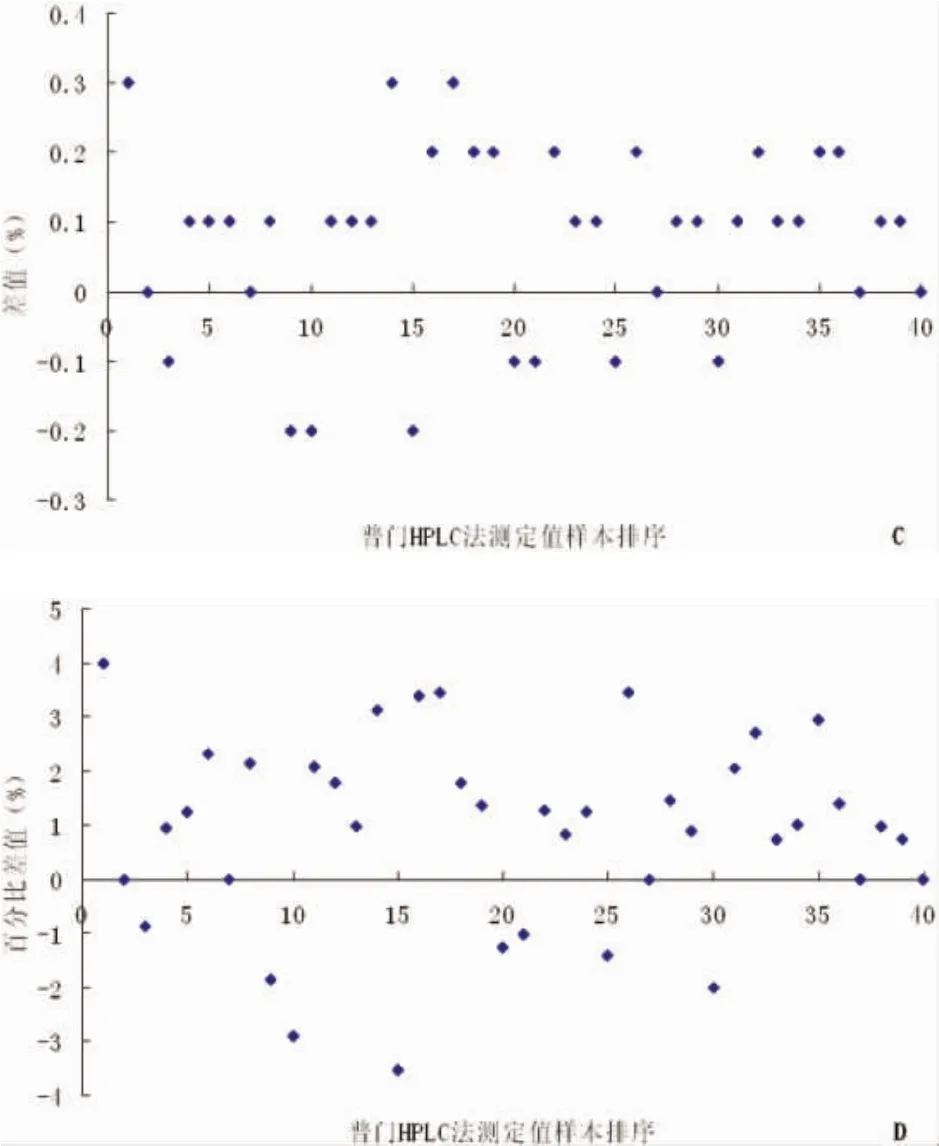
图2 普门高效液相色谱法与美康免疫比浊法测定HbA1c差值偏差图与排序偏差图
近年来,HbA1c在糖尿病的筛查、诊断和治疗中及糖尿病相关并发症的诊断和治疗中发挥着非常重要的作用[5-8],所以为临床提供准确的HbA1c结果显得尤为重要。由于目前糖化血红蛋白测定方法有很多种,如有高效液相色谱法、电泳法、免疫比浊法、亲和层析法及酶法等方法,其测定原理也各异[9],所以仪器的不同、方法学的不同及实验室人员检测能力的不同会导致HbA1c检测结果间存在较大差异[10-12]。因为工作的需要,本实验室在原普门HPLC法测定HbA1c的基础上,准备引进美康免疫比浊法试剂与日立7600组成新的HbA1c测定系统,根据医学实验室质量和能力认可准则[13]要求,实验室使用两套及以上检测系统检测同一项目时,应对其检测结果的一致性进行验证。由于普门HPLC法HbA1c仪器已在实验室使用较长时间,其室间质评成绩优秀,CV值<2%,故以此作为参比系统,新引进美康免疫比浊法试剂盒和日立7600组成的HbA1c测定系统作为待评系统与其进行结果比对和偏倚评估分析。参考EP9-A3文件及其他相关论文[14,15],我们绘制了这两种检测系统之间HbA1c测定值的散点图,没发现有明显的离群结果,然后用ESD法检验进一步确认无离群值点。接下来通过分析两种系统间的4种偏差图(差值偏差图、百分比差值偏差图、差值排序偏差图和百分比差值排序偏差图)的变化特征,发现这两种不同方法的测定HbA1c结果呈现线性变化趋势,两者差值总体呈现恒定SD变化,相关系数R2≥0.95,因此我们对这两种方法间的比较分析选取了OLR回归分析模型进行拟合,其回归方程为Y=1.0084X+0.0018。将HbA1c两个医学决定水平10%、16%分别代入回归方程中,结果显示,其两个医学决定水平处的偏移值分别为0.086%和0.136%,均在医学决定水平偏移的95%CI范围内,其比例偏移值为0.85%、0.84%,均小于±4%的可接受标准,所以普门的高效液相色谱法与美康免疫比浊法这2种不同方法测定HbA1c的结果具有可比性,均能满足临床需求。
[1]中华人民共和国国家卫生和计划生育委员会.WS/T461-2015:糖化血红蛋白检测 [S].2015-06-23)[2015-12-31].http://www.nhfpc.gov.cn/ewebeditor/uploadfile/2015/07/20150703091900134.pdf.
[2]居漪.再谈糖化血红蛋白[J].检验医学,2015,30(6):547-553.
[3]薛声能,程桦.糖化血红蛋白的研究进展[J].国际内科学杂志,2008,35(10):586-588,601.
[4]Clinical and Laboratory Standards Institute.Measurement Procedure Comparison and Bias Estimation Using Patient Samples;Approved Guideline-Third Edition[S].Wayne,PA:CLSI,2013.
[5]骆斯慧,赵咏桔.糖化血红蛋白A1c在糖尿病监测和诊断中的应用[J].国际内分泌代谢杂志,2011,31(1):9-12.
[6]刘艳梅.糖化血红蛋白在糖尿病中的临床应用[J].国际检验医学杂志,2007,28(11):1035-1037.
[7]戴晓灵.糖化血红蛋白在糖尿病诊治中的应用[J].检验医学与临床,2008,5(6):373-374.
[8]闫威,姜海燕.糖化血红蛋白检测在糖尿病监测中的价值[J].中国现代药物应用,2010,4(8):169.
[9]林莉,戴永辉,徐建华,等.三种不同方法测定糖化血红蛋白的结果比对和偏移评估分析[J].中华医学杂志,2016,96(8):650-654.
[10]雷斌,李碧.糖化血红蛋白的检测意义及常用方法比较[J].国际检验医学杂志,2015,36(10):1458-1460.
[11]田伟,陈榕方,王毅,等.糖化血红蛋白五种检测方法的评价[J].实验与检验医学,2014,32(3):252-263.
[12]宋银丹,段勇.糖化血红蛋白检测标准化的研究进展[J].实验与检验医学,2013,31(2):108-130.
[13]中国合格评定国家认可委员会.CNAS-CL02:医学实验室质量和能力认可准则[EB-OL].(2013-11-22)[2014-11-01].https://www.cnas.org.cn/images/rkgf/sysrk/jbzz/2013/12/20/1C3A61EEC69A825B0FD01ECD986D9B78.pdf
[14]徐建华,刘冬冬,黄宪章,等.CLSI EP9-A3在临床生化方法学比对中的应用[J].中华检验医学杂志,2015,38(5):346-348.
[15]徐建华,黄宪章,庄俊华,等.新指南CLSI EP9-A3在方法学比对及偏移评估中的应用 [J].中华医学杂志,2015,95(12):894-897.
