质子化壳聚糖/磁性复合材料对含磷污水中磷的吸附特性
2018-04-14祝向荣李国超陈秋荣
陈 力, 祝向荣, 李国超, 黄 雄, 陈秋荣
(1.上海第二工业大学 环境与材料工程学院,上海201209;2.浙江中科院应用技术研究院,嘉兴314022)
0 引言
水体富营养化使得河湖藻类爆发,水体发黑变臭,水体生态系统遭受破坏,许多动植物死亡,不仅如此,由此带来的水体污染也使得我国逐渐成为水质型缺水国家。导致水体富营养化的因素有:氨氮,COD,总磷等。其中磷是富营养化水体治理与修复的重点与难点所在[1],根据《地表水环境质量标准》,V类水的总磷含量不能超过0.4 mg/L,如何高效地去除含磷污水中的磷成为当前污水治理中一个非常重要的问题。
目前,处理含磷污水的方法主要有反相渗透法、生物法、膜分离法和吸附法等。其中,吸附法因其工艺简单而得到广泛应用[2],被用于吸附法的吸附剂有很多种,壳聚糖被认为是“绿色的水处理剂”[3]。壳聚糖是甲壳素脱乙酰化的产物,分子链中含有大量的—NH2和—OH等活性基团,可用作重金属离子螯合剂和吸附剂等,并且不会产生二次污染[4]。单纯地使用壳聚糖进行水体净化的效果不佳,在实际应用时往往通过对其进行改性以提高其吸附效率,如对壳聚糖的—NH2官能团进行质子化改性,使其成为,这有利于提高其对水体中、、等阴离子的吸附率[5-6];或者对壳聚糖进行交联接枝改性,提高其—NH2含量,从而达到提高对金属阳离子吸附容量的效果[7]。另外,将壳聚糖与其他材料进行复合,制备出一种新型复合材料,从而使吸附剂兼具两者共同的优点,如近年来被广泛关注的磁性壳聚糖复合材料[8-10]。壳聚糖与磁性材料的复合,可以提高壳聚糖吸附剂的稳定性,结合磁性分离技术便于回收等[11]。目前,磁性壳聚糖在去除污水中重金属离子方面的研究较多,但其应用于污水除磷方面的报道较少。
本文综合考虑质子化的壳聚糖在吸附磷方面的独特性能,将其与Fe3O4磁性颗粒进行复合,制备一种质子化磁性壳聚糖复合材料,并对模拟含磷污水中磷的吸附特性进行研究。首先采用共沉淀法制备Fe3O4磁性颗粒,采用稀硫酸溶液对壳聚糖进行质子化改性处理,再采用反相悬浮交联法将2种材料进行交联复合,研究了质子化壳聚糖磁性复合材料对模拟含磷污水中磷的吸附特性,考察了原水pH、吸附剂、吸附时间、溶液初始浓度、吸附剂投加量等对除磷效果的影响,并对吸附过程进行了动力学与等温吸附模型分析。
1 材料与方法
1.1 主要试剂和分析仪器
主要试剂:壳聚糖、浓硫酸、氢氧化钠和氨水均采购自国药集团化学试剂有限公司;FeCl2·4H2O和FeCl3·6H2O采购自上海埃彼化学试剂有限公司;磷标液由国家有色金属及电子材料分析测试中心提供,其浓度为1 000 mg/L,磷的形态为;等温吸附实验中所用磷溶液由采购自国药集团化学试剂有限公司的磷酸二氢钾配得。
主要分析仪器:电感耦合等离子体原子发射光谱(inductive coupled plasma atomic emission spectrometry,ICP-AES)仪测试溶液中磷含量,X射线衍射(X-ray diffraction,XRD)仪和傅立叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)仪测试质子化壳聚糖的结构特性,振动样品磁强计(vibrating samplemagnetometer,VSM)测量样品的磁性,扫描电子显微镜(scanning electron microscope,SEM)测试样品表面形貌特性。
1.2 磁性壳聚糖的制备
1.2.1Fe3O4的制备
采用共沉淀法制备Fe3O4材料。配制2 mol/L的 NaOH 溶液,再取 0.02 mol的 FeCl2·4H2O 和0.035 mol的FeCl3·6H2O分别配制成 50 mL水溶液。随后将其混合均匀,并立即将溶液转入500 mL烧杯,并加入配制好的2 mol/L氢氧化钠100 mL,以及60 mL氨水以隔绝空气。整个反应在水浴60◦C下搅拌1 h,在溶液经过陈化后,用磁铁吸引分离,并用蒸馏水和乙醇反复洗涤至中性,以洗去粒子表面未反应的杂质离子,在真空75◦C下干燥12 h,研磨得到磁性Fe3O4颗粒。
1.2.2质子化壳聚糖的制备
将浓硫酸按照一定的体积比加水进行稀释,配制pH分别为1.5,2.5,3.5,4.5,5.5的5种稀硫酸溶液,然后各取180 mL上述不同pH值的稀硫酸溶液于烧杯中,用电子分析天平称取3.0 g的壳聚糖粉末置于各烧杯中,搅拌均匀形成稳定的悬浊液,稳定8 h后,抽滤、用去离子水洗涤至中性,随后放入鼓风干燥箱,80◦C温度下烘干,约10 h后取出研磨,得到质子化处理的壳聚糖粉末。样品装袋封存备用,按质子化处理时的稀硫酸溶液pH值,分别标记为CS1.5,CS2.5,CS3.5,CS4.5,CS5.5。将未经质子化处理的壳聚糖样品标记为CS。样品的质子化程度由质子化处理时的稀硫酸溶液pH值衡量,pH值越低,样品质子化程度越大。
1.2.3质子化壳聚糖磁性复合材料的制备
采用反相悬浮交联法制备磁性壳聚糖。首先配制15 mL质量分数为5%的醋酸溶液,采用超声分散法将一定质量的上述6种壳聚糖样品分别溶解于其中;随后,将0.15 g的Fe3O4粉末加入该溶液,超声分散搅拌10 min,达到混匀状态。Fe3O4与每种壳聚糖质量比分别为1:1.5,1:2.5,1:3.5。再将15 mL上述悬浮液逐滴加入到由56 mL矿物油和3.75 g吐温80组成的混合液中,并在2 000 r/min转速下机械搅拌30 min,之后逐滴加入7.5 mL的戊二醛,在40◦C下再搅拌1 h以促进交联,形成油状的混合液。最后,通过磁铁吸附,将磁性微球从油相中分离出来,用乙醇和丙酮多次洗涤,在50◦C下烘干4 h,然后研磨,得到最终的磁性复合材料样品。按复合过程所用壳聚糖的质子化程度,将复合材料样品分别标为A,B,C,D,E,F,其中质子化度最高的为A,未经质子化的标为F;按照Fe3O4与壳聚糖的质量比1:1.5,1:2.5,1:3.5,将其分别标为1,2,3。这样制备出A1、A2、A3、B1、B2、B3、C1、C2、C3、D1、D2、D3、E1、E2、E3、F1、F2、F3共18种不同配比的质子化壳聚糖磁性复合材料。
1.3 吸附实验
配制含磷的模拟污水:将所购置的磷标液分别稀释到1,5,10,20 mg/L浓度,以备吸附实验用。
实验1 考察吸附时间对质子化磁性壳聚糖吸附磷的影响。分别取0.05 g的前述18种磁性壳聚糖吸附剂置于50 mL初始浓度为5 mg/L的含磷溶液,调节pH为6,在室温条件下,所取的时间点为:20 min,40 min,60 min,2 h,4 h,8 h。
实验2 考察模拟污水初始磷浓度对吸附特性的影响。另用磷酸二氢钾药品配制含磷模拟废水,浓度分别为10,250,500,1000,2000 mg/L。取0.01 g磁性壳聚糖吸附剂E2,分别置于40 mL浓度分别为10,250,500,1000,2000 mg/L的含磷溶液中,调节pH为4.5并在室温条件下吸附7 h。
实验3 五因素四水平的正交实验。因素条件分别为:①吸附剂种类:C1,C2,E2,F2;②吸附时间:6,7,8,9 h;③溶液初始pH值:2,3,4.5,6;④溶液浓度:1,5,10,20 mg/L;⑤吸附剂投加量:0.01,0.05,0.1,0.2 g。该吸附反应是在室温条件下,每个反应溶液的体积为50 mL。
1.4 ICP-AES测试溶液中磷含量的方法
ICP-AES测试过程中,先建立方法,选择特征波长为213.62 nm的磷元素谱线。通过已知磷浓度的标准溶液(分别是0,1,3,5,10,20 mg/L)的谱线强度建立标准曲线。然后,用ICP-AES检测待测含磷溶液的谱线强度,并根据标准曲线确定溶液的磷浓度。待测溶液检测前以质量分数为1%的HNO3溶液进行酸化预处理。如果待测溶液中含磷较高,需先将其稀释到标准曲线测试范围内。
2 结果与讨论
2.1 材料表征
图1为CS5.5,Fe3O4和E2的XRD图谱。首先,图中显示CS5.5样品在2θ分别为10◦和20◦时各有1个衍射峰。其次,从图中可以看出,Fe3O4具有典型的尖晶石结构特性,其6个典型特征峰2θ分别为30.4◦,35.6◦,43.2◦,53.6◦,57.3◦,62.8◦,分别对应于Fe3O4不同的晶面:(220),(311),(400),(422),(511),(440)[12]。另外,E2的XRD图谱可见,其仍保留了Fe3O4尖晶石结构特征,只是Fe3O4峰的强度有所减弱;复合材料中的壳聚糖相只在2θ为10◦时显示了较强的衍射峰,而且峰位置略微向高角度偏些,这是由于复合交联过程导致分子间氢键减弱以及壳聚糖晶体结构的变化[13]。

图1 CS5.5、Fe3 O4及E2的XRD图谱Fig.1 XRD patterns of CS5.5,Fe3O4 and E2
图2(a)和图2(b)分别为纯Fe3O4和E2的SEM图像。图中显示,所制备的Fe3O4颗粒的粒径在20~30 nm。对于E2样品,图中显示研磨不够彻底,但总体上E2的平均粒径增加到50 nm左右,这是因为Fe3O4在与质子化壳聚糖交联复合之后,质子化壳聚糖包裹在Fe3O4颗粒周围,形成粒径更大的复合材料颗粒。

图2 Fe3O4和E2的SEM图Fig.2 SEM imagesof Fe3O4 and E2
图3分别显示了CS5.5,纯Fe3O4和E2的FTIR图谱。由图可知,对于纯Fe3O4和E2样品,在557 cm−1处显示的吸收峰为Fe3O4相的Fe—O振动吸收峰。与质子化壳聚糖的FTIR图谱相对照,E2样品1 717 cm−1处的小峰为壳聚糖悬挂醛基的吸收峰,1 643 cm−1处为C==O键的特征吸收峰,说明戊二醛参与了交联反应,1 072 cm−1为壳聚糖中—CH2—的特征吸收峰,以上特征峰说明制备的磁性壳聚糖是成功的[11]。

图3 CS5.5、Fe3 O4及E2的FTIR图谱Fig.3 FTIRspectra of CS5.5,Fe3 O4 and E2
纯Fe3O4和E2的磁化曲线见图4。Fe3O4的饱和磁化强度,在与壳聚糖进行复合后有明显的下降。这是因为壳聚糖属于天然高分子有机物,不具有磁性,同时又包裹在Fe3O4的周围,从而使得复合后的磁性壳聚糖的磁化强度下降。两者的饱和磁化强度分别为53.03和4.35(A·m2)/kg。
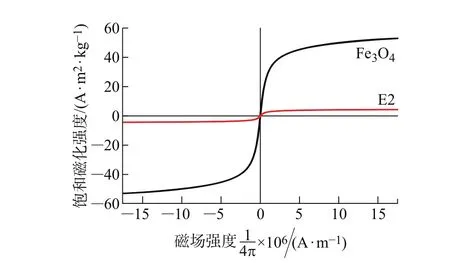
图4 Fe3O4和E2的VSM图Fig.4 The VSM curvesof Fe3O4and E2
2.2 磁性壳聚糖的除磷性能
2.2.1吸附时间的影响
在室温条件下,取0.05 g的18种磁性壳聚糖吸附剂放入浓度为5 mg/L、50 mL的含磷溶液中,考察吸附时间对除磷性能的影响,结果见图5。可以得出吸附时间在4 h以内,去除率随时间增长较快;吸附时间在4 h以后,吸附逐渐达到饱和。吸附8 h后,吸附剂E2对磷的去除率最高,可达80%左右;吸附剂A1和A3对磷的去除率最低,只有20%左右。不同配比的磁性壳聚糖在对磷的吸附性能上具有较为明显的差异,去除率的大小受壳聚糖质子化度以及Fe3O4与壳聚糖质量比的影响比较大。对于A系列样品,其质子化程度最高,但其吸附性能反而较低。
冼昶华[14]采用硫酸溶液处理壳聚糖,并研究其对含磷污水的处理效果,结果表明,0.2 g质子化壳聚糖投入浓度为5 mg/L、50 mL的含磷溶液中,其对磷的最佳去除率为74%;仉春华等[1]通过稀硫酸溶液制备质子化壳聚糖,考察了其对含磷污水的处理效果,结果表明,0.2 g的质子化壳聚糖放入浓度为5 mg/L、50 mL的含磷溶液中,其对磷的去除率在60%以上。而本文中所制备的质子化磁性壳聚糖复合吸附剂的去除率最高达到80%,吸附剂投放量为0.05 g,表明磁性复合后,吸附剂的吸附能力得到了提升。其吸附性能的提高可能是质子化壳聚糖与Fe3O4交联复合后,复合材料可能具有疏松的结构特性,且包覆的质子化壳聚糖本身对溶液中磷酸根离子具有较好的吸附性能,即壳聚糖的—NH2被质子化为—NH3,从而与以阴离子形式存在的磷酸根离子产生静电吸附作用,从而使得复合材料比未复合的质子化壳聚糖具有更好的吸附效果。
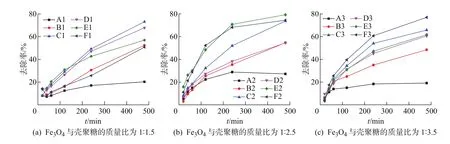
图5 磁性壳聚糖吸附剂对含磷溶液的磷去除率随时间的变化曲线Fig.5 Thecurvesof phosphorusremoval rateof magnetic chitosan adsorbents
值得注意的是,对于未质子化的样品F2,以及质子化程度居中的C1和C2样品,其饱和去除率也较高。为了更进一步探讨复合材料的吸附性能,从18种吸附剂中筛选出去除率较高的C1、C2、E2、F2这4种吸附剂进行后面的正交实验。
2.2.2浓度的影响
图6所示为实验2条件下E2对不同初始浓度的含磷溶液吸附的特性,其中吸附剂的投入量是实验1的1/5。由图6可知:一方面,由于吸附剂投放量的减少,最大磷去除率只有16%左右;另一方面,随着初始溶液浓度的增加,磷去除率逐步降低。这是因为初始浓度不断加大,而吸附剂的投加量却固定不变,单位质量吸附剂对磷的吸附量是有限的,且吸附剂逐渐达到饱和状态从而使整体去除率呈下降趋势。然而,从吸附量的曲线可以看出,随着溶液初始浓度的增加,直达到2 000 mg/L,其吸附量也逐渐增加,最高达到400 mg/g,但仍没有达到一种平衡状态,这可能是由于该吸附过程并非单分子层吸附,很可能属于多分子层吸附。

图6 E2的磷去除率与吸附量的变化曲线Fig.6 The curves of phosphorus removal rate and adsorption capacity of E2
2.2.3正交实验
采用极差分析法分析实验3中正交实验的结果,见表1。根据极差R值的大小,可以判断出各因素的影响主次,在本实验中按影响程度排序为:溶液pH值>吸附剂类别>投加量>浓度>时间;而根据K值的大小(Ki表示任意列上水平号为i时所对应的试验结果之和)可以判断每个影响因素中最优水平是哪个。将因素主次与最优水平相组合,就得到该实验的最佳吸附组合条件。在本实验中,最优组合为:pH的影响最为显著,最优pH为6;吸附剂和投加量的影响次之,最优水平分别为F2和0.1 g;而浓度和时间的影响最弱,最优水平分别为1 mg/L和8 h。
2.3 吸附动力学
同实验1,分别取0.05 g磁性壳聚糖C1,C2,E2,F2置于浓度为5 mg/L、50 mL的含磷溶液中。室温条件下,分别取20,40,60,120,240 min这5个时间点,研究磁性壳聚糖吸附磷的动力学过程。Lagergren[15]准二级动力学方程是常用的用来预测吸附过程随时间变化情况的方程之一。吸附速率大小由吸附剂表面未被占有的吸附空位数的平方决定,其动力学方程为:
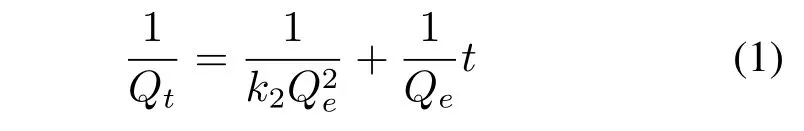
式(1)中:Qt为t时刻的吸附量,mg/g;Qe为平衡吸附量,mg/g;k2为表观吸附速率常数,g/(mg·min)。
根据Lagergren准二级动力学方程进行数据拟合处理,结果如图7和表2所示。
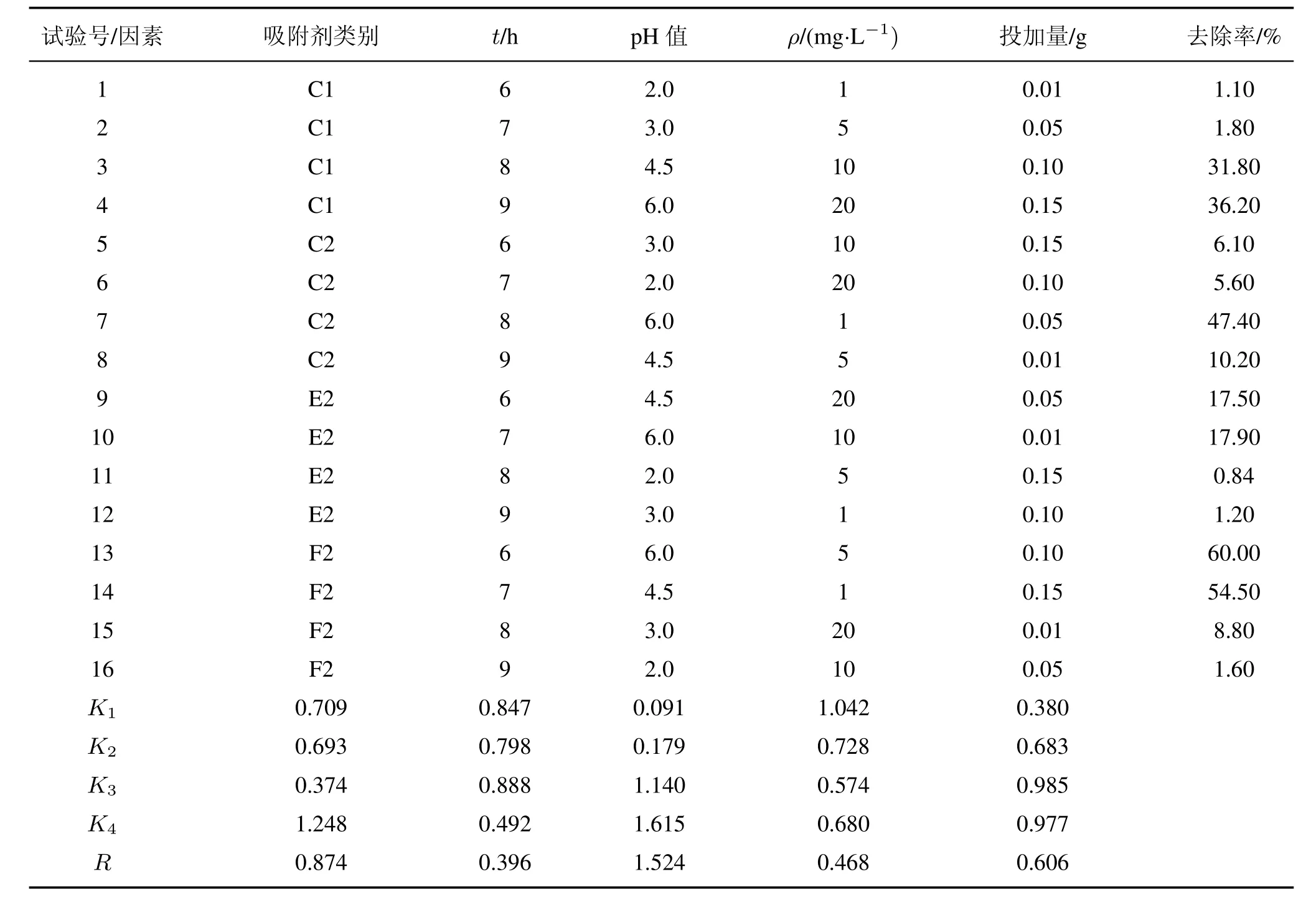
表1 磁性壳聚糖对磷吸附的正交实验分析表Tab.1 Orthogonal experimental analysis of phosphorus adsorption by magnetic chitosan
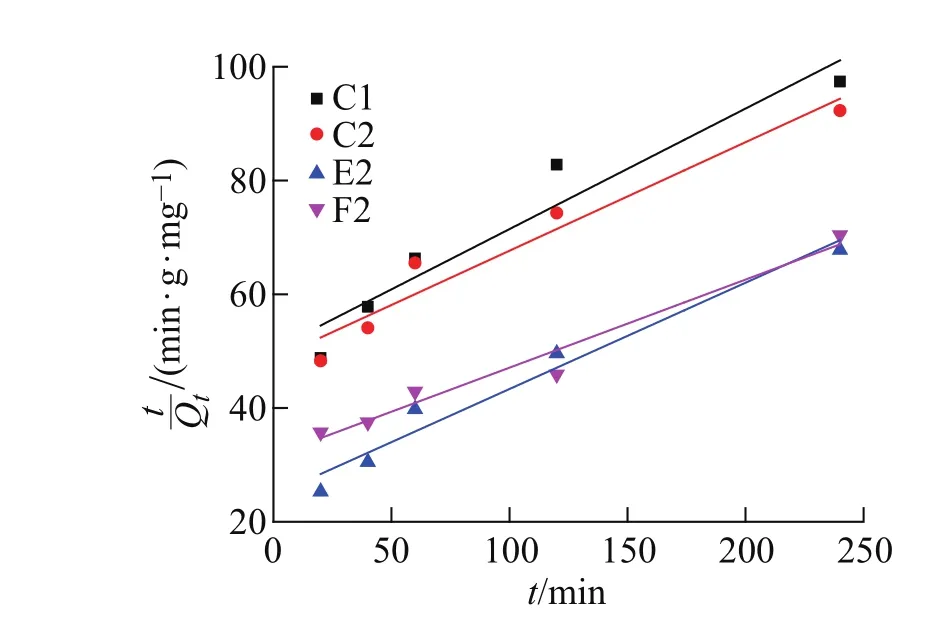
图7 质子化壳聚糖对磷吸附动力学过程Fig.7 Adsorption kinetics process of protonated chitosan for phosphorusadsorption
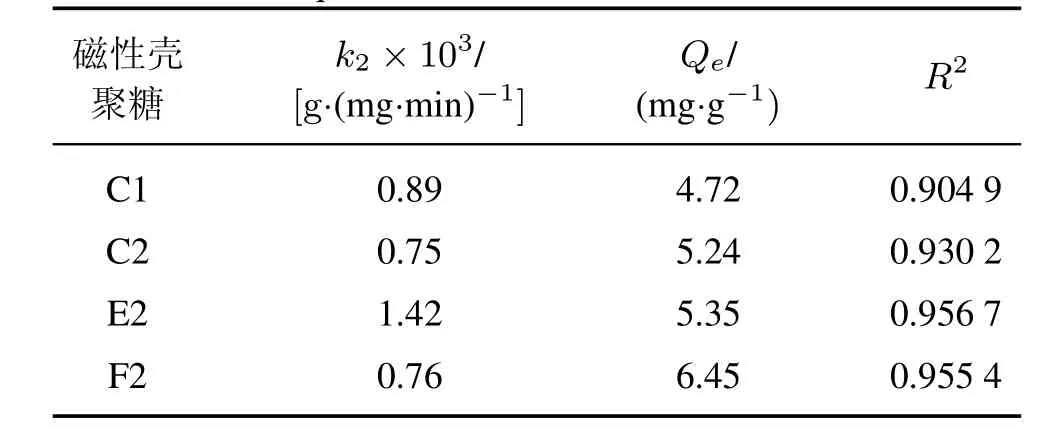
表2 Lagergren准二级动力学方程的动力学参数Tab.2 Kinetic parameters of Lagergren pseudo-second-order kinetic equation
研究结果显示各样品对应的线性相关系数的平方R2均大于0.9,揭示了较好的线性关系,这说明准二级动力学模型可以很好地描述质子化壳聚糖磁性复合材料对磷的吸附过程。由于准二级动力学吸附模型的主要影响因素在于化学键的形成,故可推断该吸附过程主要为化学吸附[16]。
3 结 论
采用反相悬浮交联法制备出18种磁性壳聚糖吸附剂,对磁性壳聚糖吸附含磷模拟污水的磷吸附特性研究结果表明:
(1)将0.05 g的18种磁性壳聚糖分别放入浓度为5 mg/L、50 mL的含磷溶液中,其去除率最高可达80%左右,最低只有20%左右。这说明不同配方的磁性壳聚糖在对磷的吸附性能上具有较为明显的差异,去除率的大小受壳聚糖质子化度以及Fe3O4与壳聚糖质量比的影响比较大。
(2)随着含磷溶液中磷浓度的增加,其去除率也逐步降低,然而其吸附量却仍然增加,并没有达到一种平衡状态,但增加的趋势变缓,这可能是由于该吸附过程并非单分子层吸附,很可能属于多分子层吸附。
(3)从正交实验可以得到,吸附溶液的pH值对整个吸附过程的影响最为明显,最佳pH为6;吸附剂和投加量的影响次之,但仍具有较明显影响;浓度和时间的影响最弱。
(4)动力学分析表明,Lagergren准二级动力学模型可以很好地描述质子化壳聚糖磁性复合材料对磷的吸附过程,吸附过程主要表现为化学吸附。
总体来说,质子化壳聚糖磁性复合材料在污水治理的研究还局限于实验室,其吸附的机理还需要进一步深入探索,但是作为一种绿色环保的吸附剂,质子化壳聚糖磁性复合材料仍旧展示了其良好的应用前景。
参考文献:
[1] 仉春华,王文君,安晓雯,等.质子化壳聚糖的除磷性能[J].环境工程学报,2013,7(2):568-572.
[2] 佘健.改性钢渣去除废水中磷酸盐的试验研究[D].武汉:武汉理工大学,2007.
[3] 姚瑞华,孟范平,张龙军,等.改性壳聚糖对重金属离子的吸附研究和应用进展[J].材料导报,2008,22(4):65-70.
[4] BRATBY J.Coagulation and fl occulation in water and wastewater treatment[M].2nd ed.IWA Publishing:London,2006.
[5] 权雪婷,李林波,郭莹娟,等.质子化改性交联壳聚糖的制备及其吸附硫酸根离子的性能[J].环境工程学报,2014,8(8):3228-3232.
[6] YAO W,RAO PH,et al.Preparation of cross-linked magnetic chitosan with quaternary ammonium and its application for Cr(VI)and P(V)removal[J].Journal of Environmental Sciences,2014,26(12):2379-2386.
[7] 周利民,王一平,黄群武.乙二胺改性壳聚糖磁性微球吸附和[J].核化学与放射化学,2007,29(3):184-188.
[8] 陈志军,朱海燕,郝营,等.Fe3O4-壳聚糖磁性微球的制备及对Cu2+的吸附性能[J].郑州轻工业学院学报(自然科学版),2012,27(2):1-4.
[9] FUNESA,VICENTE D J,VICENTE D I.Synthesis and characterization of magnetic chitosan microspheresaslowdensity and low-biotoxicity adsorbentsfor lake restoration[J].Chemosphere,2017,171:571-579.
[10]YANG W C,TANG Q Z,DONG S Y,et al.Single-step synthesis of magnetic chitosan composites and application for chromate removal[J].JCent South Univ,2016,23(2):317-323.
[11]魏艳芳.磁性壳聚糖微球的制备及对磷的吸附性能研究[J].广州化学,2010,35(4):29-34
[12]汪婷,高滢,金晓英,等.纳米四氧化三铁同步去除水中的Pb(II)和Cr(III)离子[J].环境工程学报,2013,7(9):3476-3482.
[13]XIE Y H,LI S Y,WANG F,et al.Removal of perchlorate from aqueous solution using protonated cross-linked chitosan[J].Chemical Engineering Journal,2010,156(1):56-63.
[14]冼昶华.壳聚糖对水中磷的吸附处理研究[J].化工时刊,2008,22(3):29-31.
[15]HO Y S.Second-order kinetic model for the adsorption of cadmium onto tree fern:A comparison of linear and nonlinear methods[J].Water Res,2006,40(1):119-125.
[16]孙小莉,曾庆轩,冯长根.多胺型阴离子交换纤维吸附铬(VI)的动力学[J].物理化学,2009,25(10):1951-1957.
