新型BODIPY类荧光探针及其对食品中Hg2+检测的应用
2018-04-11熊晓辉
冷 玲,李 壹,熊晓辉
(南京工业大学 食品与轻工学院,江苏 南京 211800)
汞是环境中具有很强生理毒性的重金属元素之一,即使在极低浓度下,也会通过消化道、呼吸道和皮肤进入人体内,对神经系统和内分泌系统造成实质性的损害[1-3]。汞中毒和汞污染事件常有报道,相关食品安全问题严重威胁着人们的生命健康。建立一种快速、灵敏、高选择性的食品中Hg2+的检测分析方法具有重要意义。
常见Hg2+的检测方法有冷蒸汽原子吸收光谱法(CVAAS)[4]、电感耦合等离子体原子发射光谱法(ICP-AESS)[5]、电感耦合等离子体质谱法(ICP-MS)[6]和电化学法[7]等。尽管这些方法灵敏度高、检出限低,但所需设备昂贵,样品预处理复杂。荧光分析法利用探针与Hg2+发生相互作用,诱导荧光基团结构变化,进而体系产生荧光信号响应。该方法操作简单,成本不高,可对Hg2+选择性识别,实现对样品中Hg2+的裸眼可视化实时监测,所以目前对Hg2+荧光探针的研究备受关注。
氟硼吡咯类(BODIPY)衍生物具有摩尔消光系数较大、紫外吸收峰和荧光发射峰窄、荧光量子产率高、氧化还原电位合适[8-9]、母体对极性和pH的耐受性良好、在生理环境下不易被干扰[10-11]等优点。本文中,笔者将2,4-二甲基-3-乙基吡咯与对甲酰基苯甲酸甲酯在三氟乙酸(TFA)催化下发生缩合、氧化和水解反应,制得新型探针SOH,具体合成路线见图1。基于Hg2+诱导探针发生光致诱导电子转移(PET)的原理,体系表现出荧光由强变弱的现象,从而建立Hg2+的检测方法。根据GB 2762—2017《食品安全国家标准食品中污染物限量》规定,矿泉水的总汞限量为0.001 mg/L(相当于0.004 985 μmol/L Hg2+),粮食的总汞限量为0.02 mg/kg(相当于0.099 7 μmol/L Hg2+),食肉鱼类总汞限量为1.0 mg/kg(相当于4.985 μmol/L Hg2+)。

图1 探针SOH的合成路线Fig.1 Synthetic route of probe SOH
1 材料与方法
1.1 主要原料及试剂
2,4-二甲基-3-乙基吡咯、对甲酰基苯甲酸甲酯、TFA、2,3-二氯-5,6-二氰基-1,4-苯醌(DDQ)、三氟化硼乙醚(BF3·OEt2)、磷酸缓冲盐溶液(PBS),阿拉丁试剂(上海)有限公司;三乙胺(TEA)、NaOH、浓盐酸、甲醇、无水Na2SO4、无水MgSO4,国药集团化学试剂有限公司;二氯甲烷(DCM)、乙酸乙酯、石油醚,西陇化工股份有限公司;硅胶(粒度53~75 μm),青岛海洋化工厂。
矿泉水、大米和鮟鱇鱼样品购于当地超市。
1.2 主要设备及仪器
ZF-20D型暗箱式紫外分析仪,上海宝山顾村电光仪器厂;78-1型磁力加热搅拌器,上海司乐仪器有限公司;ZNHW-II型精密电子控制仪,杭州大卫科教仪器有限公司;RE-52型旋转蒸发器,上海亚荣生化仪器厂;RF-5301PC型荧光分光光度仪,日本岛津;Cary 60型紫外-可见分光光度计,美国安捷伦公司;1100HPLC/MSD型质谱仪,美国安捷伦公司;BRUKER AM-300/500型核磁共振仪,德国Bruker公司;DZF-6050型真空干燥箱,上海一恒科学仪器有限公司;AVP2000型高压试验型均质机,丹麦AVP公司。
1.3 探针SOH的合成与表征
化合物SOMe的合成:将2,4-二甲基-3-乙基-吡咯(0.246 g,2 mmol)加入圆底四口烧瓶,再加入100 mL无水二氯甲烷,通Ar,磁力搅拌下加入对甲酰基苯甲酸甲酯(0.164 g,1 mmol),继续加入1滴TFA,室温下避光反应过夜,淡黄色澄清溶液变为深紫色溶液;薄层层析(TLC)点板监测醛是否反应完全;再加入DDQ(0.227 g,1 mmol),搅拌1 h,溶液变为深红色;然后加入TEA(2 mL,15.8 mmol),室温下搅拌10 min;再加入BF3·OEt2溶液(2 mL,15.8 mmol),搅拌2 h,得反应混合物;将反应混合物用无水Na2SO4饱和溶液洗涤,无水MgSO4干燥,旋蒸去溶剂,得粗产物;将粗产物用硅胶层析纯化,得化合物SOMe(0.171 g,产率:39.02%)。1H NMR(CDCl3,400 MHz)δ∶ 8.17(d,J=8.4 Hz,2H),7.40(d,J=8.4 Hz,2H),3.98(s,3H),2.54(s,6H),2.30(q,4H),1.25(s,6H),0.98(t,6H);ESI-MS:m/z437.47[M-H]-。
探针SOH的合成:将SOMe溶于50 mL无水甲醇中,加入5 mL 0.2 mol/L NaOH,80 ℃加热回流2 h,旋蒸去溶剂,加入少量DCM,2 mol/L HCl酸化,再加入少量蒸馏水,用二氯甲烷萃取,得化合物SOH(0.066 g,产率:39.87%)。1H NMR(CDCl3,400 MHz)δ:8.23(d,J=8.0 Hz,2H),7.45(d,J=8.0 Hz,2H),2.54(s,6H),2.29(q,4H),1.29(s,6H),0.98(t,6H);ESI-MS:m/z423.47[M-H]-。
1.4 探针SOH的光谱性能测定
1.4.1待测溶液的配制及实际样品的前处理
探针母液:将探针SOH溶解于乙腈中,配制成1.0 mmol/L标准溶液,于4 ℃冰箱中保存备用。测量时,将探针母液用乙腈溶液稀释至所需浓度。
金属离子标准溶液:用分析纯金属盐试剂分别配制Na+、K+、Ca2+、Ba2+、Mg2+、Pb2+、Cu2+、Cr3+、Cd2+、Ni2+、Co2+、Fe2+、Zn2+、Mn2+、Ag+和Hg2+储备溶液,再用二次蒸馏水稀释成10.0 mmol/L的标准溶液备用。测量时用乙腈稀释至所需浓度。
矿泉水样品处理[12]:通过0.22 μm微孔滤膜过滤,静置,待用。
大米样品处理[13]:称取大米,加入适量双蒸水,用高压均质机均质10 min,滤纸过滤匀浆以除去残余物,待测大米溶液保存在4 ℃备用。
鮟鱇鱼样品处理[14]:称取1 g鮟鱇鱼肉试样于消解罐中,加入8 mL浓H2SO4,120 ℃加热约1 h,冷却;盖好安全阀,将消解罐放入微波消解仪中,设置最佳条件(5 min由室温爬升到120 ℃,于120 ℃保持3 min,再由120 ℃升温到220 ℃,于220 ℃保持20 min)至消解完全,冷却后将溶液定量转移至小烧杯中,120 ℃加热去酸,将剩余物用PBS缓冲液(pH 7.4)稀释定容至10 mL,混匀,得待测鮟鱇鱼样品溶液。
1.4.2测定方法
在一组10 mL比色管中均加入1 mL探针SOH母液,再分别加入不同量的金属离子标准溶液,用乙腈定容,摇匀并放置4 min。室温下,取3 mL试液于1 cm石英比色皿中测量紫外-可见吸收光谱,做荧光滴定和离子选择性实验,激发和发射波长分别为520和536 nm,狭缝带宽均为5 nm。
2 结果与讨论
2.1 响应时间
向1 μmol/L探针SOH溶液中滴加2倍浓度的Hg2+,观察5 min内探针的荧光响应情况,结果如图2所示。由图2可知:未加入Hg2+时,探针SOH的荧光强度基本不受时间影响;加入Hg2+后,1.5 min内体系的荧光强度逐渐降低,1.5 min后荧光强度趋于恒定,可知探针SOH对Hg2+的响应时间为1.5 min。
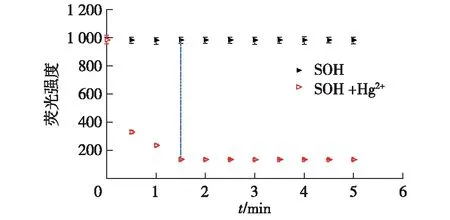
图2 探针SOH对Hg2+的荧光响应-时间曲线Fig.2 Fluorescence response of probe SOH to Hg2+ at different time
2.2 探针SOH对Hg2+的选择性
为了考察探针SOH对Hg2+的选择性识别性能,在多种常见金属离子与Hg2+共存时进行干扰试验,结果如图3(a)所示。由图3(a)可知:当在探针SOH的乙腈溶液中加入100倍浓度的碱金属离子(Na+、K+)、100倍浓度的碱土金属离子(Mg2+、Ca2+和Ba2+)和10倍浓度的过渡金属离子(Pb2+、Cu2+、Cr3+、Cd2+、Ni2+、Co2+、Fe2+、Zn2+、Mn2+和Ag+)后,荧光强度几乎无变化,如图3(b)黑色柱所示。但在上述各溶液中加入Hg2+后,荧光强度明显下降,如图3(b)红色柱所示。图3结果表明,常见的共存离子对识别Hg2+未产生显著干扰。因此,探针SOH可用于混合离子体系中高选择性识别Hg2+,具备在复杂基体条件下的应用潜力。
2.3 探针SOH的镜像实验结果
探针SOH乙腈溶液的紫外可见光吸收光谱图和荧光发射光谱图如图4所示。由图4可知:其吸收峰位于522 nm处,在491 nm处有峰肩,这是常见的含烷基取代基的BOPIPY衍生物所具有的典型特征。一旦探针SOH在520 nm受激发,其最大发射峰出现在536 nm处,探针SOH的荧光光谱图与吸收光谱图显示出镜像对称,与吸收光谱相比,斯托克斯位移14 nm。
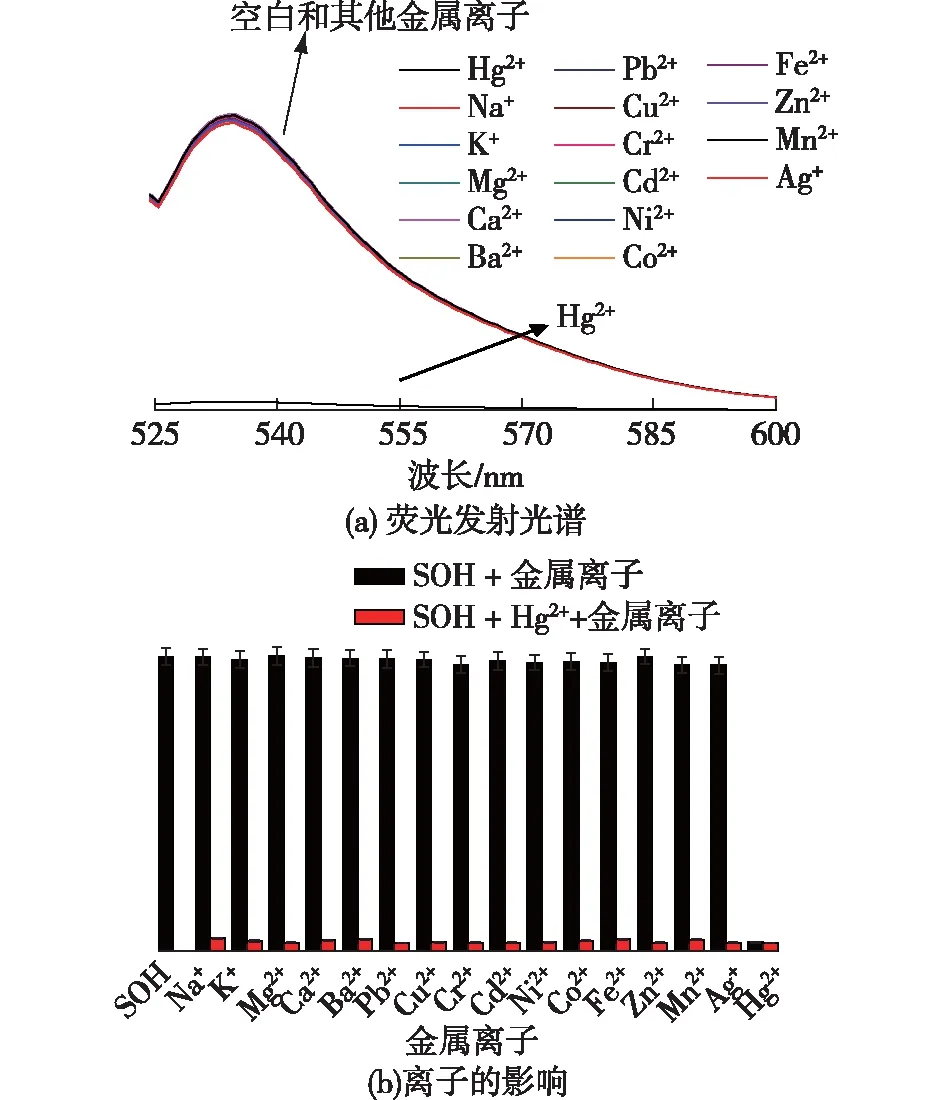
图3 纯乙腈体系中向探针SOH加入不同金属离子后的荧光发射光谱(a)和常见金属离子对探针SOH识别Hg2+的影响(b)Fig.3 Fluorescent emission spectra of probe SOH upon addition of different metal ionsin CH3CN(a)and effects of metal ions on recognition of probe SOH to Hg2+(b)

图4 乙腈中探针SOH的紫外可见光 吸收光谱和荧光发射光谱Fig.4 Absorption and emission spectra of probe SOH inCH3CN
2.4 紫外可见滴定和荧光滴定
在探针SOH的乙腈溶液中加入2倍浓度的Hg2+,光谱变化见图5。由图5可知:随着Hg2+浓度增加,522 nm处的紫外吸收峰不断下降,且略有红移。这个新产生的低能吸收带可能是由于Hg2+与苯甲酸的受体单元的选择性作用,导致了荧光团到芳环间的分子内电荷转移。向1 mL探针SOH(5 μmol/L)溶液中滴加10 μmol/L Hg2+时,溶液颜色从黄变红,表明能够实现裸眼识别Hg2+。
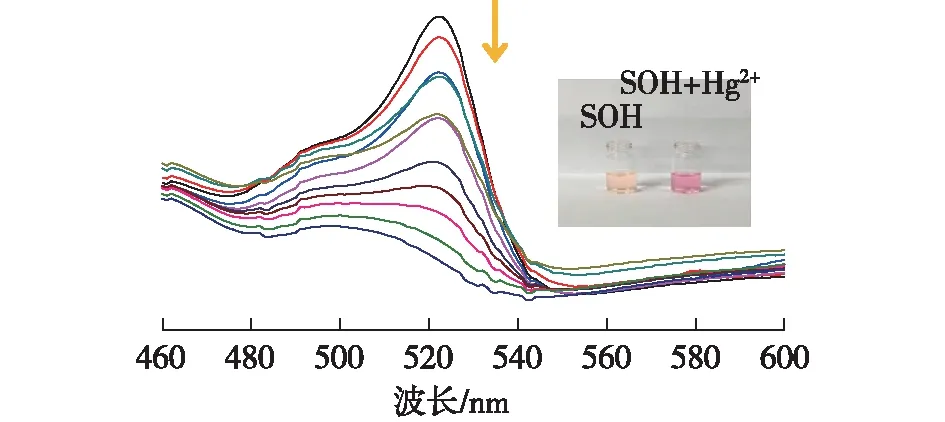
图5 乙腈中探针SOH加入不同浓度Hg2+的 紫外吸收光谱Fig.5 Absorption spectra of probe SOH upon addition of different amounts of Hg2+ in CH3CN
向1 mL探针SOH的乙腈溶液(2 μmol/L)中每次滴加10 μL Hg2+(1 μmol/L),荧光强度减弱,见图6。不同量Hg2+存在下,探针SOH在最大发射波长处的荧光强度标准曲线见图7,根据最低检出限LOD=3s/m[15],其中s为线性范围内,峰值处荧光强度的标准偏差,m为线性方程的斜率,计算得LOD为0.53 μmol/L。
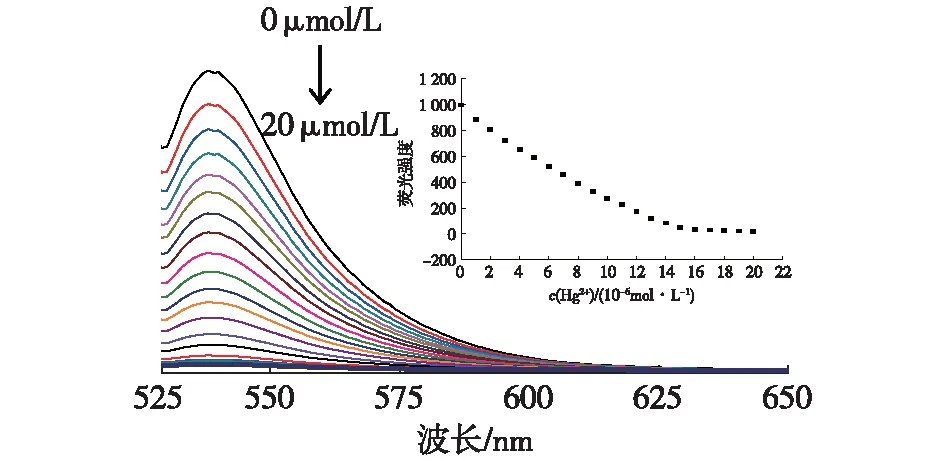
图6 乙腈中探针SOH加入不同浓度Hg2+的荧光发射光谱(激发波长520 nm,插图:随着Hg2+浓度增加,536 nm处荧光强度的变化)Fig.6 Fluorescence emission spectra of probe SOH upon addition of different amounts of Hg2+ in CH3CN(λex=520 nm,Inset:Fluorescence intensity at 536 nm as a function of Hg2+ concentration)
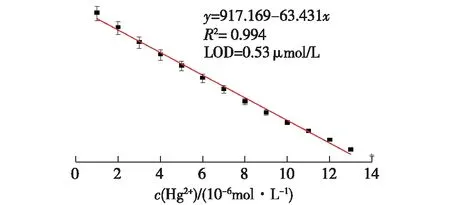
图7 探针SOH在不同浓度Hg2+下最大发射536 nm 处的荧光强度标准曲线Fig.7 Standard curve of fluorescence intensity at 536 nm of probe SOH and Hg2+ concentration
2.5 探针SOH与Hg2+的配位比
绘制探针SOH与Hg2+的Job-plot工作曲线[16]。固定探针SOH与Hg2+的恒定浓度为20 μmol/L,依次调节探针SOH与Hg2+的浓度比,分别测定探针SOH在522 nm处的吸光度,结果见图8。由图8可知:当探针SOH的摩尔分数为0.5时,吸光度最大,表明探针SOH与Hg2+的配位比为1∶ 1。
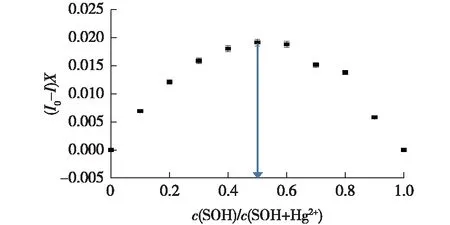
图8 乙腈中探针SOH对Hg2+的Job-plot曲线Fig.8 Job-plot of probe SOH for Hg2+ in CH3CN (c(SOH+Hg2+)=20 μmol/L)
2.6 检测原理
由Job-plot实验,结合BODIPY类衍生物的荧光特性和已有的文献报道[17-19],可推断探针SOH的识别基团未结合底物(Hg2+)时,PET过程受阻,当荧光团被激发后,发射出强荧光;当识别基团结合底物(Hg2+)后,识别基团结构由苯甲酸(—COOH)变为苯甲酸盐(—COO-),当受到特定波长激发后,处于外层轨道的电子从识别基团的HOMO轨道跃迁到荧光团的HOMO轨道,使得荧光团的HOMO轨道能级升高,同时荧光团的LUMO轨道上的电子跃迁到识别基团的HOMO轨道上,达到稳定状态,无法回到基态,发生了PET效应,从而导致荧光减弱或荧光淬灭,其检测机理见图9。
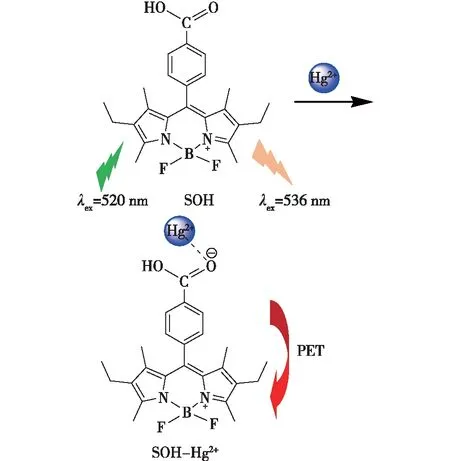
图9 探针SOH检测Hg2+的机理示意Fig.9 Schematic representation of probe SOH detecting Hg2+
2.7 实际样品检测
以空白样品基质配制一系列不同浓度的Hg2+标准溶液,利用探针SOH进行荧光测定,以Hg2+浓度为横坐标,荧光响应强度为纵坐标,分别得到矿泉水、大米和鮟鱇鱼3种基质的标准曲线及线性方程,见图10和表1。
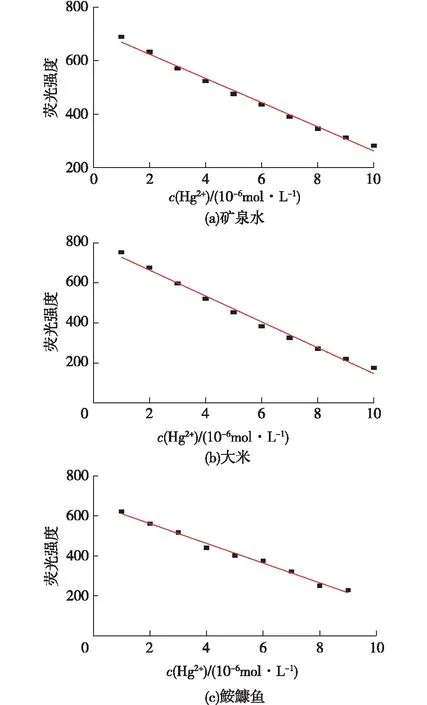
图10 基质标准曲线Fig.10 Standard curve of mineral water,rice and anglerfish
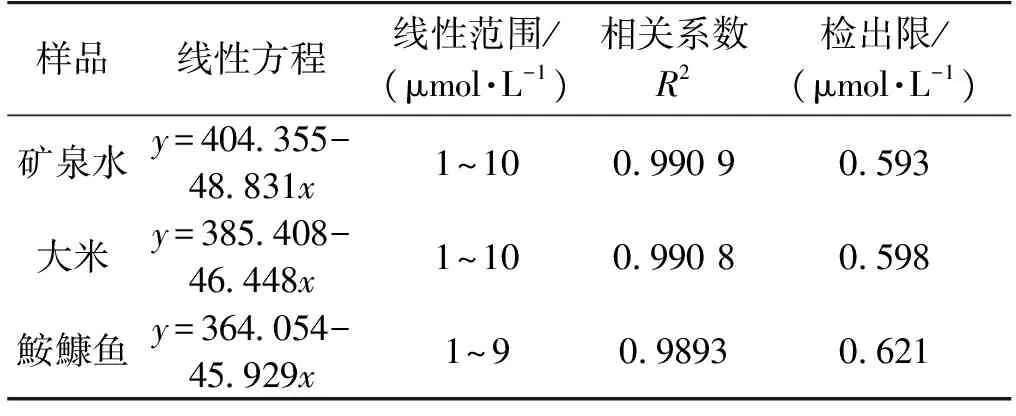
样品线性方程线性范围/(μmol·L-1)相关系数R2检出限/(μmol·L-1)矿泉水y=404355-48831x1~10099090593大米y=385408-46448x1~10099080598鮟鱇鱼y=364054-45929x1~9098930621
2.8 回收率试验
准确量取1.0 mL矿泉水、大米和鮟鱇鱼空白样品各1份,分别添加3个水平(1、2和5 μmol/L)浓度的Hg2+标准溶液,混匀,再用所建立的方法进行回收率试验。空白样品添加浓度及其回收率见表2。由表2可见,在矿泉水中Hg2+的回收率为97.48%~101.21%,相对偏差为2.10%~3.82%;在大米中Hg2+的回收率为94.36%~98.20%,相对偏差为1.80%~5.64%;在鮟鱇鱼中Hg2+的回收率为105.50%~107.80%,相对偏差为5.50%~7.80%。此结果满足痕量分析的要求,表明了该方法对复杂食品样品中Hg2+进行检测具有可行性和实用性。
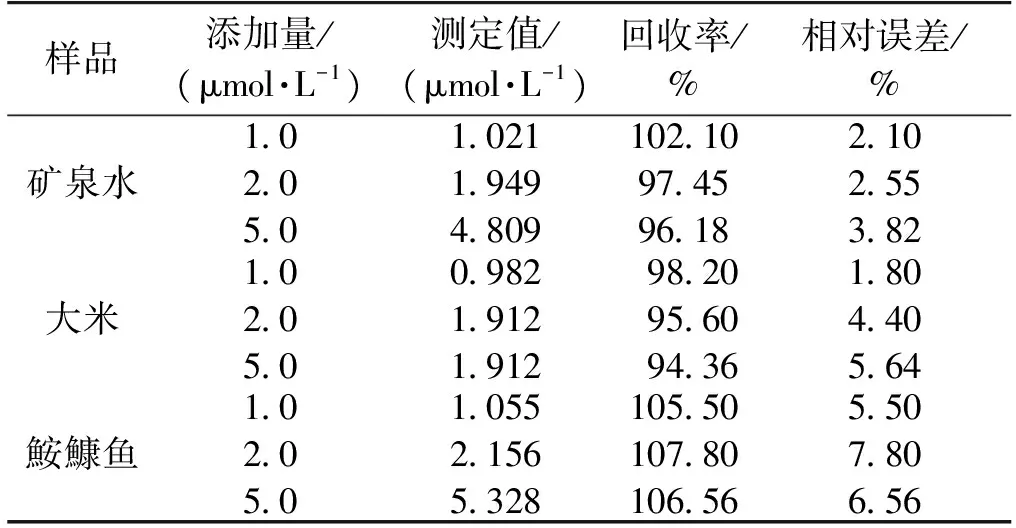
表2 实际样品中Hg2+的添加回收率实验
不同基质中Hg2+在相应的浓度范围内线性关系良好,相关系数R2>0.98,可满足定量分析的需要。
3 结论
笔者设计合成了一种BODIPY类荧光探针SOH,通过ESI-MS和1HNMR进行结构确证。实验表明,Hg2+诱导探针发生光致诱导电子转移(PET)效应,体系的荧光由强变弱,溶液颜色由黄色变为红色,在1~13 μmol/L范围内,Hg2+浓度和荧光强度的线性相关系数为0.994,检出限为0.53 μmol/L,从而建立了对Hg2+裸眼可视化和定量检测的方法。本方法成功用于矿泉水、大米和鮟鱇鱼的食品样品Hg2+检测,加标回收率为94.36%~107.80%,相对偏差为1.80%~7.80%,方法可靠,其中对矿泉水和大米中Hg2+最低检出限略高于标准,目前只适用于大批样品的快速筛查和半定量分析,而对鮟鱇鱼中Hg2+最低检出限低于标准,在食品检测方面具有较高的实际应用价值。
参考文献:
[1]CARVALHO C M L,CHEW E H,HASHEMY S I,et al.Inhibition of the human thioredoxin system[J].J Biol Chem,2008,283(18):11913-11923.
[2]JIANG J,LIU W,CHENG J,et al.A sensitive colorimetric and ratiometric fluorescent probe for mercury species in aqueous solution and living cells[J].Chem Commun,2012,48:8371-8373.
[3]BOURDINEAUD J P,ROSSIGNOL R,BRTHES D.Zebrafish:a model animal for analyzing the impact of environmental pollutants on muscle and brain mitochondrial bioenergetics[J].Int J Biochem Cell Biol,2013,45(1):16-22.
[4]LIANG P,KANG C,MO Y.One-step displacement dispersive liquid-liquid microextraction coupled with graphite furnace atomic absorption spectrometry for the selective determination of methylmercury in environmental samples[J].Talanta,2016,149:1-5.
[5]SIXTO A,FEDORUK-POGREBNIAK M,ROSENDE M,et al..A mesofluidic platform integrating restricted access-like sorptive microextraction as a front end to ICP-AES for the determination of trace level concentrations of lead and cadmium as contaminants in honey[J].J Anal At Spectrom,2016,31:473-481.
[6]DUAN H L,ZHANG N N,GONG ZB,et al.Photochemical vapor generation of lead for inductively coupled plasma mass spectrometric detection[J].Spectrochim Acta Part B:Atomic Spectroscopy,2016,120:63-68.
[7]LU M,XIAO R,ZHANG X,et al.Novel electrochemical sensing platform for quantitative monitoring of Hg(II)on DNA-assembled graphene oxide with target recycling[J].Biosen Bioelectron,2016,85:267-271.
[8]CHOU C Y,LIU S R,WU S P.A highly selective turn-on fluorescent sensor for Cu(II)based on an NSe2chelating moiety and its application in living cell imaging[J].Analyst,2013,138(11):3264-3270.
[9]HE X,ZHANG J,LIU X,et al.A novel BODIPY-based colorimetric and fluorometric dual-mode chemosensor for Hg2+,and Cu2+[J].Sensors Actuators B,2014,192:29-35.
[10]XIAO H,LI J,WU K,et al.A turn-on BODIPY-based fluorescent probe for Hg(II)and its biological applications[J].Sensors Actuators B,2015,213:343-350.
[11]ISAAD J,EL A A.A water soluble fluorescent BODIPY dye with azathia-crown ether functionality for mercury chemosensing in environmental media[J].Analyst,2013,138(13):3809-3819.
[12]LAN L,NIU Q,GUO Z,et al.Highly sensitive and fast responsive "turn-on" fluorescent sensor for selectively sensing Fe3+and Hg2+in aqueous media based on an oligothiophene derivative and its application in real water samples[J].Sensors Actuators B,2017,244:500-508.
[13]ZHANG H,ZHANG G,XU J,et al.Novel highly selective fluorescent sensor based on electrosynthesized poly(9-fluorenecarboxylic acid)for efficient and practical detection of iron(III)and its agricultural application[J].Sensors Actuators B,2016,230:123-129.
[14]ZHAO Q,CHEN S,ZHANG L,et al.Multiplex sensor for detection of different metal ions based on on-off of fluorescent gold nanoclusters[J].Anal Chim Acta,2014,852:236-243.
[15]SHORTREED M,KOPELMAN R,KUHN M,et al.Fluorescent fiber-optic calcium sensor for physiological measurements[J].Anal Chem,1996,68(8):1414-1418.
[16]YEH J T,CHEN W C,LIU S R,et al.A coumarin-based sensitive and selective fluorescent sensor for copper(II)ions[J].New J Chem,2014,38(9):4434-4439.
[17]MAHMOOD Z,ZHAO J.The unquenched triplet excited state of the fluorescent OFF/ON BODIPY-derived molecular probe based on photo-induced electron transfer[J].Photochem Photobiol Sci,2016,15(11):1358-1365.
[18]OOYAMA Y,HATO M,ENOKI T,et al.A BODIPY sensor for water based on photo-induced electron transfer method with fluorescence enhancement and attenuation systems[J].New J Chem,2016,40(9):7278-7281.
[19]KAUR N,KAUR P,BHATIA G,et al.Indole-BODIPY:a "turn-on" chemosensor for Hg2+with application in live cell imaging[J].RSC Adv,2016,6(86):82810-82816.
