长疗程西那卡塞治疗维持性血液透析患者难治性继发性甲状旁腺功能亢进症的临床观察
2018-03-22周凌辉张恒远裴娟程翱张燕林
周凌辉 ,张恒远 ,裴娟 ,程翱 ,张燕林 *
继发性甲状旁腺功能亢进症(secondary hyperparathyroidism,SHPT)是血液透析患者最常见的并发症之一,尤其是对伴有高钙血症和/或高磷血症,传统药物治疗无效的难治性SHPT〔血清全段甲状旁腺激素(iPTH)>800 pg/ml〕患者,建议采用甲状旁腺切除术治疗[1]。但随着患者年龄增长及血液透析时间延长,部分患者无法耐受或不愿意接受手术治疗。新型治疗SHPT药物拟钙剂西那卡塞于2015年在我国上市,为该部分患者提供了新的治疗策略,既往研究显示,西那卡塞已成功应用于控制血液透析患者SHPT,并能降低甲状旁腺切除术的风险[2],但其在我国人群中长期应用效果报道较少。
1 对象与方法
1.1 研究对象 选取2015年4月—2017年3月在厦门大学附属第一医院治疗的合并难治性SHPT的维持性血液透析患者11例为研究对象,其中男6例,女5例;年龄50~83岁,平均年龄(69.4±11.0)岁;透析龄4.7~18.4年,平均透析龄(8.0±3.7)年;甲状旁腺结节1个2例,2个7例,3个2例;原发病为慢性肾炎6例,糖尿病肾病3例,高血压肾损害2例。排除标准:血清钙离子浓度<2.1 mmol/L,肝脏受损(西那卡塞主要在肝脏代谢),以及对西那卡塞过敏。
1.2 治疗方法 西那卡塞〔协和发酵麒麟株式会社生产,协和发酵麒麟(中国)制药有限公司分装,剂型25.0 mg/片〕初始剂量为25.0 mg/d,晚餐后口服,每4周根据iPTH、血钙、血磷检查结果调整剂量,调整范围为加减12.5~25.0 mg/d,最大用药量不超过100.0 mg/d,治疗目标为iPTH在150~300 pg/ml。血钙<1.8 mmol/L,且出现低钙症状,如感觉异常、肌痛、手足抽搐时停用西那卡塞。
患者血钙(参考范围2.1~2.5 mmol/L)、血磷(参考范围1.13~1.78 mmol/L)降至参考范围后,决定是否联用骨化三醇(上海罗氏制药有限公司,剂型0.25 μg/片),初始用量为0.25 μg/次,3次/周,透析后当日睡前口服,并根据检查结果调整用量,调整范围为加减0.25 μg /次。未使用其他降低iPTH的药物,磷结合剂的使用不受限制。
患者血液透析3次/周,4 h/次,均使用钙离子浓度为0.75 mmol/L的碳酸氢盐透析液,透析液流量、透析泵控血流量等与西那卡塞使用前相同。
1.3 监测指标 治疗期间,前12周每隔4周检测iPTH、血钙、血磷水平,此后每隔12周检测;每隔12周检测碱性磷酸酶(ALP)、血清清蛋白(ALB)、血红蛋白(Hb)、尿素、血肌酐水平。iPTH的检测采用化学发光法(西门子iPTH测定试剂盒,IMMULITE 1000化学发光免疫分析仪),余指标采用HITACHI 7600-020全自动大型生化分析测定仪检测。每隔4周记录西那卡塞、骨化三醇剂量。
1.4 统计学方法 采用SPSS 19.0软件进行统计学分析,计量资料以(x±s)表示,治疗前后比较采用单变量的重复测量方差分析。以P<0.05为差异有统计学意义。
2 结果
2.1 病例一览 11例患者初始iPTH水平为(1 375±352)pg/ml,末期为(245±82) pg/ml,达标均值为(243±47)pg/ml,首次达标时间为12~84周;西那卡塞最大剂量(46.3±20.4) mg/d,末期剂量(20.0±13.4) mg/d,最大剂量治疗时间4~36周(见表1);10例患者联用骨化三醇。西那卡塞剂量在第8周达到最大,较初始剂量明显增加,在第60~84周时下降至初始剂量。骨化三醇剂量在第36~84周较初始剂量明显增加(见图1)。
2.2 监测指标 患者治疗后各周iPTH、血钙、血磷水平均低于初始水平,治疗后第60~84周ALP水平低于初始水平,差异均有统计学意义(P<0.05)。治疗前后ALB、Hb、尿素、血肌酐水平比较,差异无统计学意义(P>0.05,见表2)。
3 讨论
传统治疗SHPT的药物是各种活性维生素D,最常用的是骨化三醇。虽然其治疗可能会降低iPTH,但可升高血钙和血磷水平,加重患者软组织和心血管钙化。而拟钙剂类药物西那卡塞不仅降低iPTH水平,同时也能适度降低血钙和血磷水平。西那卡塞是一种Ⅱ型拟钙剂,其作为甲状旁腺细胞表面上的钙敏感受体(Calcium sensing receptor,CaSR)的变构激活剂,降低CaSR活化的阈值并增强信号传导,以增加其对细胞外钙离子的敏感性及减少iPTH分泌[3]。同时,西那卡塞是变构的激活剂而不是CaSR激动剂,不会使原CaSR的密度和亲和力改变,因此,原CaSR仍可不断感受血钙水平的增加,反应性减少iPTH的分泌。因此,西那卡塞具有持续性疗效,一项长达3年的研究显示,西那卡塞能长期降低iPTH水平,而不增加血钙、血磷水平及钙磷乘积[4]。
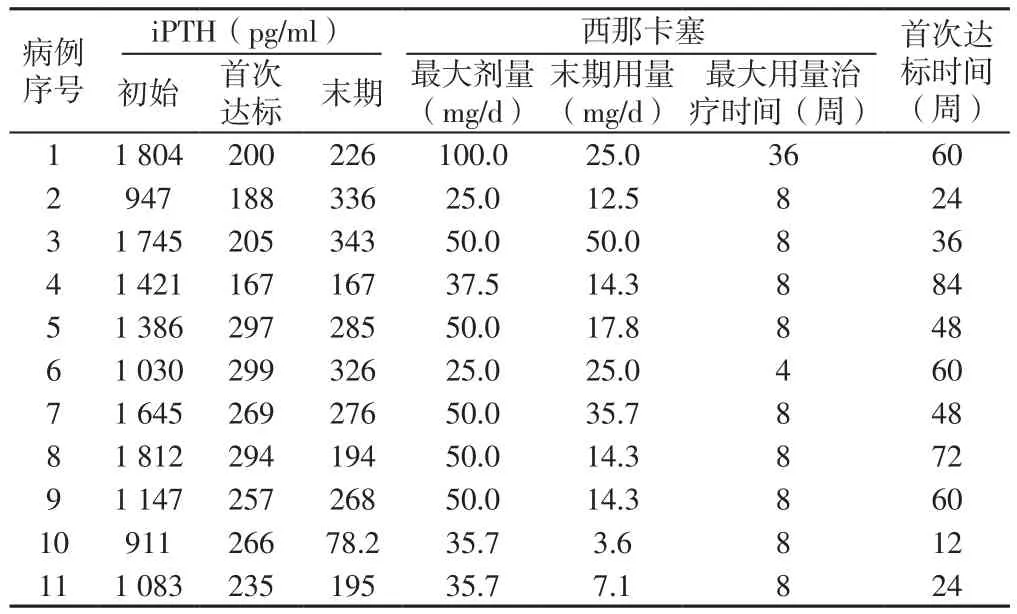
表1 11例患者治疗期间iPTH水平及西那卡塞剂量变化Table 1 Changes in iPTH level and cinacalcet dose in 11 maintenance hemodialysis patients during treatment
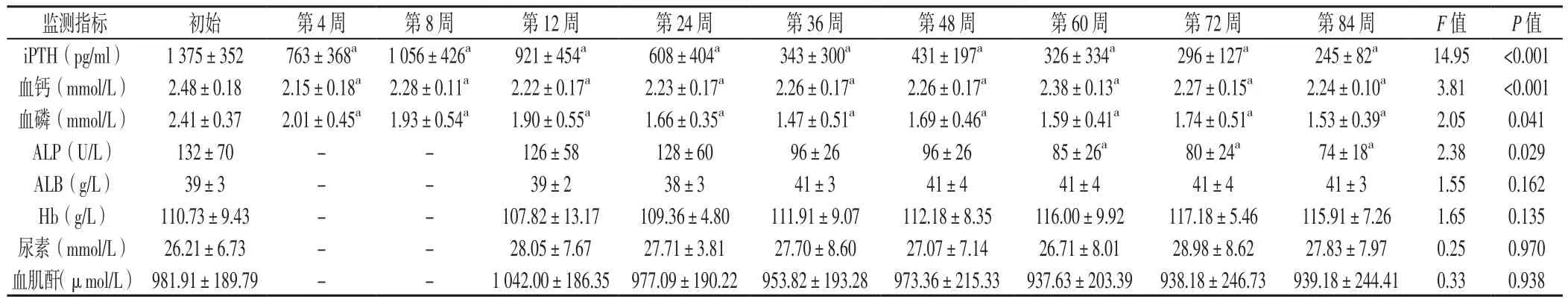
表2 患者治疗期间监测指标变化(x±s,n=11)Table 2 Changes in laboratory indicators during treatment
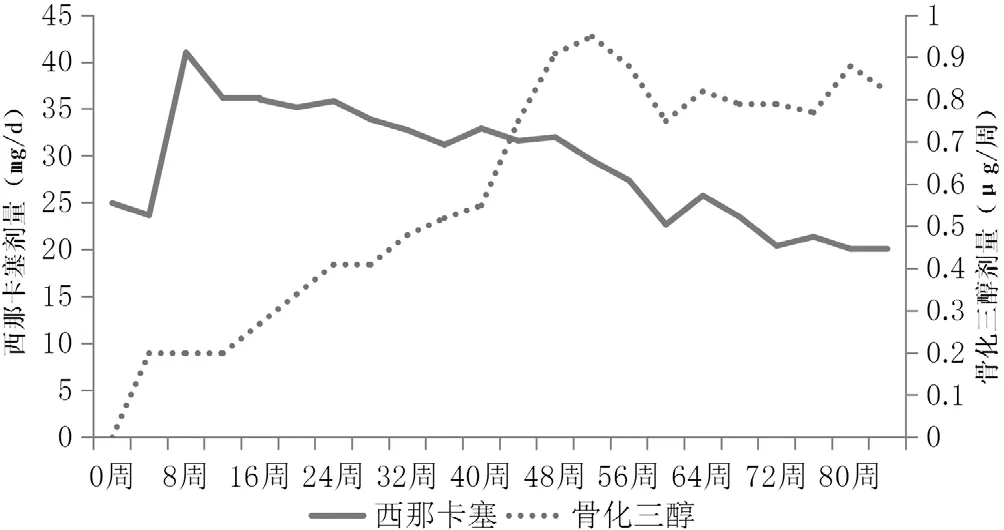
图1 治疗期间西那卡塞和骨化三醇剂量变化Figure 1 Changes in dose of cinacalcet and calcitriol during treatment
研究发现,基线iPTH水平越高,西那卡塞治疗后达目标值的比例越低,提示iPTH水平可能与疾病严重程度有关[4]。ALHARTHI等[5]发现,如果患者iPTH水平在300~500 pg/ml时应用西那卡塞治疗,80%的患者在6个月内达到治疗目标(iPTH为100~300 pg/ml),而iPTH水平>800 pg/ml的患者,常需要24个月后才能达到相同的目标,且部分患者仍无法达到治疗目标。KOMABA等[6]观察到甲状旁腺体积也影响西那卡塞的治疗效果,相对于体积≥500 mm3者,体积<500 mm3的SHPT患者达到预定目标iPTH<180 pg/ml的比例较高。本研究患者均为难治性SHPT患者,有明显的甲状旁腺增生,虽未进行甲状旁腺结节体积的测量,但治疗前iPTH平均水平高达1 375 pg/ml,故达到目标值的治疗时间较长,首次达标的平均时间为48周,且达标后iPTH水平仍有波动;同时发现,首次达标时间似乎与iPTH水平相关,iPTH水平较低者首次达标时间也较短。HIRAI等[7]进行的持续12个月的西那卡塞治疗效果观察显示,治疗前无结节性增生且腺体<500 mm3者治疗期间iPTH水平能持续下降,而治疗前伴结节性增生且腺体≥500 mm3者治疗期间iPTH水平波动明显,与治疗第3个月比较,第6个月时iPTH水平反而出现上升,并持续到第12个月。推测原因为,SHPT患者甲状旁腺细胞CaSR表达降低,尤其是结节性增生患者,西那卡塞可以在3~6个月的时间内上调CaSR表达,发挥降低iPTH的作用,6个月后西那卡塞的作用下降,结节性甲状旁腺增生患者出现该现象尚无法解释。本研究观察到类似情况,西那卡塞治疗第4周iPTH水平反而低于第8、12周,增加西那卡塞的用量并持续治疗直到第24周iPTH水平才进行性下降,该现象是否与西那卡塞加量能持续上调CaSR表达相关,又或为联用骨化三醇的协同作用所致,目前尚不明确。
SHPT导致的肾性骨营养不良包括3种类型,即高iPTH水平的高转运型骨病的囊状纤维骨炎,低iPTH水平相关的无动力性骨病,以及混合型骨病[8]。临床上最常见的是高iPTH导致的骨病,无动力性骨病及混合型骨病常为不规范使用活性维生素D所致。本研究显示,治疗第60周后,患者ALP水平出现下降,提示骨病有所改善。EVOLVE研究中发现,基线水平较高的骨碱性磷酸酶(bone alkaline phosphatase,BALP)提示较高的骨转运,与较高的临床骨折发生率相关,在64个月的随访中,西那卡塞组平均用药时间为21.2个月,使临床骨折率降低16%~29%,尤其是髋部骨折风险降低32%[9]。ALHARTHI等[5]及 SILVERSTEIN 等[10]研究显示,西那卡塞治疗后ALP水平出现明显下降,前者研究ALP水平下降的幅度超过了66%。西那卡塞可减少iPTH的释放,改善SHPT,从而减少临床骨折率。目前已经证明,西那卡塞不仅能改善慢性肾脏病(CKD)患者各种血清生化指标,也能降低甲状旁腺切除术概率、病理性骨折和与心血管并发症相关的住院率[11]。本研究随访期间无患者因骨折或需甲状旁腺切除而住院。
证据表明,慢性肾衰竭状态下,甲状旁腺增生是SHPT的重要组成部分,而拟钙剂可以阻碍甲状旁腺增生的发展。CaSR的激活不仅减少激素分泌,也能减少甲状旁腺细胞增殖[12]。即便对甲状旁腺腺体明显扩大的中重度SHPT,西那卡塞不仅能有效降低血清iPTH水平,并能减少甲状旁腺体积。目前认为可能的机制是,合成iPTH减少导致细胞体积缩小,以及促进细胞凋亡导致细胞数量减少[10]。本研究虽未对治疗前后腺体体积进行测量,但似乎可以解释,随着治疗时间延长,多数患者维持期西那卡塞使用剂量远低于最大剂量,甚至低于初始剂量,可能与西那卡塞长期治疗能诱导腺体萎缩并降低腺体功能相关。
至今,各种维生素D制剂仍是抑制CKD患者SHPT分泌iPTH的主要治疗药物,其是通过甲状旁腺细胞上的维生素D受体(Vitamin D receptor,VDR)的激活直接实现。然而,甲状旁腺增生的发展与VDR、CaSR的下调相关[13]。有临床研究表明,通过超声检查甲状旁腺体积,如体积评估>500 mm3,被认为是维生素D治疗低反应性指标[14]。超常增生的甲状旁腺对维生素D的治疗是无效的,反而因维生素D刺激肠吸收钙和磷,导致高钙、高磷血症,对血液透析患者极为不利。最近研究表明,联合西那卡塞和低剂量维生素D治疗可能是治疗SHPT的有效策略,其疗效互补,在控制iPTH的同时,也能维持血清钙、磷平衡[15]。基础实验表明,维生素D增加靶细胞CaSR的表达,而拟钙剂也能增加VDR的表达,这种相互作用是二者联合使用治疗SHPT的临床基础[16]。MEOLA等[17]发现,经过12~18个月的联合治疗后,超声提示增生的甲状旁腺结构逐渐变化,体积≥500 mm3的腺体有倾向显示出囊性变性的消声现象,而体积<500 mm3腺体变化更大,超声显示从低回声(表明具有丰富的细胞性增生)转变为高回声(表明增加了静止的脂肪细胞数量),同时腺体血流变得稀少,部分腺体体积变小,接近正常甲状旁腺,与甲状腺实质无法区分,此时提示低剂量的西那卡塞治疗足以取得良好效果。本研究10例联合使用骨化三醇的患者显示,随治疗时间的延长,西那卡塞剂量逐渐减少,而骨化三醇的剂量逐渐增加,尽管也可能与当前患者需自费使用西那卡塞的现况相关,但是联合治疗的优势是显而易见的。
综上所述,西那卡塞是治疗SHPT的有效药物,不仅能降低iPTH水平,也能维持血清钙、磷平衡,早期治疗效果更佳;对于难治性SHPT,采用有效剂量的西那卡塞、足够长的疗程才能达到治疗靶目标,与活性维生素D的联合治疗是目前最佳方案。
作者贡献:周凌辉进行文章的构思与设计、研究的实施与可行性分析,统计学处理,结果的分析与解释,撰写论文;张恒远、裴娟、程翱进行数据收集、整理;周凌辉、裴娟进行论文的修订;张燕林负责文章的质量控制及审校,对文章整体负责,监督管理。
本文无利益冲突。
[1]张建荣,张凌.慢性肾脏病继发性甲旁亢[M].北京:人民军医出版社,2010.ZHANG J R,ZHANG L.Secondary hyperparathyroidism and chronic renal disease[M].Beijing:People's Military Medical Press,2010.
[2]PALMER S C,NISTOR I,CRAIG J C,et al.Cinacalcet in patients with chronic kidney disease:a cumulative meta-analysis of randomized controlled trials[J].PLoS Med,2013,10(4):e1001436.DOI:10.1371/journal.pmed.1001436.
[3]DE FRANCISCO A L.New strategies for the treatment of hyperparathyroidism incorporating calcimimetics[J].Expert Opin Pharmacother,2008,9(5):795-811.DOI:10.1517/14656566.9.5.795.
[4]MOE S M,CUNNINGHAM J,BOMMER J,et al.Long-term treatment of secondary hyperparathyroidism with the calcimimetic cinacalcet HCl[J].Nephrol Dial Transplant,2005,20(10):2186-2193.DOI:10.1093/ndt/qfh966.
[5]ALHARTHI A A,KAMAL N M,ABUKHATWAH M W,et al.Cinacalcet in pediatric and adolescent chronic kidney disease:a single-center experience[J].Medicine (Baltimore),2015,94(2):e401.DOI:10.1097/MD.0000000000000401.
[6]KOMABA H,NAKANISHI S,FUJIMORI A,et al.Cinacalcet effectively reduces parathyroid hormone secretion and gland volume regardless of pretreatment gland size in patients with secondary hyperparathyroidism[J].Clin J Am Soc Nephrol,2010,5(12):2305-2314.DOI:10.2215/CJN.02110310.
[7]HIRAI T,NAKASHIMA A,TAKASUGI N,et al.Association of nodular hyperplasia with resistance to cinacalcet therapy for secondary hyperparathyroidism in hemodialysis patients[J].Ther Apher Dial,2010,14(6):577-582.DOI:10.1111/j.1744-9987.2010.00843.x.
[8]PLATT C,INWARD C,MCGRAW M,et al.Middle-term use of cinacalcet in paediatric dialysis patients[J].Pediatr Nephrol,2010,25(1):143-148.DOI:10.1007/s00467-009-1294-7.
[9]MOE S M,ABDALLA S,CHERTOW G M,et al.Effects of cinacalcet on fracture events in patients receiving hemodialysis:the EVOLVE trial[J].J Am Soc Nephrol,2015,26( 6):1466-1475.DOI:10.1681/ASN.2014040414.
[10]SILVERSTEIN D M,KHER K K,MOUDGIL A,et al.Cinacalcet is efficacious in pediatric dialysis patients[J].Pediatr Nephrol,2008,23(10):1817-1822.DOI:10.1007/s00467-007-0742-5.
[11]MOE S M,CHERTOW G M,COBURN J W,et al.Achieving NKF-K/DOQI bone metabolism and disease treatment goals with cinacalcet HCl[J].Kidney Int,2005,67(2):760-771.DOI:10.1517/14656566.9.5.795.
[12]WADA M,NAQANO N.Control of parathyroid cell growth by calcimimetics[J].Nephrol Dial Transplant,2003,18(Suppl 3):iii13-17.
[13]NAVEH-MANY T,RAHAMIMOV R,LIVNI N,et al.Parathyroid cell proliferation in normal and chronic renal failure rats.The effects of calcium,phosphate,and vitamin D[J].J Clin Invest,1995,96(4):1786-1793.DOI:10.1172/JCI118224.
[14]TOMINAGA Y,INAGUMA D,MATSUOKA S,et al.Is the volume of the parathyroid gland a predictor of maxacalcitol response in advanced secondary hyperparathyroidism?[J].Ther Apher Dial,2006,10(2):198-204.DOI:10.1111/j.1744-9987.2006.00364.x.
[15]BLOCK G A,ZEIG S,SUGIHARA J,et al.Combined therapy with cinacalcet and low doses of vitamin D sterols in patients with moderate to severe secondary hyperparathyroidism[J].Nephrol Dial Transplant,2008,23(7):2311-2318.
[16]PABLO A,TORRES U,COZZOLINO M,et al.Vitamin D in chronic kidney disease[M].Switzerland:Springer International Publishing,2016:537-562.
[17]MEOLA M,PETRUCCI I,BARSOTTI G.Long-term treatment with cinacalcet and conventional therapy reduces parathyroid hyperplasia in severe secondary hyperparathyroidism[J].Nephrol Dial Transplant,2009,24(3):982-989.DOI:10.1093/ndt/gfn654.
