艾司西酞普兰联合阿立哌唑治疗老年抑郁症疗效观察
2018-03-13靳庆敏葛茂宏孙红立
靳庆敏,葛茂宏,孙红立
(1.潍坊医学院,山东 潍坊 261000;2.潍坊市精神卫生中心,山东 潍坊 261000)
老年抑郁症作为发病率仅次于老年痴呆的一种精神障碍,其发病特点除了抑郁心境或言语外,往往还伴有不同程度的躯体化障碍、睡眠障碍、焦虑情绪等[1]。心理干预、药物治疗和其他生物干涉是目前临床抑郁症常用的治疗措施。然而对于老年抑郁症来说,药物治疗仍是主要治疗手段。传统治疗一般首选抗抑郁剂结合苯二氮卓类药物,但临床疗效一般。据文献报道[2],小剂量非典型抗精神病药物辅助抗抑郁剂对改善抑郁症状疗效满意。本文通过随机对照研究,探讨艾司西酞普兰联合阿立哌唑治疗老年抑郁症的疗效及安全性,现将结果报道如下。
1 资料与方法
1.1 临床资料 选取潍坊市精神卫生中心2016年5月~2017年5月收治住院的老年抑郁症患者88例。其中男32例,女56例,年龄60~78岁,平均(68.25±5.17)岁;病程3~97个月,平均(35.24±5.61)个月。两组患者临床资料比较差异无统计学意义。入组标准:①年龄≥60岁;②符合国际疾病分类第十版(ICD-10)抑郁发作诊断标准;③汉密尔顿抑郁量表17版(HAMD-17)评分>17分。排除标准:①脑器质性疾病或患有严重心、肝、肾等躯体疾病者,物质依赖及药物过敏者;②由其他精神疾病引起的抑郁症;③双相情感障碍,目前为抑郁发作。脱落标准:①依从性差,不遵从医嘱者;②病史及相关资料收集不全;③患者中途自行退出研究。纳入研究的患者及其家属均自愿接受该试验,并签署临床试验知情同意书。
1.2 方法
1.2.1 给药方法 将符合标准的88例患者分为两组,观察组(45例)给予艾司西酞普兰(商品名百适可,山东京卫制药,国药准字H20103327)联合阿立哌唑(商品名奥派,上海中西制药有限公司,国药准字H20041507)治疗。按照艾司西酞普兰使用说明,起始剂量5 mg/d,1周末,依据患者药物耐受情况及症状缓解程度逐渐加量至10~20 mg/d,阿立哌唑10 mg/d;对照组(43例)则给予艾司西酞普兰加安慰剂,给药方式及剂量同观察组。入组研究患者必须经过1周清洗期。为避免影响疗效,治疗期间禁止合并其他抗抑郁药及抗精神病药物,禁止对患者进行系统的物理治疗(如经颅磁刺激、无抽搐电休克);如有严重睡眠障碍者,可临时给予睡眠贴对症处理。
1.2.2 临床疗效及不良反应评定 观察总时间为6周。两组患者的临床疗效及不良反应采用HAMD-17、TESS进行评估,并由2名精神科主治医师单独完成。并于治疗前及治疗第2、6周末抽血化验血尿常规、血糖血脂、肝肾功能、心肌酶谱及心电图。疗效评估以 HAMD-17减分率为准,HAMD-17减分率≥75%或总分≤7分评定为痊愈,50%~74%评定为显效,25%~49%评定为好转,<25%评定为无效[3]。
1.3 统计学方法 本研究采用SPSS 19.0统计学软件进行数据统计,计量资料用表示,组内对照作配对样本的t检验,组间对照作独立样本的t检验。计数资料用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者各项指标比较 6周末,观察组有效39例,无效6例,总有效率86.67%;对照组有效28例,无效15例,总有效率65.12%,差异有统计学意义(P<0.05),见表1。治疗前,两组HAMD-17比较比较差异无统计学意义,第1、2、4、6周末两组评分与治疗前对比差异有统计学意义(P<0.05),而第2、4、6周末评估结果显示,观察组HAMD-17评分较对照组显著性降低(P<0.01),见表2。治疗6周末,HAMD-17中(除体重因子外)焦虑/躯体化因子、认知障碍因子、睡眠障碍因子及阻滞因子比较,对照组显著低于观察组(P<0.01),观察组与对照组组内比较差异有统计学意义(P<0.05),见表3。
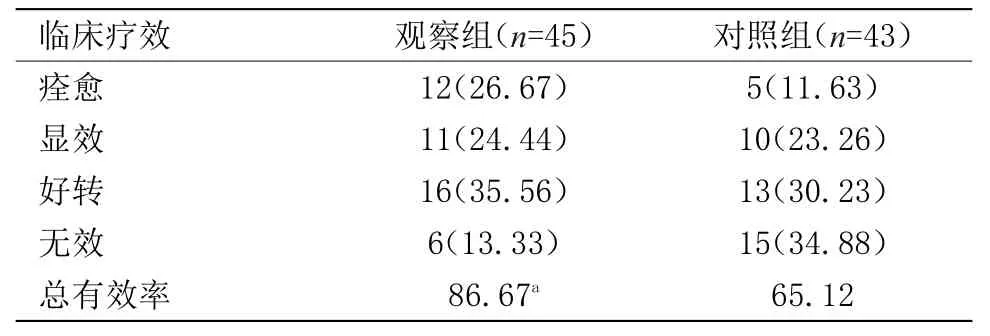
表1 临床疗效比较[n(%)]Table1 Compares the clinical efficacy[n(%)]
表2 治疗前后HAMD评分比较(Table2 Compares the HAMD score before and after treatmen
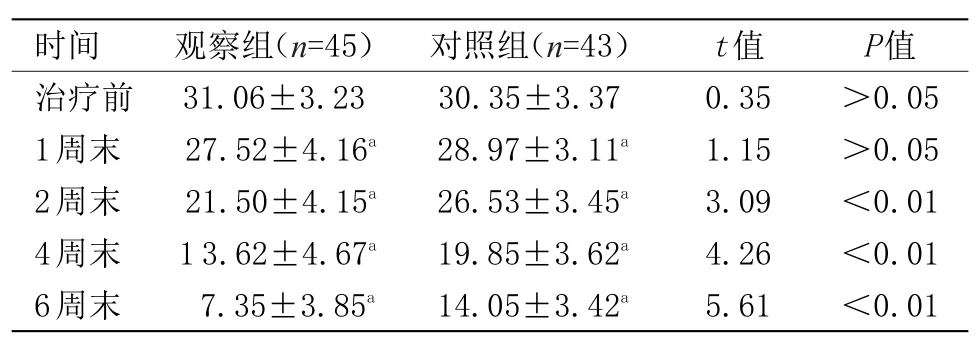
表2 治疗前后HAMD评分比较(Table2 Compares the HAMD score before and after treatmen
注:与治疗前比较,aP<0.05
?
表3 HAMD-17各因子评分比较(Table3 Compares HAMD-17 score of each factor
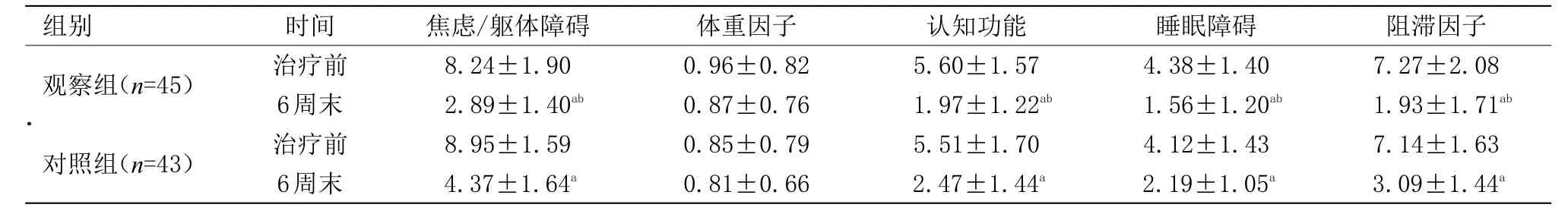
表3 HAMD-17各因子评分比较(Table3 Compares HAMD-17 score of each factor
注:与对照组相比,aP<0.05;与治疗前相比,bP<0.01
?
2.2 不良反应结果比较 在治疗过程中两组患者均有不良反应出现,但程度均较轻,患者基本能忍受,随治疗疗程延长,不良反应渐减轻或消失,未给予特殊处理。在整个治疗过程中,观察组共出现不良反应13例,发生率占28.89%;对照组12例不良反应,发生率27.90%。所有患者治疗依从性好,无1例脱落病例。治疗前后两组患者血尿常规、血糖血脂、肝肾功能、心肌酶谱及心电图基本处于正常范围内,个别患者指标比较差异无统计学意义,见表4。
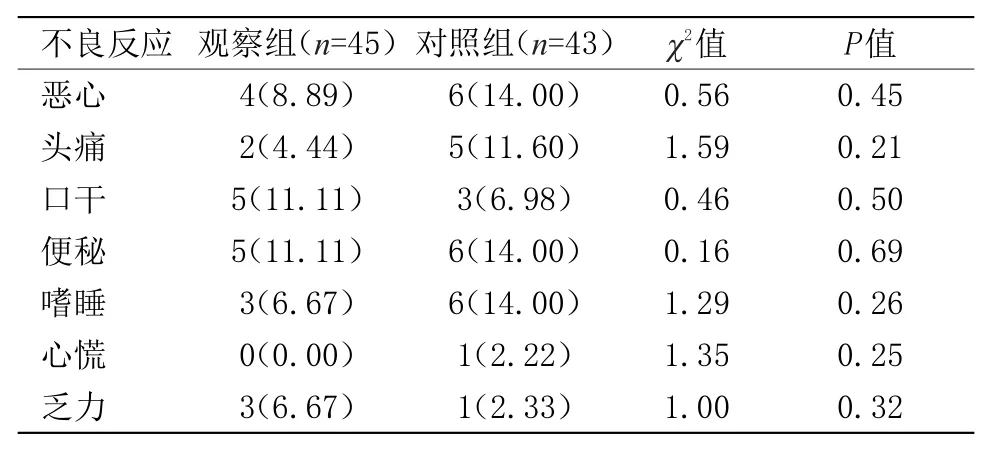
表4 不良反应结果比较[n(%)]Table4 Compares the adverse reaction results[n(%)]
3 讨论
抑郁状态在一定程度上不仅影响患者心理健康,还对其肢体功能、神经功能以及生活能力造成不同程度的损害,致使老年人的生活质量下降。因此,十分有必要采取积极有效的治疗措施。除了抗抑郁药,近年来大量的研究结果显示[4],部分二代抗精神病药物(SGA)与抗抑郁剂联合使用取得满意的效果,临床医师也越来越重视这种药物联用的增效作用。艾司西酞普兰为选择性5-羟色胺再回收抑制剂(SSRI),其作用机制主要是选择性抑制中枢神经元5-HT运载体对5-HT的再回收,进而使突触间隙5-HT水平升高[5]。因具有良好的改善抑郁症状、缓解焦虑情绪作用,临床应用广泛。阿立哌唑是既具有多巴胺D2、D3受体和5-HT1A受体激动作用,同时又具有5-HT2A受体拮抗作用的新型二代抗精神病性药物[6],除对血糖、血脂代谢影响小外,它几乎不引起体质量的增加,也较少引起血清泌乳素水平的变化。这与阿立哌唑特有的药理特性密不可分。阿立哌唑对中脑边缘系统的多巴胺D2受体具有较高的占有率,可改善患者的认知功能、调节精神运动[7]。Kim E等的研究显示[8],阿立哌唑对顶叶皮质区5-HT1A受体的激动作用可以调节大脑的血流量,从而改善患者焦虑症状。阿立哌唑治疗也会增加脑源性神经营养因子、糖原合成酶激酶3b和Bcl-2的磷酸化,促进神经再生[9-10]。另外其5-HT2A受体拮抗作用可以很好的中和抗抑郁剂对体重的影响,还能稳定血清泌乳素水平。严重的抑郁症患者具有自杀倾向,Reimherret[11]研究表明阿立哌唑部分多巴胺受体激动作用可迅速改善抑郁症的核心症状,如情绪、疲乏、无力的感觉,自我价值,和自杀的想法。
阿立哌唑的5-HT2受体的拮抗作用不仅可以增强SSRI的5-羟色胺能效应,而且还可以中和部分SSRI所致的药物副作用。临床许多研究也证明了两药联用效果优于单用艾司西酞普兰[12-13]。本研究结果显示,艾司西酞普兰合并阿立哌唑治疗老年抑郁症有效39例,总有效率86.67%,明显高于艾司西酞普兰加安慰剂组的65.12%,差异有统计学意义(P<0.05)。治疗前,两组HAMD-17评分比较差异无统计学意义,第2、4、6周末观察组评分均较对照组低(P<0.05)。6周末,HAMD-17各因子(除体质量因子外)比较显示,差异有统计学意义(P<0.05),提示在缓解老年抑郁症患者的焦虑情绪、躯体不适、认知障碍、阻滞及睡眠障碍方面,两药联用效果更佳,且对体重没有影响。两组不良反应程度均较轻,患者可耐受,未予以处理,说明两药联用安全性可靠。综上所述,艾司西酞普兰与阿立哌唑联用对于老年抑郁症的治疗效果是显著的,不仅症状改善快,而且不良反应并未叠加,值得临床推广应用。但由于样本量小、研究时间短,使本研究存在一定的局限性,两药联用的远期效果有待进一步证实。
[1] 周勤.米氮平合并喹硫平治疗老年抑郁症的疗效[J].江苏医药,2015,41(9):1057-1058.
[2] 王金龙,赵和丹.小剂量喹硫平治疗躯体化障碍的增效作用[J].医药导报,2011,30(6):754-756.
[3] 吴蒙.米氮平与帕罗西汀治疗抑郁症的临床对照研究[J].中国医药指南,2015,13(12):164-165.
[4] 张威,郗小明.非典型抗精神病药在抑郁症治疗中的增效作用[J].中国药物滥用防治杂志,2009,15(1):55-57.
[5] 李晓青,安娜,李峰,等.艾司西酞普兰治疗伴焦虑症状的抑郁症疗效和安全性的研究进展[J].精神医学杂志,2013,26(2):158-160.
[6] 钟华,刘少华.小剂量阿立哌唑与艾司西酞普兰治疗55例伴躯体症状抑郁症的疗效[J].上海医药,2015,36(23):25-26,38.
[7] 邹晓华,金艳,吴筱芬,等.艾司西酞普兰联合小剂量阿立哌唑治疗难治性抑郁症的对照研究[J].现代实用医学,2015,25(11):1463-1464,1495.
[8] Kim E,Howes OD,Turkheimer FE,et al.The relationship between antipsychotic D(2) occupancy and change in frontal metabolism and working memory:A dual [(11)C]raclopride and [(18)F] FDG imaging study with aripiprazole[J]. Psychopharmacology,2013,227(2):221-229.
[9] Park SW,Lee JG,Ha EK,et al.Differential effects of aripiprazole and haloperidol on BDNF-mediated signal changes in SH-SY5Y cells[J].Eur Neuropsychopharmacol,2009,19(5):356-362.
[10] Yoshimura R, Hori H, Ikenouchi-Sugita A, et al. Aripiprazolealtered plasma levels of brain- derivedneurotrophic factor and catecholamine metabolitesin first- episode untreated Japanese schizophreniapatients[J]. Hum Psychopharmacol, 2012,27(1):33-38.
[11]Reimherr FW,Martin ML,Eudicone JM,et al.A pooled MADRS/IDS cross-correlation analysis:Clinician and patient self-reportassessment of improvement in core depressive symptoms with adjunctive aripiprazole[J].Clin Psychopharmacol,2010,30(3):300-305.
[12]王丽娜,潘飞,王东平.文拉法辛联合氨磺必利治疗难治性抑郁症的临床效果观察[J].中国当代医药,2014,21(12):86-88.
[13]吴红东.文拉法辛联合氨磺必利治疗难治性抑郁症的效果观察[J].长江大学学报(医学版),2014,11(30):33-34.
