注射器中盐酸氢吗啡酮和盐酸吗啡在不同温度下的稳定性*
2018-03-13史学莲刘小立宋姗姗宛春甫杨娟丽杨书芳
史学莲 刘小立△ 陈 丽 梁 平 宋姗姗 宛春甫 杨娟丽 杨书芳
(河北医科大学第四医院1疼痛科;2药剂科,石家庄 050011)
大约75%的癌症病人伴有疼痛,其中30%~50%的病人伴有中到重度疼痛,严重影响了病人的生活质量。世界卫生组织制定的三阶梯镇痛方法能够缓解大部分癌痛,但是由于进一步增加剂量导致的严重副作用,使得10%~30%的癌性疼痛仍然不能得到理想的控制[13]。对于晚期癌症病人,抗肿瘤治疗不再有效,而且他们的生存期短,这一部分病人在疼痛诊疗中出现副作用时应尽早进行阿片类药物的轮换,进行充分的镇痛,尽可能提高他们的生活质量。
临床上如果口服、透皮贴剂等途径效果不佳时或者病人入院既存在难治性疼痛时,通常会选择皮下自控镇痛 (patient-controlled analgesia, PCA) 或静脉PCA进行滴定或者以控制晚期癌症病人的疼痛。此外,一部分晚期癌痛病人存在消化道出血或者肿瘤等导致的不能口服镇痛药物,此时需要更换给药途径,甚至更换镇痛药物例如氢吗啡酮。多项研究证明,对于难治性疼痛,阿片类药物的轮换或者改变给药途径如皮下或静脉给药通常是有效的[2-5],而皮下给药途经具有更多的优势,比如不需要维持静脉液路,可以5~7天更换一次皮下注射位点,并且没有必要密切观察穿刺部位,同时感染也很少见[6],因此,连续皮下输注可能更适合晚期肿瘤病人或者临终关怀的病人。
连续皮下输注需要的容器是注射器或自控镇痛泵泵盒。皮下输注装置 (port) +鞘内置管 (intrathecal catheters connected to a subcutaneous injection port ,ICSP) + 专用镇痛泵泵盒持续输注吗啡可显著降低晚期重度癌痛病人的疼痛[7,8]。但临床上,出于经济的考虑,有时会采用50 ml塑料注射器为储药容器配合微量泵进行皮下镇痛治疗,辛险峰等人[9]应用50 ml注射器作为储药容器,并与硬膜外置管连接以治疗晚期癌痛(均为居家使用),并且观察了病人居家使用镇痛泵的情况,认为非专业镇痛泵(50 ml注射器+硬膜外置管),减轻了病人经济负担,同时也取得了满意疗效。张川等人[10]认为微泵联合用药的镇痛治疗效果优于口服吗啡缓释片,不良反应较少,能较好的控制晚期癌症病人的疼痛和其他痛苦症状。但尚未见关于盐酸吗啡注射液或盐酸氢吗啡酮注射液与0.9%氯化钠注射液混合溶液储存在注射器中药物稳定性情况以及不同温度对药物浓度影响的报道。因此,本文对50 ml塑料注射器中,暴露于25℃、37℃条件下的药物稳定性进行了测定及分析,以期更好地为临床应用提供参考。
方 法
1.材料
盐酸氢吗啡酮原料药(宜昌人福药业有限责任公司,批号:QM141201),盐酸氢吗啡酮注射液(宜昌人福药业有限责任公司,规格:2 mg:2 ml,批号:1150601),盐酸吗啡对照品(纯度 > 99.0%,批号:20150505,青海制药厂有限公司),盐酸吗啡注射液(沈阳第一制药厂,批号:151112-2),0.9%氯化钠注射液(中国大冢制药有限公司,规格:500 ml:4.5 g,批号:5L84G4),Waters高效液相色谱仪:515型泵,Waters 2487型紫外检测器(美国Waters公司), E-201-C型PH复合电极(上海仪电科学仪器股份有限公司),TC-100型恒温箱(天津市金洲科学仪器有限公司),AB104-S 型电子天平(瑞士梅特勒-托利多)。甲醇、乙腈为色谱纯(赛默飞世尔科技有限公司),醋酸、庚烷磺酸钠为分析纯,蒸馏水自制。50 ml一次性使用塑料注射器(PVC为主要原料)。
2.色谱条件
色谱柱:Diamonsil C18柱(200 mm×4.6 mm,5 µm);流动相:5 mmol·L-1的庚烷磺酸钠水溶液:甲醇:醋酸= 59:49:1(V:V:V);流速:0.8 ml/min;柱温:30℃;检测波长:281 nm;进样量:20 µl。
3.试验方法
分别于塑料注射器中加入0.9%氯化钠注射液38 ml、盐酸氢吗啡酮注射液2 mg (2 ml),配成氢吗啡酮终浓度为0.05 mg/ml;加入0.9%氯化钠注射液39 ml、盐酸吗啡注射液10 mg (1 ml),配成吗啡终浓度为0.25 mg/ml。所得混合溶液再分别储存于恒温箱中,保持25℃、37℃两种恒温条件,并分别于第 0、1、3、5、7、9、11、13、15 天取样。
4.观察指标
每次取样平行操作3次取平均值,以高效液相色谱法 (High Performance Liquid Chromatography,HPLC)测定盐酸氢吗啡酮、盐酸吗啡的浓度,同时观察盐酸吗啡注射液、盐酸氢吗啡酮注射液的外观变化。
5.统计学分析
应用SPSS 21.0软件进行统计学分析。计量资料采用均数±标准差(±SD)表示,P< 0.05为差异有统计学意义。
结 果
储存于注射器中的盐酸氢吗啡酮混合溶液、盐酸吗啡混合溶液在2种恒定温度(25℃、37℃)下,随时间的变化其外观透明澄清无明显变化。两种药物在不同温度下的浓度情况(见表1),因同一温度下,2种药物的初始浓度不同,因此,采用不同天数保留初始浓度百分数的方式进行比较,以便更直观地观察不同药物浓度的变化情况。
高效液相色谱法检测结果显示,储存于注射器中的盐酸氢吗啡酮混合溶液、盐酸吗啡混合溶液分别放置在25℃、37℃恒温条件下时,盐酸氢吗啡酮、盐酸吗啡的浓度在前5天均是稳定的,均能保持初始浓度的98%以上(见图1)。25℃条件下,在第7天时吗啡浓度明显下降(保留初始浓度的91.91%),此后吗啡浓度进行性下降,至第15天时浓度下降至初始浓度的83.76%。而盐酸氢吗啡酮浓度则相对稳定,直到第11天浓度未见大的波动或改变(第11天占初始浓度的94.84%),第13天时浓度下降,占初始浓度的90.10%,第15天时浓度仍占初始浓度的90%以上。
37℃条件下,在第7天时吗啡浓度明显下降(保留初始浓度的89.35%),此后吗啡浓度下降,至第15天时浓度下降至初始浓度的86.54%。盐酸氢吗啡酮浓度相对稳定,直到第13天时浓度占初始浓度的96.09%,第15天时浓度明显下降,占初始浓度的91.12%。
表1 注射器中不同温度、不同药物的浓度(μg/ml,±SD)Table1 The concentration of morphine and hydromorphone in the syringes under the condition of 25 ℃ and 37 ℃ (μg/ml,±SD)
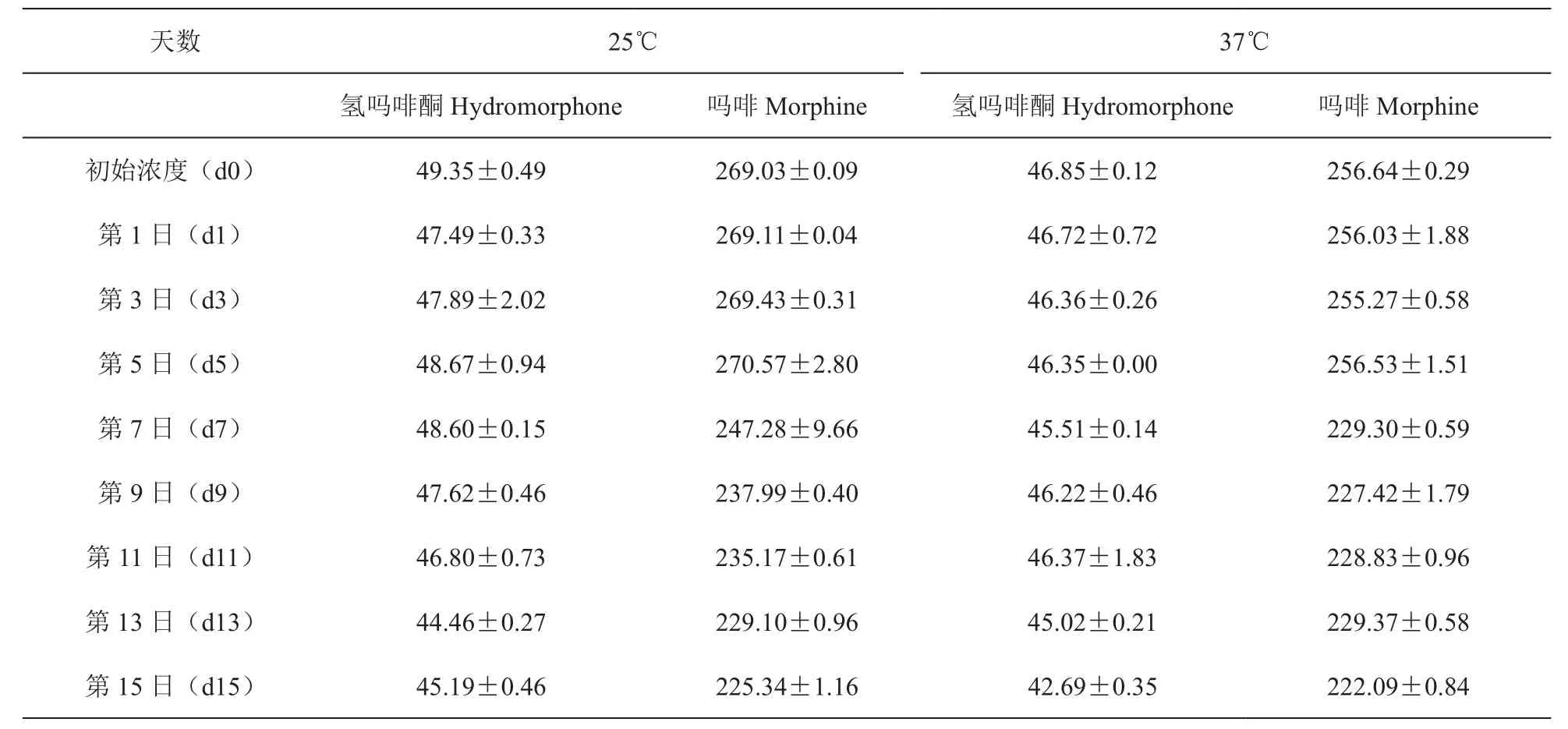
表1 注射器中不同温度、不同药物的浓度(μg/ml,±SD)Table1 The concentration of morphine and hydromorphone in the syringes under the condition of 25 ℃ and 37 ℃ (μg/ml,±SD)
3 7℃氢吗啡酮 H y d r o m o r p h o n e 吗啡 M o r p h i n e 氢吗啡酮 H y d r o m o r p h o n e 吗啡 M o r p h i n e初始浓度(d 0) 4 9.3 5±0.4 9 2 6 9.0 3±0.0 9 4 6.8 5±0.1 2 2 5 6.6 4±0.2 9第 1 日(d 1) 4 7.4 9±0.3 3 2 6 9.1 1±0.0 4 4 6.7 2±0.7 2 2 5 6.0 3±1.8 8第 3 日(d 3) 4 7.8 9±2.0 2 2 6 9.4 3±0.3 1 4 6.3 6±0.2 6 2 5 5.2 7±0.5 8第 5 日(d 5) 4 8.6 7±0.9 4 2 7 0.5 7±2.8 0 4 6.3 5±0.0 0 2 5 6.5 3±1.5 1第 7 日(d 7) 4 8.6 0±0.1 5 2 4 7.2 8±9.6 6 4 5.5 1±0.1 4 2 2 9.3 0±0.5 9第 9 日(d 9) 4 7.6 2±0.4 6 2 3 7.9 9±0.4 0 4 6.2 2±0.4 6 2 2 7.4 2±1.7 9第 1 1 日(d 1 1) 4 6.8 0±0.7 3 2 3 5.1 7±0.6 1 4 6.3 7±1.8 3 2 2 8.8 3±0.9 6第 1 3 日(d 1 3) 4 4.4 6±0.2 7 2 2 9.1 0±0.9 6 4 5.0 2±0.2 1 2 2 9.3 7±0.5 8第 1 5 日(d 1 5) 4 5.1 9±0.4 6 2 2 5.3 4±1.1 6 4 2.6 9±0.3 5 2 2 2.0 9±0.8 4天数 2 5℃
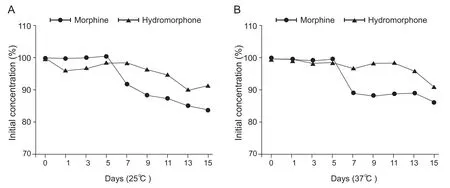
图1 盐酸氢吗啡酮注射液、盐酸吗啡注射液在25℃(A)、37℃(B)条件下,不同天数占初始浓度的百分数Fig.1 The percentage of morphine or hydromorphone concentration in the initial concentration under 25℃ (A) and 37℃ (B) at different days
讨 论
疼痛是肿瘤病人常见的并发症,可影响处在肿瘤任何阶段的病人。正确的药物选择、合理的给药途径、个体化的给药剂量等是癌痛药物治疗的重要原则。强效阿片类药物如吗啡、氢吗啡酮、羟考酮、芬太尼等为世界卫生组织推荐的第三阶梯的治疗癌痛的基本药物[11~13]。吗啡是姑息治疗的首选阿片类药物,主要作用于μ受体,少部分作用于δ受体,但对于出现恶心、吞咽问题或肠梗阻,以及口服大剂量吗啡和疾病晚期的病人不再适用[14,15]。在这些情况下,可以更换药物如盐酸氢吗啡酮,其镇痛作用是吗啡的5~10倍[11,16]。氢吗啡酮是一种半合成的阿片类镇痛药,主要作用于μ受体,并在较小程度上作用于δ受体,起效快,主要代谢产物无活性,适合用于急慢性疼痛治疗,临床应用安全有效[11]。
微创给药是目前临床上兴起的给药途径,包括持续输注、自控镇痛给药,其优势在于血药浓度稳定,镇痛效果持续,不良反应较少。当癌症病人伴有严重的难治性癌性疼痛经其他阿片类药物治疗仍不能控制疼痛时,连续注射氢吗啡酮通常可以得到长效的、足够的镇痛效果[1],如胃肠外便携式泵系统的使用。由于经济原因,专业镇痛泵泵盒在临床上的应用有时会受到限制。本研究模拟临床上微量泵系统联用注射器方法的环境,将装有盐酸氢吗啡酮混合溶液、盐酸吗啡混合溶液的注射器分别储存于25℃、37℃两种恒定温度下,研究结果显示盐酸氢吗啡酮、盐酸吗啡在前5天均是稳定,药物浓度稳定保证了输注剂量和速度准确,剂量调控也更加精确。盐酸氢吗啡酮在2种不同温度下,于第7、9、11天时浓度依然无明显下降,直到第15天时浓度仍能保持初始浓度的90%以上。
有临床研究表明,采用氢吗啡酮微创给药治疗癌痛的镇痛、镇静效果好,不良反应发生率低,安全性好[17]。此外,李化民等人[18]通过对60例难治性神经病理性疼痛病人进行研究后认为氢吗啡酮治疗难治性神经病理性疼痛的疗效较好,不良反应少,可在临床进行推广。因此,对于吗啡耐受或出现明显副作用的癌性疼痛病人推荐更换氢吗啡酮。本研究表明,25℃条件下,与吗啡相比,盐酸氢吗啡酮浓度在第7天时浓度无明显下降(保留初始浓度的98.49%);37℃条件下,盐酸氢吗啡酮浓度亦比吗啡稳定。临床荟萃分析表明[19],盐酸氢吗啡酮注射液对于癌性疼痛病人的镇痛效果优于其他阿片类镇痛药,氢吗啡酮在镇痛方面比吗啡具有优势。梁平等人[20]对近几年氢吗啡酮在不同镇痛泵中的临床应用以及稳定性 (外观、pH值和浓度的变化情况)等进行归纳总结,发现盐酸氢吗啡酮不论是单药或混合其他药物配制都具有较强的稳定性。本研究结果与上述研究结论相一致。因此,当预计病人生存期长且病人需要大剂量阿片类药物时,可以考虑应用盐酸氢吗啡酮,即使应用注射器作为容器、不同温度下也可应用10天以上。当然,本研究只是对两种恒温条件下药物浓度的变化进行了分析,临床上,药物浓度随时间的变化可能受到PH值、外界温度变化等因素的影响。因此,需结合临床研究以进一步证实。
综上所述,储存于注射器中的盐酸氢吗啡酮混合溶液、盐酸吗啡混合溶液在2种温度下放置时,盐酸氢吗啡酮、盐酸吗啡在前5天均是稳定的。储存于注射器中的盐酸氢吗啡酮浓度在2种不同温度下放置15天时仍能保持初始浓度的90%以上。以注射器作为容器时,25℃、37℃条件下盐酸氢吗啡酮的药物浓度稳定性较好,可达10天以上,而盐酸吗啡的药物浓度1周后明显下降。因此,临床应用吗啡以注射器为容器持续镇痛时,应用时间不超过1周。
[1]Oldenmenger WH.Efficacy of opioid rotation to continuous parenteral hydromorphone in advanced cancer patients failing on other opioids.Supportive Care in Cancer, 2012, 20(8): 1639~ 1647.
[2]Fine PG, Portenoy RK.Establishing "Best Practices"for Opioid Rotation: Conclusions of an Expert Panel.J Pain Symptom Manag, 2009, 38(3):418~ 425.
[3]Enting RH, Oldenmenger WH, van der Rijt CC,et al.A prospective study evaluating the response of patients with unrelieved cancer pain to parenteral opioids.Cancer, 2002, 94(11):3049~ 3056.
[4]Enting RH, Oldenmenger WH, Van Gool AR,et al.The effects of analgesic prescription and patient adherence on pain in a Dutch outpatient cancer population.J Pain Symptom Manage, 2007, 34(5):523~ 531.
[5]Kumar MG, Lin S.Hydromorphone in the management of cancer-related pain: an update on routes of administration and dosage forms.J Pharm Pharm Sci,2007,10(4):504~ 518.
[6]Negro S.Morphine, haloperidol and hyoscine N -butyl bromide combined in s.c.infusion solutions: Compatibility and stability: Evaluation in terminal oncology patients.Int J Pharm, 2006, 307(2):278~ 284.
[7]宛春甫, 王学君, 唐月.鞘内自控镇痛治疗阿片类药物不能耐受 晚 期 癌 痛 患 者 一 例 . 中 华 医 学 杂志, 2016, 96(10): 825~ 826.
[8]毛鹏, 李春蕊, 朱谦, 等.经皮下输注装置鞘内输注吗啡治疗晚期重度癌痛.中国疼痛医学杂志, 2016,22(11): 833~ 837.
[9]辛险峰, 杨秀娟, 李晓健,等.晚期癌症病人硬膜外自控镇痛(PCEA)的临床观察.中国疼痛医学杂志,2002, 8(2):92~ 92.
[10]张川,陈慧平,李金祥,等.微泵联合用药治疗癌痛及其他痛苦症状的临床研究.现代预防医学, 2010,37(8):1585~ 1587, 1589.
[11]Murray A, Hagen NA, Hydromorphone.J Pain Symptom Manag, 2005, 29(5):57~ 66.
[12]Bao YJ, Hou W, Kong XY,et al.Hydromorphone for cancer pain.Cochrane Db Syst Reviews, 2016,10(10):CD011108.
[13]Aldington D, Cole P, Knaggs R,et al.Hydromorphone for neuropathic pain in adults.Cochrane Db Syst Rev,2015:CD011604.
[14]燕琳, 张传汉.氢吗啡酮的药理作用及临床研究进展.中国疼痛医学杂志.2015, 21(9): 701~ 703.
[15]Viano A, Auvinen A.And members of the symptom prevalence group Prevalence of symptoms among patients with advanced cancer: an international study.J Pain Symptom Manage, 1996, 12:3~ 10.
[16]Barcia E.Stability and compatibility of binary mixtures of morphine hydrochloride with hyoscine-n-butyl bromide.Support Care Cancer, 2005, 13(4): 239~245.
[17]李波, 何仲琴.氢吗啡酮微创给药对癌痛病人应用的安全性及有效性.实用癌症杂志, 2016, 31(10):1731~ 1733.
[18]李化民, 曹观海,韩雪初.氢吗啡酮治疗的临床应用及不良反应分析.中外医疗, 2015,6: 54~ 55.
[19]Felden L.Comparative clinical effects of hydromorphone and morphine: a meta-analysis.Brit J Anaesth,2011, 107(3): 319~ 328.
[20]梁平, 史学莲, 候娟,等.氢吗啡酮微创给药泵临床应用及稳定性研究进展.国际药学研究杂志, 2017,44(3):240~ 244.
