肝移植术后移植物抗宿主病六例临床分析
2018-03-10王跃彭伟张洪涛李琳陶开山窦科峰杨诏旭
王跃 彭伟 张洪涛 李琳 陶开山 窦科峰 杨诏旭
移植物抗宿主病(graft versus host disease,GVHD)是肝移植术后一种十分罕见的并发症,分为体液免疫和细胞免疫两种类型[1]。体液免疫型通常与ABO血型不合有关,引起轻度、自身限制性溶血性贫血。而细胞免疫型是非常严重的疾病过程,发病率约为0.1%~2%,病死率高,在75%以上[2-4]。我们在这里探讨的主要是后者。
肝移植术后急性GVHD通常发生在术后的2~6周,常常导致多系统疾病,预后极差,临床表现主要是皮疹、腹泻、发热、全血细胞减少等,其中皮疹、发热是最常见的首发症状[2, 5]。大多数病人最终会死于多器官功能衰竭、败血症或者胃肠道出血[6]。该病早期诊断困难,尚无统一的诊断标准和治疗方案。本文对本中心6例肝移植术后GVHD进行回顾性分析,并对目前的治疗策略进行了探讨。
资料与方法
一、研究对象
回顾性分析1997年3月至2017年12月在空军军医大学附属西京医院肝胆外科器官移植中心420例行肝移植术病人的临床资料,对其中据临床表现和病理检查诊断为GVHD的受者临床资料和随访资料进行总结、分析。内容包括病人的一般资料、移植术前肝功能Child-Pugh分级、终末期肝病模型(model for end-stage liver disease,MELD)评分、手术方式以及GVHD的诊断、治疗经过、治疗后的并发症及疗效等,由于没有常规对肝移植受者和供者进行组织相容性白细胞抗原(histocompatibility leukocyte antigen,HLA)分型,因此我们不能获取供者和受者HLA类型的数据。
二、一般资料
共有6例病人(1.43%)最终被诊断为急性GVHD。6例病人均为男性。原发病分别为肝细胞癌(hepatocellularcarcinoma,HCC)合并乙型肝炎后肝硬化失代偿期4例,乙型肝炎后肝硬化失代偿期1例,酒精性肝硬化失代偿期1例。5例乙型肝炎表面抗原(HBsAg)阳性。5例病人肝移植术前有手术史,2例曾行经导管动脉化学栓塞(transcatheter arterial chemoembolization, TACE)治疗,2例曾行肝癌切除术,1例曾行经颈静脉肝内门腔静脉分流术(transjugular intrahepatic portosystemic shunt,TIPS)。术前Child-Pugh评级:A级2例,B级2例,C级2例。手术方式:背驮式肝移植术2例,原位经典肝移植术4例。ABO血型均匹配。4例受、供者年龄差在20岁以上。(表1)
病人肝移植术中于开放门静脉血流前静脉滴注巴利昔单抗20 mg,术中给予5 mg/kg甲泼尼龙琥珀酸钠(methyprednisolone,MP)静脉滴注,术后免疫抑制方案采用他克莫司+吗替麦考酚酯+MP三联免疫抑制方案治疗,前3 d每天予以MP 80 mg静脉滴注,此后逐渐减量,口服维持。拔除气管插管后口服吗替麦考酚酯0.5 g、2次/d,他克莫司1 mg、2次/d,动态监测肝功能,调整他克莫司血药浓度为10 μg/L左右。
三、GVHD的诊断和临床表现
肝移植术后GVHD尚无统一明确的诊断标准。目前对于GVHD的诊断主要参考以下三个方面:①靶器官受累出现的临床症状和体征,如发热、皮疹、消化道症状及骨髓抑制;②皮肤或骨髓病理学检查结果;③HLA配型检测到供者来源T细胞的嵌合现象。由于本中心缺少供受者HLA配型资料,我们主要依靠典型的临床表现,如发热、皮疹、腹泻、白细胞减少等,和皮肤组织病理活检证据对GVHD进行诊断。
本组6例GVHD病人在移植术后13~105 d发病(表2),最早出现的症状体征为发热(3例)或局部皮疹伴发热同时出现(3例)。随后数日内,病人出现皮疹或皮疹加重,恶心、呕吐、腹泻、便血等胃肠道症状也相继出现,随着病情的进展,往往还会伴随着严重的骨髓抑制。当发热和皮疹首次出现在这些病例时,由于缺乏特异性的表现,大多数最初被误诊为感染或药疹。典型的皮肤改变首先为颈部、躯干及四肢的红色斑丘疹,随后局部斑丘疹融合成片状,伴全身皮肤潮红,严重者可有表皮剥脱、口腔黏膜或全身皮肤溃烂(图1A~D)。对所有出现皮疹的病例取部分皮肤组织进行活检,可见角化不良、表皮或真皮层淋巴细胞浸润、炎性损害、基底层细胞空泡样变等改变(图2A~B)。典型胃肠道症状轻者表现为恶心、呕吐、水样腹泻,严重者可出现便血甚至呕血,在本组病例中,有5例出现典型的胃肠道症状,表现为稀水样便或大量便血。例1在出现全身皮疹后,连续6 d无大便,出现类似肠梗阻表现,第7天方才出现大量便血,考虑消化道出血;例3发病期间大便基本正常。骨髓抑制主要以白细胞减少为主,到后期可伴全血细胞减少,除例4在治疗期间白细胞基本正常外,其余均出现白细胞减少,严重者如例1和例2出现全血细胞极度减少。手术创伤、白细胞的降低以及术后免疫抑制剂和大剂量皮质激素的使用,导致病人感染的风险增大,因此我们会常规行病原学检查。最终发现例1的感染病原菌为嗜麦芽窄食单胞菌和大肠埃希菌,例2的感染病原菌为阴沟肠杆菌和嗜麦芽窄食单胞菌,例6的感染病原菌肺炎克雷伯亚种,其余未培养出致病菌,6例GVHD病人均没有发现真菌感染的证据。另外,例3在治疗过程中出现不明原因视物模糊,例6出现不明原因癫痫,考虑可能和GVHD相关,目前尚未见其他文献报道。(表2)
四、GVHD的治疗策略
1.免疫抑制治疗方案的调整 糖皮质激素具有抗炎特性以及破坏淋巴细胞和免疫抑制作用,可作为肝移植术后GVHD的一线用药。由于例1是本中心第一例肝移植术后GVHD病人,缺乏诊治经验,早期病人出现高热和皮疹时,考虑是肺部感染或药疹引起的,没有引起足够重视,当皮肤病理证实为GVHD时,方给予大剂量(MP 80 mg,1次/d)治疗,并暂停使用他克莫司和吗替麦考酚酯,此时已合并严重肺部感染。例2在皮肤病理确诊为GVHD后,即予以MP 500 mg、1次/d冲击治疗3 d,具体方案如下:500 mg×3 d,300 mg×1 d,160 mg×3 d,80 mg×3 d,40 mg×3 d,然后逐渐减量至口服维持。同时停止使用他克莫司和吗替麦考酚酯,并给予巴利昔单抗20 mg静脉滴注。例3、例4和例6在出现发热和皮疹之后即开始使用MP 300 mg、1次/d冲击治疗,而后逐渐减量,但是没停他克莫司和吗替麦考酚酯,而是将剂量减半。例5在出现发热和皮疹后即开始使用MP 300 mg、1次/d冲击治疗,同时暂停使用他克莫司和吗替麦考酚酯。
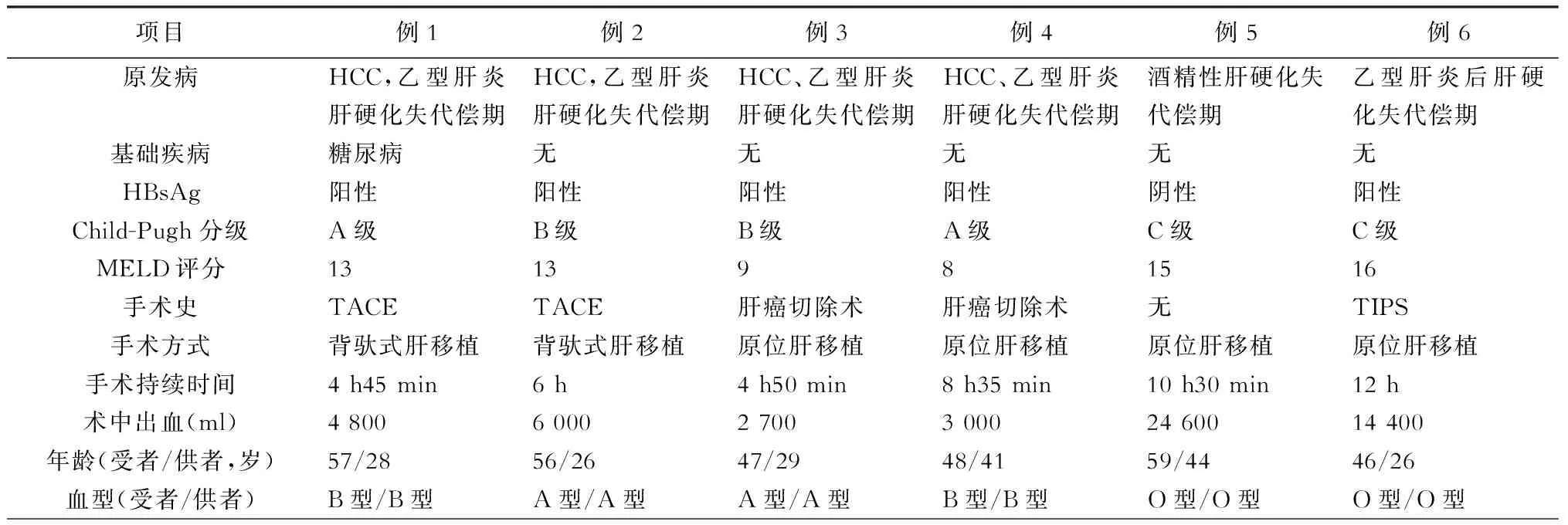
表1 移植物抗宿主病一般资料
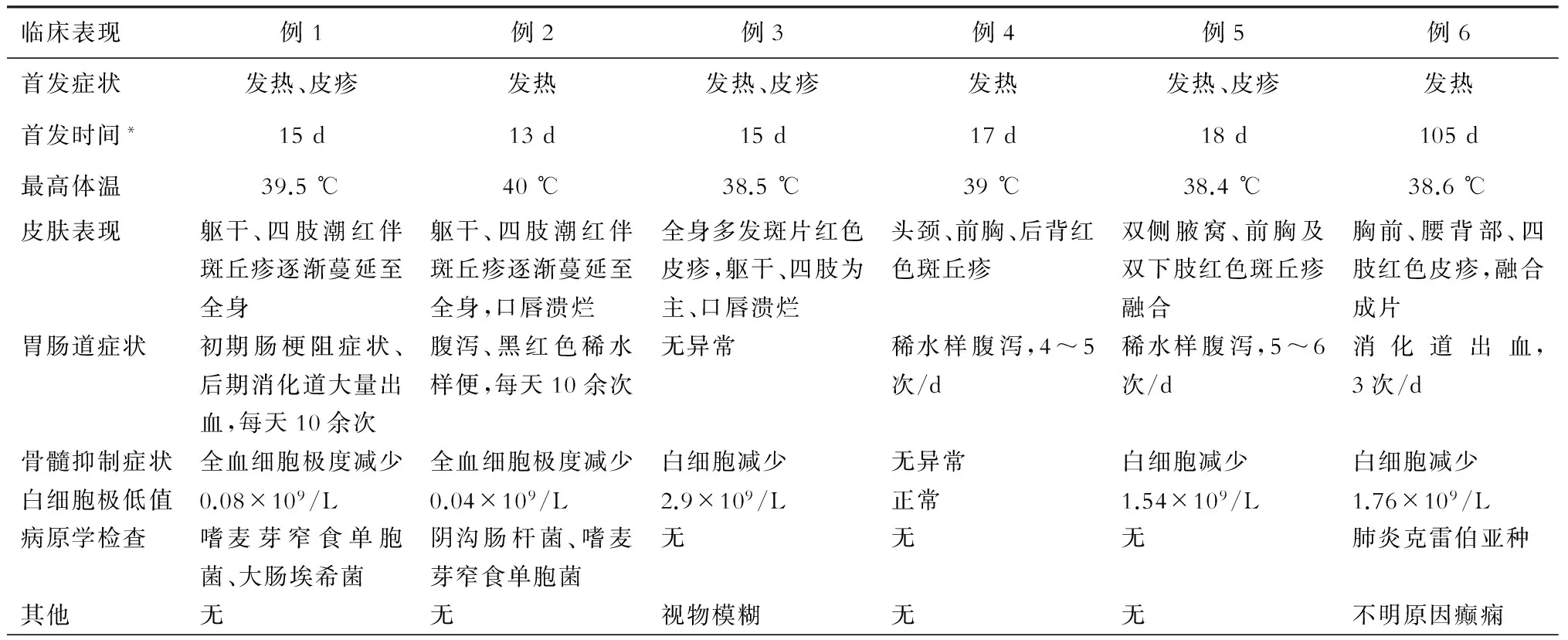
表2 移植物抗宿主病的临床表现
注:*发生肝移植术后GVHD相关症状距离手术时间的天数
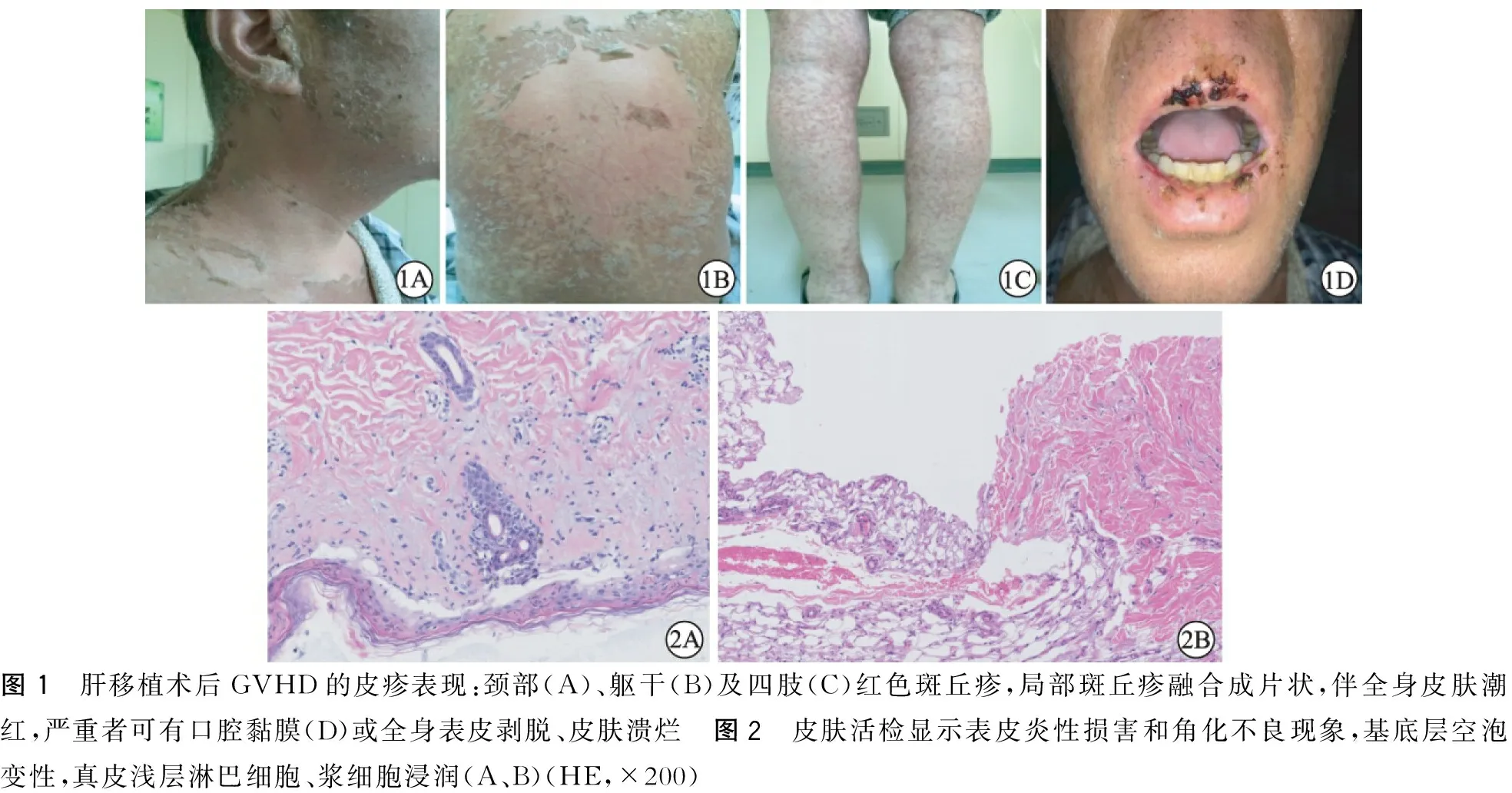
图1 肝移植术后GVHD的皮疹表现:颈部(A)、躯干(B)及四肢(C)红色斑丘疹,局部斑丘疹融合成片状,伴全身皮肤潮红,严重者可有口腔黏膜(D)或全身表皮剥脱、皮肤溃烂 图2 皮肤活检显示表皮炎性损害和角化不良现象,基底层空泡变性,真皮浅层淋巴细胞、浆细胞浸润(A、B)(HE,×200)
2.造血细胞因子的使用 在外周血发现白细胞计数有下降趋势或骨髓穿刺发现骨髓抑制的时候,应避免使用具有骨髓毒性的药物,还需要粒细胞集落刺激因子(G-CSF)和促血小板生成素(TPO)作为辅助治疗。在本组病例中,在发现外周血白细胞计数或血小板计数下降后,均每日皮下注射G-CSF或TPO以辅助治疗。
3.抗感染及强力支持治疗 肝移植术后GVHD病人需要积极提高机体免疫力,改善机体免疫紊乱状态,并预防性地使用广谱抗生素、抗真菌药及抗病毒药物。在所有6例肝移植术后GVHD病人中,例1在发病后予以胸腺肽20 mg/d皮下注射,例2~例6均予以静注人免疫球蛋白(intravenous immunoglobulin,IVIG)20~30 g/d(表3)。6例病人在早期发热时即经验性使用抗生素治疗,预防性给予伏立康唑或卡泊芬净抗真菌治疗。同时反复进行血培养、痰培养、大便培养、尿培养等,严密监测感染情况,并根据药敏结果调整抗生素使用。同时,给予强力的支持治疗。动态监测病人的生命体征及病情变化情况,根据需要进行抑酸、预防出血、成分输血、营养支持、维持水电解质平衡等治疗。
结 果
肝移植术后GVHD病人的预后较差。例1在开始干预时已经出现严重并发症,最终因严重肺部感染和多脏器功能衰竭死亡。例2在皮肤病理明确为GVHD后开始治疗,病情有所恢复,体温降至正常,皮疹基本消退,但此时病人已经出现严重骨髓抑制(全血细胞减少)和消化道出血,在积极治疗43 d后,虽然白细胞计数有所恢复,但最终还是因消化道大量出血死亡。总结前2例的治疗经验,我们发现,及早进行干预,减轻或防止出现严重并发症,如感染、消化道出血及骨髓抑制等,在治疗本病中具有至关重要的意义。因此,在治疗例3~例6时,一旦出现不明原因的发热及皮疹时,即开始减半或停止常规免疫抑制剂他克莫司和吗替麦考酚酯,并使用大量糖皮质激素联合免疫球蛋白冲击治疗。我们观察到,越早进行干预,疾病的进展越缓慢,腹泻、便血的症状轻,骨髓抑制的程度也较低。经过治疗后,4例病人的病情均有所好转,皮疹消退,白细胞基本恢复正常,病情稳定,均痊愈出院。(表3)
讨 论
肝移植术后GVHD的发病率极低,病死率极高,病因尚不明确。Chan等[7]的研究中,糖耐量异常、自身免疫性肝炎、酒精性肝病、肝细胞癌可能是肝移植术后GVHD的危险因素。另外,Elfeki等[8]研究表明:受者与供者年龄差大于20岁和HLA-Ⅰ类的近似匹配是高危因素,在匹配供者和受者时,同时去除这两个风险因素,可以明显减少肝移植术后GVHD的发生率,在本研究的6例GVHD中,4例原发病为肝细胞癌、1例为酒精性肝硬化,1例术前合并糖尿病,4例受供者年龄差在20岁以上,与之前的报道基本一致。
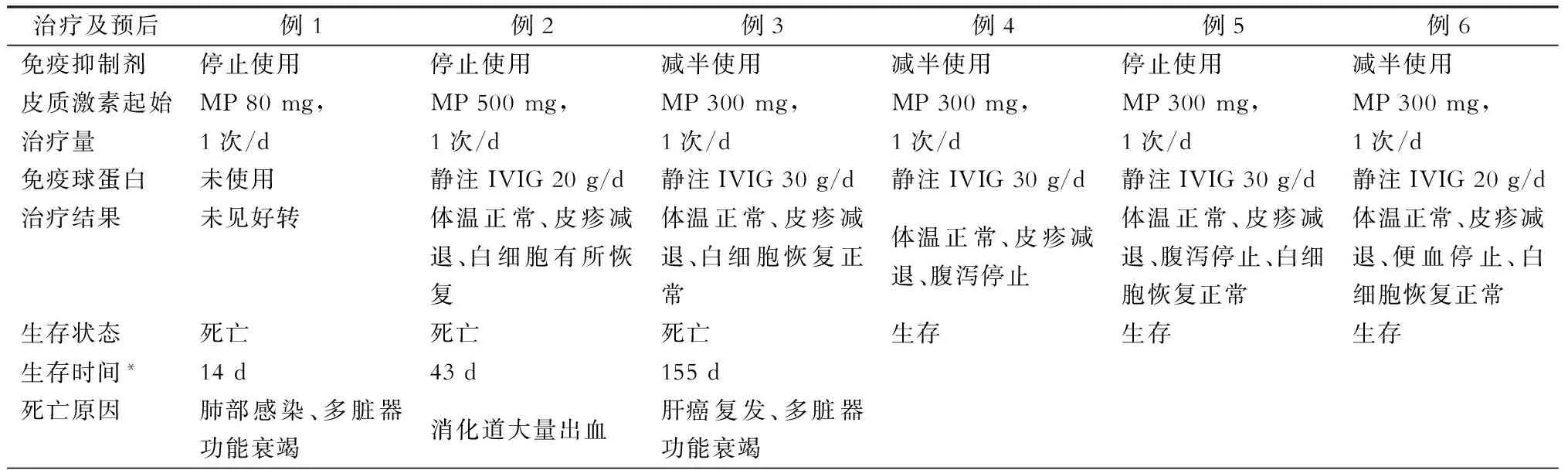
表3 急性移植物抗宿主病病人的治疗及预后
注:*肝移植术后至死亡时间
肝移植术后GVHD的发病机制十分复杂。目前一般认为:供者肝脏在经器官保存液灌洗后,仍有约109~1010的淋巴细胞存在于供肝肝门管区和实质内,这些残留的供者淋巴细胞与受者免疫系统处于博弈的状态,一旦供者淋巴细胞占优势,识别宿主体内主要组织相容性复合物抗原而致敏激活,进而增殖分化。由受者组织表达的细胞毒性T淋巴细胞攻击受者的皮肤、消化道、骨髓等,导致靶向细胞的死亡和组织功能障碍,进一步破坏受者免疫系统,释放的细胞因子又激活供者淋巴细胞,如此恶性循环,导致受者发生严重的全身性疾病甚至死亡[2,9]。
肝移植术后GVHD多发于术后2~6周,发生在100 d以后的称为慢性GVHD,但是也有研究认为移植后天数不足以区分急性和慢性GVHD,需要更重要的临床表现和病理描述[3]。由于缺乏典型临床表现,GVHD容易被误诊为感染或药疹。目前主要根据临床表现、组织活检和HLA配型检测进行诊断[10]。早期可表现为发热、皮疹、腹泻“三联征”,随着病情进展,病人可出现消化道出血和骨髓抑制状态,外周血白细胞显著减少,严重时可导致全血细胞极度减少,病情进展至此,病人往往已处于濒危状态。在我们观察的病例中,除例3无腹泻外,其余5例均出现了“三联征”。值得注意的是,例1早期连续6 d无大便,出现类似肠梗阻症状,到后期才出现大量便血,这可能预示着肠道功能破坏严重,导致肠道处于无功能状态。另外,例3和例6在疾病进展期间分别出现了视物模糊和癫痫症状,可能与相关组织器官细胞毒性T淋巴细胞攻击受损有关。对皮疹部位行皮肤活检,如果发现表皮松解及大疱形成、基底细胞呈空泡样改变、淋巴细胞浸润、角化不良等,有助于诊断GVHD,但这些并不是GVHD的特征性改变[11]。另外,通过PCR-STR检测到外周血或其他组织中有供者来源T细胞的嵌合体也有助于诊断GVHD[6]。
目前尚未有对GVHD特别有效的药物或治疗方案。糖皮质激素一方面具有抑制淋巴细胞增殖分化的作用,另一方面有着强大的抗炎作用,同时又可降温,延缓皮疹的进展,因此大多数的研究推荐使用皮质激素作为治疗肝移植术后GVHD的一线用药。在我们的病例中,所有病人均给予了不同剂量的MP。根据经验,我们建议,一旦高度怀疑或者确诊GVHD,即开始使用MP 5 mg·kg-1·d-1以上冲击治疗,以延缓病情进展,连用3 d后根据病情逐渐减量。大剂量IVIG可有效抑制单核巨噬细胞Fc受体活性,减少细胞因子的生物活性,中和循环中的自身HLA抗体,减轻受者靶器官的免疫损伤,在治疗心脏移植排斥反应获得了显著疗效[12-13],对于肝移植病人,可静注IVIG 20~40 g/d,以调整病人免疫状态,同时能增强病人被动免疫力,预防感染。对于常规免疫抑制剂的使用目前争议较大,有研究者认为增加免疫抑制剂的剂量能阻断某些通道的激活并能抑制T细胞活性,达到治疗的效果。但是也有研究表明增加免疫抑制剂的使用,并不能改善病人预后,是一种无效方案[14]。笔者认为,供者淋巴细胞在与受者免疫系统的博弈中占优势,导致受者不能有效清除供者T淋巴细胞是导致GVHD的病因。因此减半甚至停止免疫抑制剂,提高受者免疫力是治疗GVHD的一个重要方面。有研究者[15]对3例肝移植术后GVHD的病人实施减少免疫抑制的治疗方法,2例病人的T细胞嵌合体迅速消失,症状消失,并且在开始治疗后,其他症状出现的更晚,受者外周血中CD3 T细胞表达水平更低。也有研究者[16]对3例GVHD病人停止常规免疫抑制剂,结果全部病人体温降至正常,皮疹逐渐消退。其中2例病人腹泻停止,白细胞和血小板计数逐渐恢复,痊愈出院,1例病人出现继发性再生障碍性贫血,死于败血症。韩国的一项研究[17]报道了6例肝移植后GVHD的救治经验,前5例病人最初在出现发热及皮疹时被误诊为感染或药疹,治疗上减少或停止了免疫抑制剂,并给予抗生素和抗组胺治疗,但是没有效果。而后行皮肤或直肠活检确诊为GVHD,并谨慎地加用了MP(0.5~2 mg·kg-1·d-1)等治疗措施,症状稍有缓解,但由于治疗开始时间较晚,已并发严重细菌感染,且MP剂量较小,最终未救治成功。其第6例病人在发热及皮疹早期即诊断为GVHD,并予以大剂量MP(2 mg·kg-1·d-1)和减半使用他克莫司,同时予以预防性抗感染治疗,最终痊愈出院。值得注意的是,早期完全撤除免疫抑制剂可能会增加急性排斥反应的风险,因此我们也有减半使用免疫抑制剂的病例。除此之外,积极对症治疗,如抑酸、抗感染、粒细胞刺激因子、输血、营养支持等在GVHD的治疗中均是必不可少的。其他的一些疗法,如间充质干细胞(MSCs)[18]和抗CD25单克隆抗体[19-20]等,均有个别治疗成功的经验,这些方案是否可以作为皮质激素治疗无效的备选方案,或者能否作为辅助用药在GVHD的治疗中扮演重要的角色,均需要更大样本的深入研究。
总结所治疗的6例肝移植术后GVHD病人,我们认为,肝移植术后GVHD的早期诊断较为困难,依靠皮肤活检和骨髓穿刺活检确诊往往需要数天的时间,而疾病却进展迅速,很快便会出现消化道出血和严重的骨髓抑制,一旦出现这些症状,往往预示着病人已处于濒危的状态,因此我们强调尽早开始治疗。越早干预,病人受益的可能性越大。当肝移植术后病人早期出现不明原因的发热、皮疹及腹泻,即可开始给予积极的干预,一方面可以控制体温,加快皮疹恢复,避免免疫系统遭受破坏,另一方面可以减轻腹泻、便血的症状和骨髓抑制的程度,延缓病情进展。在治疗方面,我们认为如何恢复供受者免疫活性细胞之间的平衡是治疗的关键,及时减半或停止免疫抑制剂,再使用大量皮质醇激素联合免疫球蛋白的冲击疗法,是治疗GVHD有效的方法。此外,还应采取积极的预防感染和防治并发症的方案,同时给予强力支持治疗。
总之,肝移植术后GVHD是一种罕见但致命的疾病,临床表现不典型,目前尚无特别有效的治疗方案,一旦发现GVHD的可能,应尽早开始治疗。此外,需要大样本、更深入的研究来揭示GVHD的机制,预防其发生,并改善病人的预后。
1 阎冰,李捷,郭文治,等.ABO血型不合肝移植术后急性抗体介导的排斥反应研究进展.中华肝脏外科手术学电子杂志,2014,3:124-126. DOI:10.3877/cma.j.issn.2095-3232.2014.02.014.
2 Taylor AL,Gibbs P,Bradley JA.Acute graft versus host disease following liver transplantation: the enemy within. Am J Transplant, 2004,4:466-474.DOI:10.1111/j.1600-6143.2004.00406.x.
3 Akbulut S,Yilmaz M,Yilmaz S.Graft-versus-host disease after liver transplantation: a comprehensive literature review.World J Gastroenterol,2012,18:5240-5248.DOI:10.3748/wjg.v18.i37.5240.
4 Chaib E,Silva FD,Figueira ER,et al.Graft-versus-host disease after liver transplantation.Clinics(Sao Paulo),2011,66:1115-1118.DOI:10.1590/S1807-59322011000600035.
5 Smith DM,Agura E,Netto G,et al.Liver transplant-associated graft-versus-host disease.Transplantation,2003,75:118-126.DOI:10.1097/01.TP.0000039845.31111.B1.
6 Taylor AL,Gibbs P,Sudhindran S,et al.Monitoring systemic donor lymphocyte macrochimerism to aid the diagnosis of graft-versus-host disease after liver transplantation.Transplantation,2004,77:441-446.DOI:10.1097/01.TP.0000103721.29729.FE.
7 Chan EY, Larson AM,Gernsheimer TB,et al.Recipient and donor factors influence the incidence of graft-vs.-host disease in liver transplant patients.Liver Transpl,2007,13:516-522.DOI:10.1002/lt.21082.
8 Elfeki MA,Pungpapong S,Genco PV,et al.Graft-versus-host disease after orthotopic liver transplantation: multivariate analysis of risk factors.Clin Transplant,2015,29:1063-1066.DOI:10.1111/ctr.12627.
9 Rai V, Dietz NE,Agrawal DK.Immunological basis for treatment of graft versus host disease after liver transplant.Expert Rev Clin Immunol,2016,12:583-593.DOI:10.1586/1744666X.2016.1145056.
10吕国悦,蒋超,刘雪岩,等.肝移植术后急性移植物抗宿主病研究进展.中华肝脏外科手术学电子杂志,2017,6:144-146. DOI:10.3877/cma.j.issn.2095-3232.2017.02.016.
11Schrager JJ, Vnencak-Jones CL,Graber SE,et al.Use of short tandem repeats for DNA fingerprinting to rapidly diagnose graft-versus-host disease in solid organ transplant patients. Transplantation,2006,81:21-25.
12Leech SH,Lopez-Cepero M,LeFor WM,et al.Management of the sensitized cardiac recipient:the use of plasmapheresis and intravenous immunoglobulin.Clin Transplant, 2006,20:476-484.DOI:10.1111/j.1399-0012.2006.00509.x.
13Jordan SC,Vo AA, Peng A,et al.Intravenous gammaglobulin(IVIG):a novel approach to improve transplant rates and outcomes in highly HLA-sensitized patients.Am J Transplant, 2006,6:459-466.DOI:10.1111/j.1600-6143.2005.01214.x.
14Murali AR,Chandra S,Stewart Z,et al.Graft versus host disease after liver transplantation in adults:a case series, review of literature,and an approach to management.Transplantation,2016,100:2661-2670.DOI:10.1097/TP.0000000000001406.
15Chinnakotla S,Smith DM,Domiati-Saad R,et al.Acute graft-versus-host disease after liver transplantation: role of withdrawal of immunosuppression in therapeutic management.Liver Transpl,2007,13:157-161.DOI:10.1002/lt.20982.
16谢森,唐礼功,李志雄,等.肝移植受者急性移植物抗宿主病的治疗.华中科技大学学报(医学版),2014:344-347.DOI:10.3870/j.issn.1672-0741.2014.03.023.
17Kang WH,Hwang S,Song GW,et al.Acute graft-vs-host disease after liver transplantation:experience at a High-volume Liver Transplantation Center in Korea. Transplant Proc,2016,48:3368-3372.DOI:10.1016/j.transproceed.2016.08.051.
18Gregoire-Gauthier J,Selleri S,Fontaine F,et al.Therapeutic efficacy of cord blood-derived mesenchymal stromal cells for the prevention of acute graft-versus-host disease in a xenogenic mouse model. Stem Cells Dev,2012,21:1616-1626. DOI:10.1089/scd.2011.0413.
19Lu Y,Wu LQ,Zhang BY,et al.Graft-versus-host disease after liver transplantation: successful treatment of a case.Transplant Proc,2008,40:3784-3786.DOI:10.1016/j.transproceed.2008.03.164.
20Sudhindran S,Taylor A,Delriviere L,et al.Treatment of graft-versus-host disease after liver transplantation with basiliximab followed by bowel resection.Am J Transplant,2003,3:1024-1029.DOI:10.1034/j.1600-6143.2003.00108.x.
