LIMK1调控骨肉瘤细胞耐药的实验研究及机制分析
2018-01-23高奕瑶杨建增荣小丽
陈 瑞,高奕瑶,杨建增,荣小丽,王 岩
(吉林大学中日联谊医院 科学研究中心,吉林 长春130033)
骨肉瘤是儿童和青少年多发的恶性骨肿瘤[1],其治疗主要是以手术为主,放、化疗为辅,联合化疗不仅控制肿瘤细胞增殖,消除局部或远处转移,而且改善患者生存率[2]。然而化疗中多药耐药(Multidrug resistance,MDR)的发生成为了治疗的主要障碍[3],约有40%的患者在治疗初期表现出化疗耐药[4]。LIMK1 属于LIM 激酶蛋白家族成员[5],本项目组的前期研究发现LIMK1在骨肉瘤多药耐药细胞中呈高表达,同时验证了LIMK1对骨肉瘤多药耐药细胞耐药及迁移具有重要的调控作用[6,7]。
本实验通过瞬时转染技术验证了LIMK1基因表达上调对人成骨肉瘤细胞耐药的影响,并通过MEM和DAVID平台分析LIMK1及其共表达基因富集情况,进一步探讨可能的耐药机制,为临床防治肿瘤、开发靶向治疗研究奠定基础。
1 材料和方法
1.1材料
1.1.1细胞系及质粒 本实验的人成骨肉瘤细胞系(MG63)来自吉林大学中日联谊医院科学研究中心,重组质粒CFP- LIMK1- WT cDNA由中日联谊医院科学研究中心王岩教授赠送。
1.1.2主要试剂耗材及仪器 高糖 DMEM(H- DMEM)来自Gibico/USA,特级胎牛血清来自北京元亨金马/China,Lipofectamine 2000来自Invitrogen/USA,Trizol来自Invitrogen/USA,(DL- 2000) Marker 来自北京康为/China,RT- PCR 试剂盒来自Thermo/USA,2×Taq PCR MasterMix来自TaKaRa/Japan,引物来自上海生工/China,预染 marker来自NEB/USA。CCK- 8检测试剂盒来自Dojindo/Japan,长春新碱来自上海新华联制药有限公司/China, CO2 孵箱来自SANYO/Japan,超净工作台来自VS- 1301L- U 苏州安泰/ China。
1.1.3数据库分析 利用基因共表达网络分析平台MEM(http://biit.cs.ut.ee/mem/index.cgi)获得LIMK1的共表达基因;通过DAVID(https://david.ncifcrf.gov/summary.jsp)筛选LIMK1与其共表达基因相关联的信号转导通路,分析LIMK1可能的作用机制。
1.2方法
1.2.1质粒瞬时转染 取对数生长期的MG63细胞,用含 10%FBS的DMEM 培养基将细胞浓度稀释至 1×105/ml,接种于 6 孔板中,每孔300 μl,放置细胞培养箱内培养,条件为37℃、CO2,待细胞密度达70%- 80%时进行转染。瞬时转染采用 Lipofectamine 2000 进行,将重组质粒CFP- LIMK1- WT cDNA 按0 μg/ml、2.5 μg/ml、10 μg/ml三个浓度稀释到300 μl 无血清培养基中;放入培养箱内孵育4- 5小时,更换成含有 10%FBS的培养基。所有组别设3个复孔。
1.2.2RT- PCR实验检测 LIMK1及MDR1基因表达 取对数生长期的上述细胞,用 Trizol法提取各组细胞总 RNA(浓度为1 000 ng/μl),用Thermo 反转录试剂盒逆转录合成 cDNA,用TaKaRa试剂盒进行RT- PCR检测LIMK1及MDR1表达,以β- Actin内参进行比较,结果用2-△△ct计算相对表达量。所用引物见表1。
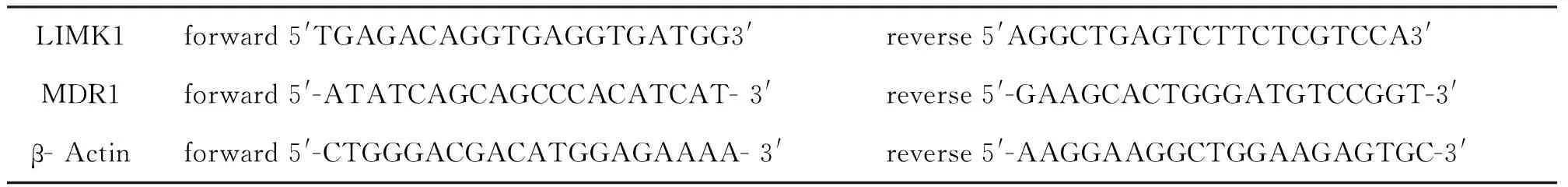
表1 引物序列
1.2.3药物抑制率测定 将上述细胞至于96孔板中培养,待细胞密度达70%- 80%时分别加入不同浓度的长春新碱,以其临床血浆峰浓度为参照设7个浓度梯度,分别为0 ng/ml、0.0625 ng/ml、0.25 ng/ml、1 ng/ml、4 ng/ml、16 ng/ml、64 ng/ml继续培养 48 h。更换为含10%CCK- 8 的无血清培养基,于孵箱内避光培养 2 h后用酶标仪检测,选用450 nm 波长测吸光度A值,以不含细胞的孔作为空白对照组调零。抑制率公式:抑制率(%)=1-[A(阴性)-A(实验)]/[A(阴性)]×100%,利用GraphPad Prism软件算出长春新碱对各细胞的半数抑制浓度 IC50值。
1.2.4统计学分析 IC50及RT- PCR采用 GraphPad Prism进行统计学分析,用mean±SD表示。MEM、DAVID及实验中的数据通过t检验获得P值,且P值<0.05为差异具有统计学意义。
2 结果
2.1瞬转后RT-PCR结果
用RT- PCR检测瞬时转染后各实验组中LIMK1及MDR1基因表达水平,结果如图1所示,转染浓度越高,LIMK1基因表达水平越高;同时,多药耐药基因MDR1的表达也随着LIMK1基因表达增强而增高。提示LIMK1基因表达上调增强骨肉瘤细胞的耐药能力,二者呈正相关。
2.2LIMK1表达上调增强细胞耐药能力
根据药物抑制率实验结果,应用抑制率公式计算抑制率;采用 GraphPad Prism统计软件,计算亲本及转染细胞的半数抑制浓度 IC50值。结果如表2所示,随着转染浓度增加,IC50值增加,二者呈正相关。
上述结果证明LIMK1表达上调,细胞耐药能力增强。

图1 RT- PCR 结果。A为LIMK1、MDR1及内参β- Actin的电泳结果。B为LIMK1及MDR1基因的相对表达量直方图。

cDNA浓度(μg/ml)02.510IC50(ng/ml)1.407±0.1112.083±0.0133.443±0.083P值-0.001<0.0001
2.3LIMK1影响肿瘤耐药可能的作用机制
通过MEM平台搜索LIMK1基因,筛选出与其密切相关的50个共表达基因,主要包括SRC,CSF1,EFNA2,FGF6等(见下图2)。同时通过DAVID平台分析上述共表达基因主要的富集信号通路,结果如表3所示,表中从左往右分别为信号通路名称、该通路中共表达基因所占百分比(%)、检验富集显著性的p值、相关联的共表达基因名称。与LIMK1共表达基因密切相关联的信号通路主要有Rap1 signaling pathway、TNF signaling pathway、Osteoclast differentiation、Influenza A、Calcium signaling pathway等,其中以Rap1 signaling pathway中共表达基因所占比例最高,相关性最强。
此外,利用Cancer Hallmarks Analytics Tool(CHAT,http://t.cn/Rp21Yxy)网络平台分析LIMK1在肿瘤中的主要作用,通过计算标准化逐点交互信息值,绘制成雷达图。如图3所示,图中10个扇形分别代表了10个不同的作用,分别是肿瘤侵袭和转移(0.1894)、免疫破坏(-0.0340)、细胞力学(-1)、永久复制(-1)、逃避生长抑制(0.0526)、基因组不稳定和突变(0.0002)、诱导血管生成(0.0718)、抵抗细胞死亡(0.0208)、维持增殖信号(0.1402)、肿瘤促进炎症(0.0121)。其中,以肿瘤侵袭和转移的标准化逐点交互信息值最高,达0.1894,提示LIMK1在肿瘤中以侵袭和转移作用为主。

图2 LIMK1及其共表达基因热图。如图所示,颜色深红,相关性大。
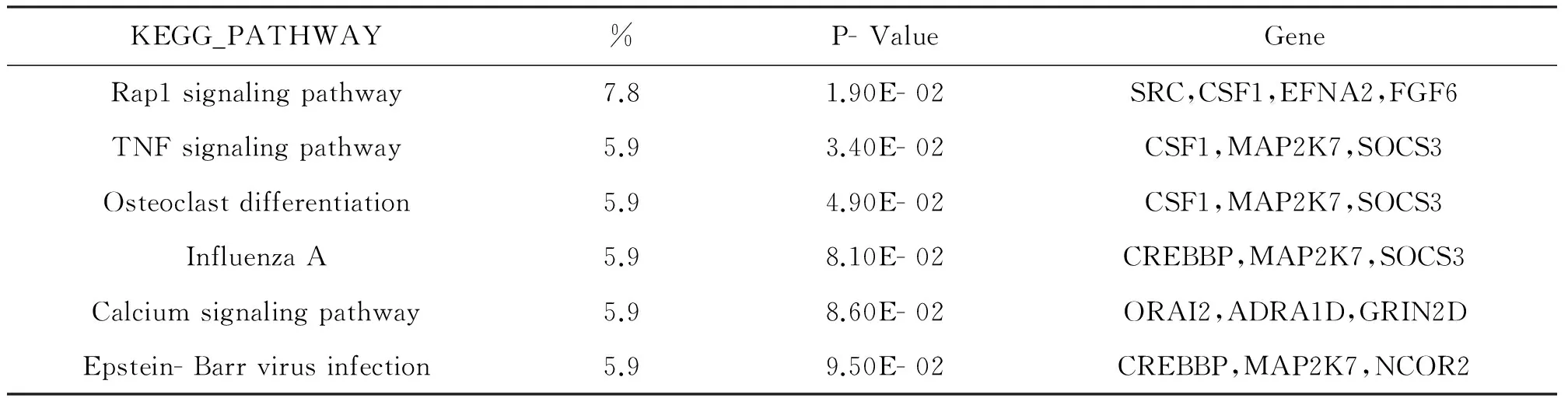
KEGG_PATHWAY%P-ValueGeneRap1signalingpathway7.81.90E-02SRC,CSF1,EFNA2,FGF6TNFsignalingpathway5.93.40E-02CSF1,MAP2K7,SOCS3Osteoclastdifferentiation5.94.90E-02CSF1,MAP2K7,SOCS3InfluenzaA5.98.10E-02CREBBP,MAP2K7,SOCS3Calciumsignalingpathway5.98.60E-02ORAI2,ADRA1D,GRIN2DEpstein-Barrvirusinfection5.99.50E-02CREBBP,MAP2K7,NCOR2
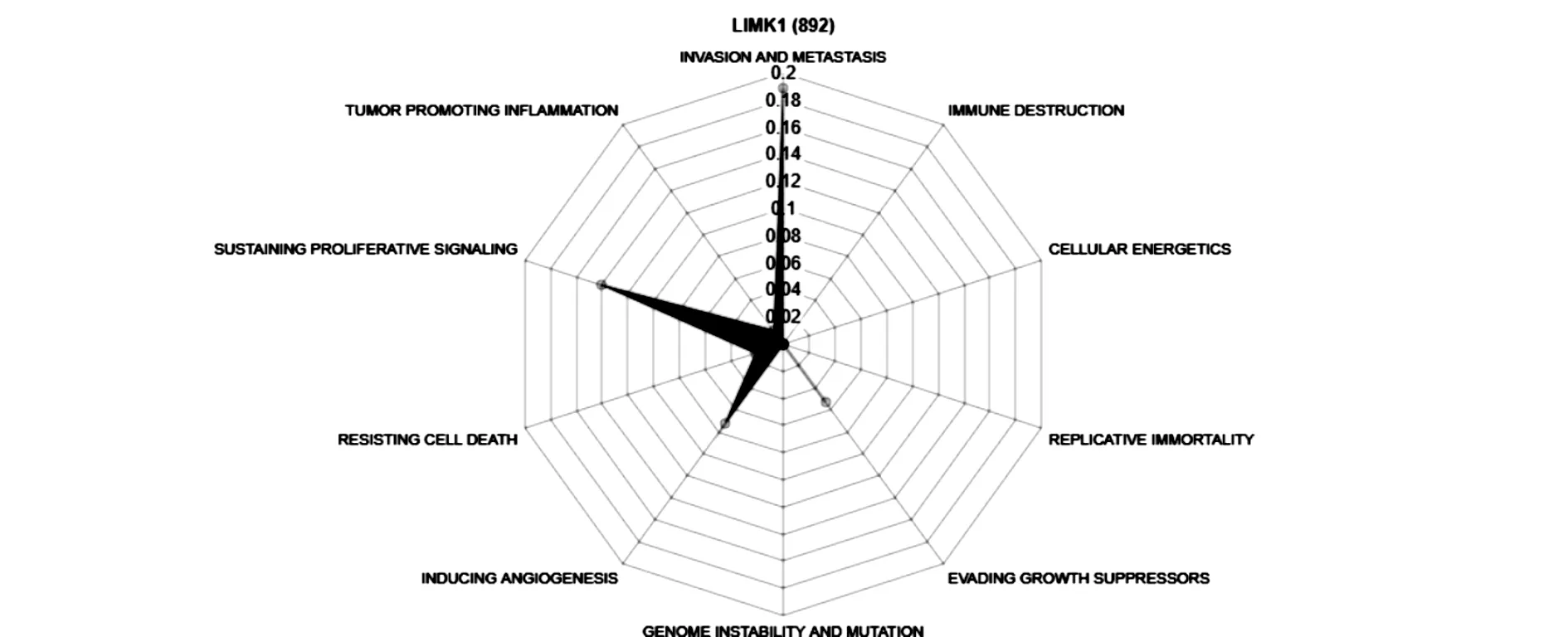
图3 LIMK1在肿瘤中主要作用的雷达图。图中10个扇形分别代表了10个不同的作用,十个同心圆代表标准化逐点交互信息值。
3 讨论
肿瘤耐药是当前肿瘤治疗与研究中面临的首要难题[8]。虽然已有不少对肿瘤耐药的分子机制方面的研究,比如增加药物外排,改变药物靶点,DNA损伤的修复等等[9],但肿瘤耐药是一个非常复杂的机制。MDR1又称ABCB1基因,编码P- gp蛋白,该蛋白属于ATP- 结合盒转运体,MDR1基因高表达提示细胞多药耐药,是肿瘤细胞多药耐药程度的主要评价标准[10]。LIMK1是一种包含两个LIM/锌指结构域N端的丝/苏氨酸激酶[11]。相关研究表明,LIMK1是调节肿瘤进展、转移和耐药的元素之一[12,13]。本文通过CHAT网络平台分析LIMK1在肿瘤中的主要作用,发现LIMK1主要与肿瘤侵袭和转移、免疫破坏、细胞力学、永久复制、逃避生长抑制、基因组不稳定和突变、诱导血管生成、抵抗细胞死亡、维持增殖信号、肿瘤促进炎症等多方面有关,其中,以肿瘤侵袭和转移为主,其次为维持增殖信号、诱导血管生成等(图3)。此外,还有研究证明LIMK1促进上皮- 间质转换(EMT,epithelial- mesenchymal transition),影响肿瘤患者生存率[14]。
将含有LIMK1激酶活性的重组质粒CFP-LIMK1-WT cDNA按不同浓度梯度瞬时转染人骨肉瘤细胞MG63,发现上调LIMK1基因表达,细胞的耐药能力及多药耐药基因MDR1的表达增强,二者呈正相关趋势(图1及表2)。说明LIMK1能促进骨肉瘤细胞的耐药能力,其可能成为克服肿瘤耐药的靶基因,旨在为开发新的靶向治疗提供理论支撑。
DAVID是由整合的生物学知识库和分析工具组成的生物信息学数据库分析平台[15],本文应用该平台从LIMK1及其共表达基因中筛选出主要富集的信号通路,如Rap1 signaling pathway、TNF signaling pathway、Osteoclast differentiation、Influenza A、Calcium signaling pathway等(表3)。有研究表明在非小细胞肺癌中,RAP1-NF-κB轴对细胞增殖和耐药有调节作用[16],还有研究显示TNF可以激活多药耐药肿瘤细胞中的新的细胞毒性通路[17]。上述信号通路为LIMK1影响肿瘤耐药的作用机制的研究提供线索和思路。
[1]Cai S,Zhang T,Zhang D,et al.Volume-sensitive chloride channelsare involved in cisplatin treatment of osteosarcoma[J].Mol Med Rep,2015,11:2465.
[2]Wang Y,Teng JS.Increased multi- drug resistance and reduced apoptosis inosteosarcoma side population cells are crucial factors for tumor recurrence[J].Exp Ther Med,2016,12:81.
[3]Xiaojie Wang,Hong Zheng,Tao Shou,et al.Effectiveness of multi- drug regimen chemotherapy treatment in osteosarcoma patients:a network meta- analysis of randomized controlled trials[J].J Orthop Surg Res,2017,12(1):52.
[4]Hattinger CM,Pasello M,Ferrari S,et al.Emerging drugs for highgrade osteosarcoma[J].Expert Opin Emerg Drugs,2010,15:615.
[5]Arber S,Barbayannis FA,Hanser H,et al.Caroni P:Regulation of actin dynamics through phosphorylation of cofilin by LIM- kinase[J].Nature,1998,393:805.
[6]Zhang H1,Wang Y,Xing F,et al.Overexpression of LIMK1 promotes migration ability of multidrug- resistant osteosarcoma cells[J].Oncol Res,2011,19(10- 11):501.
[7]Jianzeng Yang,Lihong Huang,et al.LIM kinase 1 serves an important role in themultidrug resistance of osteosarcoma cells[J].Oncology Letters,2017,73(17):1792.
[8]Luetke A,Meyers P A,Lewis I,et al.Osteosarcoma treatment-Where do we stand A state of the art review[J].Cancer Treatment Reviews.2014,40(4):523.
[9]Holohan C,Van Schaeybroeck S,Longley D B,et al.Cancer drug resistance:an evolving paradigm[J].Nature Reviews Cancer,2013,13(10):714.
[10]Rajkumar T,Yamuna M.Multiple pathways are involved in drug resistance to doxorubicin in an osteosarcoma cell line [J].Anticancer Drugs,2008,19(3):257.
[11]Okano I,Hiraoka J,Otera H,et al.Identification and characterization of a novel family of serine/threonine kinases containingtwo N- terminal LIM motifs[J].J Biol Chem,1995,270(52):31321.
[12]Tiangeng You,Wei Gao,Jun Wei,et al.Overexpression of LIMK1 promotes tumor growth and metastasis ingastric cancer [J].Biomed Pharmacother,2015,69:96.
[13]Qingyong Chen,Demin Jiao,Huizhen Hu,et al.Downregulation of LIMK1 Level Inhibits Migration ofLung Cancer Cells and Enhances Sensitivity to Chemotherapy Drugs[J].Oncol Res,2013,20(11):491.
[14]Bo Su,Jian Su,Ying Zeng,et al.Diallyl disulfide suppresses epithelial- mesenchymal transition,invasion and proliferation by downregulation of LIMK1 in gastriccancer[J].Oncotarget,2016,7(9):10498.
[15]Dennis GJr,Sherman BT,Hosack DA,et al.DAVID:Database for Annotation,Visualization,and Integrated Discovery [J].Genome Biol,2003,4(5):3.
[16]Lu Xiao1,Xiaoying Lan,Xianping Shi,et al.Cytoplasmic RAP1 mediates cisplatin resistance ofnon- small cell lung cancer [J].Cell Death Dis,2017,8(5):e2803.
[17]D′Alessandro N1,Flugy A,Tolomeo M,et al.The apoptotic signaling of TNF- alpha in multidrug resistant Friend leukemia cells[J].Anticancer Res,1998,18(4C):3065.
