百脉根化学成分的研究
2018-01-22李小强杨怡昱陈业高
李小强,杨怡昱,彭 伟,陈业高
(云南师范大学 化学化工学院,云南 昆明 650500)
百脉根(LotuscorniculatusLinn)为豆科(Leguminosae)百脉根属(Lotus)植物,产自西北、西南和长江中上游各省区,生于湿润而呈弱碱性的山坡、草地、田野或河滩地.亚洲、欧洲、北美洲和大洋洲均有分布[1].百脉根作为传统中草药,具有清热祛湿、止渴解毒、活血散瘀和治疗扁桃体炎、咽炎的功效.百脉根属植物中主要有尖齿百脉根、兰屿百脉根、短果百脉根、细叶百脉根和翅荚百脉根等.迄今为止,已从百脉根属植物中分离得到了大量化合物,主要包括黄酮类、酚苷类和三萜皂苷等.百脉根植物的提取物及活性成分具有较强的抗炎、抗菌作用,对肿瘤细胞有明显的抑制作用[2-5].为了探索新的活性天然产物,我们对云南产百脉根的化学成分进行了分离鉴定,采用包括硅胶柱层析、反相柱层析和Sephadex LH-20柱层析等方法,从中分离得到了6个化合物.经过波谱分析鉴定其结构为:kaempherol (1), quercetin (2), quercetin-3-O-α-L-arabinofuranose (3), 2′,4′,3,4-α-pentahydroxychalcone (4), trimerhylester dehydrochebulic acid (5), syringic acid (6).其中化合物1-5为首次从该种植物中分离得到.
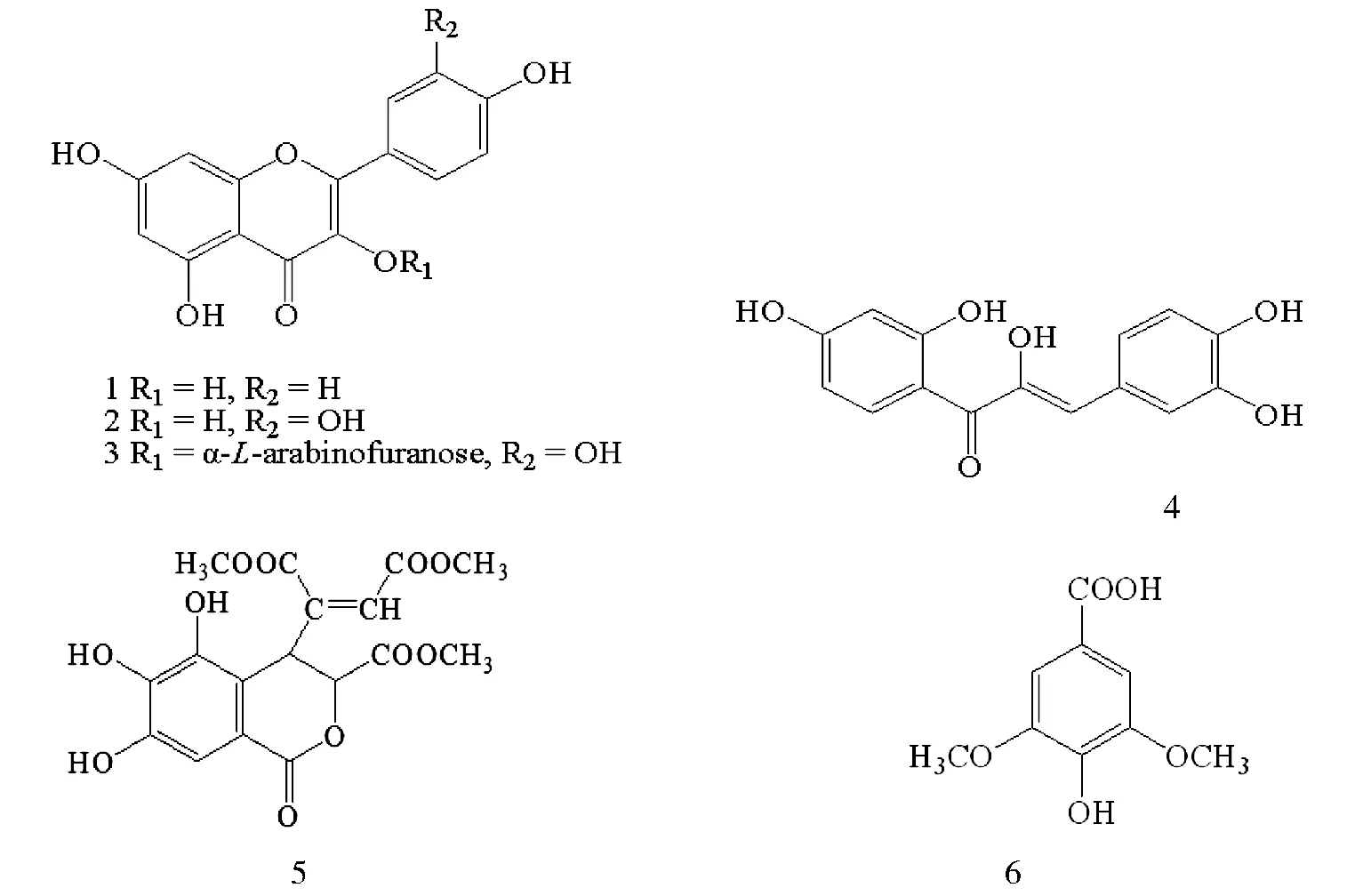
图1 化合物1-6的结构
1 药材与仪器
1.1 仪器
Bruker DRX-500 MHz 超导核磁共振仪(瑞士Bruker公司);ZF-II型紫外分析仪(上海顾村中实仪器厂);Sephadex LH-20:20~80μm(Pharmacia Fine Chemical Co., Ltd.);反相色谱硅胶 RP-C 18:(40-63μm,德国Merck公司);EYELA IV-1100型旋转蒸发仪(上海爱朗仪器有限公司).
1.2 试剂
高效薄层层析硅胶板GF 25(烟台化工研究院);层析硅胶(青岛海洋化工厂);显色剂10%浓硫酸-乙醇溶液;所用溶剂为工业纯(重蒸),其它试剂为化学纯或分析纯.
1.3 药材
百脉根(LotuscorniculatusLinn) 地上部分5.0 kg,由昆明医科大学药学院陈丽君老师采集自云南寻甸,并鉴定.
2 提取与分离
百脉根地上部分5.0 kg,粉碎后用工业甲醇室温浸提4次,浸出液减压浓缩得甲醇提取物320 g.将浸膏加入到2.0 L蒸馏水中,使其完全溶解,然后用乙酸乙酯萃取4次,共用乙酸乙酯2.0 L,得到乙酸乙酯部分(185 g).再将乙酸乙酯部分用丙酮溶解,用288 g硅胶(80-100目)拌样后上柱,用氯仿-甲醇(1 ∶0→0 ∶1)梯度洗脱,经薄层层析检验,分为9个部分F-1(35.0 g)、F-9(11.8 g)、F-9(16.5 g)、F-9(25.4 g)、F-9(45.8 g)、F-9(22.6 g)、F-9(11.4 g)、F-9(12.5 g)、F-9(18.6 g)、F-9(16.6 g).取氯仿/甲醇(20 ∶1)部分,经反复的硅胶柱层析,Sephadex LH-20柱层析和反相硅胶柱层析进行分离纯化,得到kaempherol (1, 20 mg), quercetin (2, 9 mg), quercetin-3-O-α-L-arabinofuranose (3, 24 mg), 2′,4′,3,4-α-pentahydroxychalcone (4, 18 mg), trimerhylester dehydrochebulic acid (5, 45 mg)和syringic acid (6, 18 mg).
3 结构鉴定
化合物1:黄色粉末,分子式C15H10O6,溶于甲醇.1H-NMR (500 MHz, CD3OD): δ 6.21 (1H, d,J= 2.0 Hz, H-6), 6.42 (1H, d, J = 2.0 Hz, H-8), 8.09 (2H, d,J= 8.5 Hz, H-2′, 6′), 6.92 (2H, d,J= 8.5 Hz, H-3′, 5′);13C-NMR (125 MHz, CD3OD): δ 176.0 (s, C-4), 164.2 (s, C-7), 161.1 (s, C-9), 159.1 (s, C-4′), 156.9 (s, C-5), 146.7 (s, C-2), 135.7 (s, C-3), 129.3(d, C-2′, 6′), 122.3 (s, C-1′), 114.9 (d, C-3′, 5′), 103.2 (s, C-10), 97.9 (d, C-6), 93.1 (d, C-8). 以上数据与文献中kaempherol的数据一致[6],故鉴定化合物1为kaempherol.
化合物2:黄色粉末,分子式C15H10O7,溶于甲醇.1H-NMR (500 MHz, CD3OD): δ 7.75 (1H, d,J= 2.0 Hz, H-2′), 7.65 (1H, dd,J= 2.0, 8.5 Hz, H-6′), 6.90 (1H, d,J= 8.5 Hz, H-5′), 6.41 (1H, d,J= 2.0, H-8), 6.20 (1H, d,J= 2.0 Hz, H-6);13C-NMR (125 MHz, CD3OD): δ175.9 (s, C-4), 164.2 (s, C-7), 161.0 (s, C-5), 156.8 (s, C-9), 147.4 (s, C-4′), 146.6 (s, C-2), 144.8 (s, C-3′), 135.8 (s, C-3), 122.7 (s, C-1′), 120.3 (d, C-6′), 114.8 (d, C-5′), 114.6 (d, C-2′), 103.1 (s, C-10), 97.9 (d, C-6), 93.0 (d, C-8). 以上数据与文献中quercetin的数据一致[7],故鉴定化合物2为quercetin.
化合物3:黄色粉末,分子式为C20H18O11,溶于甲醇.1H-NMR (500 MHz, CD3OD): δ 7.55 (1H, d,J= 8.0 Hz, H-6′), 7.55 (1H, s, H-2′), 6.91 (1H, d,J= 8.0 Hz, H-5′), 6.41 (1H, s, H-8), 6.22 (1H, s, H-6), 5.49 (1H, s, H-1′′), 4.35 (1H, brs, H-4′′), 3.93 (1H, d,J= 10.8 Hz, H-5′′b), 3.86 (1H, dd,J= 10.8, 6.3 Hz, H-5′′a), 3.52 (2H, brs, H-2′′, 3′′);13C-NMR (125 MHz, CD3OD): 178.6 (s, C-4), 164.6 (s, C-7), 161.7 (s, C-5), 157.9(s, C-9), 157.2(s, C-2), 148.4 (s, C-4′), 144.9 (s, C-3′), 133.5 (s, C-3), 121.7 (d, C-6′), 121.6 (s, C-1′), 115.4 (d, C-5′), 115.0 (d, C-2′), 108.1 (d, C-1′′), 104.2 (s, C-10), 98.5 (d, C-6), 93.4 (d, C-8), 86.6 (d, C-4′′), 81.9 (d, C-2′′), 77.3 (d, C-3′′), 61.1 (t, C-5′′). 以上数据与文献中的quercetin-3-O-α-L-arabinofuranose数据一致[8],故鉴定化合物3为quercetin-3-O-α-L-arabinofuranose.
化合物4:黄色晶体,分子是为C15H12O6,溶于甲醇.1H-NMR (500 MHz, CD3OD): δ 7.60 (1H, d,J= 2.0 Hz, H-2), 7.52 (1H, d,J= 8.0 Hz, H-6′), 7.23 (1H, dd,J= 8.0, 2.0 Hz, H-6), 6.85 (1H, d,J= 8.0 Hz, H-5), 6.70 (1H, dd,J= 8.0, 2.0 Hz, H-5′), 6.69 (1H, s, H-β), 6.68 (1H, d,J= 2.0 Hz, H-3′); 13C-NMR (125 MHz, CD3OD): δ 183.1 (s, C-β′), 168.4 (s, C-2′), 166.9 (s, C-4′), 148.0 (s, C-4), 146.3 (s, C-α), 145.3 (s, C-3), 125.4 (d, C-6′), 125.1 (d, C-6), 124.2 (s, C-1′), 117.6 (d, C-2), 115.3 (d, C-5), 113.5 (s, C-1), 113.3 (d, C-3′), 112.7 (d, 5′), 98.0 (d, C-β). 以上数据与文献中2′,4′,3,4-α-pentahydroxychalcone的数据一致[9],故鉴定化合物4为2′,4′,3,4-α-pentahydroxychalcone.
化合物5:白色粉末,分子式为C17H16O11,溶于甲醇.1H-NMR (500 MHz, CD3OD): δ 7.08 (1H, s, H-7), 6.84 (1H, s, H-3′), 5.37 (1H, d,J= 1.5 Hz, H-3), 5.32(1H, d,J= 1.5 Hz, H-2), 3.71 (3H, s, OCH3), 3.66 (3H, s, OCH3), 3.65 (3H, s, OCH3);13C-NMR (125 MHz, CD3OD): 165.4 (s, C-1), 78.6 (d, C-2), 34.3 (d, C-3), 114.9 (s, 3-a), 143.0 (s, C-4), 145.5 (s, C-5), 139.1 (s, C-6), 107.4 (d, C-7), 116.3 (s, C-7a), 166.4 (s, C-1′), 141.6 (s, C-2′), 129.0(d, C-3′), 165.7 (s, C-4′), 169.8 (C=O), 51.8 (q, OCH3), 52.2 (q, OCH3), 51.4 (q, OCH3). 以上数据与文献中trimerhylester dehydrochebulic acid的数据一致[10],故鉴定化合物5为trimerhylester dehydrochebulic acid.
化合物6:白色针状晶体,分子式为C9H10O5,溶于甲醇.1H-NMR (500 MHz, CD3OD): δ 3.83 (6H, s, -OCH3× 2), 7.08 (2H, d,J= 2.0 H-2, 6);13C-NMR (125 MHz, CD3OD): δ 51.1 (q, OCH3× 2), 108.8 (d, C-2, 6), 120.1 (s, C-1), 138.5 (s, C-4), 145.1 (s, C-3, 5), 167.9 (s, COOH). 以上数据与文献中syringic acid的数据一致[11],故鉴定化合物6为syringic acid.
4 结论
从百脉根地上部分分离得到6个化合物,通过波谱解析和理化性质对其进行了结构鉴定,分别鉴定为:kaempherol (1), quercetin (2), quercetin-3-O-α-L-arabinofuranose (3), 2′,4′,3,4-α-pentahydroxychalcone (4), trimerhylester dehydrochebulic acid (5)和syringic acid (6).其中化合物1-5为首次从该种植物中分离得到.
[1]中国科学院中国植物志编辑委员会.中国植物志(42卷)[M].北京: 科学出版社, 1998.
[2]Jay M, Hasan A, Viricel M R, et al. Les flavonides duLotuscoeniculatus[J]. Phytochemistry, 1978, 17(4): 827-829.
[3]Rafiq S, Majeed R, Qazi A K, et al. Isolation and antiproliferative activity ofLotuscorniculatuslectin towards human tumour cell lines[J]. Phytomedicine, 2013, 21(1): 30-38.
[4]Janaina K, Dianaana P, Julianabastos D, et al. Evaluation of the anti-inflammatory efficacy ofLotuscorniculatus[J]. Food Chem, 2010, 117(3): 444-450.
[5]Golea L, Haba H, Lavaud C, et al. Chemical constituents fromLotuspusillusMedik[J]. Biochem Syst Ecol, 2012, 45(6): 12-15.
[6]Liu C D, Chen J, Wang J H, et al. A novel kaempferol triglycoside from flower buds ofPanaxquinquefolium[J]. Chem Nat Compd, 2009, 45(6): 808-810.
[7]Jung M, Park M. Acetylcholinesterase inhibition by flavonoids fromAgrimoniaPilosa[J]. Molecules, 2007, 12(9): 2130-2139.
[8]Chin Y W, Lim S W, Kim Y C, et al. Hepatoprotective flavonol glycosides from the aerial parts ofRodgersiapodophylla[J]. Planta Med, 2004, 70(6): 576-577.
[9]Metunoa R, Ngandeu F, Tchinda A T, et al. Chemical constituents ofTreculiaacuminataandTreculiaafricana(Moraceae)[J]. Biochem Syst Ecol, 2008, 36(2): 148-152.
[10]姚庆强, 左春旭.叶下珠化学成分的研究[J]. 药学学报, 1993, 28(11): 829-835.
[11]Chang S W, Kim K H, Choi S U, et al. Phytochemical constituents ofGeraniumeriostemon[J]. Na Prod Sci, 2009, 15(3): 151-155.
