电感耦合等离子体原子发射光谱法测定油田含油污泥中钾
2018-01-19,,,,,
, , , , ,
(1. 中国石化 江苏油田分公司工程院, 扬州 225009; 2. 扬州大学 化学化工学院, 扬州 225002; 3. 中国石化 江苏油田分公司采油一厂, 扬州 225009)
油田含油污泥是在油田开发、油水分离、原油脱水、污水处理、油品运输和油品加工、贮存时产生的一种污染物。据不完全估计,我国每年油田含油污泥的生产量为10×104~44×104t。油田含油污泥已被列入《危险废物目录》中,根据2011年国务院颁布的《排污费征收使用管理条例》中的规定,每吨油田含油污泥的排污费达1 000元,这将大幅提高相关企业的生产成本[1-2]。现场油田含油污泥由于产生来源不同,有毒、有害物质的组成与含量差异巨大。2016年5月31日国务院颁布的《土壤污染防治行动计划》中一个较为明显的变化,不是将污染物取出来,而是实现土壤的安全利用。由此带来现场急需了解油田含油污泥中有什么有多少的问题,由于现场油田含油污泥中存在的油类及其他杂质的影响,常规方法无法实现油田含油污泥中钾含量的测定。
近年来,关于油田含油污泥资源化应用的研究和报道很多,较为成熟的方法有超声破乳后冷冻和机械分离、蒸汽萃取或超临界萃取等,通过这些技术可实现水-油-泥三相的基本分离[3-4]。分离后的废水、废油均可以得到处置或利用[5],分离后的残渣中土壤营养元素的含量,直接决定残渣资源化应用的价值。处理后污泥中残存0.3%左右的油类等物质,导致其中钾含量仍然无法测定。
钾的含量是评价土壤肥力价值的重要指标[6],土壤中的钾不仅能促进激活植物体中主要的3种酶类(合成酶、氧化还原酶及转移酶),而且可以提高植物光合作用的强度,促进植物体内淀粉及植物蛋白的形成,同时还能提高养分的输送效率[7-8]。准确测定油田含油污泥残渣中的钾含量对油田含油污泥残渣的资源化应用具有非常重要的指导意义。
本工作在分离油田含油污泥中水、油和渣后,用混合酸消解剩余残渣,通过电感耦合等离子体原子发射光谱法(ICP-AES)对消解液中钾的含量进行测定。
1 试验部分
1.1 仪器与试剂
PerkinElmer Optima 8000型电感耦合等离子体发射光谱仪;DH 257-9030A型电热恒温鼓风干燥箱;L-350-A型石墨电热板;BYJ 1-10L-D型超纯水机。
钾标准储备溶液:1 000 mg·L-1。
钾为优级纯,硝酸钾为光谱纯,其余试剂均为分析纯,试验用水为超纯水。
试验器皿均用10%(体积分数,下同)硝酸溶液浸泡过夜,用自来水反复冲洗后,再用超纯水冲洗备用。
1.2 仪器工作条件
射频功率为1 300 W;雾化气流量为0.8 L·min-1,辅助气流量为0.2 L·min-1,等离子气流量为15 L·min-1;试液提升量为1.5 mL·min-1;观测方式为轴向观测,观测高度为15 mm。自动积分;点火预热30 min;钾测定波长为766.49 nm。
1.3 试验方法
1.3.1 油田含油污泥样品的水-油-渣三相分离
取250 mL油田含油污泥样品于500 mL烧杯中,搅拌0.5 h后,取8.00 g于无胶滤筒中,并将滤筒放入索氏提取器中,移取200 mL甲苯于下方250 mL烧瓶中,上方依次连接玻璃分水器和球形冷凝管,打开冷凝水和电热套开关,加热回流4~6 h[9],当萃取液澄清后继续回流1 h。关火,待装置冷却后,取出滤筒,于393 K下烘干12 h。将残渣取出,粉碎过0.25 mm筛,收集6.25 g试样[10],混匀后装入试剂瓶中。
1.3.2 钾的测定
称取上述粉碎过筛试样0.500 0 g于聚四氟乙烯坩埚中,用水润湿后加入盐酸10 mL,于电热板上低温加热,使样品初步分解,待蒸发至约3 mL,稍冷后加入硝酸5 mL,氢氟酸5 mL和高氯酸3 mL,加盖,于电热板上中温加热约1 h后,开盖继续加热除硅,经常振动坩埚,以确保除硅效率。当加热至冒浓厚白烟(高氯酸)时,加盖分解黑色物质(有机碳化物)。待坩埚壁上的黑色物质消失后,开盖,驱赶白烟并蒸至黏稠状(视消解情况,可补加硝酸3 mL,氢氟酸3 mL和高氯酸1 mL,重复以上消解过程)[11]。取下坩埚稍冷,加入硝酸1 mL和少量水,温热溶解残渣,冷却后全部转移至100 mL容量瓶中,用水定容至100 mL,摇匀,按仪器工作条件进行测定,并做试样空白[12]。
1.3.3 钾的计算
按公式(1)计算钾的质量分数:
wK=ρK×f×Vm×1 000(1)
式中:wK为钾在残渣中的质量分数,mg·kg-1;ρK为试样消解后经ICP-AES测定,在标准曲线上读取的质量浓度,mg·L-1;V为试样消解后定容的体积,L;f为稀释的倍数,一般取20;m为称取油水分离后渣土的质量,g。
2 结果与讨论
2.1 油田含油污泥加热回流时间的选择
按试验方法对ZW站、T83站和SN站的含油污泥进行油水分离,在索氏提取器中的甲苯萃取液澄清后,取出于393 K下烘干6 h。称取烘干后的滤筒质量,将称重完毕后的滤筒放回提取器中,之后每加热回流0.5 h,取出滤筒,以相同的温度和时间进行烘干,称重,记录累计回流3 h每次称取的滤筒质量,考察萃取液澄清后的加热回流时间对测定的影响,结果见表1。

表1 加热回流时间的优化试验结果Tab. 1 Results of optimization experiment of heating reflux time
由表1可知:油田含油污泥样品的水-油-渣三相组成随样品采取地的不同差异悬殊,因而在对含水,含油和含渣量差异较大的油田含油污泥样品进行油水分离时,不能简单地以总的回流时间来判断其油水分离的完全程度;当索氏提取器中萃取液澄清后,继续加热回流1 h,滤筒的质量已不再减少。试验选择加热回流时间为当萃取液澄清后继续回流1 h。
2.2 干扰试验
取不同来源的3组油田含油污泥样品,按试验方法进行消解,将消解液定容至100 mL后,分别取消解液5.00 mL于8个100 mL容量瓶中,再向容量瓶中加入等物质的量的干扰金属元素(干扰物钠、氧化镁、氧化铝、氧化钙、铁的质量浓度依次为22.99,40.30,50.98,56.08,55.85 mg·L-1),定容后按仪器工作条件进行测定,并记录仪器的响应值。结果表明:加入等物质的量的土壤中常见的金属元素干扰物后,仪器的响应值变化很小,最大不超过0.80%,可见土壤中常见的金属元素并不影响钾的测定。
2.3 标准曲线和检出限
将1 000 mg·L-1钾标准储备溶液用1%硝酸溶液逐级稀释,配制钾质量浓度为1.0,5.0,20,40,60,80 mg·L-1的标准溶液。按仪器工作条件对上述标准溶液系列进行测定,并绘制标准曲线。结果表明:钾的质量浓度在1.0~80 mg·L-1内与其对应的发射强度呈线性关系,线性回归方程为y=6.553×104x-4.290×104,相关系数为0.999 8。
重复测定10份1%的硝酸溶液(空白溶液),以测定值的3倍标准偏差计算方法的检出限(3s)为3.03 μg·L-1。
2.4 精密度试验
按试验方法分别对ZW站和T83站的含油污泥样品进行10次平行测定,结果见表2。
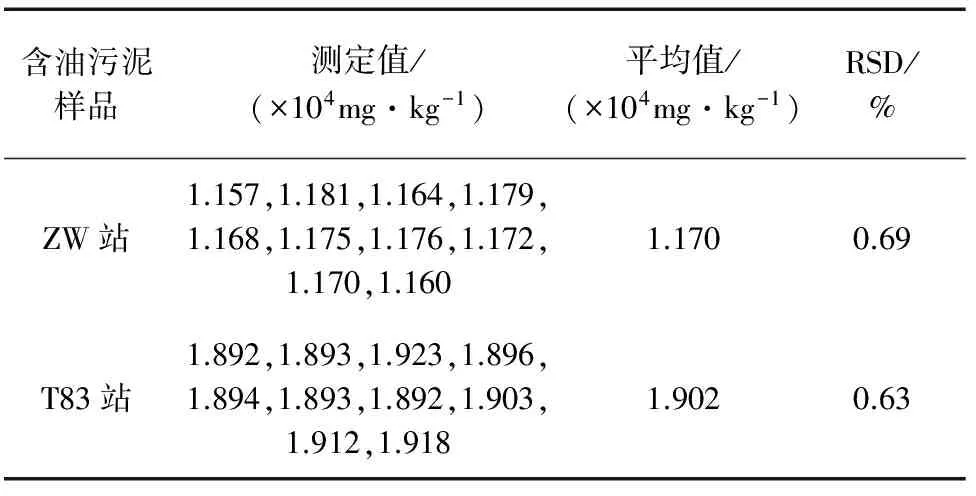
表2 精密度试验结果(n=10)Tab. 2 Results of test for precision(n=10)
由表2可知:该方法对油田含油污泥中钾的测定具有良好的重现性。
2.5 回收试验
加入硝酸钾(标准物质)于ZW站和T83站的含油污泥样品中,进行加标回收试验,其结果见表3。
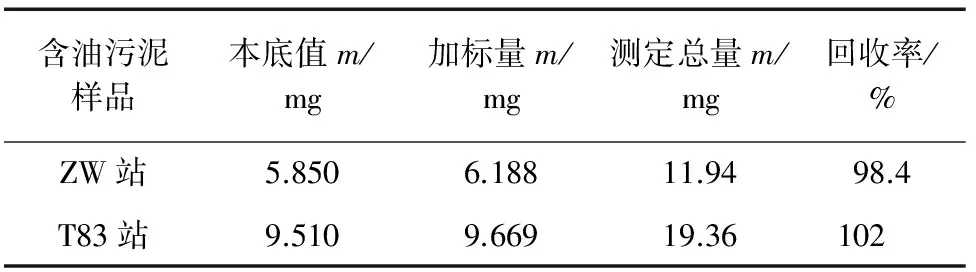
表3 回收试验结果Tab. 3 Results of test for recovery
由表3可知:该方法测定油田含油污泥中钾准确性较好。
本工作用甲苯回流萃取,将油田含油污泥水-油-渣三相分离,采用电感耦合等离子体原子发射光谱法测定油田含油污泥中钾。方法不仅准确,精密,而且不受矿物中共存金属元素的干扰。目前,众多新型破乳剂不断应用于油田含油污泥的油水分离[13],对分离所得残渣的土壤修复及资源利用的研究也在逐步深入。在未来大规模地对油水分离后的油田含油污泥残渣进行土壤修复前后,本方法为其中钾含量的测定提供了一种有效的方法。
[1] 刘志林,完石光,于莹.石化含油污泥的资源化利用[J].环境保护与循环经济, 2010(12):58-61.
[2] 金浩,石丰,刘鹏,等.含油污泥的干燥研究[J].石油与天然气化工, 2011,40(5):522-526.
[3] HU G J, LI J B, ZENG G M. Recent development in the treatment of oily sludge from petroleum industry: A review[J]. J Hazard Mater, 2013,261(8):470-490.
[4] ZHANG J, LI J B, THRING R W, et al. Oil recovery from refinery oily sludge via ultrasound and freeze/thaw[J]. J Hazard Mater, 2012,203/204:195-203.
[5] OUYANG W, LIU H, MURYGINA V, et al. Comparison of bio-augmentation and composting for remediation of oily sludge: A field-scale study in China[J]. Process Biochem, 2005,40(12):3763-3768.
[6] JANSSENS F, PEERERS A, TALLOWIN J R B, et al. Relationship between soil chemical factors and grassland diversity[J]. Plant Soil, 1998,202(1):69-78.
[7] 沈瑞之.钾对植物的生理作用[J].上海农业科技, 1982(5):32-34.
[8] PAL P K, KUMAR R, GULERIA V, et al. Crop-ecology and nutritional variability influence growth and secondary metabolites of stevia rebaudiana bertoni[J]. BMC Plant Biology, 2015,15(67):3-16.
[9] 朱嘉卉.含油污泥的理化特性研究与分析[D].杭州:浙江大学, 2014.
[10] LEHOTAY S J, COOKJ J M. Sampling and sample processing in pesticide residue analysis[J]. Agric Food Chem, 2015,63(18):4395-4404.
[11] 齐文启,汪志国,孙宗光.土壤污染分析中样品采集与前处理方法探讨[J].现代科技论文, 2007(1):55-58.
[12] JOHN W O. Elemental analysis using ICP-OES and ICP/MS[J]. Anal Chem, 1991,63(1):12-21.
[13] LI X B, LIU J T, XIAO Y Q, et al. Modification technology for separation of oil sludge[J]. J Cent South Univ Technol, 2011,18(2):367-373.
