贝伐珠单抗联合化疗引起肾脏相关不良反应的临床观察
2017-11-21李小影陈建胜潘景业
李小影,陈建胜,潘景业
·临床医学·
·论著·
贝伐珠单抗联合化疗引起肾脏相关不良反应的临床观察
李小影,陈建胜,潘景业
目的观察晚期结直肠癌患者应用贝伐珠单抗联合化疗后出现高血压及蛋白尿的发生率。方法选取2012年1月至2016年12月我科收治的晚期结直肠癌患者64例,行贝伐珠单抗联合化疗。贝伐珠单抗用药:第1天予5 mg/kg静脉滴注30~90 min,以2周为1个周期;或第1天予7.5 mg/kg静脉滴注30~90 min,以3周为1个周期。应用贝伐珠单抗后定期监测血压,贝伐珠单抗每个周期给药前48 h内,行尿常规或24 h尿蛋白定量检查。结果贝伐珠单抗联合化疗后患者高血压发生率为26.6%,其中3级高血压发生率为7.8%,4级高血压发生率为1.6%。贝伐珠单抗联合化疗后患者蛋白尿的发生率为10.9%,其中3级蛋白尿的发生率为3.1%,无肾病综合征发生。结论贝伐珠单抗联合化疗不良反应发生率较低,安全性较好,使用该药过程中应定期监测及时处理发生的不良反应。
贝伐珠单抗;不良反应;高血压;蛋白尿
结直肠癌是起源于结直肠黏膜上皮的恶性肿瘤,是临床最常见的消化系统恶性肿瘤。随着现代人们生活方式和饮食结构的改变,我国目前每年新发的结直肠癌病例已超过25万,死亡病例约14万[1]。不同分期的结直肠癌患者应用贝伐珠单抗治疗已在临床十分常见,贝伐珠单抗是重组人源化抗血管内皮生长因子(vascular endothelial growth factor, VEGF)的单克隆抗体,它的主要作用机制是通过与细胞表面的VEGF结合,从而阻断VEGF与受体结合,之后进一步阻断VEGF介导的下游信号通路,发挥抗肿瘤效应[2]。目前该药已经过FDA批准与他药联合化疗应用于转移性结直肠癌患者的治疗。
高血压和蛋白尿是贝伐珠单抗在临床应用期间常见的与肾脏相关的不良反应。高血压的发生可增加蛋白尿的风险,蛋白尿的发生与肾脏损伤有关,2种肾脏相关不良反应均需中途停止使用贝伐珠单抗,而这会影响患者的整体治疗效果。因此笔者总结了2012年1月至2016年12月瑞安市中医院晚期结直肠癌患者行贝伐珠单抗治疗后出现高血压及蛋白尿不良反应的发生情况,以期提高疗效降低不良反应,为临床提供更有价值的参考建议。
1 资料与方法
1.1 一般资料 选取瑞安市中医院64例晚期结直肠癌患者,发病年龄31~65岁,中位年龄48岁。其中行结直肠癌根治术后出现复发转移31例,未行根治性手术切除33例。所有患者均经病理明确诊断,其中结肠癌47例,直肠癌17例。转移部位经B超、CT、MRI、骨ECT或穿刺活检病理等检查确诊。所有患者均有应用贝伐珠单抗治疗指征,均无贝伐珠单抗治疗禁忌证,所有患者随访至停用贝伐珠单抗治疗后1个月。见表1。

表1 64例晚期结直肠癌患者一般情况
注:ECOG评分:美国东部肿瘤协作组评分
1.2 治疗方法 贝伐珠单抗(Bevacizumab,商品名Avastin,规格:100 mg 4 ml,注册证号S20120068 Genentech Inc)第1天以5 mg/kg静脉滴注30~90 min,以2周为1个周期;或第1天以7.5 mg/kg静脉滴注30~90 min,以3周为1个周期。贝伐珠单抗持续应用至病情进展2次或出现Ⅲ度以上不良反应,经减量处理仍无法耐受为止。所有患者化疗4个周期至20个周期不等,排除化疗药物造成有肾脏相关不良反应的患者。每个周期评价药物不良反应,化疗3个周期后评价疗效。
1.3 疗效评价及不良反应监测 (1)按实体瘤疗效评价标准(response evaluation criteria in solid tumor,RECIST)评价,分为完全缓解(complete remission, CR)、部分缓解(partial remission, PR)、稳定(stable disease, SD)、进展(progressive disease, PD)。若患者3个周期后评价为CR、PR及SD,应在4周后再次重新测量肿瘤病灶,仍为CR、PR及SD的患者最后评定为CR、PR及SD。有效率(response rate, RR)为CR及PR的患者数占患者总数的百分比,疾病获益率(disease control rate, DCR)为CR、PR及SD的患者数占患者总数的百分比,无进展生存期(progression free survival, PFS)为化疗开始至肿瘤出现进展的时间。(2)不良反应监测方法。静脉滴注贝伐珠单抗后每小时1次,连续监测血压3次,后每日定时监测血压。每个周期在贝伐珠单抗给药前48 h内,行尿常规检查或24 h尿蛋白定量检查,对于已出现高血压或基础血压较高的患者加强监测。不良反应分级标准参考美国国立癌症研究所常见不良事件标准(National Cancer Institute′s common terminology criteria,NCI-CTC)分级分为0~4级。1级高血压指无症状一过性的(<24 h)血压增高>20 mmHg(舒张压),或之前血压处于正常范围,但本次测量血压>150/100 mmHg(1 mmHg=0.133 kPa),无需进行干预。2级高血压指反复或持续性(>24 h)或出现症状,血压增高>20 mmHg(舒张压)或以前血压处于正常范围,但该次测量血压>150/100mmHg,可使用一种抗高血压药物进行治疗。3级高血压指需要一种以上抗高血压药物或比以前更高强度的治疗。4级高血压指危及生命,例如出现高血压危象。1级蛋白尿指尿蛋白+或24 h尿蛋白定量<1 g。2级蛋白尿指尿蛋白++~+++或1 g≤24 h尿蛋白定量≤2 g。3级蛋白尿指尿蛋白++++或24 h尿蛋白>2 g。4级蛋白尿指符合肾病综合征诊断标准。
1.4 统计学处理 采用SPSS 18.0统计学软件进行数据分析,2组数据间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 临床特征 所有患者进入本研究时均为晚期结直肠癌,均有明确的贝伐珠单抗应用的适应证,无贝伐珠单抗使用的禁忌证,合并使用的化疗药物均无明显肾脏相关不良反应。64例患者共接受贝伐珠单抗靶向治疗325个周期,平均每位患者治疗约5个周期,全组患者均可评价疗效及不良反应。
2.2 近期疗效 所有患者均可评价疗效,其中CR 2例,PR 18例,SD 23例。所有患者平均PFS为10.6个月,总有效率为31.2%,总疾病控制率为67.2%。
2.3 不同情况结直肠癌患者高血压及蛋白尿的发生率 所有患者经贝伐珠单抗治疗后,高血压的发生率为26.6%,其中3级高血压发生率为7.8%,4级高血压发生率为1.6%。所有患者蛋白尿的发生率为10.9%,其中3级蛋白尿的发生率为3.1%,未发生肾病综合征。见表2。
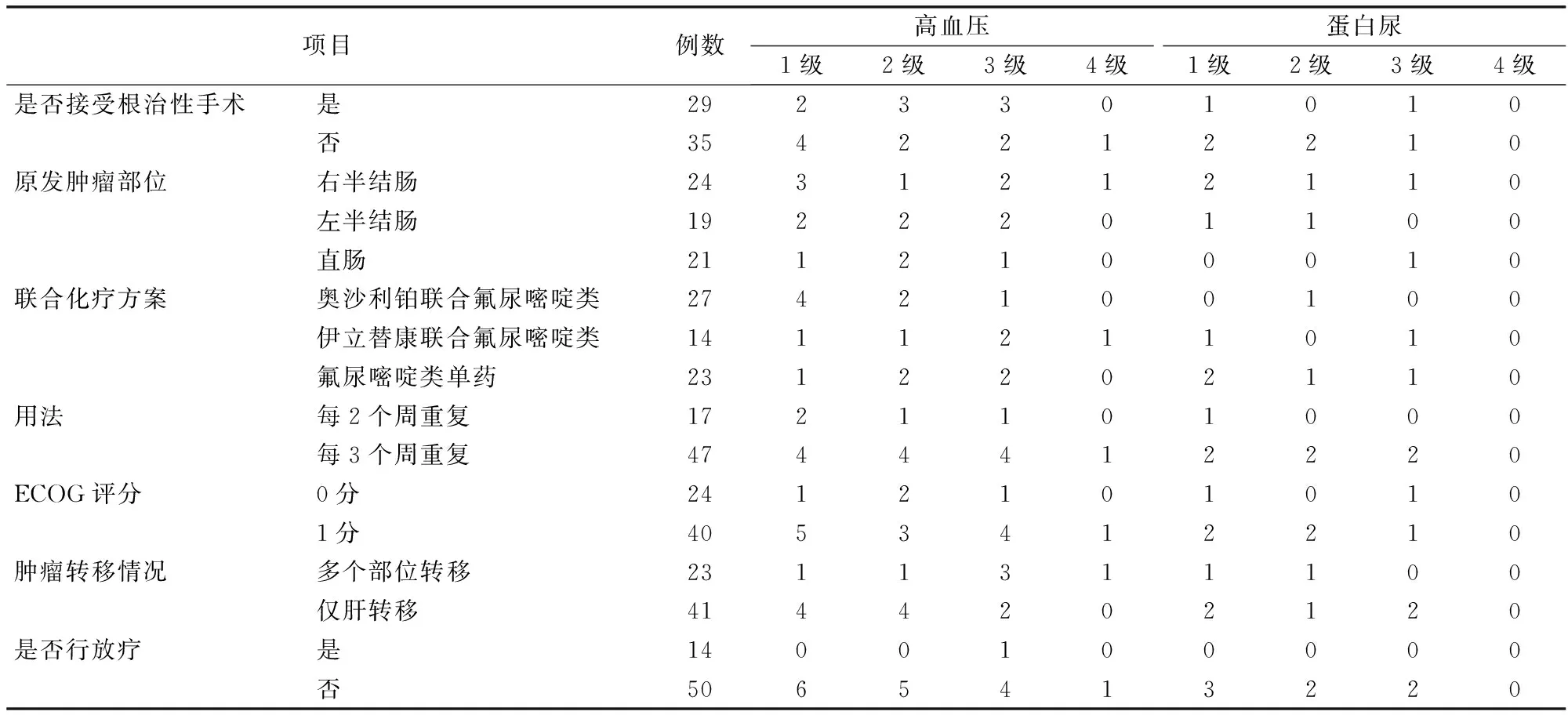
表2 不同情况结直肠癌患者高血压及蛋白尿发生例数(例)
注:ECOG评分:美国东部肿瘤协作组评分
3 讨论
在目前世界上进行的应用贝伐珠单抗联合化疗治疗转移性结直肠癌的关键性临床试验中,其中报道贝伐珠单抗联合化疗组患者3~4级高血压的发生率为4%~11%,3~4级蛋白尿发生率<1%。所有有适应证的患者进行化疗联合贝伐珠单抗靶向治疗期间,高血压的发生率为34%,其中3~4级高血压的发生率为0.4%~17.9%,4级高血压的发生率为1%。所有有适应证的患者进行化疗联合贝伐珠单抗治疗期间,出现各级蛋白尿的发生率为0.7%~38%,其中3级蛋白尿的发生率<3%,4级蛋白尿(肾病综合征)的发生率为1.4%。在国内进行的贝伐珠单抗联合化疗用于晚期结直肠癌的临床研究中,贝伐珠单抗联合化疗组患者的高血压发生率为15.6%,其中3级高血压发生率为3.5%。蛋白尿的发生率为17%,其中3级蛋白尿发生率为1.4%[3-5]。
关于晚期结直肠癌患者应用贝伐珠单抗联合治疗后出现高血压,其机制目前尚未明确。文献中提出的有以下理论机制:(1)与NO信号通路抑制有关。血管内皮生长因子作用于血管内皮细胞后,可以增加NO合成酶的形成,从而使NO合成增加。患者经药物作用,NO信号通路受抑制,NO合成减少而影响了血管平滑肌细胞顺应性,并激活了肾素-血管紧张素-醛固酮系统,引起了肾脏尿钠排泄减少,血钠增高,进而导致了高血压的发生[6-7]。(2)与抑制新生血管形成有关。贝伐珠单抗除了抑制肿瘤的新生血管外,还可降低外周组织和器官中的微血管密度。血管内皮生长因子减少,从而血管内皮的反应性下降,进而造成了外周血管的阻力增加,导致血压升高[8-9]。(3)与增加血栓发生的风险有关。应用贝伐珠单抗后可促进肾小球微血管血栓的形成,从而使肾小球入球和出球小动脉的两侧血管张力失去平衡,其刺激肾素-血管紧张素系统而增加了外周血循环的阻力,进而导致血压升高[9]。研究认为应用贝伐珠单抗治疗后出现蛋白尿的发生机制:(1)与抗血管内皮生长因子治疗后引起肾小球滤过屏障损伤有关。血管内皮生长因子由肾小囊脏层上皮细胞产生,通过血管内皮细胞生长因子受体2(vascular endothelial growth factor receptor 2,VEGFR-2)作用于内皮细胞而维持正常的滤过功能[10-11]。当血管内皮生长因子的分泌受到抑制后,引起内皮细胞肿胀、脱落、肾小囊上皮细胞功能异常,同时形成血栓性微血管病变[12],导致正常滤过功能丧失,肾小球滤液中的蛋白质增多。当蛋白质的量超过肾小管的重吸收能力,导致肾小管上皮细胞内所含的蛋白水解酶丢失,进而引起肾小管功能障碍,重吸收能力降低,最终即导致蛋白尿,严重者可引起肾病综合征[13]。(2)其他部分原因也与贝伐珠单抗引起高血压相关。出现蛋白尿的患者往往同时也有高血压的发生,贝伐珠单抗治疗后出现蛋白尿,因该类患者多为晚期恶性肿瘤而极少行肾脏活检明确病因,据文献报道,行肾病理活检的该类患者主要表现为血栓性微血管病变[12]。
本研究通过对本院收治的64例晚期结直肠癌患者进行了贝伐珠单抗相关的高血压及蛋白尿的发生率统计,统计结果与文献报道基本一致。但因不良反应发生率较低,并未发现高血压与蛋白尿的发生与各亚组(包括有无接受根治性手术切除、原发肿瘤部位、联合化疗方案、贝伐珠单抗用法、给药阶段及患者的一般状况和疾病状态)有相关性。但Zhu X等[14]进行的Meta分析提示,在应用小剂量的贝伐珠单抗(3.0、5.0或7.5 mg/kg,2周为1个周期)治疗时,高血压发生的相对风险比为3.0,而应用大剂量贝伐珠单抗(10或15 mg/kg,2周为1个周期)治疗时,高血压发生的相对风险比升至7.5。因此对高龄(>75岁)和接受大剂量贝伐珠单抗治疗患者需密切监测血压情况,这可能与患者的血管顺应性有关。此外高血压和蛋白尿的发生还可能与疗效呈正相关。
目前晚期结直肠癌患者中断贝伐珠单抗治疗的主要原因为病情进展或反复出现3级及以上的不良反应。因此临床加强对不良反应的预防、监测和及时处理,可以让患者更好地接受贝伐珠单抗长期维持治疗。从本研究结果看,高血压是患者行贝伐珠单抗治疗后出现的最常见的不良反应,而蛋白尿的发生往往也与高血压密切相关,因此加强患者的血压监测并及时处理至关重要。对于已出现高血压及蛋白尿的患者,常规处理均可控制良好,对化疗周期的进行影响较小,安全性较高。在良好地预防、严格地监测、及时地处理高血压及蛋白尿后,贝伐珠单抗在临床的应用将更为广泛和持久。
[1] 中华医学会消化内镜学分会, 中国抗癌协会肿瘤内镜学专业委员会. 中国早期结直肠癌筛查及内镜诊治指南(2014,北京)[J]. 中华医学杂志, 2015, 95(28): 2235-2252. DOI:10.3760/cma.j.issn.0376-2491.2015.28.002.
[2] Vaziri SA, Kim J, Ganapathi MK, et al. Vascular endothelial growth factor polymorphisms: role in response and toxicity of tyrosine kinase inhibitors[J]. Curr Oncol Rep, 2010, 12(2): 102-108. DOI:10.1007/s11912-010-0085-4.
[3] Hurwitz H, Fehrenbacher L, Novotny W, et al. Bevacizumab plus irinotecan, fluorouracil, and leucovorin for metastatic colorectal cancer[J]. N Engl J Med, 2004, 350(23): 2335-2342. DOI:10.1056/NEJMoa032691.
[4] Saltz LB, Clarke S, Díaz-Rubio E, et al. Bevacizumab in combination with oxaliplatin-based chemotherapy as first-line therapy in metastatic colorectal cancer: a randomized phase III study[J]. J Clin Oncol, 2008, 26(12): 2013-2019. DOI:10.1200/JCO.2007.14.9930.
[5] Giantonio BJ, Catalano PJ, Meropol NJ, et al. Bevacizumab in combination with oxaliplatin, fluorouracil, and leucovorin (FOLFOX4) for previously treated metastatic colorectal cancer: results from the Eastern Cooperative Oncology Group Study E3200[J]. J Clin Oncol, 2007, 25(12): 1539-1544. DOI:10.1200/JCO.2006.09.6305.
[6] Hood JD, Meininger CJ, Ziche M, et al. VEGF upregulates ecNOS message, protein, and NO production in human endothelial cells[J]. Am J Physiol, 1998, 274(3 Pt 2): H1054-H1058.
[7] Shen BQ, Lee DY, Zioncheck TF. Vascular endothelial growth factor governs endothelial nitric-oxide synthase expression via a KDR/Flk-1 receptor and a protein kinase C signaling pathway[J]. J Biol Chem, 1999, 274(46): 33057-33063. DOI:10.1074/jbc.274.46.33057.
[8] Mourad JJ, des Guetz G, Debbabi H, et al. Blood pressure rise following angiogenesis inhibition by bevacizumab. A crucial role for microcirculation[J]. Ann Oncol, 2008, 19(5): 927-934. DOI:10.1093/annonc/mdm550.
[9] Hayman SR, Leung N, Grande JP, et al. VEGF inhibition, hypertension, and renal toxicity[J]. Curr Oncol Rep, 2012, 14(4): 285-294. DOI:10.1007/s11912-012-0242-z.
[10] Sugimoto H, Hamano Y, Charytan D, et al. Neutralization of circulating vascular endothelial growth factor (VEGF) by anti-VEGF antibodies and soluble VEGF receptor 1 (sFlt-1) induces proteinuria[J]. J Biol Chem, 2003, 278(15): 12605-12608. DOI:10.1074/jbc.C300012200.
[11] Gurevich F, Perazella MA. Renal effects of anti-angiogenesis therapy: update for the internist[J]. Am J Med, 2009, 122(4): 322-328. DOI:10.1016/j.amjmed.2008.11.025.
[12] Eremina V, Jefferson JA, Kowalewska J, et al. VEGF inhibition and renal thrombotic microangiopathy[J]. N Engl J Med, 2008, 358(11): 1129-1136. DOI:10.1056/NEJMoa0707330.
[13] Izzedine H, Massard C, Spano JP, et al. VEGF signalling inhibition-induced proteinuria: mechanisms, significance and management[J]. Eur J Cancer, 2010, 46(2): 439-448. DOI:10.1016/j.ejca.2009.11.001.
[14] Zhu X, Wu S, Dahut W L, et al. Risks of proteinuria and hypertension with bevacizumab, an antibody against vascular endothelial growth factor: systematic review and meta-analysis[J]. Am J Kidney Dis, 2007, 49(2): 186-193. DOI:10.1053/j.ajkd.2006.11.039.
(本文编辑:甘辉亮,边冬冬)
Clinicalobservationoftheadversereactionsonkidneyinducedbybevacizumabcombinedwithchemotherapy
LiXiaoying,ChenJiansheng,PanJingye
(DepartmentofNephrology,RuianHospitalofTraditionalChineseMedicien,Ruian325200,China)
ObjectiveTo observe the adverse effects of bevacizumab combined with chemotherapy on the incidence of hypertension and proteinuria in the patients with advanced colorectal cancer.MethodsSixty-four patients with advanced colorectal cancer, who
medical care in our department of the hospital from January 2012 to December 2016, were enrolled for the study. The patients were treated with bevacizumab combined with chemotherapy. The treatment profiles of bevacizumab medication were: venous dropping at a dosage of 5 mg/kg for a duration of 30~90 minutes was administered the first day, with 2 weeks as a treatment cycle; or venous dropping at a dosage of 7.5 mg/kg for a duration of 30~90 minutes was given the first day, with 3 weeks as a treatment cycle. Following medication of bevacizumab, blood pressure was detected regularly. Forty-eight hours before each treatment cycle, urine routines or 24 hour quantitative urine protein were detected.ResultsThe incidence of hypertension for the patients treated with bevacizumab combined with chemotherapy was 26.6%, of which the incidence of grade 3 hypertension was 7.8% and that of grade 4 hypertension was 1.6%. After combined treatment of bevacizumab and chemotherapy, the incidence of proteinuria was 10.9%, of which the incidence of grade 3 proteinuria was 3.1%, but without the occurrence of nephrotic syndromes.ConclusionAdverse drug reactions in the combined use of bevacizumab and chemotherapy were relatively low, with good safety. Nevertheless, regular monitoring of hypertension and proteinuria should be made for the sake of safety.
Bevacizumab; Adverse reactions; Hypertension; Proteinuria
R979.19
A
10.3969/j.issn.1009-0754.2017.05.017
325200 浙江 瑞安,瑞安市中医院肾内科(李小影、陈建胜);温州医科大学附属第一医院急诊科(潘景业)
潘景业,电子信箱:panjingye@wzhospital.cn
2017-07-02)
