卵巢癌中Tiam1蛋白过表达的临床病理学意义
2017-11-20朴俊杰林贞花
杨 洋,孙 洁,朱 光,朴俊杰,林贞花
·论 著·
卵巢癌中Tiam1蛋白过表达的临床病理学意义
杨 洋,孙 洁,朱 光,朴俊杰,林贞花
目的探讨卵巢癌中Tiam1过表达的临床病理学意义。方法采用免疫组化SP两步法检测Tiam1蛋白在98例浆液性卵巢癌组织、64例黏液性囊腺癌组织以及27例良性病变组织中的表达,并分析其过表达与卵巢癌临床病理特征的关系。应用Kaplan-Meier进行生存分析。结果Tiam1蛋白主要表达于卵巢癌细胞胞质和胞核中。在浆液性卵巢癌组织中,Tiam1蛋白的阳性率和强阳性率分别为84.7%(83/98)和70.4%(69/98);在黏液性囊腺癌组织中,Tiam1蛋白的阳性率和强阳性率分别为87.5%(56/64)和73.4%(47/64),显著高于良性卵巢肿瘤组织(22.2%和7.4%)(P均<0.01)。Tiam1蛋白表达水平与卵巢癌组织学分级、FIGO分期和转移情况密切相关(P均<0.05);与患者年龄及绝经情况无关(P均>0.05)。Kaplan-Meier生存分析显示,Tiam1蛋白高表达的卵巢癌患者总生存期和无瘤生存期均明显低于Tiam1蛋白低表达患者(P均<0.05),且Tiam1蛋白高表达的转移性卵巢癌患者总生存期也明显低于Tiam1蛋白低表达患者(P<0.05)。结论Tiam1蛋白在卵巢癌组织中明显高表达,其表达水平与卵巢癌患者的预后密切相关。
卵巢肿瘤;Tiam1;免疫组织化学;预后;生存分析
卵巢癌是临床最常见的妇科恶性肿瘤之一,也是女性癌症死亡的常见病因[1]。由于该病的发病部位较为隐蔽,且早期症状不明显,患者通常在初诊时已为晚期,一般预后差,生存期短[2]。因此,探寻早期识别卵巢癌、有效预测患者预后的分子靶标已成为当今医学界研究的热点。
Tiam1首次发现于小鼠T淋巴瘤细胞中,位于人类第21号染色体q22上,是Rac1特定的鸟嘌呤核苷酸交换因子[3-4]。近年研究发现,Tiam1在多种恶性肿瘤中呈高表达,如胰腺癌[4]、乳腺癌、肝癌和鼻咽癌[5]等。同时,Tiam1高表达参与肿瘤的进程,如细胞凋亡[6-7]、淋巴结转移等[8]。Li等[9]报道Tiam1蛋白异常表达与乳腺癌的发生、发展密切相关,可作为预测乳腺癌临床预后的独立风险因素。目前,Tiam1在卵巢癌组织的表达及其发生、发展的关系尚未见报道。本文应用免疫组化SP两步法检测189例卵巢癌中Tiam1蛋白的表达及其与临床病理特征的关系,探讨Tiam1蛋白对卵巢癌预后的评估价值。
1 材料与方法
1.1材料收集2005年5月~2013年5月吉林大学第二医院存档的189例卵巢癌标本,包括浆液性卵巢癌98例、黏液性囊腺癌64例、良性病变组织27例,其中浆液性囊腺瘤19例、黏液性囊腺瘤8例。所有病例临床资料完整,患者在术前均未接受过放、化疗。统计189例卵巢癌标本的临床病理资料,包括患者年龄(>48岁和≤48岁)、绝经情况、组织分化程度、FIGO分期(根据美国癌症联合委员会的最新分期标准)以及淋巴结转移等。
1.2主要试剂Tiam1鼠抗人单克隆抗体购自美国圣克鲁斯公司(sc-872),免疫组化SP两步法试剂盒购自北京中杉金桥公司。
1.3免疫组化染色所有标本均经过10%中性福尔马林固定、常规脱水、透明、浸蜡、石蜡包埋、4 μm厚连续切片以及免疫组化染色。具体步骤按本组前期实验进行[10],主要包括:4 μm厚组织切片,常规脱蜡,梯度乙醇水化,抗原热修复,滴加Tiam1抗体(稀释比例1 ∶200),4 ℃孵育过夜;滴加二抗,孵育45 min,DAB显色,苏木精对比染色,中性树胶封固。由于本实验室前期研究显示Tiam1蛋白在卵巢癌组织中呈阳性[7],因此选择Tiam1蛋白强阳性染色的切片作为阳性对照,以PBS代替一抗的染色结果作为阴性对照。
1.4判断标准根据Beesley分级法,以细胞质和细胞核中出现棕褐色颗粒的比例作为判定Tiam1蛋白阳性染色的标准。根据细胞染色强度判断:无着色为0分,淡黄色为1分,棕黄色为2分,棕褐色为3分;根据阳性细胞数判断:≤5%为0分,6%~25%为1分,26%~50%为2分,51%~75%为3分,>75%为4分。将两项结果相乘:0分为(-),1~4分为(+),5~8分为(),9~12分为()。以“-”为阴性,“+”为阳性,“~”为强阳性。
1.5统计学方法应用统计学软件SPSS 17.0进行统计学分析,采用χ2检验或Fisher精确检验法进行病理分析,运用Kaplan-Meier进行生存分析。P<0.05为差异有统计学意义。
2 结果
2.1Tiam1蛋白在卵巢病变组织中的表达Tiam1在卵巢良性病变组织中呈低表达;在卵巢癌组织中呈强阳性且主要表达于细胞质和细胞核中。卵巢浆液性癌中Tiam1蛋白的阳性率和强阳性率分别为84.7%(83/98)和70.4%(69/98);黏液性囊腺癌中Tiam1蛋白的阳性率和强阳性率分别为87.5%(56/64)和73.4%(47/64);卵巢良性病变中Tiam1蛋白的阳性率和强阳性率分别为22.2%(6/27)和7.4%(2/27)。卵巢浆液性癌和黏液性囊腺癌组织中Tiam1蛋白的阳性率和强阳性率显著高于卵巢良性病变组织,差异均有显著性(P<0.01,表1,图1)。
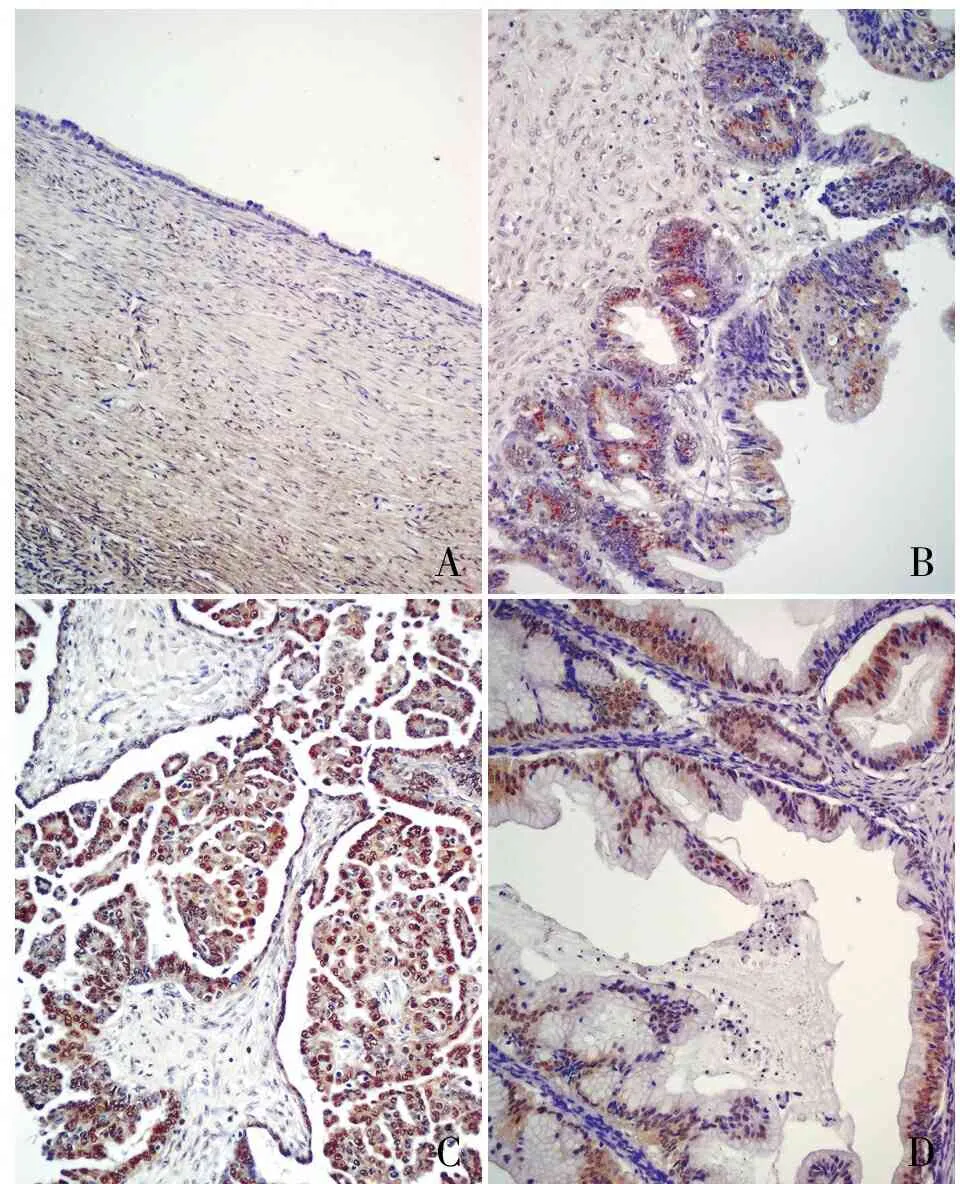
ABCD
图1Tiam1在卵巢病变组织中的表达,SP两步法:A.Tiam1蛋白在卵巢良性病变组织中呈阴性;B.Tiam1蛋白在交界性肿瘤中呈阳性;C.Tiam1蛋白在浆液性卵巢癌中呈强阳性,主要表达于细胞质和细胞核;D.Tiam1蛋白在黏液性囊腺癌中呈强阳性
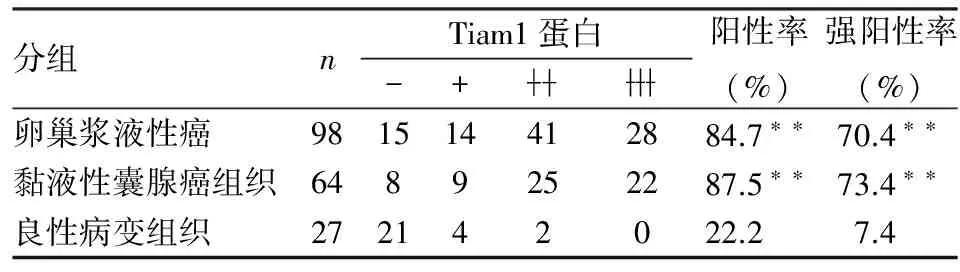
表1 Tiam1蛋白在卵巢病变组织中的表达
**P<0.01
2.2Tiam1蛋白过表达与卵巢癌临床病理特征的关系为了解Tiam1蛋白在卵巢癌发生、发展中的作用,我们对其过表达与卵巢癌临床病理特征的关系进行分析发现,Tiam1蛋白的表达水平与卵巢癌患者年龄及绝经情况无关,但与组织学分级、FIGO分期和转移情况密切相关(P均<0.05)。其中,Tiam1蛋白在低分化组织中的强阳性率(78.4%)明显高于高分化组织(52.1%)和中分化组织(76.6%,P=0.006);Tiam1蛋白在晚期(III+IV)组织中的强阳性率(77.0%)明显高于早期(Ⅰ+Ⅱ)组织(62.7%,P=0.019);在有转移的组织中其强阳性率(79.2%)明显高于无转移的组织(55.4%,P=0.001,表2)。
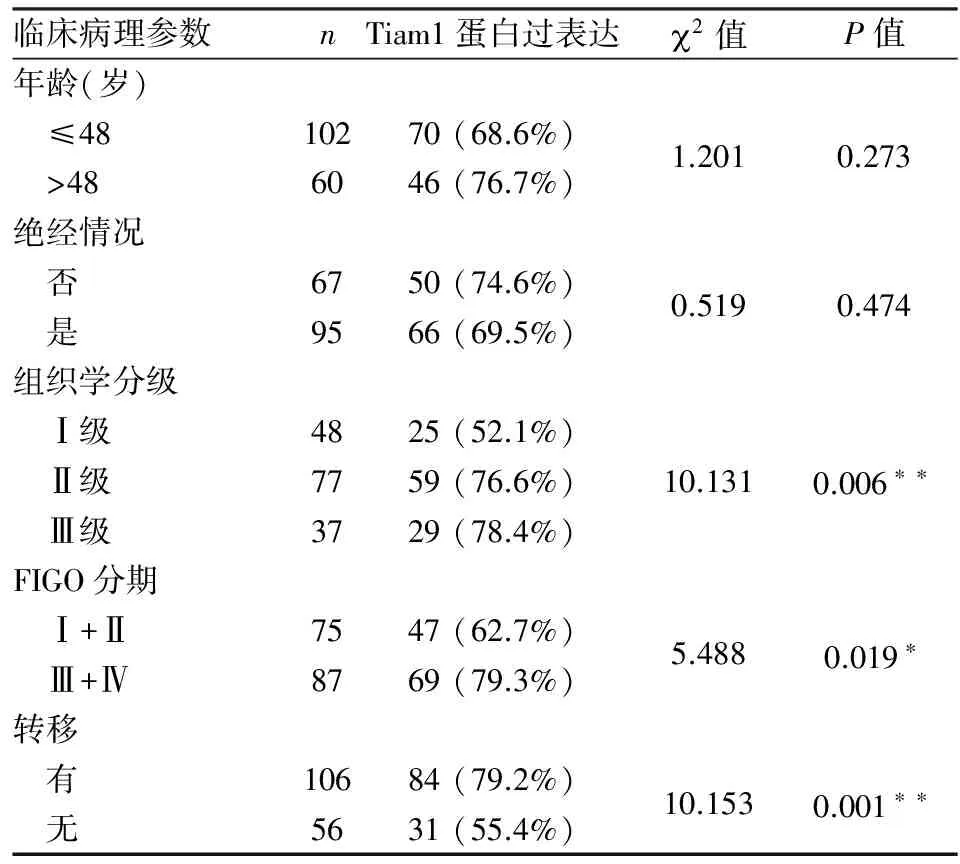
表2 Tiam1蛋白过表达与卵巢癌临床病理特征的关系
*P<0.05,**P<0.01
2.3生存分析Kaplan-Meier生存分析显示,Tiam1对卵巢癌患者生存期有显著影响。Tiam1蛋白高表达的卵巢癌患者的总生存期和无瘤生存期均明显低于Tiam1蛋白低表达者(Log-rank分别为4.850和4.488,P值分别为0.028和0.034,图2)。Tiam1蛋白高表达的转移性卵巢癌患者总生存期也明显低于Tiam1蛋白低表达患者(Log-rank=7.968,P=0.006,图3)。
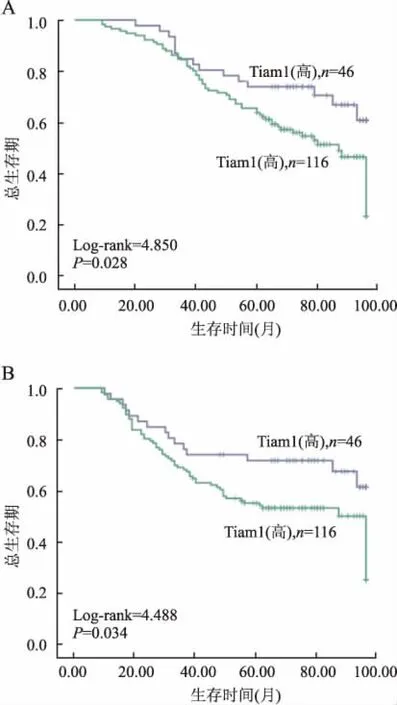
图2 Tiam1表达与卵巢癌患者预后的Kaplan-Meier生存曲线
A. Tiam1表达与总生存期之间的关系;B.Tiam1表达与无瘤生存期之间的关系
3 讨论
卵巢癌是全球高发的妇科恶性肿瘤之一。由于缺乏对卵巢癌的有效早期诊断以及分子治疗靶点的识别,近30年来卵巢癌患者的5年生存率较低。目前,临床上用于诊断卵巢癌的标志物主要为上皮来源标志物,如CA125和人附睾蛋白4(HE4)。CA125是来源于胚胎发育期体腔上皮并可与单克隆抗体OC125结合的糖蛋白,该蛋白主要见于上皮源性卵巢肿瘤患者的血清中,但因其诊断特异性差,所以未用于卵巢癌的筛查。HE4来源于附睾上皮的分泌型糖蛋白。该蛋白在正常组织和良性肿瘤中呈低表达或不表达,在卵巢癌和子宫内膜癌中呈高表达。HE4与CA125相比,其在卵巢良恶性肿瘤的鉴别中具有较大的优势,但一般仅用于卵巢癌患者的治疗监测。因此,发现更为有效的卵巢癌早期诊断以及预后评估分子标志物至关重要。
Tiam1最早于1994年由荷兰癌症研究发现,它可以促使Racl由失活状态转变为激活状态,进而参与调控细胞骨架重组、细胞迁移、细胞浸润及增强细胞能动性等过程[11-13]。Michiels等[14]研究显示,Tiam1-Rac信号轴参与肿瘤细胞的浸润与转移;而Tiam1-Rac信号轴还可调控其他信号通路,如c-Jun氨基末端激酶通路(p38 MAPK)和细胞外信号调节的激酶通路,提示Tiam1-Rac信号通路参与基因的转录过程中。另外,作为鸟嘌呤核苷酸交换因子,Tiam1蛋白已被证明在一定范围内可以通过调节Rho GTP酶参与肿瘤的信号转导[15],进而抑制肿瘤的发生、发展及转移[11,16]。因此,Tiam1表达/功能的改变可能会促进肿瘤发生、发展。
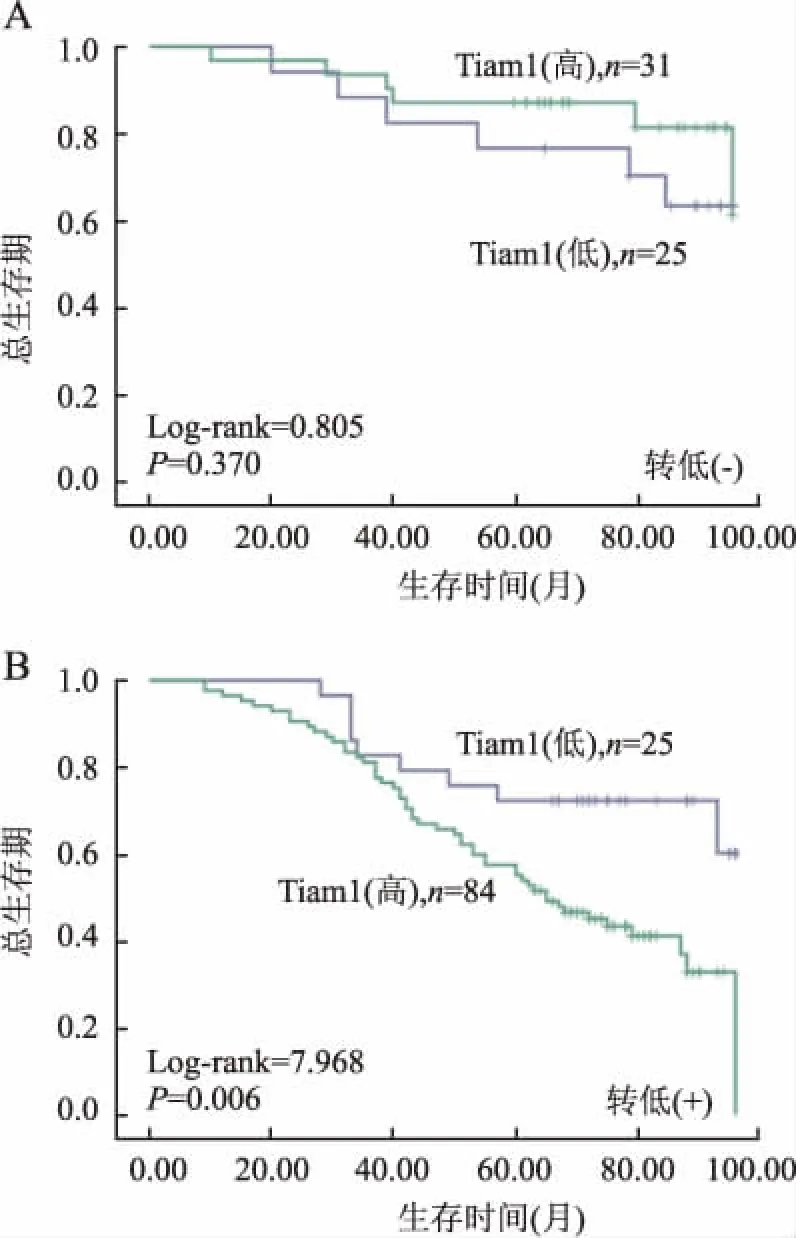
图3 Tiam1表达与卵巢癌有无转移患者预后的Kaplan-Meier生存曲线
A.Tiam1表达与卵巢癌无转移患者总生存期之间的关系;B.Tiam1表达与卵巢癌转移患者总生存期之间的关系
近年多项研究致力于Tiam1蛋白在肿瘤进展和转移过程中的调控机制。Liu等[15]报道Tiam1蛋白在肺癌中呈高表达,进一步分析发现Tiam1高表达与肺癌的转移密切相关。Yu等[13]研究证实,Tiam1蛋白在结直肠癌组织中呈显著的高表达且与肿瘤的转移密切相关,而将Tiam1基因沉默后则显著抑制结直肠癌细胞的增殖和转移能力。目前,Tiam1蛋白在卵巢癌中的作用尚未阐明。本组采用免疫组化SP两步法染色明确Tiam1蛋白在卵巢癌中的表达,其主要定位于细胞质和细胞核。与卵巢良性病变组织相比,Tiam1蛋白在卵巢癌呈阳性或强阳性(P均<0.01)。与Li等[17]的研究结果一致,其报道显示Tiam1在原发性和转移性卵巢癌组织中的表达显著高于正常卵巢组织。提示Tiam1蛋白高表达与卵巢癌的恶性程度密切相关。进一步分析Tiam1蛋白过表达与卵巢癌临床病理特征的关系发现,Tiam1蛋白在晚期卵巢癌组织中的强阳性率显著高于早期卵巢癌。此外,Tiam1蛋白的高表达与卵巢癌的转移密切相关,提示Tiam1蛋白在卵巢癌的进展过程中发挥重要作用。相同的是,与高分化的卵巢癌相比,低分化卵巢癌的Tiam1强阳性率亦显著升高。以上均提示Tiam1蛋白的表达可能在卵巢癌的发生、发展中发挥重要作用。作为肿瘤转移诱导的关键基因,Tiam1蛋白在恶性肿瘤中高表达的分子机制有待于进一步分析。
许多研究表明,Tiam1可初步预测胃腺癌[18]、鼻咽癌[6]和食管癌[19]等多种肿瘤的预后,即Tiam1蛋白高表达患者生存期短、预后差。Ding等[20]研究显示Tiam1高表达是肝癌预后的评估指标之一;Li等[9]通过免疫组化染色发现,Tiam1高表达是影响乳腺癌患者不良预后的独立风险因素,可作为患者预后的重要辅助指标。本组运用Log-rank分析法发现Tiam1蛋白高表达与卵巢癌患者的总生存期及无瘤生存期密切相关,即Tiam1蛋白高表达的患者生存时间明显少于低表达的患者。进一步分析生存期显示,与无转移的卵巢癌患者相比,Tiam1蛋白高表达的转移性卵巢癌患者的总生存期明显缩短,提示Tiam1蛋白高表达可成为卵巢癌患者不良预后的重要分子指标。
综上所述,Tiam1参与卵巢癌的演进过程,在卵巢癌的转移、侵袭中起着非常重要的作用,对于判断卵巢癌的进展及预后具有重要的临床价值,Tiam1的表达水平有望成为卵巢癌预后不良的有效监测指标。但Tiam1在恶性肿瘤中高表达的具体机制和途径尚不清楚,有待进一步的分子生物学研究证实。
[1] Siegel R, Ma J, Zou Z,etal. Cancer statistics, 2014[J]. CA Cancer J Clin, 2014,64(1):9-29.
[2] 徐 明,杨 洋,车拴龙,等. NQO1过表达在卵巢黏液性囊腺癌预后评估中的意义[J]. 中国病理生理杂志, 2016,32(8):1461-1465.
[3] Habets G G, Scholtes E H, Zuydgeest D,etal. Identification of an invasion-inducing gene, Tiam-1, that encodes a protein with homology to GDP-GTP exchangers for Rho-like proteins[J]. Cell, 1994, 77(4):537-549.
[4] Cvitkovic E, Bachouchi M, Boussen H,etal. Leukemoid reaction, bone marrow invasion, fever of unknown origin, and metastatic pattern in the natural history of advanced undifferentiated carcinoma of nasopharyngeal type: a review of 255 consecutive cases[J]. J Clin Oncol, 1993,11(12):2434-2442.
[5] Engers R, Mueller M, Walter A,etal. Prognostic relevance of Tiam1 protein expression in prostate carcinomas[J]. Br J Cancer, 2006,95(8):1081-1086.
[6] Qi Y, Huang B, Yu L,etal. Prognostic value of Tiam1 and Rac1 overexpression in nasopharyngeal carcinoma[J]. ORLJ Otorhinolaryngol Relat Spec, 2009,71(3):163-171.
[7] Otsuki Y, Tanaka M, Kamo T,etal. Guanine nucleotide exchange factor, Tiam1, directly binds to c-Myc and interferes with c-Myc-mediated apoptosis in rat-1 fibroblasts[J]. J Biol Chem, 2003, 278(7):5132-5140.
[8] Bourguignon L Y, Zhu H, Shao L,etal. Ankyrin-Tiam1 interaction promotes Rac1 signaling and metastatic breast tumor cell invasion and migration[J]. J Cell Biol, 2000,150(1):177-191.
[9] Li Z, Liu Q, Piao J,etal. Clinicopathological implications of Tiam1 overexpression in invasive ductal carcinoma of the breast[J]. BMC Cancer, 2016,16(1):681.
[10] Li H, Cui X, Chen D,etal. Clinical implication of Tiam1 overexpression in the prognosis of patients with serous ovarian carcinoma[J]. Oncol Lett, 2016,12(5):3492-3498.
[11] Mertens A E, Roovers R C, Coilard J G. Regulation of Tiaml-Rac signalling[J]. FEBS Lett, 2003, 546(1):11-16.
[12] Bourguignon L Y, Zhu H, Shao L,etal. Ankyrin-Tiaml interaetion promotes Racl signaling and metastaticbreast tumor cell invasion and migration[J]. J Cell Biol, 2000,150(1):177-191.
[13] Yu L N, Zhang Q L, Li X,etal. Tiaml transgenic mice display increased tumor invasive and metastatic potential of colorectal cancer after 1,2-dimethylhydrazine treatment[J]. PLoS One, 2013,8(9):e73077.
[14] Michiels F, Habets G G, Stam J C,etal. A role for Rac in Tiam1-induced membrane ruffling and invasion[J]. Nature, 1995,375(6529):338-340.
[15] Liu S, Li Y, Qi W,etal. Expression of Tiam1 predicts lymph node metastasis and poor survival of lung adenocarcinoma patients[J]. Diagn Pathol, 2014,9:69.
[16] Minard M E, Kim L S, Price J E,etal. The role of the guanine nucleotide exchange factor Tiam1 in cellular migration, invasion, adhesion and tumor progression[J]. Breast Cancer Res Treat, 2004,84(1):21-32.
[17] Li J, Liang S, Jin H,etal. Tiam1, negatively regulated by miR-22, miR-183 and miR-31, is involved in migration, invasion and viability of ovarian cancer cells[J]. Oncol Rep, 2012,27(6):1835-1842.
[18] 张 源,杨 洋,车拴龙,等. 胃腺癌预后评估中Tiaml蛋白过表达的意义[J]. 临床与实验病理学杂志, 2016, 32(2):128-130,135.
[19] Wu Q Y, Wang Y, Tong J C,etal. Expression and clinical significance of Tiam1 gene in esophageal carcinoma[J]. Int J Clin Exp Med, 2015,8(11):21229-21234.
[20] Ding Y, Chen B, Wang S,etal. Overexpression of Tiam1 in hepatocellular carcinomas predicts poor prognosis of HCC patients[J]. Int J Cancer, 2009,124 (3):653-658.
ClinicalimplicationofTiam1proteinoverexpressioninovariancarcinoma
YANG Yang, SUN Jie, ZHU Guang, PIAO Jun-jie, LIN Zhen-hua
(DepartmentofPathology,YanbianUniversityMedicalCollege,Yanji133002,China)
PurposeTo investigate the clinicopathological significance of Tiam1 overexpression in ovarian carcinoma.MethodsTiam1 protein was detected in 98 serous carcinomas, 64 ovarian mucinous cystadenocarcinomas and 27 benign ovarian tumors using immunohistochemical of SP two-step staining. Correlations between Tiam1 overexpression and clinicopathological features of ovarian carcinoma were evaluated. Overall survival and disease-free survival rates of ovarian carcinoma patients were calculated by Kaplan-Meier method.ResultsTiam1 protein showed a cytoplasmic and nuclear staining pattern in ovarian carcinoma. The positive rate and strongly positive rate of Tiam1 protein were 84.7% (83/98) and 70.4% (69/98) in serous carcinoma, the positive rate and strongly positive rate of Tiam1 protein were 87.5% (56/64) and 73.4% (47/64) in ovarian mucinous cystadenocarcinoma, both of which were significantly higher than those in benign ovarian tumor (bothP<0.01). High-level expression of Tiam1 was positively correlated with the histological grade, FIGO stage, and metastasis in ovarian carcinoma (bothP<0.05), while independent of age and menopausal status (bothP>0.05). Kaplan-Meier survival analysis showed that overall survival and disease-free survival of ovarian cancer patients with high expression of Tiam1 protein were significantly lower than those of patients with lower expression of Tiam1 protein (P<0.05), overall survival in metastatic ovarian cancer patients with high expression of Tiam1 protein was significantly lower than those in patients with low Tiam1 protein expression (P<0.05).ConclusionTiam1 expression is significantly high in ovarian carcinoma. Tiam1 protein is closely associated with ovarian carcinoma progression, which may be a new potential prognostic biomarker and a therapeutic target for ovarian carcinoma.
ovarian neoplasm;Tiam1;immunohistochemistry; prognosis; survival analysis
时间:2017-9-18 6:23 网络出版地址:http://kns.cnki.net/kcms/detail/34.1073.R.20170918.0623.001.html
R 737.31
A
1001-7399(2017)09-0945-05
10.13315/j.cnki.cjcep.2017.09.001
接受日期:2017-07-25
国家自然科学基金(61371067)
延边大学医学院病理学教研室,延吉 133002
杨 洋,女,博士研究生。E-mail: 313828301@qq.com
林贞花,女,教授,博士生导师,通讯作者。Tel:(0433)2435056,E-mail: zhlin720@ybu.edu.cn
