康艾注射液在淋巴造血系统肿瘤患者治疗中价值的Meta分析
2017-11-16凌春徐士云牛小伟达晓静
凌春++徐士云+牛小伟++达晓静


[摘要] 目的 評价康艾注射液在淋巴造血系统肿瘤患者治疗中的价值。 方法 计算机检索PubMed、Embase、Web of Science、CENTRAL、中国生物医学数据库、维普、中国知网和万方数据库,检索时限从建库至2017年1月,纳入KA联合常规方案治疗淋巴造血系统肿瘤的随机对照试验,采用RevMan 5.1软件进行Meta分析。 结果 共纳入10项随机对照试验,包括619例患者。与对照组相比,康艾注射液能提高临床疗效[RR=1.17,95%CI(1.04,1.32),P=0.008],改善患者的生活质量[RR=1.79,95%CI(1.42,2.24),P < 0.001],同时能降低化疗引起的不良反应如白细胞减少[RR=0.48,95% CI(0.33,0.70),P < 0.001]、血小板减少[RR=0.39,95% CI(0.20,0.75),P=0.005]、贫血[RR=0.59,95%CI(0.36,0.98),P=0.04],及胃肠道不良反应的发生率[RR=0.63,95% CI(0.53,0.74),P < 0.001]。 结论 康艾注射液联合常规化疗方案能提高淋巴造血系统肿瘤患者的治疗有效性、生活质量,并降低骨髓抑制率、消化道不良反应的发生率。
[关键词] 康艾注射液;淋巴造血系统肿瘤;Meta分析
[中图分类号] R73 [文献标识码] A [文章编号] 1673-7210(2017)10(b)-0098-05
A Meta-analysis of the value of Kang′ai Injection in treating patients with tumor of lymphoid hematopoietic system
LING Chun1 XU Shiyun1▲ NIU Xiaowei2 DA Xiaojing3
1.Department of Hematology, the First People′s Hospital of Chuzhou, Anhui Province, Chuzhou 239000, China; 2.Department of Cardiology, the First Hospital of Lanzhou University, Gansu Province, Lanzhou 730000, China; 3.Department of Hematology, the First Hospital of Lanzhou University, Gansu Province, Lanzhou 730000, China
[Abstract] Objective To assess the value of Kang′ai Injection for patients with tumor of lymphoid hematopoietic system. Methods The following databases such as PubMed, Embase, Web of Science, CENTRAL, CBM, VIP, CNKI, Wanfang Data were retrieved from the time of the database established to January 2017. Randomized controlled clinical trials (RCTs) that Kang′ai Injection combined with routine therapy in the treatment of tumor of lymphoid hematopoietic system were included. Meta-analysis was conducted by RevMan 5.1 software. Results 10 randomized trials involved 619 patients were included. In the Kang′ai Injection group, the clinical effects [RR=1.17, 95%CI (1.04, 1.32), P=0.008], living quality [RR=1.79, 95%CI (1.42, 2.24), P < 0.001] were increased, and adverse events such as hypoleukia [RR=0.48, 95%CI (0.33, 0.70), P < 0.001], thrombocytopenia [RR=0.39, 95%CI (0.20, 0.75), P=0.005], anemia [RR=0.59, 95%CI (0.36, 0.98), P=0.04] and gastrointestinal side effects [RR=0.63, 95%CI (0.53, 0.74), P < 0.001] were decreased, compared with control group. Conclusion The combination of Kang′ai Injection combined with conventional chemotherapy can improve the efficacy and quality of treatment of patients with tumor of lymphoid hematopoietic system, and reduce the incidence of bone marrow rejection rate and digestive tract adverse reactions.endprint
[Key words] Kang′ai Injection; Tumor of lymphoid hematopoietic system; Meta-analysis
淋巴造血系统肿瘤是严重影响人类健康的疾病[1]。化疗是淋巴造血系统肿瘤目前的主要治疗手段之一,但由于化疗的毒副作用较大,部分患者难以顺利完成整个治疗过程,且化疗还会对患者生活质量产生影响[1]。中成药用于恶性肿瘤的辅助治疗,已越来越受到人们的重视。康艾注射液(Kang′ai Injection,KA)主要成分为黄芪、人参、苦参素,具有益气扶正、增强机体免疫力的功效,亦有促进造血干细胞定向分化,及造血集落因子表达的作用。目前已有多项评估KA作用的随机对照试验[2-11],但大多数研究样本含量少,同时这些试验的质量并没有得到全面的评价,疗效还不能完全肯定。因此,本研究拟利用Meta分析的方法,评价KA在淋巴造血系统肿瘤患者中的应用价值。
1 资料与方法
1.1 文献来源
计算机检索PubMed、Embase、Web of Science、CENTRAL、中国生物医学数据库、维普、中国知网和万方数据库,以“Kang′ai Injection”“leukemia”“lymphoma”“multiple myeloma”为英文检索词,“康艾注射液”“白血病”“淋巴瘤”“多发性骨髓瘤”为中文检索词,检索时限从建库至2017年1月。
1.2 入选标准
1.2.1 研究对象 参照文献[12],诊断为白血病、淋巴瘤、多发性骨髓瘤的患者。
1.2.2 干预措施 试验组患者采用KA联合常规治疗方案。对照组患者仅接受常规治疗方案。
1.2.3 结局指标 ①临床疗效:参照WHO评价标准[1],分为完全缓解、部分缓解、稳定和进展,有效率=(完全缓解例数+部分缓解例数)/总例数×100%。②生活质量:根据患者治疗后的卡氏评分(Karnofsky score,KPS)变化,将增加10分以上者归为改善,减少10分以上者归为减退,增加或减少10分以内者归为稳定,改善率=生活质量改善病例数/总例数×100%。③骨髓抑制作用、消化道不良反应均按WHO毒性反应分级标准进行评估[1]。
1.2.4 研究类型 随机对照试验。
1.3 排除标准
①重复文献;②无法提取数据进行合成的研究。
1.4 文献筛选和资料提取
首先通过EndNote去重后,由两名作者排除明显不符合纳入标准的研究,再阅读研究全文,确定其是否真正符合纳入标准,并对纳入文献提取及交叉核对资料。提取资料内容包括:①试验的基本情况;②两组患者的基线情况;③试验组与对照组的干预措施;④结局指标。
1.5 方法学质量评价
根据Cochrane Handbook 5.1.0版[13]推荐的“偏倚风险评估”工具对纳入研究进行方法学质量评价。
1.6 统计学方法
使用RevMan 5.1软件进行统计分析。计数资料选用相对危险度(risk ratio,RR)及其95%可信区间(confidence interval,CI)[13]。运用χ2检验进行异质性分析,检验水准α=0.1;并以I2判断异质性大小。如不存在异质性或异质性较小,采用固定效应模型合并效应量;反之,若异质性较大(I2 > 50%,P < 0.10),运用Meta回归及亚组分析探索异质性来源,如仅有统计学异质性时,采用随机效应模型合并效应量。绘制漏斗图判断发表偏倚。以双侧P < 0.05为差异有统计学意义。本次研究遵循PRISMA声明[14]。
2 结果
2.1 文献筛选流程与结果
初步检索123篇文献,通过软件及阅读文题、摘要和全文后,排除113篇,最终纳入10篇文献[2-11]。文献检索流程及结果见图1。
2.2 纳入研究的概况
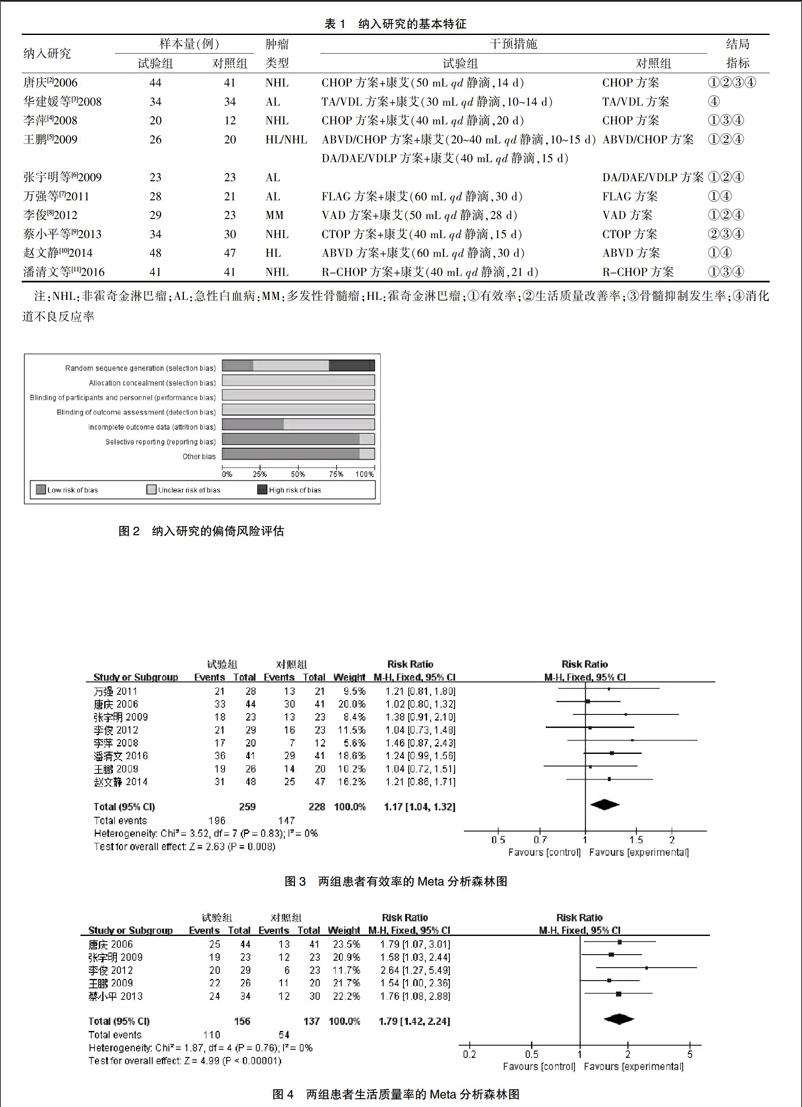
共纳入619例患者,其中327例采用了KA联合化疗,292例单用化疗。纳入研究均报告了基线资料可比,1项研究[8]是关于多发性骨髓瘤,3项研究[3,6-7]关于急性白血病,6项研究[2,4-5,9-11]关于淋巴瘤。各研究的主要特征及患者的基本资料见表1。
纳入文献中有2项研究[9,11]采用了随机数字表进行分组,2项研究按照就诊顺序进行分配。各研究的分配隐藏方案、盲法实施情况均不清楚。结果数据完整性、选择性报告结果、其他偏倚的风险较小(图2)。
2.3 Meta分析结果
2.3.1 有效率 8项研究[2,4-8,10-11]报道了两组治疗后的有效率,共487例患者。异质性检验显示各研究间无统计学异质性(P=0.83,I2=0%),采用固定效应模型进行合并。结果提示试验组的有效率高于对照组[RR=1.17,95%CI (1.04,1.32),P=0.008](图3)。
2.3.2 生活质量改善率 5项研究[2,5-6,8-9]报道了两组患者的生活质量,共293例患者。异质性检验显示各研究间无统计学异质性(P=0.76,I2=0%),采用固定效应模型进行合并。结果提示试验组的生活质量改善率高于对照组[RR=1.79,95%CI(1.42,2.24),P < 0.001]。见图4。
2.3.3 骨髓抑制发生率 4项研究[2,4,9,11]报道了Ⅱ度及以上白细胞减少发生率,共263例患者,异质性检验显示各研究间存在轻度异质性(P=0.21,I2=34%),采用固定效应模型进行合并。结果提示试验组的白细胞减少发生率低于对照组[RR=0.48,95%CI(0.33,0.70),P < 0.001]。2项研究[4,9]报道了Ⅱ度及以上血小板减少发生率,共96例患者,异质性检验显示各研究间无统计学异质性(P=0.66,I2=0%),采用固定效應模型进行合并。结果提示试验组的血小板减少发生率低于对照组[RR=0.39,95%CI(0.20,0.75),P=0.005]。3项研究[2,4,9]报道了Ⅱ度及以上贫血发生率,共181例患者,异质性检验显示各研究间无统计学异质性(P=0.82,I2=0%),采固定效应模型进行合并。结果提示试验组的贫血发生率低于对照组[RR=0.59,95%CI(0.36, 0.98),P=0.04]。见图5。endprint
2.3.4 胃肠道不良反应发生率 10项研究[2-11]报告了胃肠道不良反应发生率,共573例患者,异质性检验显示各研究间存在轻度异质性(P=0.15,I2=34%),采用固定效应模型进行合并。结果提示试验组的胃肠道不良反应发生率低于对照组[RR=0.63,95%CI(0.53, 0.74),P < 0.001]。见图6。
2.3.5 漏斗图分析 对纳入文献进行漏斗图分析,结果提示发表偏倚较小。见图7。
3 讨论
本研究在全面检索中英文数据库的基础上,共纳入10项RCT,包括619例患者。Meta分析结果显示,KA联合常规化疗方案能提高淋巴造血系统肿瘤患者的治疗有效性、生活质量,并降低骨髓抑制率、消化道不良反应率。
联合中药制剂增强化疗方案的临床疗效、降低化疗药物的毒副作用,一直是研究的热点问题。KA主要成分为黄芪、人参、苦参素,其抗肿瘤的主要作用机制有:黄芪能增加T细胞亚群以及NK细胞活性,提高免疫功能[15-16];人参可以调控造血微环境,诱导造血干细胞定向分化[17-18];苦参碱对肿瘤细胞诱导的血管内皮细胞增生具有抑制作用[19-20]。这些成分的合用可产生多靶点治疗的效果,既抑制癌细胞增殖,促进分化、凋亡,又通过增强免疫功能延长患者的生命,并改善生存质量。既往研究表明,KA能提高肝癌、肺癌、结直肠癌患者的治疗有效率、生存质量;并减少恶心、呕吐、白细胞减少、血小板降低的发生率[21]。但对于淋巴造血系统肿瘤的Meta分析尚未见报道。
本研究结果提示在常规化疗方案的基础上,联合KA能提高淋巴造血系统肿瘤患者的临床疗效,降低骨髓抑制率、消化道不良反应率,从而改善生活质量。这为KA在淋巴造血系统肿瘤患者中的临床应用提供了循证医学证据,有望使治疗方案进一步优化。但由于对结局指标的评价均停留在较短的随访期,KA对于改善患者长期预后的作用,尚有待进一步研究。另外,本次Meta分析中纳入文献的质量整体偏低,未来开展的研究应注意遵循国际通用的“随机对照试验报告标准”,详尽描述研究的设计和实施过程,提高研究质量。
综上所述,KA联合常规化疗方案能提高淋巴造血系统肿瘤患者的治疗有效性、生活质量,并降低骨髓抑制率、消化道不良反应的发生率。未来高质量的随机对照试验应进一步确定KA的临床应用价值。
[参考文献]
[1] 孙燕.内科肿瘤学[M].北京:人民卫生出版社,2003.
[2] 唐庆.康艾注射液对非霍奇金淋巴瘤患者血清VEGF水平的影响[J].白血病·淋巴瘤,2006,15(1):30-31.
[3] 华建媛,贺文凤,张凌.康艾注射液联合化疗治疗急性白血病60例[J].肿瘤研究与临床,2008,20(12):838-839.
[4] 李萍.康艾注射液联合CHOP方案治疗非霍奇金淋巴瘤的临床观察[J].中华肿瘤防治杂志,2008,15(22):1751-1752.
[5] 王鹏.康艾注射液联合化疗治疗恶性淋巴瘤的临床观察[J].中国中医药现代远程教育,2009,7(6):25-26.
[6] 张宇明,熊丹,李庆华,等.康艾注射液协同化疗治疗急性白血病[J].中华全科医学,2009,7(7):693-694.
[7] 万强,郗爱华,张丑丑,等.康艾注射液联合FLAG方案治疗复发性、难治性急性髓性白血病的临床研究[J].中国中药杂志,2011,36(22):3207-3209.
[8] 李俊.康艾注射液联合改良VAD方案治疗多发性骨髓瘤临床疗效观察[J].中国现代医生,2012,50(21):66-67.
[9] 蔡小平,郑翠苹,石岳坚.康艾注射液在辅助非霍奇金淋巴瘤化疗中的作用观察[J].中国药房,2013,24(31):2959-2961.
[10] 赵文静.康艾注射液联合化疗治疗恶性淋巴癌的临床探讨[J].中国卫生标准管理,2014,5(5):1-2.
[11] 潘清文,陈哲,罗俭权,等.康艾注射液联合美罗华治疗恶性淋巴瘤的临床疗效及安全性研究[J].国际医药卫生导报,2016,22(21):3245-3247.
[12] 中华医学会.临床诊疗指南:血液学分册[M].北京:人民卫生出版社,2008.
[13] Higgins Jp T,Green S. Cochrane handbook for systematic reviews of interventions. Version 5.1.0 [J]. Cochrane Data?鄄base of Systematic Reviews,2008,5(2):S38.
[14] 張珺,葛龙,赵晔,等. PRISMA系列报告规范简介[J].中国药物评价,2015,(5):257-261.
[15] 吴宝明,李俊.黄芪多糖在免疫调节中的作用[J].安徽医药,2008,12(7):577-579.
[16] 孙政华,邵晶,郭玫,等.黄芪化学成分及药理作用研究进展[J].中医临床研究,2015(25):22-25.
[17] 王欣,麻柔.人参单药及其组分对造血影响的基础研究与临床应用[J].中国中西医结合杂志,2006,26(12):1139-1141.
[18] 杨武韬.人参的化学成分和药理研究进展[J].中国医药指南,2014(3):33-34.
[19] 郭林丰,童姗姗,余江南,等.苦参碱抗肿瘤作用机制研究进展[J].中国中药杂志,2013,38(20):3409-3412.
[20] 彭艳,官成浓.苦参碱类生物碱在鼻咽癌治疗中的作用[J].中国医药导报,2016,13(33):68-71.
[21] 赵燕林,薛育东,刘芬.康艾注射液联合全身化疗治疗中、晚期恶性肿瘤的近期疗效及安全性的Meta分析[J].中华临床医师杂志:电子版,2013,7(22):10192-10196.
(收稿日期:2017-06-16 本文编辑:李岳泽)endprint
