国产SM160H高通量透析器有效性和安全性验证临床试验
2017-11-10罗来敏
罗来敏, 杨 柳, 鄢 杰
国产SM160H高通量透析器有效性和安全性验证临床试验
罗来敏1, 杨 柳1, 鄢 杰2
肾透析; 砜类; 透析仪器和设备
中空纤维型透析器是目前全世界广泛使用的主流透析器,透析膜是决定其性能的最关键组成部分。从纤维素膜、铜仿膜、醋酸纤维素膜到现在广泛使用的合成膜,透析膜的发展经历了多次更新换代。对水和溶质的高清除率以及良好的生物相容性是判断透析器性能的主要指标,聚醚砜膜透析器是目前临床上使用的性能最好的合成膜透析器之一[1-2]。我国目前使用的聚醚砜膜高通量透析器大部分依赖进口,国内仅有少数几家企业能够生产。三鑫医疗科技股份有限公司生产的SM160H聚醚砜膜高通量透析器尚未上市销售,为验证其在血液透析患者中使用的有效性和安全性,经国家食品药品监督管理局批准进行以下多中心临床试验,报道如下。
1 临床资料
1.1一般资料 采用多中心、完全随机、平行对照设计,样本量按非劣性检验计算需224例,考虑到脱落率后确定为250例。选取4家三级甲等医院血液透析中心为试验参加单位,样本量分配其中3个中心各70例(试验组和对照组各35例),1个中心40例(试验组和对照组各20例)。250例按1∶1比例随机进入SM160H组和B-16H组,其中SM160H组125例,男性80例,女性45例,年龄
(53.6±13.5)岁(21~75岁);B-16H组125例,男性84例,女性41例,年龄(54.8±14.5)岁(20~75岁)。本试验通过各参加单位伦理委员会审查并批准,所有受试者入组前均签署知情同意书。
入选标准:(1)规律血液透析>3月的慢性肾功能衰竭患者;(2)年龄18~75岁、病情平稳、性别不限;(3)自愿参加本临床试验,并签署知情同意书。排除标准:(1)急、慢性感染者;(2)严重心、肺、肝功能不全者;(3)严重贫血者(血红蛋白<60 g/L);(4)有聚醚砜材料过敏史;(5)急性脑血管意外的患者;(6)精神障碍者;(7)孕妇及哺乳期妇女;(8)过敏体质患者;(9)同时使用其他血液净化法并对试验的评价有影响的患者;(10)3月内参加过其他临床试验者;(11)研究者认为不宜参加本临床试验者。
1.2方法
1.2.1透析器 SM160H组和B-16H组受试者均进行一次透析治疗,前者使用SM160H透析器(批号:20130606,江西三鑫医疗科技股份有限公司),后者使用B-16H透析器(批号:1401031030,广州贝恩医疗设备有限公司),该透析器采用德国Membrana公司生产的新一代聚醚砜膜,是目前市场上使用的主流透析器,2种透析器的相关参数基本一致(表1)。

表1 2种透析器参数
1 mmHg=133.3 Pa.
1.2.2血液透析治疗方案 所有受试者均为规律透析患者,每周3次,每次4 h,均使用动静脉内瘘作为血管通路。试验中使用低分子肝素钙抗凝,血流量250 mL/min,透析液流量500 mL/min,血透机(4008S,德国费森尤斯公司)。
1.2.3评价方法 按国家食品药品监督管理局2013年1月4日发布的《一次性使用透析器产品注册技术审查指导原则》规定[3],主要有效评价指标为:透析器的肌酐(serum creatinine, Scr)、尿素氮(blood urea nitrogen, BUN)清除率及β2-微球蛋白(β2-microglobulin, β2-MG)下降率;次要评价指标为:整体Scr、BUN下降率及β2-MG清除率等;其他评价指标包括:血常规、血生化、血气分析、C反应蛋白(C-reactive protein, CRP)、超滤率、不良事件、严重不良事件等。
1.2.4透析器溶质清除率和下降率的计算 (1)透析器溶质清除率检测:透析开始后60 min,固定工作状态下血流量和透析液流量不变,设置超滤率为0,10 s后分别于透析器血液侧入口、出口处采血测定BUN、Scr、磷酸盐及β2-MG。(2)透析器溶质下降率检测:在透析开始和结束时采血,停止超滤,血流量先减至100 mL/min,停泵15 s后于透析器血液侧入口处采血,查BUN、SCr、磷及β2-MG。清除率和下降率按照国家食品药品监督总局发布的《一次性使用透析器产品注册技术审查指导原则》规定的公式进行计算[3]。
1.2.5安全性评价 通过检测透析前后和透析过程中的血常规、生化、血气分析、CRP的变化并观察试验过程中发生的不良事件、严重不良事件评价透析器的安全性。
1.3统计学处理 采用SPSS 12.0统计软件进行统计分析。统计推断采用双侧检验,具有统计意义的检验水准定为0.05,参数的可信区间估计采用95%可信区间。
1.4结果 入组250例中,脱落剔除16例,包括因不良事件未完成试验6例,随机后撤回知情同意2例,因不符合入选标准剔除8例。2组患者的年龄、性别、血流量、透析液流量、超滤率等差别均无统计学意义,所有病例均未发生透析器凝血及破膜现象。2组透析器的有效性及安全性比较见表2~4。2组受试者各发生不良事件3例,其中SM160H组发生腹痛2例、恶心1例;B-16H组发生腹痛、呕吐、低血压各1例;不良事件发生率2.4%,经对症处理后均恢复,未发生严重不良事件。
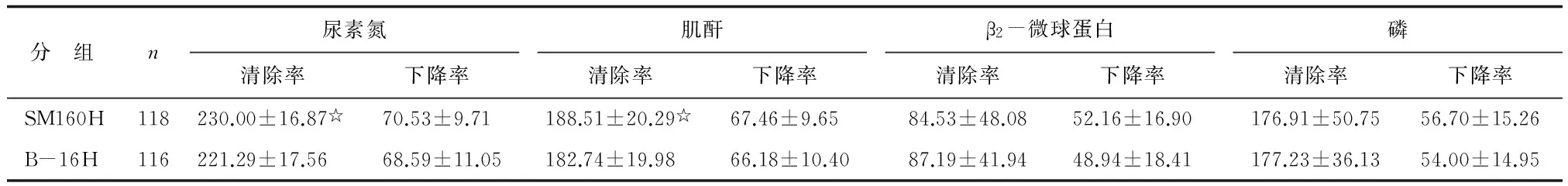
表2 2组透析器溶质清除率和下降率的比较
清除率:单位为mL/min;下降率:单位为%. 与B-16H组比较,☆:P<0.05.

表3 2组透析器安全性比较
透析前n=124,透析后n=122.

表4 2组C反应蛋白比较
表中数据为n.
2 讨 论
随机对照研究证实,以BUN为代表的小分子溶质的清除与患者死亡率有明显的相关性[4]。单次血液透析的尿素清除指数(Kt/V,其中K为尿素清除率,t为有效透析时间,V为尿素分布容积)>1.2或尿素下降率>65%能有效改善患者的预后[5]。维持性透析患者的t值和V值相对固定,所以透析器性能的评价中通常以BUN及Scr这类小分子毒素的K值和尿素下降率(urea reduction ratio, URR)来衡量其有效性,通常认为高通透析器BUN清除率为185~192 mL/min,Scr清除率为172~180 mL/min[6]。本研究结果显示,SM160H组BUN和Scr清除率略高于B-16H组(P<0.05),下降率2组差别无统计学意义。说明2种透析器对各类小分子毒素都有良好的清除能力,达到了高通透析器对小分子毒素清除能力的要求。
终末期肾病(end stage renal disease, ESRD)患者的死亡率明显高于非ESRD患者[7],其原因和β2-MG、甲状旁腺激素、晚期糖基化终末产物等中、大分子毒素有关[8],β2-MG作为中、大分子毒素的代表,其在维持性血透患者中的血清水平和血透的清除量与血透患者的死亡率和预后有明显的相关性[9]。高通透析器能增加中、大分子毒素的清除,改善预后,美国肾脏病基金会血液透析充分性指南2015年更新版中再次推荐使用高通量透析器[4]。一般认为,高通量透析器的超滤系数要求>15 mL/h/mmHg,对β2-MG的清除率>20 mL/min[8]。本研究SM160H组和B-16H组透析器的超滤系数及β2-MG清除率、下降率均在要求的范围内,表明这2种透析器都能有效清除患者体内的β2-MG。
透析器的生物相容性主要与透析膜的材料相关,是评价透析器安全性的重要方面。血液与透析膜接触激活血细胞、凝血系统、炎症因子和补体等引发多种生物学反应,被称为血-膜反应,以聚醚砜膜为代表的合成膜能减轻血-膜反应,部分吸附和清除激活的炎症因子和补体成分,拥有更好的生物相容性[10]。本试验2组透析器均为聚醚砜膜。生物相容性可通过透析15 min白细胞、血小板计数等指标来反映[6]。本试验2组透析器在开始透析15 min均可见白细胞和血小板轻度减少,但都在正常范围内,且2组间差别无统计学意义。透析患者体内存在微炎症状态,产生的原因之一是透析膜激活循环中的单核细胞[11]。CRP能反映这种炎症状态,是透析患者心血管事件的独立预测因子[12]。本试验2组受试者组间及治疗前后CRP水平无明显变化,2组间比较差别也无统计学意义。其他安全性指标如白细胞计数、血小板计数、血红蛋白和白蛋白血透后均较血透前略有升高,考虑与透析脱水后的血液浓缩有关,血红蛋白低于正常范围与慢性肾衰患者合并肾性贫血的疾病状态有关,2组透析器均未发生透析器凝血、破膜的现象,2组各发生不良事件3次,发生率为2.4%,主要不良事件为消化道症状,组间比较差别无统计学意义,2组均未发生严重不良事件,显示2种透析器均具有良好的安全性。
与徐斌等报道的国产聚砜膜高通量透析器的相关数据比较,本研究所使用的2种聚醚砜膜高通量透析器在安全性和有效性上与之相似,且聚醚砜膜较聚砜膜拥有更好的耐热性、可加工性和稳定性,可避免因与强氧化剂接触产生自由基而给人体带来的不利影响[6,13]。
[1] Nitta K. Chronic kidney diseases-recent advances in clinical and basic research[J].ContributionstoNephrology, 2015,185:Ⅶ-Ⅺ.
[2] Brandt T, Wiese F. Physical and chemical characteristics of different polyethersulfone membranes[J].ContributionstoNephrology, 2003,138:1-12.
[3] 国家食品药品监督管理总局. 一次性使用透析器产品注册技术审查指导原则[S]. 北京:国家食品药品监督管理总局网站,2013.
[4] Foundation N K. KDOQI clinical practice guideline for hemodialysis adequacy: 2015 update[J].AmJKidneyDis, 2015,66(5):884-930.
[5] Barzegar H, Moosazadeh M, Jafari H,etal. Evaluation of dialysis adequacy in hemodialysis patients: a systematic review[J].UrologyJournal, 2016,13(4):2744-2749.
[6] 王质刚. 血液净化学[M]. 3版. 北京:北京科学技术出版社, 2010:33.
[7] Sameiro-Faria M D, Ribeiro S, Costa E,etal. Risk factors for mortality in hemodialysis patients: two-year follow-up study[J].DiseaseMarkers, 2013, 35(6):791-798.
[8] Karkar A. Modalities of hemodialysis: quality improvement[J].SaudiJournalofKidneyDiseases&TransplantationAnOfficialPublicationoftheSaudiCenterforOrganTransplantationSaudiArabia, 2012,23(6):1145-1161.
[9] Topciu-Shufta V, Miftari R, Haxhibeqiri V,etal. Association of beta-2 microglobulin with inflammation and dislipidemia in high-flux membrane hemodialysis patients[J].MedicalArchives, 2016, 70(5):348-350.
[10] Kokubo K, Kurihara Y, Kobayashi K,etal. Evaluation of the biocompatibility of dialysis membranes[J].BloodPurification, 2015,40(4):293-297.
[11] Bossola M, Sanguinetti M, Scribano D,etal. Circulating bacterial-derived DNA fragments and markers of inflammation in chronic hemodialysis patients[J].ClinicalJournaloftheAmericanSocietyofNephrologyCjasn, 2009,4(2):379-385.
[12] Adejumo O A, Okaka E I, Okwuonu C G,etal. Serum C-reactive protein levels in pre-dialysis chronic kidney disease patientsin southern Nigeria[J].GhanaMedicalJournal, 2016, 50(1):31-38.
[13] 徐 斌, 张 文, 龚德华,等. 国产高通量透析器在血液透析治疗中的有效性和安全性评估[J]. 肾脏病与透析肾移植杂志, 2012,21(6):524-529.
R459.5
B
1672-4194(2017)05-0339-03
2017-04-20
1.南昌大学 第一附属医院肾内科,南昌 330006;
2. 江西三鑫医疗科技股份有限公司 法规注册部,南昌 330002
罗来敏,男,副主任医师,医学硕士. Email: llm090626@163.com
(编辑:何佳凤)
