魔芋葡甘聚糖拓扑链对茶多酚的稳定性机理研究
2017-11-03倪永升林婉媚李源钊王林王维海张馨月林玉春杜雨吴先辉庞杰
倪永升,林婉媚,李源钊,王林,王维海,张馨月,林玉春,杜雨,吴先辉,庞杰*
1(福建农林大学 食品科学学院,福建 福州,350002) 2(宁德职业技术学院,福建 福安,355000)
魔芋葡甘聚糖拓扑链对茶多酚的稳定性机理研究
倪永升1,林婉媚1,李源钊1,王林1,王维海1,张馨月1,林玉春1,杜雨1,吴先辉2*,庞杰1*
1(福建农林大学 食品科学学院,福建 福州,350002) 2(宁德职业技术学院,福建 福安,355000)
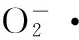
魔芋葡甘聚糖(konjac glucomannan, KGM);茶多酚(tea polyphenols, TP);直流电场;拓扑结构;抗氧化性
茶多酚(tea polyphenols, TP)是茶叶中一类主要的化学成分,由于其具有良好的生物学活性和多种药理作用受到国内外有关科学家的重视[1-2]。但TP不稳定,对其活性进行保护成为目前研究的热点[3-4]。关于TP活性保护的报道很多,目前主要采用简单混合的方法将TP包埋起来[5],该方法可在一定程度上保护TP的活性,但其保护程度较低,不可实现TP的有效缓慢释放,大大减少了TP在人体中起到的有益作用[6-7]。拓扑作为一种典型的数学方法在分析分子链环方面己经具有重要应用。拓扑理论是近年来发展迅速的新研究领域,它可以解释大分子物质是如何通过作用而引起分子链空间结构改变,并形成复杂网络的,进而对其功能进行预测、调控。利用拓扑结构对TP活性进行保护仍然是一个难题。
魔芋葡甘聚糖(konjac glucomannan, KGM)是由葡萄糖和甘露糖以β-1,4糖苷键连接起来的高分子杂多糖,是一种性能独特、应用广泛的天然高分子[8]。KGM在外加作用条件下可形成拓扑结构,有利于提高活性物质的稳定性。目前,国内外关于多糖拓扑结构的研究,仅发现了拓扑结构的存在而没有深入分析其形成及稳定存在的原因,更没有深入地探讨拓扑结构的形成规律[9]。
本文尝试运用现代分析手段和拓扑学分析相结合的方法,通过外加电场制备了KGM-TP复合凝胶,实现了KGM拓扑链对TP活性的保护,并对其形成机理进行了探究。
1 材料与方法
1.1材料与试剂
魔芋精粉(葡甘聚糖含量为88%),云南三艾有机魔芋发展有限公司;茶多酚(TP,纯度为98%),混合物,福州鑫伟诚有限公司;DPPH, 日本东京化成工业株式会社; KH2PO4、K2HPO4等均购自国药集团化学试剂有限公司。
1.2KGM的制备
取10 g魔芋精粉,用含 0.1%叠氮钠的体积分数为50%乙醇洗涤(50 mL×3),自然晾干后用50 mLV(无水乙醚)∶V(无水乙醇)=2∶1在 40 ℃搅拌8 h脱脂,将脱脂样品以去离子水配成6 g/L水溶胶,用超速冷冻离心机离心,转速16 000 r/min,时间20 min。取上清液,加入适量淀粉酶于常温下酶解,酶解完全后,酶解液以Sevage 法脱蛋白,重复5次,再次离心。取上层水相,加入相同体积的体积分数为95%的乙醇沉淀样品,随后分别用无水乙醇和乙醚处理以进一步除去乙醇溶剂,再经冷冻干燥后得到白色絮状KGM,存放于冰箱。
1.3KGM-TP溶胶的制备
准确称量TP 0.1 g,加入到一定量的去离子水中,超声均匀分散,在350 r/min的转速,45℃水浴加热条件下缓慢加入1.0 g KGM,匀速搅拌1 h得KGM-TP溶胶。
1.4KGM-TP复合凝胶的制备
准确称量TP 0.1 g,加入到一定量的去离子水中,超声均匀分散,在350 r/min的转速,45 ℃水浴加热条件下缓慢加入1.0 g KGM,匀速搅拌1 h形成均匀KGM-TP溶胶,在溶胶内插入直流电极,20~50 V条件下处理40 min,形成KGM-TP复合凝胶。
1.5KGM-TP复合凝胶表征及性能测试
1.5.1 SEM测试
在JSM-5600LV扫描电子显微镜下观察KGM粉末、KGM-TP溶胶、KGM-TP复合凝胶的表面形貌,最大加速电压:15kV。
1.5.2 FTIR测试
采用KBr压片,红外光谱测定波数为4 000~400 nm,仪器分辨率0.5 nm,扫描次数为32/64。
1.5.3 TGA测试
设置温度区间为25~600 ℃,氮气氛围,升温速率为20 K/min,以温度为横坐标,重量为纵坐标得到图像。


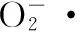
(1)
式中:ν空为KGM-TP复合凝胶抑制邻苯三酚自氧化的速率;ν样为空白管中以蒸馏水作对照抑制邻苯三酚自氧化的速率。
1.5.5 DPPH·清除力的测定
参照LOFFREDO等[14-15]的方法,用体积分数(下同)95%乙醇溶液配制浓度为0.2 mmol/L 的DPPH溶液。 取2 mL DPPH溶液于试管中,在暗室下避光反应30 min后在517 nm处测定吸光值 (As)。以95%乙醇溶液作为对照 (Ac) ,空白对照以95%乙醇溶液代替DPPH溶液 (Ab)。DPPH清除力按下式计算:
(2)
1.6理论分析
由于TP是混合物,以TP中含量较多的EGCG分子结构为代表,基于BURNS等拓扑学分析[16-18],用折点和端点分别代表结构中的碳原子和氧原子,略去KGM分子基团中的—OH和C—H键,用直线表示碳氧和碳碳之间的作用力,运用拓扑结构图把复杂的KGM转变成了相对简单的平面拓扑结构。
2 结果与分析
2.1直流电场下KGM-TP复合凝胶的形成
利用直流电处理KGM-TP的水溶胶,观察到直流电处理初期正负电极上都产生气泡,这是由于水电解产生H+和OH-,施加 20~50 V电压,连续处理40 min,可以观察到在正极上产生了白色凝胶。电处理装置及凝胶见图1。
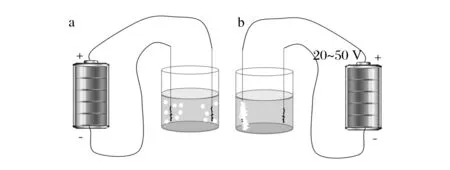
a-处理初期两电极上产生气体;b-40 min后正极上产生白色凝胶图1 直流电场下KGM-TP复合凝胶的制备Fig.1 Preparation of KGM-TP composite gel under DC electric field
2.2SEM分析
图2(a)为KGM粉末的扫描电镜,由图2(a)可以看出,KGM在粉末状态下,外表呈现规则的微纤维状,并在紧密排布的直链之间有很短的支链,微纤维之间相互胶着,这可能是KGM分子之间形成了氢键,而该键对KGM的紧密排布的微纤维链状结构起到了至关重要的稳定作用。从微纤维的尺寸知,此时观察到的并非单个的分子链,而是形成了伸直链的许多连接链的聚集体。
图2(b)和图2(c)为直流电处理前KGM-TP溶胶不同放大倍数的扫描电镜,由图2(c)可知,KGM长分子链仍然存在,而原有的规则的微纤维状结构消失,呈现出杂乱无章的絮状结构。这可能是由于KGM分子与水分子相互作用,形成了大量的分子间氢键,水分子束缚并充满KGM分子链之间。冷冻干燥处理时,水分子快速升华脱离KGM分子链,留下水分子逃逸的通道,从而呈现空洞结构。

图2 粉末KGM(a)和KGM-TP溶胶(b.c)扫描电镜图Fig.2 SEM of KGM powder and KGM-TP sol
图3为直流电处理后KGM-TP复合凝胶扫描电镜图,从图3可以看出,在直流电处理的条件下,KGM-TP复合凝胶冻干后成了环状的拓扑结构,这可能是KGM分子链在直流电场的作用下进一步发生穿孔聚合,形成拓扑链将TP分子包裹其中。另外还可以看到冻干后的扫描电镜呈现均匀的支架结构,电处理未使KGM链的糖苷键发生断裂,其余部分存在着细的条带和大小不均匀的孔洞,这可能是电极上电场强度分布不均匀所致。
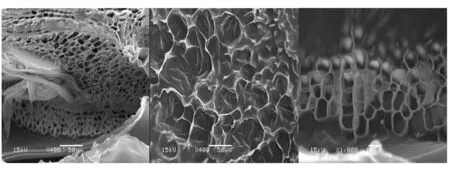
图3 KGM-TP复合凝胶扫描电镜图Fig.3 SEM of KGM-TP composite gel
2.3FTIR分析
红外光谱是一种研究聚合物间氢键相互作用的强有力工具,氢键作用使吸收峰移向低波数,频率(或波数)相对变化越大,氢键相互作用越强[19-20]。图4为KGM-TP溶胶、KGM-TP复合凝胶的红外光谱图。
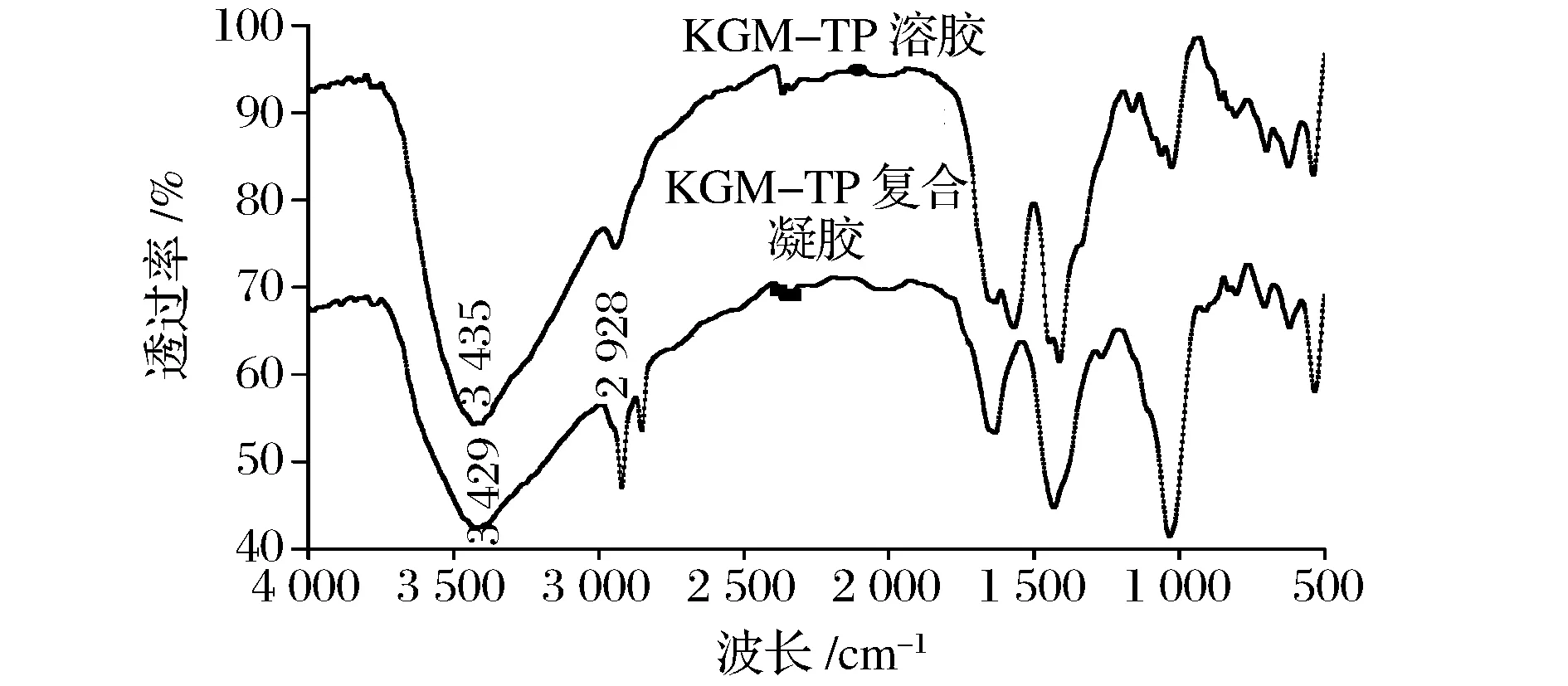
图4 KGM-TP溶胶、复合凝胶的红外光谱图Fig.4 FTIR of KGM-TP sol and KGM-TP composite gel
3 435 cm-1处显示强大的峰,为—OH的吸收峰,而KGM-TP复合凝胶在此处的吸收峰强度减弱,且略向低峰方向移动,表明KGM-TP复合凝胶中有更多氢键的形成,导致—OH吸收峰强度降低。同时KGM-TP复合凝胶在2 928 cm-1出现了吸收峰,这正是甲基中C—H的吸收峰,印证了复合凝胶KGM分子之间拓扑链的形成,与电镜测定结果相一致。
2.4TGA分析
如图5所示,KGM-TP溶胶、KGM-TP复合凝胶都出现了2个主要的热跃迁峰,其中第1个为起始变性温度峰,发生在200 ℃左右,第2个为变性温度峰,发生在300 ℃左右。KGM-TP复合凝胶的吸热峰尖而窄,而KGM-TP溶胶吸热峰平而宽,说明前者较后者更稳定。对于热焓值(ΔH)而言,KGM-TP复合凝胶热焓值大于KGM-TP溶胶热焓值,这说明KGM-TP复合凝胶可提高TP的热稳定性。

图5 KGM-TP溶胶、复合凝胶的热重分析Fig.5 TGA of KGM-TP Sol, KGM-TP Composite gel



图6 不同浓度下清除力(a)、DPPH·清除力(b)的测定Fig.6 · scavenging ability and DPPH· scavenging ability at different concentration
2.6理论分析
基于电镜、红外及对KGM-TP复合凝胶抗氧化性能的测试,结合拓扑学分析方法,推测KGM-TP复合凝胶结构网络,KGM-TP复合凝胶拓扑结合方式分别见图7,图8。
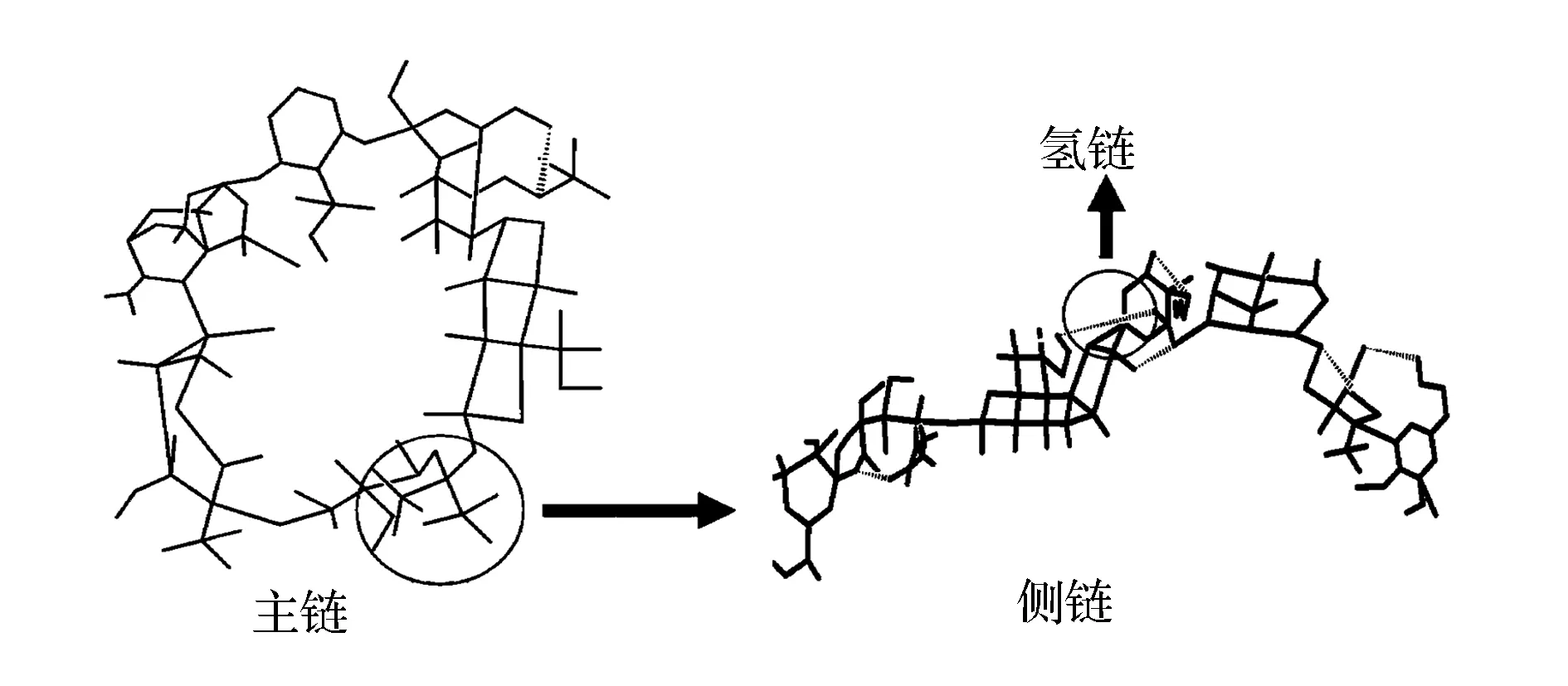
图7 KGM-TP复合凝胶结构网络图Fig.7 The probable network structure of KGM-TP Composite gel
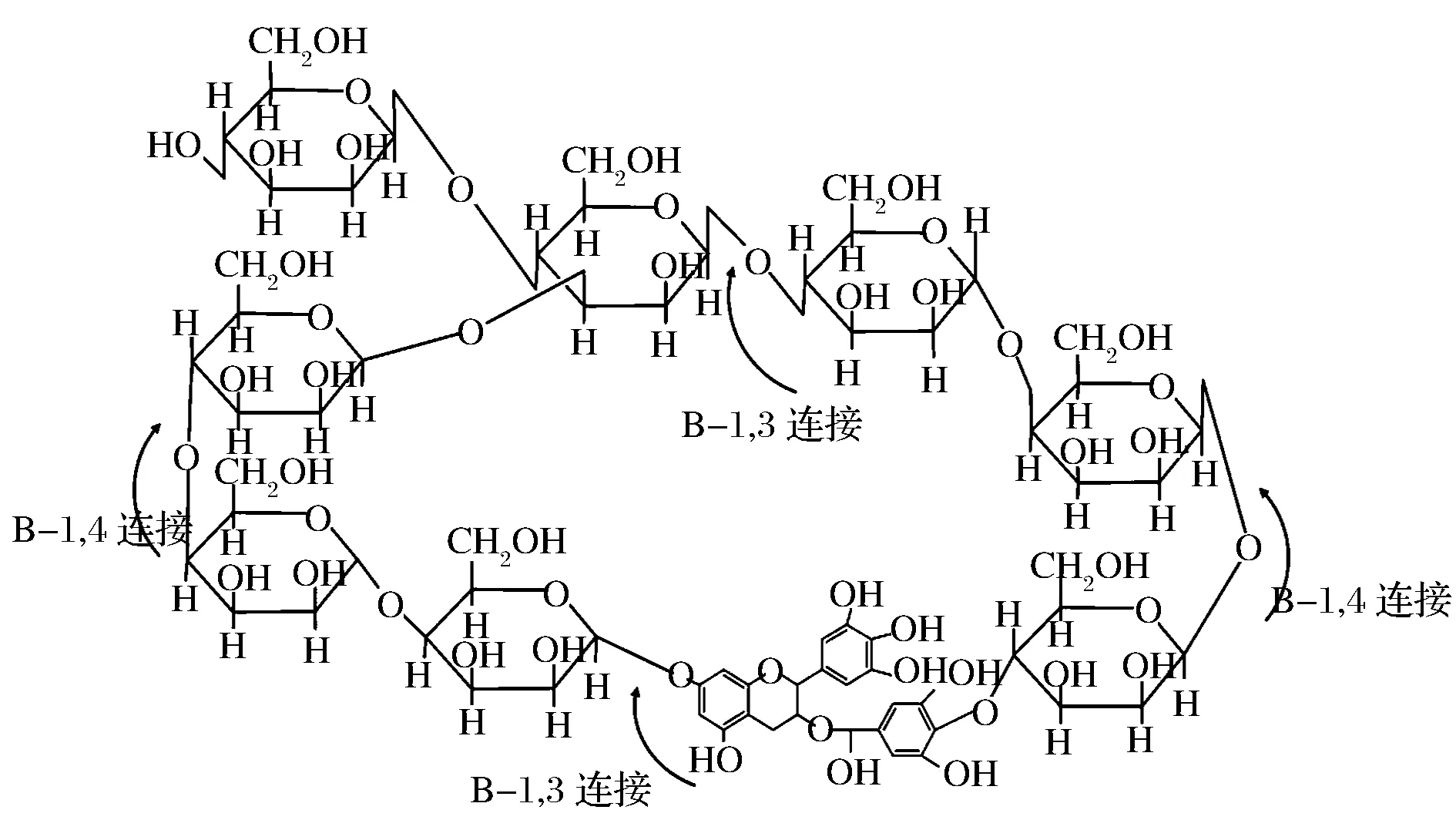
图8 KGM-TP复合凝胶拓扑结合方式示意图Fig.8 Schematic diagram of topological mode of KGM-TP composite gel
如图7所示,在外加直流电场的条件下,KGM分子内、分子间以氢键为主要作用力,主链相互连接形成了环状拓扑结构,侧链各—OH之间互相连接,使环状拓扑结构更加牢固,这与电镜观察到的结果相一致。TP分子表面—OH众多,在KGM拓扑链存在的情况下,与其表面—OH以氢键作用力的方式紧密结合,从而减少外界条件对其表面—OH的破坏,达到保护活性的目的,这与红外结果相一致(图8)。当KGM-TP复合凝胶溶于水溶液中时,在水分子作用下KGM与TP氢键打开,完成TP的高效释放,这与KGM-TP复合凝胶氧化性能测试结果相一致。
3 讨论
在直流电场的作用下KGM-TP溶胶穿孔聚合,形成KGM-TP复合凝胶,以KGM-TP溶胶做对照,用SEM测试了KGM-TP复合凝胶的微结构,在不同的放大倍数下均可观察到KGM分子链构成的环状拓扑结构;然后用FTIR检测到KGM分子内,分子间及KGM和TP分子之间均以氢键为主要作用力并且KGM-TP复合凝胶的热性能明显提高;最后通过对KGM-TP复合凝胶抗氧化性能测试及基于拓扑学的理论分析,推测的KGM拓扑链与TP分子最可能的结合方式。本研究一定程度上解决了TP不稳定的难题,大大提升了TP的应用领域,为今后将KGM拓扑链用于对各种敏感活性成分的保护奠定了基础。
[1] ZORILLA R,LIANG L,REMONDETTO G,et al.Interaction of epigallocatechin-3-gallate with β-lactoglobulin: molecular characterization and biological implication[J].Dairy Science & Technology,2011,91(5):629-644.
[2] YANG Chung,WANG Xin,LU Gang,et al.Cancer prevention by tea: animal studies, molecular mechanisms and human relevance[J].Nature Reviews Cancer,2009,9(1):429-439.
[3] 桑鹏,高春燕.不同极性地参茶多酚抗氧化活性的比较[J].食品研究与开发,2016,37(17):6-9.
[4] 谭琳,郑晓燕,王甲水,等.大果榕果实乙醇提取物抗氧化活性及对α-葡萄糖苷酶和乙酰胆碱酯酶抑制活性[J].食品科学,2016,37(13):77-81.
[5] 李谣,陈金龙,夏春燕,等.基于HepG2细胞模型的香菇柄粉茶多酚抗氧化及抗增殖活性[J].食品科学,2016,37(11):190-196.
[6] 闫亚美,米佳,禄璐,等.黑果枸杞多酚体外抗氧化活性研究[J].食品工业科技,2016,37(13):49-52.
[7] 吴昆明,凌阿静,胡新中,等.干燥方式对苦荞麦芽色泽、茶多酚及抗氧化活性的影响[J].食品与发酵工业,2016,42(11):115-120.
[8] WANG Li-xia,ZHANG Yu,PANG Jie,et al.The textural properties and microstructure of konjac glucomannan-tungsten gels induced by DC electric fields[J].Food Chemistry,2016,212(6):256-263.
[9] WANG Li-xia,PANG Jie.Rheological properties and formation mechanism of DC electric fields induced konjac glucomannan-tungsten gels[J].Carbohydrate Polymers,2016,(142):293-299.
[10] NI Yong-sheng,MU Ruo-jun,TAN Xiao-dan,et al.Stability of the konjac glucomannan topological chain based on quantum spin model[J].Chinese Journal of Structural Chemistry,2017,36(6):1 043-1 048.
[11] ASIMINA K,GARY W.At the interface of antioxidant signalling and cellular function: Key polyphenol effects[J].Molecular Nutrition & Food Research,2016,60(8):1 770-1 788.
[12] RAJAN V K,MURALEEDHARAN K.A computational investigation on the structure, global parameters and antioxidant capacity of a polyphenol, Gallic acid[J].Food Chemistry,2017,220(4):93-99.
[13] UCHIDA K,TOMITA H,TAKEMORI T,et al.Effects of grilling on total polyphenol content and antioxidant capacity of eggplant (SolanummelongenaL)[J].Journal of Food Science,2016,82(1):202-207.
[14] LOFFREDO L,PERRI L,NOCELLA C,et al.Antioxidant and antiplatelet activity by polyphenol-rich nutrients: focus on extra-virgin olive oil and cocoa[J].British Journal of Clinical Pharmacology,2017.83(1):96-102.
[15] NIU Rui-wu,PAN Gui-jun.Self-organized optimization of transport on complex networks[J].Chinese Physics Letters,2016,33(6):153-156.
[16] ZHU Liu-hua.Effects of reduced frequency on network configuration and synchronization transition[J].Chinese Physics Letters,2016,33(5):14-17.
[17] WANG Q H, ZHENG H, WU X M.Simulation invitroon inhibition of calcium oxalate calculus in lithogenic urine by sulfated polysaccharide isolated from laminarin[J].Journal of Synthetic Crystals, 2006,35(10):1 296-1 300.
[18] PANG Jie,MA Zhen,SHEN Ben-shu,et al.Hydrogen bond networks' QSAR and topological analysis of konjac glueomannan chains[J].Chin J Struct Chem, 2014,33(3):480-489.
[19] MU Ruo-jun,PANG Jie,YUAN Yi,et al.Progress on the Structures and Functions of Aerogels[J].Chin J Struct Chem,2016,35(5):487-497.
[20] CAO Yun-gang,XIONG You-ling.Chlorogenic acid-mediated gel for-mation of oxidatively stressed myofibrillar protein[J].Food Chemistry,2015,180(4):235-243.
[21] JONGBERG S,TERKELSEN L S,MIKLOS R,et al.Green tea extract impairs meat emulsion properties by dis-turbing protein disulfide cross-linking[J].Meat Science,2015,100(3):2-9.
[22] YUKSEL Z,AVCI E,EDEM Y K.Characterization of binding interactions between green tea flavanoids and milk proteins[J].Food Chemistry,2010,121(2):450-456.
[23] HARBBOURNE N,JACQUIER J C,O’RIORDAN D.Effects of addition of phenolic compounds on the acid gelation of milk[J].International Dairy Journal,2011,21(3):185-191.
Themechanismofkonjacglucomannanonthestabilityoftopologicalchainandteapolyphenols
NI Yong-sheng1, LIN Wan-mei1, LI Yuan-zhao1, WANG Lin1, WANG Wei-hai1, ZHANG Xin-yue1, LIN Yu-chun1, DU Yu1, WU Xian-hui2*, PANG Jie1*
1(College of Food Science, Fujian Agriculture and Forestry University, Fuzhou 350002, China) 2(Ningde Vocational and Technical College, Fuan 355000, China)
The konjac glucomannan (KGM) composite gel was prepared by direct current in order to solve the problem of unstable and easy oxidation of tea polyphenols(TP). According to the research, KGM topological chain can protect TP under the action of electric field force. The research was focused on both microstructure and thermal stability of KGM-TP Gel, KGM-TP sol was the control. The degree of protection and release of KGM-TP gel for TP is also studied in the same way. The experiment analyzed the force of maintaining the stability of TP as well as revealed the possible mechanism of stabilization. The results showed that KGM chain forms the cyclic topology through intramolecular and intermolecular hydrogen bonds under the action of external electric field. KGM chain protected the TP molecules in the form of hydrogen bonding force. KGM-TP Gel has stronger O2-scavenging power and DPPH scavenging power compared with KGM-TP sol under the same condition. The KGM topology chain can not only protect TP but also can improve the release of TP.
konjac glucomannan(KGM); tea polyphenols(TP); DC electric field; topology; antioxidant properties
硕士研究生(庞杰博士和吴先辉教授为通讯作者,E-mail:pang3721941@163.com;E-mail:1141091857@qq.com)。
国家自然科学基金(31471704,31772045);福建省自然科学基金(2017J01155)
2017-02-03,改回日期:2017-05-31
10.13995/j.cnki.11-1802/ts.013969
