军队医院9819例喹诺酮类药物药品不良反应/事件报告分析
2017-11-01黄翠丽郭代红赵粟裕赵鹏芝解放军总医院药学部临床药学中心北京00853重庆医科大学药学院重庆4033
黄翠丽,郭代红,朱 曼,吴 旭,2,苏 畅,2,赵粟裕,马 亮,赵鹏芝,赵 靓(.解放军总医院药学部临床药学中心,北京 00853;2.重庆医科大学药学院,重庆 4033)
军队医院9819例喹诺酮类药物药品不良反应/事件报告分析
黄翠丽1,郭代红1,朱 曼1,吴 旭1,2,苏 畅1,2,赵粟裕1,马 亮1,赵鹏芝1,赵 靓1(1.解放军总医院药学部临床药学中心,北京 100853;2.重庆医科大学药学院,重庆 401331)
目的:通过对军队医院喹诺酮类药物药品不良反应/事件(ADR/ADE)报告的相关因素分析,了解喹诺酮类药物ADR/ADE发生特点及规律。方法:采用回顾性方法,收集2009 – 2015年军队ADR监测管理系统中喹诺酮类药物ADR/ADE报告9819例,对患者年龄、性别、药品种类、给药途径、药品剂型,累及系统/器官及临床表现、ADR/ADE报告类型、关联性评价及转归情况等进行描述性统计分析。结果:9819例喹诺酮类药物ADR/ADE中,男女比例为1.02 : 1,平均年龄为(45.67±22.73)岁,给药途径和药品剂型以静脉滴注和注射剂型为主,共涉及17个药物品种,单品种中左氧氟沙星4660例(47.46%)位于首位,其次为莫西沙星1681例(17.12%)、加替沙星1597例(16.26%)。9819例喹诺酮类药物ADR/ADE共累及多个系统/器官,14740例次,最常见的为皮肤及其附件损害5731例次(38.88%),其次为胃肠系统损害2749例次(18.65%)和心外血管损害2162例次(14.67%)。结论:喹诺酮类药物品种繁多,所致的ADR/ADE涉及不同年龄段患者,累及多个系统/器官,在使用中应加强用药安全风险防范,及时识别并处理ADR/ADE。
喹诺酮类药物;药品不良反应;药品不良事件
[KEY WORDS]Quinolones; Adverse drug reaction; Adverse drug event
喹诺酮类药物是临床使用广泛的一类抗感染药物,具有抗菌谱广,对G-杆菌活性高、口服吸收好、组织浓度高、半衰期长、使用方便等优点[1]。近年来发展十分迅速,但其在控制感染、降低患者死亡率等方面发挥重要作用的同时,也引发了一系列临床问题,如细菌耐药、不良反应的发生等。药品不良反应(adverse drug reaction,ADR)是合格药品在正确的用法用量下出现的与用药目的无关的有害反应,ADR监测报告在药品安全风险早期预警、促进合理用药、保障用药安全等方面发挥着重要作用。笔者对解放军ADR监测中心2009 – 2015年喹诺酮类药物的药品不良反应/事件(ADR/ADE)报告进行回顾性分析,了解其ADR/ADE发生的特点及规律,旨为喹诺酮类药物合理应用提供药品安全信息。
1 资料与方法
1.1 数据来源
基于军队ADR监测管理系统,调取数据库中2009年1月1日– 2015年12月31日期间来自158所网点医院的ADR/ADE报告,按照国家ADR监测中心的6级关联性评价标准[2],纳入评价为“肯定”、“很可能”和“可能”的有效报告,从中筛选第一怀疑药品药物类别为喹诺酮类药物的ADR/ADE报告9819例。
1.2 数据规整
采用回顾性分析方法,对涉及ADR/ADE的患者年龄、性别、药品种类、药品剂型、给药途径、累及系统/器官损害以及报告人职业分布、报告类型、关联性评价、转归等运用Excel软件进行数据汇总和分析。
ADR名称按照《WHO药品不良反应术语集》[3]进行整理,并对其累及的系统/器官进行分类,对同一报告累及多个系统/器官,涉及多个临床表现的分别计算频次。按照《临床用药须知》(2010年版)[4]和《新编药物学》(17版)[5]对喹诺酮类药物类别进行分类,同一药品不同剂型不同厂家的计为1个品种。
1.3 统计学方法
采用SPSS20.0软件进行统计分析,计量资料采用t检验,计数资料采用χ2检验,P< 0.05为差异有统计学意义。
2 结果
2.1 患者的性别和年龄
9819例ADR/ADE患者中,男性4969例(50.61%),女性4850例(49.39%),男女比例为1.02 :1。患者年龄最大为110岁,最小为新生儿,平均年龄(45.67±22.73)岁,各年龄段分布组间比较差异有统计学意义(χ2= 102.28,P< 0.05),详见表1。

表1 患者的年龄和性别分布Tab 1 Age and gender distribution of patients
2.2 涉及的给药途径和药品剂型
9819例ADR/ADE报告中主要涉及4种给药途径,包括静脉滴注9279例(94.50%)、口服428例(4.36%)、静脉注射108例(1.10%)、眼内用药4例(0.04%)。
9819例ADR/ADE共涉及8个药品剂型,按构成比由高到低的顺序依次为:注射剂8445例(86.01%)、粉针剂808例(8.23%)、片剂339例(3.45%)、胶囊剂81例(0.82%),其他剂型(如滴眼剂、分散片、凝胶剂、眼膏剂等)为146例(1.49%)。
2.3 涉及的药物品种
9819例ADR/ADE报告共涉及17个药物品种,详见表2。其中位居前五位的分别为:左氧氟沙星4660例(47.46%)、莫西沙星1681例(17.12%)、加替沙星1597例(16.26%)、环丙沙星799例(8.14%)、依诺沙星383例(3.90%)。
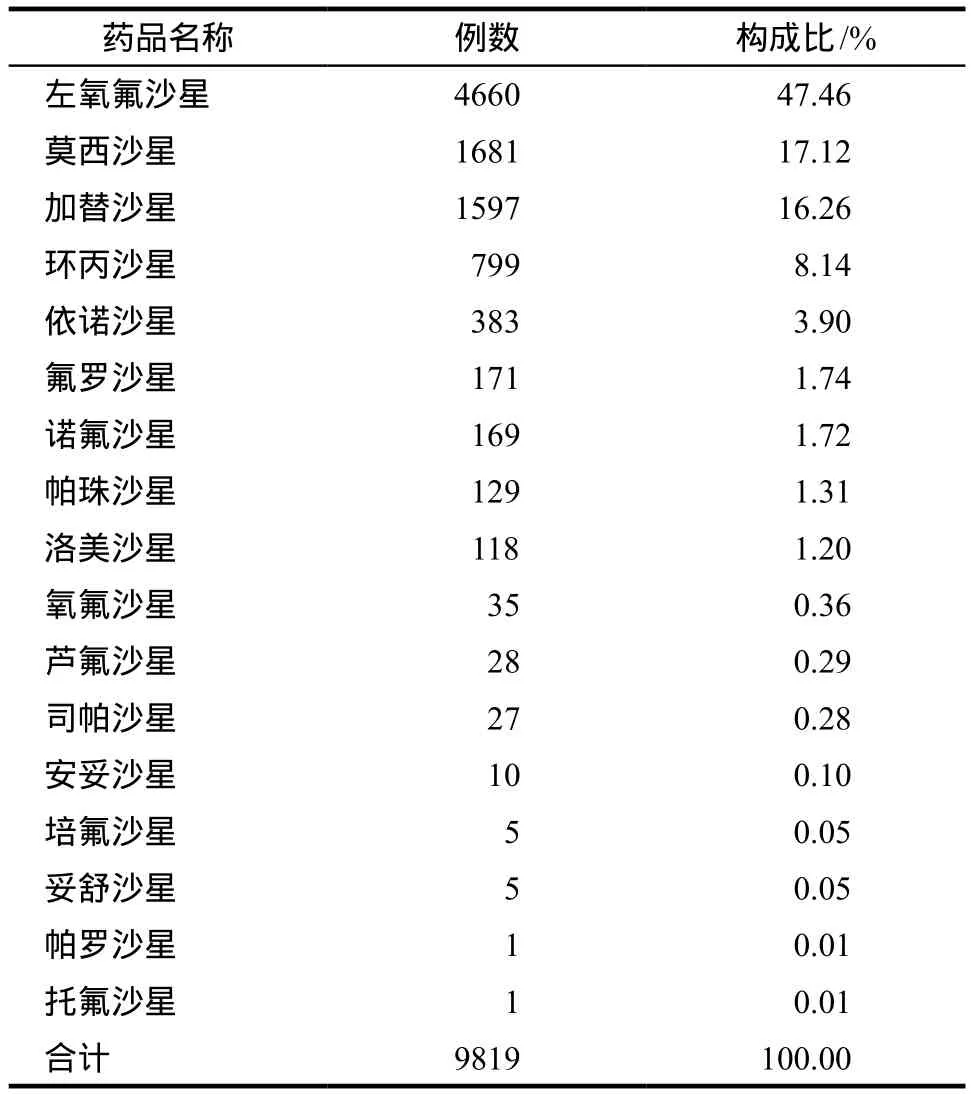
表29819例ADR/ADE的药物品种分布Tab 2 The drug category distribution of 9819 ADR/ADE
2.4 累及的系统/器官及主要临床表现
9819例ADR/ADE累及多个系统/器官,共计14740例次,详见表3。其中最常见的为皮肤及其附件损害5731例次(38.88%),主要的不良反应表现为皮疹、瘙痒、红斑疹、荨麻疹、斑丘疹等;其次为胃肠系统损害2749例次(18.65%),主要的不良反应表现为恶心、呕吐、腹痛、腹泻、口干等;心外血管损害2162例次(14.67%)位居第3位,其主要的不良反应表现为静脉炎、潮红等。
2.5 ADR/ADE的报告类型及报告人职业分布
根据《药品不良反应报告和监测管理办法》中ADR严重等级的定义,将ADR分为一般的、新的一般的、新的严重的和严重的4种报告类型,其中后3种统称为新的和严重的ADR[2]。9819例喹诺酮类药物ADR/ADE中一般的9422例(95.96%),新的和严重的397例(包含新的一般的87例,新的严重的12例、严重的298例),占报告总数的4.04%。
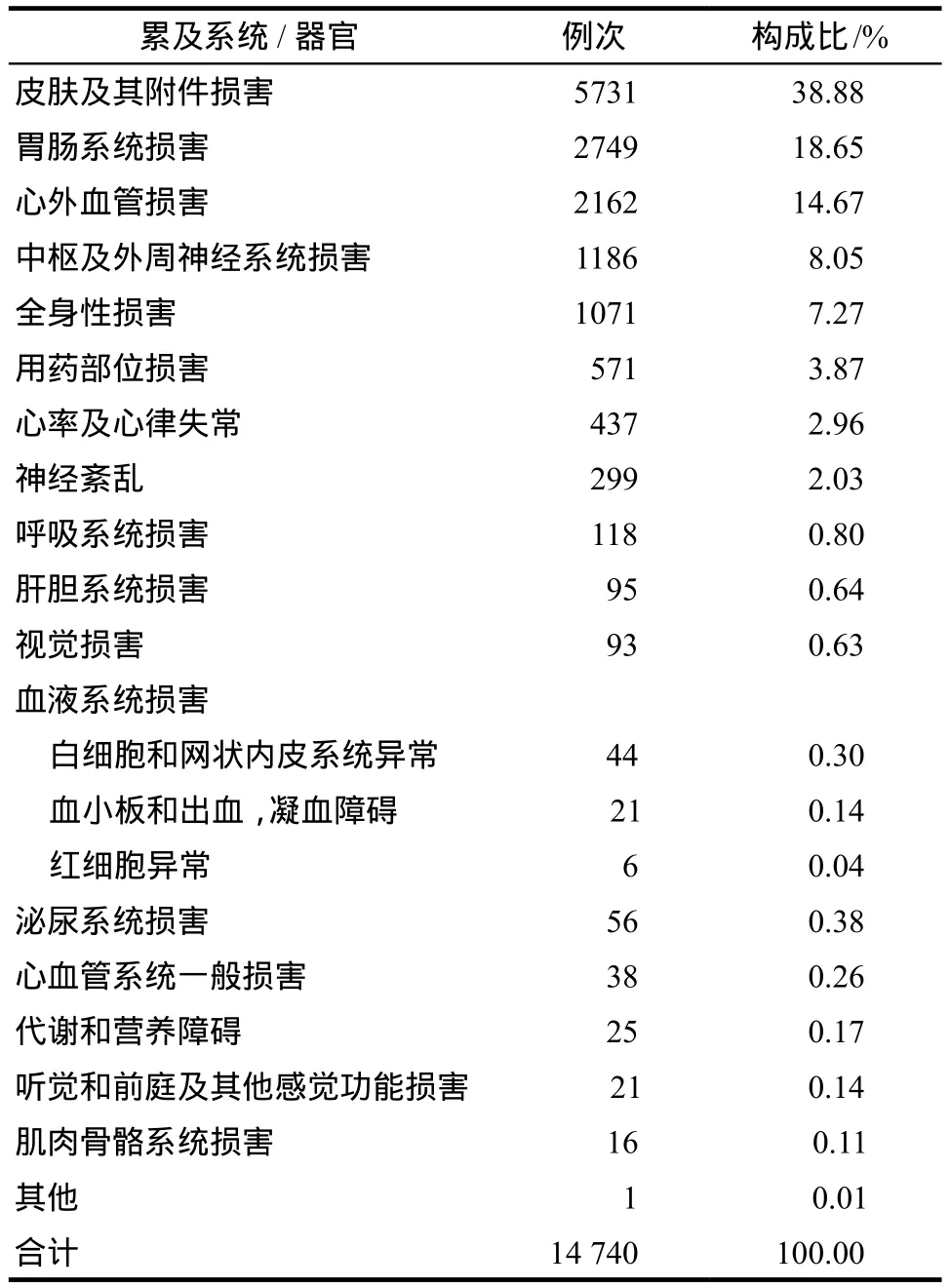
表3 ADR/ADE累及的系统/器官分布Tab 3 The distribution of systems/organs involved in ADR/ADE
从报告人的职业分布看,报告主体为医生和护士,分别上报了3783例(38.53%)和4853例(49.42%),药师仅上报了1154例(11.75%),其他医务人员上报29例(0.30%)。新的和严重ADR/ADE的报告人职业分布中医生、护士、药师分别占2.13%、0.83%和1.08%,报告人职业的报告类型组间比较,有统计学差异(χ2= 102.28,P< 0.05),详见表4。
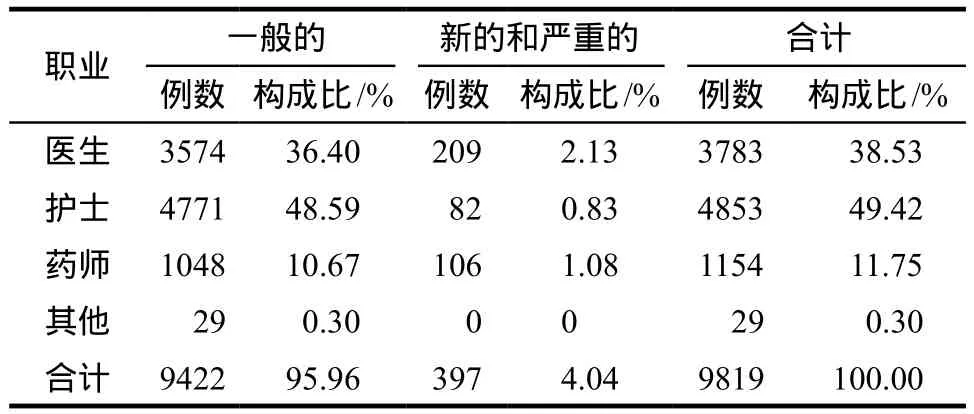
表4 喹诺酮类药物ADR/ADE的报告类型及报告人职业分布Tab 4 The category of quinolones associated ADR/ADE and the reporters' profession distribution
2.6 ADR/ADE的关联性评价和转归
9819例ADR/ADE报告中肯定的377例(3.84%);很可能的6617例(67.39%);可能的2825例(28.77%)。从转归情况看:治愈4946例(50.38%),好转4734例(48.21%),持续116例(1.18%),自动出院17例(0.17%),有后遗症的4例(0.04%),死亡2例(0.02%)。
3 讨论
3.1 患者的性别和年龄
9819例ADR/ADE报告涉及的男性和女性患者比例为1.02 : 1,患者的年龄呈正态分布,20 ~ 69岁比例高,< 10岁和> 70岁比例低,与我国人群不同年龄段分布基本一致[6],各年龄段分布组间比较差异有统计学意义。需要指出的是:儿童由于器官生理功能包括自身调节功能尚未发育成熟,免疫功能较低,药物代谢酶分泌不足或缺少,肾功能发育不完善,对药物清除能力差等因素,易发生ADR;而老年患者常患多种疾病,往往需要联合用药、长期用药,且随着年龄增长,肝肾功能呈不同程度的减退,影响药物的代谢和排泄,易发生药物蓄积,此外老年患者血浆白蛋白低,血中游离药物浓度偏高,易导致药物疗效过强而发生ADR[6-7],用药中应予以关注。喹诺酮类药物在动物实验中有一定的关节软骨毒性,在未成年动物中可引起关节病,因此禁用于未成年患者。此次分析报告中,仍有229例未成年患者使用喹诺酮类药物,存在明显临床不合理用药现象,提示临床医生应高度重视喹诺酮类药物的安全使用。
3.2 ADR/ADE与给药途径及给药剂型
9819例ADR/ADE报告中,静脉滴注给药(9279例,94.50%)和注射剂型(注射剂8445例,86.01%;粉针剂808例,8.23%)引起的ADR/ADE显著高于其他给药途径和剂型。静脉途径给药起效快,主要用于急症、重症和不能口服给药病人的救治和治疗,然而作为一种有创的给药途径,药物直接进入血液,一旦发生ADR,很难快速从体内清除。输液中pH、内毒素、微粒、药物浓度等因素为引起ADR/ADE的直接诱因[7],也与药物浓度、药液的稳定性、给药时间、滴注速度等密切相关[8]。因此,应尽量控制或减少经静脉途径给药、规范用药细节,避免配伍不恰当、浓度不适宜、滴速过快。实际上,喹诺酮类药物口服生物利用度较高,多数能达到90% ~ 100%,故建议尽量采用口服给药,以避免不良反应的发生[1]。
3.3 引起ADR/ADE的药物品种
从单品种排名前10位看,左氧氟沙星、莫西沙星、加替沙星等药品不良反应报告的数量位居前三位,这与该类药物抗菌谱广、活性强、口服吸收良好等特点使其在临床广泛应用有关[9]。随着氟喹诺酮类药品的大量应用,一些新的不良反应或一些不良反应新的发生特点逐渐被认识,值得关注的是国家食品药品监督管理局先后在《药品不良反应信息通报》第11期、22期、24期、35期、56期和58期对喹诺酮类抗菌药物的ADR进行通报,国外监测机构陆续发布了氟喹诺酮类药品可能引起重症肌无力加重和周围神经病变的风险提示,并对氟喹诺酮类产品说明书进行了修订。最新病例报告和研究表明,部分氟喹诺酮类药品品种可能影响糖尿病患者的血糖控制水平。警示医务工作者应高度重视喹诺酮类抗菌药物引起的ADR,遵循《抗菌药物临床应用指导原则》,合理使用抗感染药物。
3.4 ADR/ADE累及的系统/器官
9819例A D R/A D E中以皮肤病变最常见(38.88%),其次为胃肠系统损害(18.65%),分析与皮疹、恶心、呕吐等皮肤及胃肠道系统等不良反应表现最为直观,更易引起医务人员的关注有关。心外血管损害2162例(14.67%),中枢及外周神经系统损害1186例(8.05%)、全身性损害1071例(7.27%)较为常见,以及肝胆系统损害95例(0.64%)、血液系统损害71例(0.48%)及泌尿系统损害56例(0.38%)等的构成比较低,推测与这些ADR/ADE相对隐蔽,通常在导致严重损害或表现出明显的症状/体征后才被识别和报告有关。
3.5 ADR/ADE报告例数及报告类型
喹诺酮类药物引起的ADR/ADE报告比例领先于其他类别抗感染药物,与其他报道[10]结果一致。分析原因:1)可能与喹诺酮类药物在临床的应用范围广泛,使用频率高有关;2)不排除喹诺酮类药物的不规范使用导致的ADR/ADE报告增加。9819例报告中新的和严重ADR/ADE报告总计397例(4.04%),低于WHO推荐的成熟的ADR监测系统中新的和严重的报告比例应达到30%以上的标准,推测可能与医务人员对新的和严重的ADR认识不够或对上报严重ADR存在一定的思想顾虑以及部分医疗机构片面追求报告数量或报告比例达标,从而导致已知的一般ADR报告上报数量偏多等因素有关。
3.6 报告人的职业分布
报告人职业分布和报告类型的组间比较差异有统计学意义,提示与医生、护士在药物临床应用过程中的直接参与程度相关。一旦患者发生ADR,医生和护士往往是患者的直接接触者或第一信息接收人,而我国大多数医疗机构药师长期以来主要负责药品采购、调配、药物制剂的配制等工作,在整个医疗活动中参与度不高,限制了其在ADR/ADE监测中发挥作用。397例新的和严重ADR/ADE报告人职业分布中药师的报告比例有所增加,高于护士的报告比例,提示药师具有专业知识的优势,随着国家临床药学服务的深入,药师在用药安全方面特别是严重ADR/ADE的识别和报告中将会发挥越来越重要的作用[11]。
4 小结
《药品不良反应监测管理办法》自1999年发布以来,经过2004年和2011年两次修订之后,我国的ADR监测工作日臻完善,ADR监测数据快速增长。为临床应用喹诺酮类药物提供了一定的药物安全信息参考。然而由于被动监测模式本身存在的漏报、低报、缺乏细节信息、无法统计发生率、信号偏倚等缺陷问题[12],对喹诺酮类药物的ADR信号识别、发生规律、ADR发生率等方面还存在不足。未来运用信息化手段,加强主动监测模式的ADR工作,弥补自发报告系统的局限性,使药品安全性评价更加全面和科学,是今后我国ADR监测的发展方向;此外,运用信号检测方法挖掘ADR数据库,并与临床紧密结合,辅助发现药品安全性信号,弥补专家评价方式的局限[13],也将为ADR监测提供新的和更广阔的思路。
[1] 付铁梅,田丽娟.喹诺酮类药物的严重不良反应及合理应用[J].中国药业,2011,20(23):48-49.
[2] 国家食品药品监督管理局.药品不良反应报告和监测管理办法[S].2011.
[3] 国家药品不良反应监测中心.WHO药品不良反应术语集[M].北京:中国医药科技出版社,2003.
[4] 国家药典委员会.中华人民共和国药典·临床用药须知[M].2010年版.北京:中国医药科技出版社,2011:622-852.
[5] 陈新谦,金有豫,汤光.新编药物学[M].17版.北京:人民卫生出版社,2011:34-134.
[6] 曹军华,韩勇,陈东生.1596例药品不良反应报告分析[J].药物流行病学杂志,2012,21(9):431-433.
[7] 孙言才,刘斌,苏丹,等.12249例药品不良反应报告中年龄分布的分析与评价[J].药物流行病学杂志,2014,23(1):29-34.
[8] 任淑娟,吉金燕,解娟,等.我院304例药品不良反应报告分析[J].西北药学杂志,2014,29(1):93-96.
[9] 温爱萍,赵业婷.181例抗感染药品严重不良反应报告回顾性分析[J].中国药物应用与监测,2014,11(5):304-307.
[10] 朱曼,郭代红,凡超,等.军队医院22605例抗感染药物药品不良反应/事件报告分析[J].中国药物应用与监测,2015,12(5):284-288.
[11] 朱曼,凡超,郭代红,等.军队医院1175例抗感染药物严重药品不良反应/事件报告分析[J].中国药物应用与监测,2015,12(3):163-167.
[12] 田春华,杜晓曦.论我国药品不良反应监测工作几点进展[J].药物流行病学杂志,2014,23(1):1-4.
[13] 詹思延.药物流行病学研究方法与药品风险管理[J].药物流行病学杂志,2013,22(4):199-204.
Analysis on 9819 cases of ADR/ADE associated with quinolones in military hospitals
HUANG Cui-li1, GUO Dai-hong1, ZHU Man1, WU Xu1,2, SU Chang1,2, ZHAO Su-yu1, MA Liang1, ZHAO Peng-zhi1,ZHAO Liang1(1. Department of Clinical Pharmacy, PLA General Hospital, Beijing 100853, China; 2. The College of Pharmacy, Chongqing Medical University, Chongqing 401331, China)
Objective:To analyze adverse drug reaction reports and events (ADR/ADE) of quinolones in military hospitals in order to investigate the characteristics and regular patterns of quinolones related ADR/ADE.Methods:With the retrospective method, a total of 9819 ADR/ADE of quinolones case reports were collected from 2009 to 2015 in the database of PLA ADR monitoring center. Age and gender of patients, categories of suspected quinolones, route of administration, dosage form systems/organs involved and clinical manifestations, relevance evaluation and prognosis were analyzed.Results:Among 9819 ADR/ADE reports, the male to female ratio was 1.02 : 1. The average age of the patients was (45.67 ± 22.73) years. Intravenous infusion and injection type was the main administration route and pharmaceutical forms. The ADRs were related to 17 kinds. Levofloxacin related reports were 4660 cases (47.46%), followed by moxifloxacin (1681 cases, 17.12%) and gatifloxacin (1597 cases, 16.26%). A total of 9819 cases of the ADR/ADE involved multiple systems/organs (14740 cases). The most common was the skin and its appendages damage (5731 cases, 38.88%), followed by gastrointestinal system damage (2749 cases, 18.65%) and vascular disorders (2162 cases, 14.67%).Conclusion:The ADR/ADE induced by quinolones involved different age of patients, various drug categories and multiple systems/organs. In order to recognize and treat ADR/ADE in time, drug safety risk prevention should be strengthened in the quinolones application.
R969.3
A
1672 – 8157(2017)05 – 0293 – 04
2014年全军后勤科研重点项目(BWS14R039)
郭代红,女,主任药师,硕士生导师,主要从事药事管理及临床药学工作。E-mail:guodh301@163.com
黄翠丽,女,副主任药师,主要从事临床药学工作。
E-mail:qingbo20012001@163.com
2017-03-08
2017-06-01)
