恩替卡韦治疗肺结核合并HBV携带者抗结核药物所致肝损伤临床初步研究
2017-10-19冉仁玉江自成杨才勇
李 奎,冉仁玉,江自成,杨才勇,朱 凤
恩替卡韦治疗肺结核合并HBV携带者抗结核药物所致肝损伤临床初步研究
李 奎,冉仁玉,江自成,杨才勇,朱 凤
目的探讨恩替卡韦预防性治疗HBV携带者合并肺结核(PTB)患者抗结核药物所致肝损伤(ATDH)的作用。方法171例HBV携带者合并PTB患者接受2HRZE/4HR方案抗结核治疗,57例B组患者同时接受甘草酸二铵肠溶胶囊口服,54例C组患者接受恩替卡韦治疗。结果在治疗早期,C组患者ATDH发生率显著低于A组或B组(P<0.05),但在治疗3个月时,由于临床干预,3组ATDH发生率无显著性相差(P>0.05);在治疗6 m末,C组血清HBV DNA、ALT和TBIL水平分别为(2.4±0.8)copies/ml、(35.2±5.8)U/L 和(13.0±4.2) μmol/L,与 A 组[分别为(5.4±0.9) copies/ml、(65.4±9.0)U/L 和(32.4±7.6) μmol/L]或 B 组[分别为(4.9±1.1)copies/ml、(50.6±8.0)U/L 和(25.5±8.0) μmol/L]比,差异显著(P<0.05)。结论HBV 携带者合并 PTB 患者在抗结核开始时,给予恩替卡韦抗病毒治疗可抑制HBV DNA复制,防止HBV再激活,降低ATDH的发生。
HBV携带者;肺结核;恩替卡韦;抗结核药物所致肝损伤
在临床上,慢性HBV感染者合并PTB感染的情况很常见,如何在抗结核化疗顺利进行的同时,做好保肝及抗病毒治疗,不因ATDH的加重而导致抗结核治疗的中断,我们对慢性HBV感染合并PTB患者在常规抗结核过程中使用恩替卡韦抗病毒治疗,观察了肝功能和血清HBV DNA的变化,现将结果报告如下。
1 资料与方法
1.1 研究对象 2012年8月~2016年8月我科门诊及住院的HBV携带者合并肺结核患者171例,男108例,女63例;年龄在16~60岁,平均年龄(38.5±12.3)岁。HBV携带者诊断依照中华医学会肝病学分会和感染病学分会联合修订的《HBV携带者防治指南(2015年更新版)》[1]。PTB和结核性胸膜炎的诊断依照中华医学会结核病学分会《肺结核诊断和治疗指南》[2]。排除血清ALT升高、矽肺、肝硬化、糖尿病、癫痫、肾病、血液系统疾病、HIV或HCV感染、正在进行抗病毒治疗的乙型肝炎、复治的PTB、血行播散性结核、结核性脑膜炎、关节结核、肠结核患者,排除孕妇及哺乳期妇女,排除对一种或多种抗结核药过敏而无法组成有效治疗方案者。
1.2 治疗方法 采用随机数字表法将患者分为3组,A组采用 2HRZE/4HR 化疗方案,其中 H 0.3 g·d-1,Z 1.5 g·d-1,E 0.75 g·d-1,R 0.45~0.6 g·d-1;B 组患者在 A 组化疗方案的基础上加用甘草酸二铵肠溶胶囊(江苏正大天晴药业股份有限公司)150 mg口服,3次/d;C组在A组化疗方案的基础上加用恩替卡韦分散片(苏州东瑞制药有限公司)0.5 mg口服,1次/d。治疗过程中监测肝功能,对于出现肝损害持续加重,药物性肝损伤≥3级时,则停止抗结核治疗,转为抗HBV治疗。
1.3 观察指标 使用奥林巴斯 AU2700全自动生化分析仪检测血生化指标(北京利德曼生化股份有限公司试剂);采用时间分辨免疫荧光法检测血清HBV标记物(达安生物工程公司生产的DR6608型检测仪及其配套试剂);采用PCR-荧光探针法检测血清HBV DNA水平(德国凯杰公司Rotor-Gene Q型检测仪及其配套试剂)。
1.4 统计分析 应用SPSS 16.0统计软件,计数资料的比较采用x2检验,多组率之间两两比较采用Bonferroni校正卡方检验;计量资料以±s表示,多组均数之间比较采用方差分析,两两比较采用SNK法,以P<0.05为差异具有统计学意义。
作者单位:725000陕西省安康市中心医院感染性疾病科
2 结果
2.1 三组患者ATDH发生情况 在治疗早期,C组患者ATDH发生率显著低于A组或B组(P<0.05),但在治疗3个月时,由于临床干预,3组ATDH发生率无显著性相差(P>0.05,表 1)。

表1 三组ATDH发生率(%)比较
2.2 三组治疗前后血清HBV DNA和肝功能指标变化的比较 治疗前各组患者HBV DNA和肝功能指标无明显差异(P>0.05);治疗后A组和B组患者HBV DNA无显著性变化,ALT和TBIL显著升高,C组患者治疗前后HBV DNA显著性降低,ALT和TBIL无显著变化;在治疗6 m时,C组血清HBV DNA及ALT和TBIL水平显著低于A组和B组,差异有统计学意义(P<0.05,表 2)。
表2 三组血清HBV DNA和肝功能指标(±s)的变化
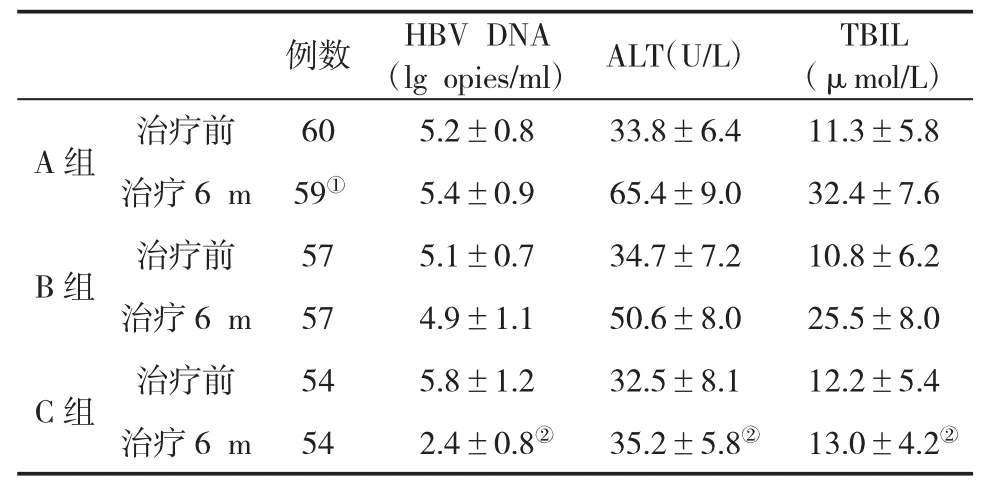
表2 三组血清HBV DNA和肝功能指标(±s)的变化
① 死亡1例;与A组或B组比,②P<0.05
?
2.3 转归 在治疗过程中,A组11例、B组4例 和C组1例因严重肝损害无法完成抗结核而转为抗病毒治疗,A组因肝衰竭死亡1例,其他各组发生ATDH患者经保肝治疗后肝功能好转而继续抗结核治疗,完成规定疗程。
3 讨论
抗结核药物对肝功能的影响表现为短暂性肝功能受损和药物性肝损伤,前者为一适应性过程,后者可以引起急性肝衰竭,不仅导致治疗结核的失败,还能形成耐药性结核病,甚至死亡。其原因如下:(1)药物及其代谢产物对肝脏产生直接损伤及线粒体功能下降[3];(2)药物作为全抗原或半抗原通过免疫机制造成过敏反应,肝细胞处于免疫兴奋状态易发生肝损伤,与目前一线抗结核药物所推荐的剂量无相关性[4];(3)与易感机体的基因多态性[5-7]等相关。最为常用的抗结核药物如异烟肼、利福平和吡嗪酰胺均有明确的肝损伤副作用,尤其是这三药联合应用增加了肝损伤的可能性,在临床用药时要权衡利弊,适时对高危因素给予干预,避免或降低ATDH发生率。
HBV携带者合并结核感染是否增加ATDH发生风险一直存在争议,de Castri et al[8,9]报道两者有统计学相关,而Saha et al[10]未发现两者的相关性。其机理可能是在ATDH发生后,肝细胞被破坏,HBV释放入血,激活了机体针对HBV的特异性细胞免疫反应,从而加重了肝损伤的风险,故HBV合并PTB患者在进行化疗时更易发生肝损伤[11],高HBV载量者风险性可能更大[12]。恩替卡韦抗病毒作用强大。本研究中,A组ATDH发生率为31.7%,明显高于B组的24.6%或C组的7.4%,提示抗结核治疗的基础上加用恩替卡韦抗病毒优于单纯化疗和预防性保肝治疗,ATDH的发生率降低。
肝损伤的严重程度和所使用的药物具有一定的相关性[13-15]。本研究提示抗病毒治疗降低了严重肝损伤的发生率。急性重症ATDH发生率远低于相关报道[18,19]。
[1]中华医学会肝病学分会和感染病学分会.慢性乙型肝炎防治指南(2015年版).实用肝脏病杂志,2016,19(3):Ⅴ-ⅩⅩⅢ.
[2]中华医学会结核病学分会.肺结核诊断和治疗指南.中华结核和呼吸杂志,2001,24(2):70-74.
[3]Elmorsy E,Attalla SM,Fikry E,et al.Adverse effects of antituberculosisdrugson HepG2 cellbioenergetics.Hum Exp Toxicol,2016[ahead of print].
[4]Jeong I,Park JS,Cho YJ,et al.Drug-induced hepatotoxicity of anti-tuberculosis drugs and their serum levels.J Korean Med Sci,2015,30(2):167-172.
[5]Heinrich MM,Zembrzuski VM,Ota MM,et al.Factors associated with anti-TB drug-induced hepatotoxicity and genetic polymorphisms in indigenous and non-indigenous populations in Brazil.Tuberculosis(Edinb),2016,101:15-24.
[6]Ji GY,Wang Y,Wu SQ,et al.Association between TXNRD1 polymorphisms and anti-tuberculosis drug-induced hepatotoxicityin a prospective study.Genet Mol Res,2016,5 (3)[ahead of print].
[7]Gupta VH,Singh M,AmarapurkarDN,etal.Association of GST null genotypes with anti-tuberculosis drug induced hepatotoxicity in Western Indian population.Ann Hepatol,2013,2(6):959-965.
[10]de Castro L,do Brasil PE,Monteiro TP,et al.Can hepatitis B virus infection predict tuberculosis treatment liver toxicity Development of a preliminary prediction rule.Int J Tuberc Lung Dis,2010,14(3):332-340.
[11]Wong WM,Wu PC,Yuen MF,et al.Antituberculosis drugrelated liver dysfunction in chronic hepatitis B infection.Hepatology,2000,31(1):201-206.
[12]Saha A,Shanthi FXM,Winston AB,et al.Prevalence of hepatotoxicity from antituberculosis therapy:A five-year experience from south India.J Prim Care Community Health,2016,7(3):171-174.
[13]朱育银,郑春玉,叶春娟,等.短程化疗中乙型肝炎病毒标志物阳性对肝功能影响及处理.中国防痨杂志,2004,26:50-52.
[14]许东,赵满芝,孙登顺,等.87例肺结核合并HBV携带者患者抗结核治疗的回顾性分析.中西医结合肝病杂志,2013,23(2):112-113.
[15]Liu YM,Cheng YJ,Li YL,et al.Antituberculosis treatment and hepatotoxicity in patients with chronic viral hepatitis.Lung,2014,192(1):205-210.
[16]Shang P,Xia Y,Liu F,et al.Incidence,clinical features and impact on anti-tuberculosis treatment of anti-tuberculosis drug induced liver injury (ATLI) in China.PLoS One,2011,6(7):e21836.
[17]Abera W,Cheneke W,Abebe G.Incidence of antituberculosis-drug-induced hepatotoxicity and associated risk factors among tuberculosis patients in Dawro Zone,South Ethiopia:A cohort study.Int J Mycobacteriol,2016,5(1):14-20.
[18]王晓丽,虞朝辉,陈韶华,等.药物性肝病临床特征及预后分析.中华内科杂志.2008,47(5):385-388.
(收稿:2017-02-23)
(本文编辑:陈宗炳)
Clinical observation of entecavir in prophylactic effect of antituberculosis-drug-induced hepatotoxicity in patients with chronic hepatitis B virus carrier and pulmonary tuberculosis
LI Kui,Ran Renyu,Jiang Zicheng,et al.Department of Infectious Diseases,Central Hospital,Ankang 725000,Shaanxi Province
Hepatitis B;Pulmonary tuberculosis;Entecavir;Antituberculosis-drug-induced hepatotoxicity
10.3969/j.issn.1672-5069.2017.05.027
李奎,男,36岁,硕士研究生,主治医师。主要从事结核病诊断与治疗研究。E-mail:42131642@qq.com
杨才勇,E-mail:1141665079@qq.com