芦丁在水溶液中的降解动力学研究△
2017-09-21霍红娜王萌孙立丽张慧杰任晓亮邓雁如戚爱棣
霍红娜,王萌,孙立丽,张慧杰,任晓亮*,邓雁如,戚爱棣
(1.天津中医药大学 中药学院,天津 300193;2.天津中医药大学 中医药研究院,天津 300193)
·基础研究·
芦丁在水溶液中的降解动力学研究△
霍红娜1,王萌2,孙立丽1,张慧杰1,任晓亮1*,邓雁如1,戚爱棣1
(1.天津中医药大学 中药学院,天津300193;2.天津中医药大学 中医药研究院,天津300193)
目的:研究芦丁水溶液在不同的pH、温度、离子强度、初始浓度条件下降解反应的动力学特征。方法:采用高效液相色谱法考察不同条件下芦丁含量随时间的变化,利用化学反应动力学的方法计算芦丁在不同环境下的降解反应动力学参数,预测其半衰期(t1/2)和活化能。结果:芦丁在不同环境条件下的降解反应均遵循一级动力学规律,在pH=3环境中最为稳定,强酸碱性条件下较容易降解,pH=9时的室温条件下半衰期为57.75h,活化能为39.3kJ·mol-1,随着离子强度的增加降解速率也随之加快,但初始浓度对其降解影响不大。结论:芦丁在酸性水溶液中较为稳定,随着pH的增大降解速率逐渐加快,呈现pH和温度依赖型,提示芦丁的使用和保存适宜在低温偏酸性条件下,避免碱性环境和高温条件。
芦丁;水溶液;降解动力学
芦丁(Rutin),又名芸香苷、维生素P、紫槲皮苷,是槲皮素(Quercentin)的3-O-芸香糖苷,属于黄酮醇类。主要存在于豆科植物槐SophorajaponicaL.的花蕾(槐米)、果实(槐角),芸香科植物芸香RutagraveolenslensL.全草,金丝桃科植物红旱莲HypericumascyronL.全草及蓼科植物荞麦FagopyrumesculentumMoench的籽苗中。研究表明,芦丁具有抗氧自由基活性[1]、抗脂质过氧化[2]、血管保护[3]、抗菌[4]、神经保护[5]、提高免疫力[6]、抗肿瘤[7]、降糖[8]、促进泌乳[9]、肾保护[10]等多种活性,临床上广泛用于防止脑出血、高血压等心脑血管疾病。由于芦丁为黄酮苷类化合物,其在水溶液中苷键可能发生水解,酚羟基可能被氧化而降解。本实验依照ICH指导原则,采用化学反应动力学方法研究了芦丁水溶液在不同pH、温度、离子强度及初始浓度等条件下的降解规律,以期为含有芦丁的药物的合理应用提供参考依据。
1 仪器和试剂
1.1试剂和药品
芦丁对照品(中国食品药品检定研究院,批号:100080-200707);甲醇(色谱纯,SPECTRO,美国TEDIA);纯水(由Milli-Q纯水器制备);甲酸(色谱纯,美国TEDIA);NaOH(分析纯,天津市北方天医化学试剂厂);HCl(分析纯,天津化学试剂一厂)。
1.2仪器
Waters高效液相色谱系统(600EHPLCpump,2487DualλAbsorbanceDetecter,Empower色谱工作站);AX205分析天平(瑞士METTLERTOLEDO公司);XW-80A微型旋涡混合仪(上海沪西分析仪器厂);恒温水浴(天津市泰斯特仪器有限公司)。
2 降解规律的研究
2.1HPLC色谱条件
色谱柱:Agilent C18(150mm×4.6mm,5μm);流动相:0.1%甲酸-甲醇(58∶42,V/V);流速:1.0mL·min-1;检测波长:283nm;温度:25℃。在该色谱条件下,芦丁可在10min内完成检测(保留时间8.2min),降解产物不会干扰测定。配制系列浓度为0.2、0.5、1.0、2.0、5.0、10.0μg·mL-1的芦丁对照品溶液,按上述色谱条件测定,以峰面积(Y)为纵坐标,浓度(X,μg·mL-1)为横坐标进行线性回归,得回归方程:Y=1.1292×104X-2012(r=0.9996),结果表明峰面积在芦丁质量浓度0.2~10.0μg·mL-1线性关系良好。取质量浓度为2.0μg·mL-1的对照品溶液,重复进样6次,测得芦丁峰面积的RSD=0.8%,结果表明此法精密度良好。
2.2对照品溶液的制备
精密称取芦丁对照品6.3mg,置于10mL棕色量瓶中,用甲醇定容至刻度,摇匀,配制得到浓度为0.63mg·mL-1的芦丁储备液。
精密吸取上述芦丁储备液200μL,置于10mL棕色量瓶中,用甲醇定容至刻度,摇匀,配制得到浓度为12.6μg·mL-1的芦丁对照品溶液。
2.3芦丁稳定性研究
2.3.1pH值对稳定性的影响 为了考察pH值对芦丁稳定性的影响,采用HPLC测定了一段时间内芦丁在不同pH值水溶液中的含量变化,得到不同pH值下芦丁的降解动力学曲线并计算降解速率常数k。
2.3.1.1样品溶液的制备pH2~6水溶液:分别向100mL纯水中加入适量HCl,由精密pH计测定pH值,配制成pH2~6水溶液。
pH7水溶液:为纯水,由精密pH计测定pH值为7。
pH8~11水溶液:分别向100mL纯水中加入适量NaOH,由精密pH计测定pH值,配制成pH8~11水溶液。
精密吸取芦丁储备液(0.63mg·mL-1)200μL于10mL棕色量瓶中,用事先配制好的不同pH值的水溶液定容至刻度,摇匀即得,该样品溶液中芦丁的起始浓度为12.6μg·mL-1。
2.3.1.2样品的测定与结果 为了排除光照和温度的影响,所有芦丁样品均保存在棕色容量瓶中。经实验测定,芦丁在不同pH水溶液中的降解速率相差较大,当溶液pH在2~10时,样品室温放置,芦丁降解速度较为缓慢,因此将上述的样品放入80℃水浴中,每隔一定时间,精密吸取样品溶液10μL注入高效液相色谱仪,测定芦丁峰面积,计算样品中芦丁的含量。见图1。
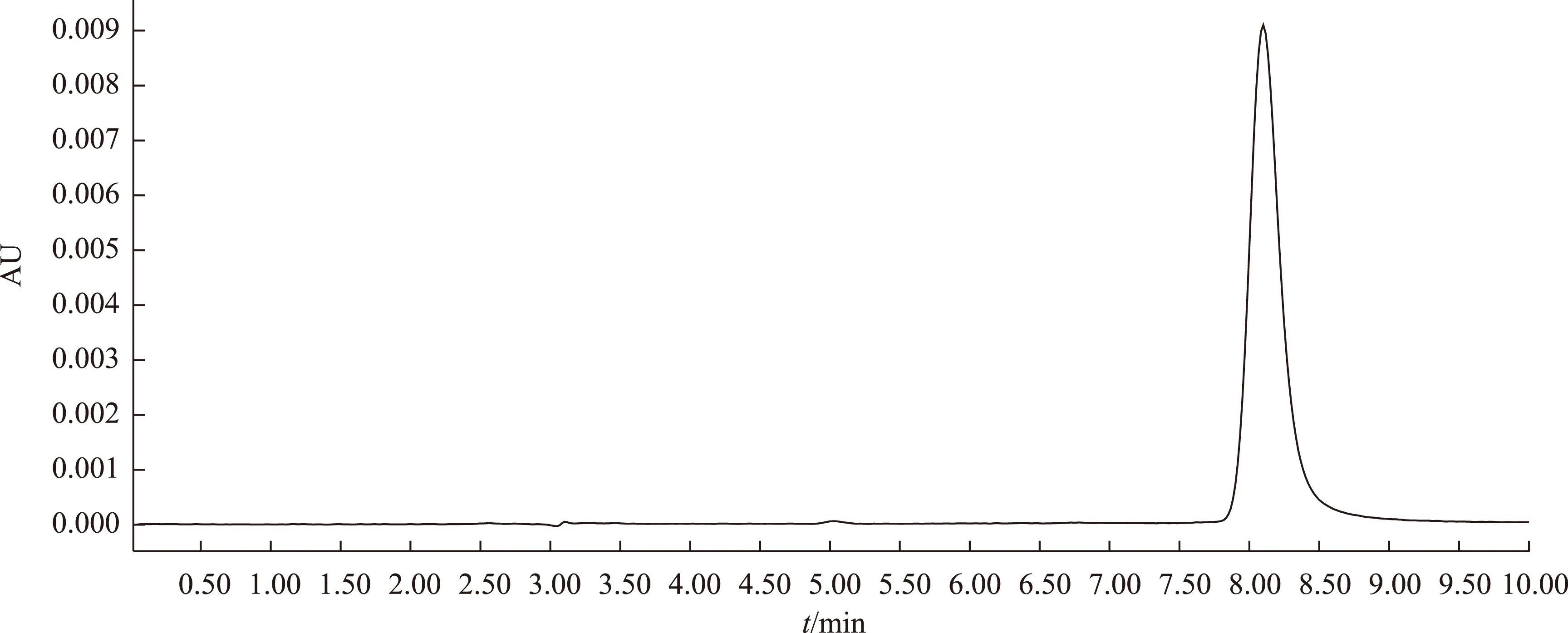
图1 芦丁液相色谱图
在芦丁质量浓度(12.6μg·mL-1)和温度恒定的条件下,以ln(Ct/C0)为纵坐标,水解时间为横坐标作图,得到在不同pH值条件下芦丁的降解动力学曲线,见图2。通过线性回归运算,得到在不同pH值条件下芦丁的降解速率常数及其他动力学参数,结果见表1。可以看出,所有实验条件下的一级反应动力学曲线的相关系数r<0.960,证明芦丁在不同pH值水溶液中的降解过程符合一级动力学。
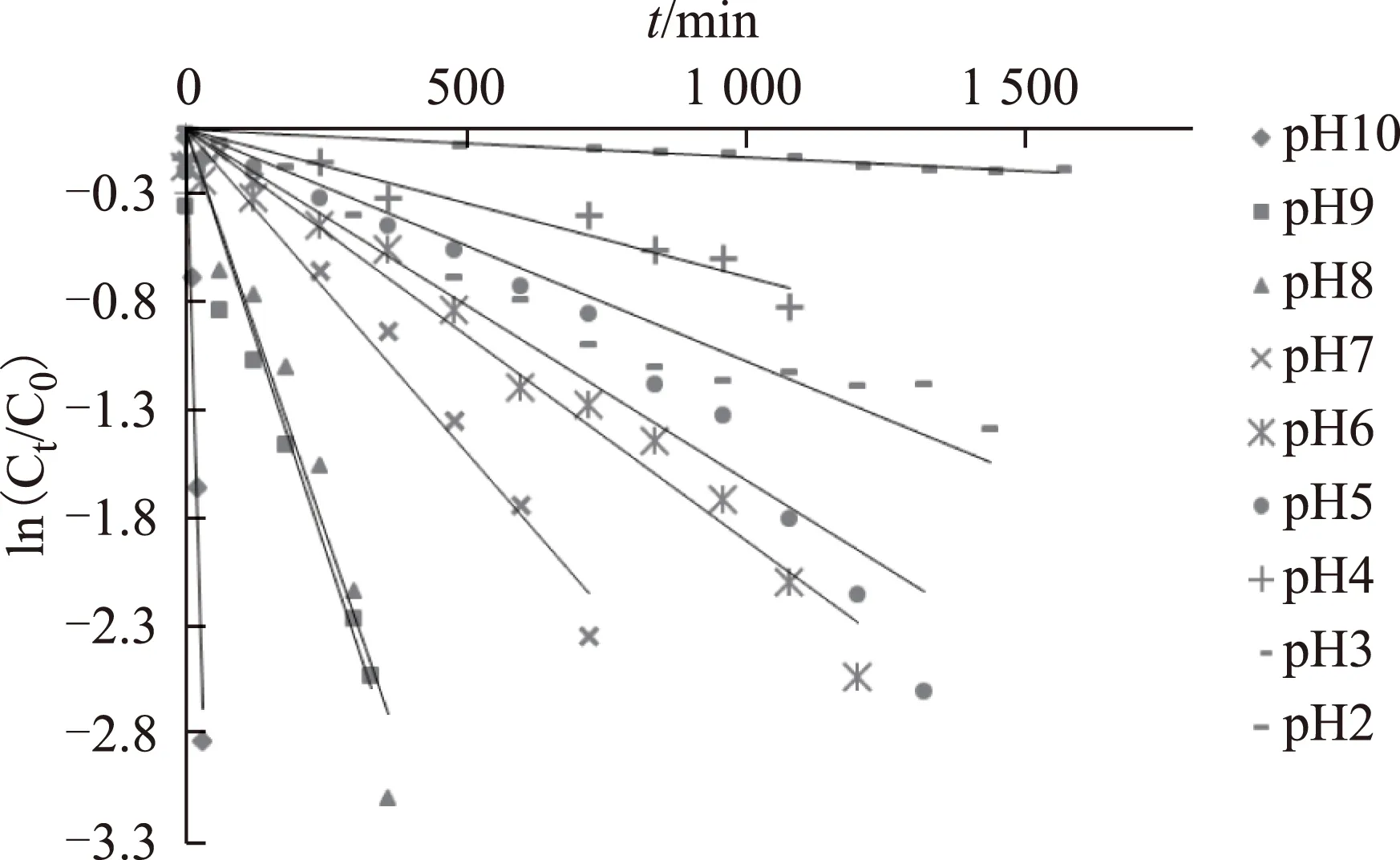
图2 不同pH值下芦丁的降解动力学曲线
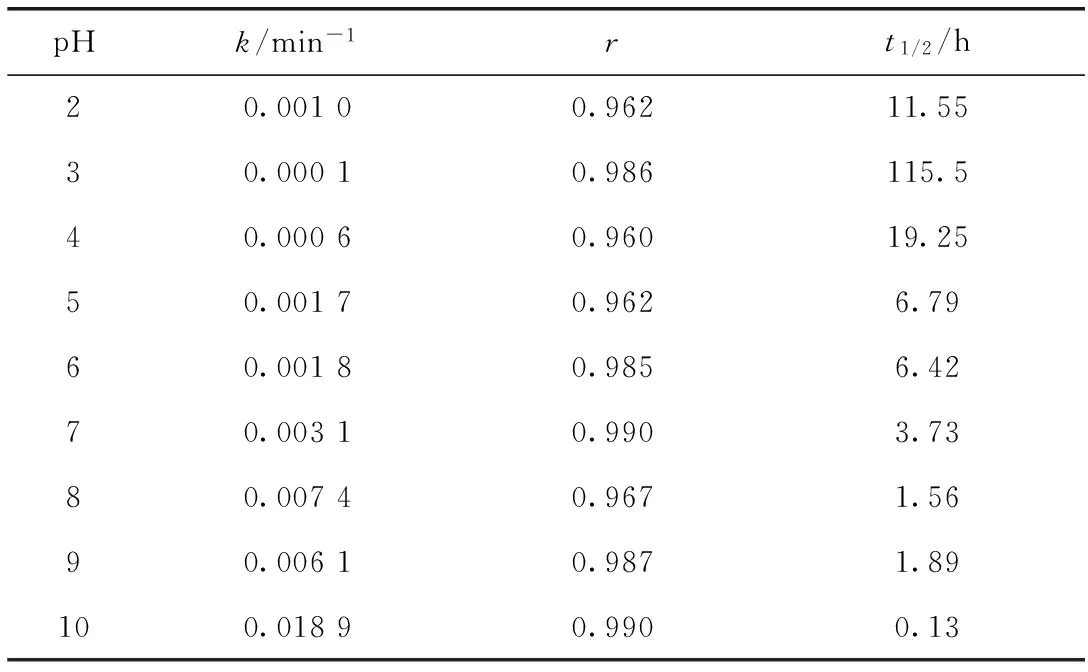
pHk/min-1rt1/2/h20.00100.96211.5530.00010.986115.540.00060.96019.2550.00170.9626.7960.00180.9856.4270.00310.9903.7380.00740.9671.5690.00610.9871.89100.01890.9900.13
为了更直观地表示pH对芦丁在水溶液中降解速率的影响,以ln(k)为纵坐标,pH值为横坐标作图,得到pH值与芦丁降解速率的关系图(见图3)。可知芦丁在酸性条件下(pH=3)比较稳定,在碱性条件下,特别是强碱条件下易降解。推测出水解反应可能是氢氧根离子催化下的反应。在pH 3~10下,随着pH的增大,降解速率加快,表明碱性溶液中的降解反应可能是氢氧根离子的催化作用;且在pH 2~3下,降解速率随pH的增加而降低,表明在酸性溶液中,芦丁也会发生降解反应,可能是氢离子的催化作用,但是反应强度明显弱于碱性条件下。

图3 80 ℃下芦丁在不同pH值下降解速率常数比较
2.3.2 温度对稳定性的影响
2.3.2.1 样品溶液的制备 pH 10水溶液的配制:同2.3.1.1项下的方法。
精密吸取芦丁储备液(0.63 mg·mL-1)200 μL于10 mL棕色量瓶中,用pH 10水溶液定容至刻度,摇匀即得,该样品溶液中芦丁的起始浓度为12.6 μg·mL-1。
2.3.2.2 样品的测定与结果 将配制好的样品溶液分别放置于70、80、90 ℃的恒温水浴中,每隔一定时间,精密吸取样品溶液20 μL注入高效液相色谱仪,测定芦丁峰面积,计算样品中芦丁的含量。
以ln(k)为纵坐标,1/T为横坐标作图,得到温度对芦丁降解速率的影响,如图4所示,通过阿仑尼乌斯方程可计算降解反应的活化能为39.3 kJ·mol-1。

图4 不同温度下芦丁的降解速率常数图
2.3.3 离子强度对稳定性的影响
2.3.3.1 样品溶液的制备 pH 10水溶液的配制:同2.3.1.1项下的方法。
精密吸取芦丁储备液(0.63 mg·mL-1)200 μL于10 mL棕色量瓶中,用pH 10水溶液定容至刻度,摇匀得样品1;精密吸取芦丁储备液(0.63 mg·mL-1)200 μL于10 mL棕色量瓶中,加入含有0.5 mol·L-1NaCl的 pH 10水溶液定容至刻度,摇匀得样品2。
2.3.3.2 样品的测定与结果 将芦丁样品保存在棕色容量瓶中,室温放置。每隔一定时间,分别精密吸取上述各样品溶液20 μL注入高效液相色谱仪,测定芦丁峰面积,计算样品中芦丁的含量。
结果表明,芦丁在pH 10水溶液和加入0.5 mol·L-1NaCl的水溶液中的降解速率分别为0.009 7、0.024 7 h-1,可以证明Na+、Cl-对芦丁的水解反应有一定的影响,离子的存在可使芦丁的降解速率增加155%,降解反应变快。
2.3.4 初始浓度对稳定性的影响
2.3.4.1 样品溶液的制备 pH 10水溶液的配制:同2.3.1.1项下的方法。
精密吸取芦丁储备液(0.63 mg·mL-1)100、200、400 μL分别置于10 mL棕色量瓶中,用pH 10水溶液定容至刻度,摇匀即得,各样品溶液中芦丁的起始浓度为对照品浓度的6.3、12.6、25.2 μg·mL-1。
2.3.4.2 样品的测定与结果 将芦丁样品保存在棕色容量瓶中,室温放置。每隔一定时间,精密吸取样品溶液20 μL注入高效液相色谱仪,测定芦丁峰面积,计算样品中芦丁的含量。
对降解结果加以分析,以降解速率常数对3个浓度的样品浓度进行作图,结果见图5。由图5可知,芦丁的起始浓度不同,但反应速率略微增大,反应物初始浓度对反应速率的影响并不明显。

图5 初始浓度对芦丁降解速率的影响
3 结论
研究表明芦丁在多种物理、化学环境中均不稳定,且在各条件下的水解作用均遵循(伪)一级动力学过程。其降解过程呈现出明显的pH及温度依赖性,且初始浓度对降解速率的影响不明显。
随着Na+及Cl-的引入,芦丁在碱性条件下的降解反应速率加快,通常认为,离子强度的变化对非电解质的反应影响较小,而本实验的结果可能是因为丰富离子存在可促进OH-进攻芦丁,而促使其
氧化降解所致。
芦丁的降解速率是pH依赖型的。在强酸及碱性环境中均不稳定,在pH=3水溶液环境中,芦丁的稳定性最强,随着溶液碱性的增加,降解反应的速度也明显加快,推测在酸性条件下可发生苷键的水解,而在碱性条件下发生氧化及水解反应。实验结果还表明,随着温度升高,芦丁降解反应速度加快,利用阿伦尼乌斯方程计算其在pH=10的条件下反应活化能为39.3 kJ·mol-1,说明芦丁在碱性条件下易降解,该反应可在室温下发生。
因此,芦丁及含有芦丁的相关药物应该在低温条件下保藏,在开发、生产及使用含有芦丁的药物时应使用弱酸性的条件,并控制溶剂中存在的离子浓度,避免芦丁的降解。
[1] 王胜利,孙金香,席改卿,等.槐花中芦丁超声辅助提取工艺优化及抗氧化活性研究[J].食品工业科技,2012,33(18):306-308,381.
[2] 段煜,杜宗良,吴大诚.芦丁脂肪酸酯对Fe2+诱导的卵磷脂氧化的抑制作用[J].天然产物研究与开发,2009,21(4):586-588.
[3] 黄金珠.芦丁对大鼠肠缺血再灌注损伤的保护作用[J].中国现代药物应用,2012,6(16):131-132.
[4] 杨丹,郝再彬,胡淑田,等.光照对芦丁稳定性及抑菌活性的影响[J].应用与环境生物学报,2011,17(2):223-226.
[5] 何国荣,成银霞,穆鑫,等.木犀草素联合芦丁抗6-羟多巴胺诱导的帕金森病大鼠震颤及神经保护作用[J].中国药理学通报,2012,28(5):626-632.
[6] 汶希,潘华山,冯毅翀,等.芦丁对耐力训练大鼠免疫和抗氧化功能的影响[J].河北北方学院学报(自然科学版),2011,27(5):67-70,74.
[7] 占平,彭新生,徐秀梅,等.丹皮酚和芦丁的联合抗癌研究[J].中华中医药学刊,2010,28(8):1710-1712.
[8] 王明华,陈松瑞,郭思楠,等.芦丁对大鼠体内外葡萄糖苷酶活性的影响[J].中国煤炭工业医学杂志,2009,12(8):1276-1277.
[9] 郭旭东,刁其玉,王月影,等.芦丁促进大鼠泌乳性能的研究[J].动物营养学报,2010,22(6):1775-1782.
[10] 王素琴,汤玲君,王艳.芦丁对糖尿病肾病大鼠的保护作用及其机制探讨[J].医学研究杂志,2012,41(10):144-148.
Studies on Degradation Kinetics of Rutin in Aqueous Solution
HUO Hongna1,WANG Meng2,SUN Lili1,ZHANG Huijie1,REN Xiaoliang1*,DENG Yanru1,QI Aidi1
(1.College of Traditional Chinese Medicine,Tianjin University of Traditional Chinese Medicine,Tianjin 300193,China;2.Institute of Traditional Chinese Medicine,Tianjin University of Traditional Chinese Medicine,Tianjin 300193,China)
Objective:To investigate the degradation kinetic characteristics of rutin in aqueous solution under different pH and temperatures.Methods:The concentration change of rutin in aqueous solution was determined by HPLC under different pH and temperatures.Base on the chemical reaction kinetic,the parameters of degradation kinetics were calculated under different conditions.The activation energy and half-life were evaluated.Results:The results indicated that thermal degradation kinetic model of rutin in aqueous solution follows first-order degradation kinetic process.The half-life period(t0.5)was 57.75 h under pH 9 in aqueous solution,and the energy of activation(Ea)was 39.3 kJ·mol-1.Conclusion:Rutin was more stable in acidic aqueous solution and low temperature condition.The degradation of rutin can be observed in strong alkali conditions.
Rutin;aqueous solution;degradation kinetics
国家自然科学基金面上基金(81473543)
] 任晓亮,副教授,研究方向:药物分析;Tel:(022)59596221,E-mail:xiaoliang_ren@sina.com
10.13313/j.issn.1673-4890.2017.1.013
2016-05-09)
*[
