替吉奥联合康莱特注射液二线治疗晚期胰腺癌临床观察
2017-09-15,,,,,
, , ,,,
(郑州人民医院肿瘤内科,河南 郑州 450053)
替吉奥联合康莱特注射液二线治疗晚期胰腺癌临床观察
肖鹏,白桦,栗敏,李瑞君,刘桂举,梅家转
(郑州人民医院肿瘤内科,河南 郑州 450053)
目的探讨替吉奥联合康莱特注射液在晚期胰腺癌二线治疗中的疗效和安全性。方法44例含吉西他滨一线化疗失败的晚期胰腺癌患者分别给予单药替吉奥(单药组21例)、替吉奥联合康莱特(联合组23例)治疗,评价2组患者的疗效和不良反应。结果单药组和联合组患者的疾病控制率分别为52.4%和60.9%,差异无统计学意义(P>0.05)。单药组和联合组患者的中位疾病无进展生存时间分别为2.3个月和3.1个月,差异有统计学意义(P<0.05)。中位生存时间分别为6.0个月和6.7个月,差异无统计学意义(P>0.05)。2组患者不良反应均主要为白细胞减少、血小板减少、贫血、恶心、呕吐、腹泻。结论替吉奥联合康莱特注射液二线治疗晚期胰腺癌比替吉奥单药更能延长患者的疾病无进展生存时间,且安全性好。
胰腺肿瘤;二线治疗;替吉奥;康莱特注射液
胰腺癌是一种严重的致死性消化系统恶性肿瘤,5 a生存率低于5%。根据美国癌症协会最新公布的数据,在全世界范围内胰腺癌导致的死亡居第4位[1]。虽然FOLFIRINOX方案已经成为晚期胰腺癌的标准治疗方案,但严重的不良反应限制了其在临床上的应用[2]。对身体状况良好的患者吉西他滨联合紫杉醇也是不错的选择[3]。对体质差的患者可选择吉西他滨单药、氟尿嘧啶类药物或最佳支持治疗[4]。吉西他滨一线治疗失败的患者可给予氟尿嘧啶为基础的二线治疗[4]。替吉奥二线单药治疗晚期胰腺癌客观缓解率15%,中位疾病无进展生存时间为2.0个月,中位生存时间为4.5个月[5],替吉奥联合奥沙利铂、顺铂、亚叶酸钙等患者获益不明显,且不良反应加重,需进一步探讨新的治疗方案[6-8]。本研究观察替吉奥联合康莱特治疗晚期胰腺癌的疗效及不良反应。现报道如下。
1 资料与方法
1.1病例资料入组我院2009年10月至2014年7月收治的经细胞学或组织学确诊晚期胰腺癌患者44例,均为吉西他滨为主的方案一线化疗失败者,其中男26例,女18例;年龄42~75岁,中位年龄61岁;至少有1处可测量病灶;ECOG评分≤2分;重要器官功能基本正常。每周期化疗后复查血常规、肝功能、肾功能等,根据CT或MRI等行疗效评价。
1.2治疗方法44例患者随机分为2组,单药组21例给予单药替吉奥,联合组23例给予替吉奥联合康莱特治疗。单药组患者口服替吉奥,每次40~60 mg(体表面积≤1.25 m2时给予40 mg,1.25~<1.5 cm2时给50 mg,≥1.5 cm2时给予60 mg),2次/d,连续口服28 d,休息14 d,6周为1周期)。联合组患者口服替吉奥的同时给予康莱特注射液200 mL,静脉滴注,1次/d,连用21 d。每周期评价疗效。化疗过程中给予止吐、保护胃黏膜等治疗。根据患者不良反应情况进行剂量减少或推迟治疗。
1.3评价标准按实体瘤疗效评价标准[9]分为完全缓解(CR)、部分缓解(PR)、病变稳定(SD)、疾病进展(PD)。以CR + PR+ SD计算疾病控制率。药物不良反应采用常见不良事件评价标准[10]评价,分为0~Ⅳ度。1.4随访疾病无进展生存时间为从接受治疗开始到肿瘤客观进展时间或死亡时间。生存时间指从接受治疗开始到因任何原因死亡或随访截止时间。
1.5统计学处理采用SPSS 21.0进行统计,计数资料采用百分数表示,比较采用χ2检验,生存情况采用Kaplan-Meier法及log rank检验分析,检验水准α=0.05。
2 结果
2.1近期疗效单药组和联合组患者的疾病控制率分别为52.4%和60.9%,差异无统计学意义(P>0.05)。见表1。
2.2生存分析单药组和联合组患者的中位疾病无进展生存时间分别为2.3(95%CI为0.8~3.8)个月和3.1(95%CI为2.2~4.0)个月,差异有统计学意义(P<0.05)。中位生存时间分别为6.0(95%CI为3.8~7.2)个月和6.7(95%CI为 4.3~9.1)个月,差异无统计学意义(P>0.05)。见图1、2。
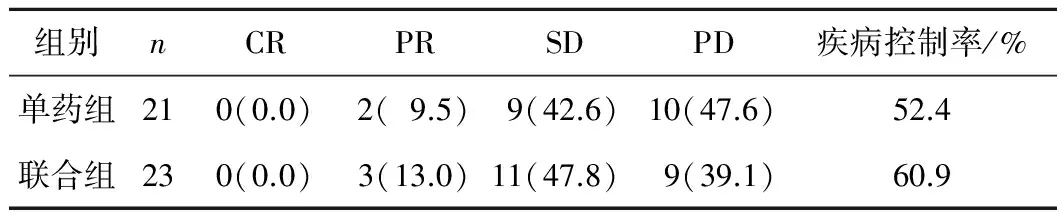
表1 2组近期疗效比较 n(%)
注:2组疾病控制率比较,χ2=0.322,P=0.570
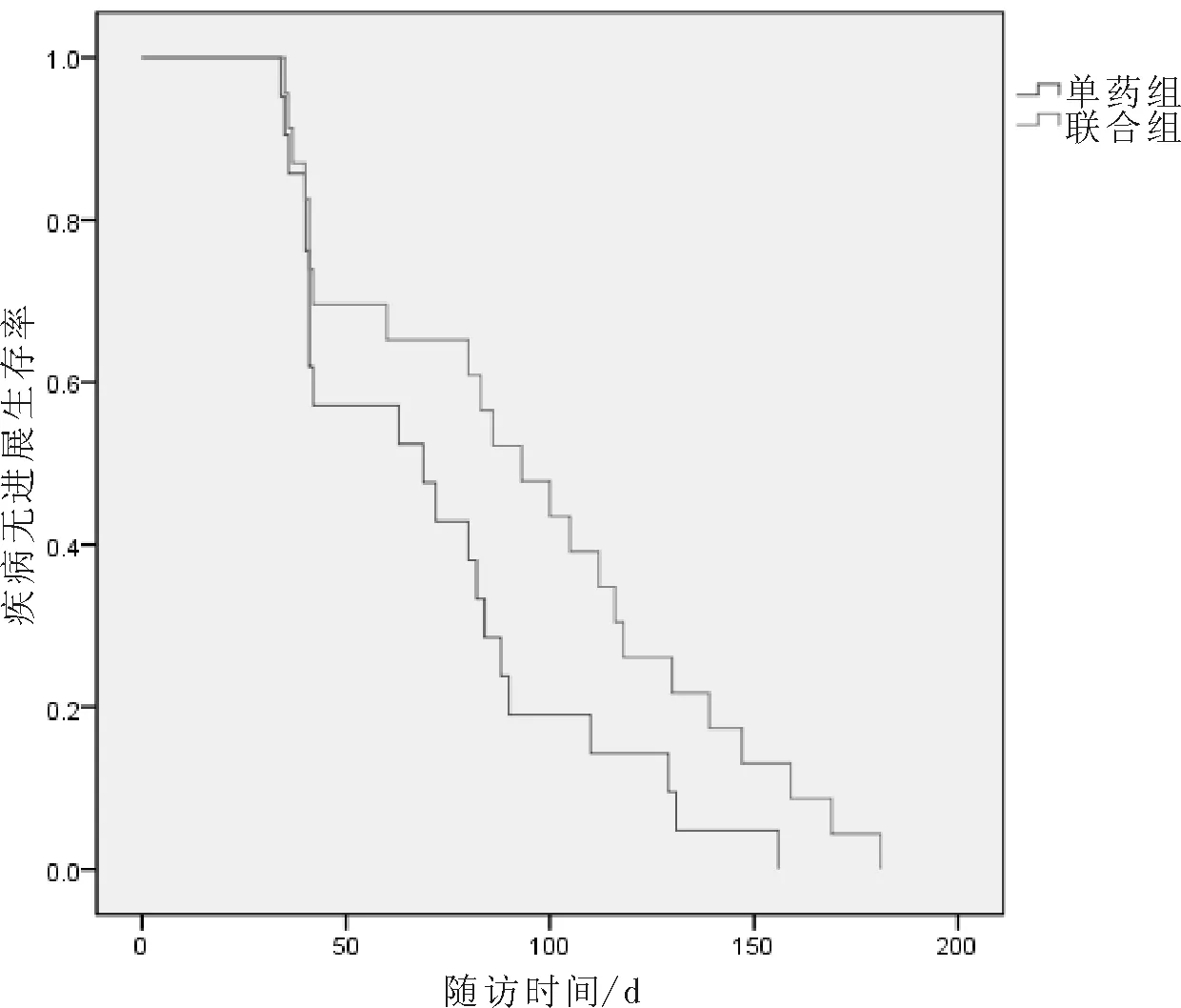
图1 2组患者疾病无进展生存曲线比较

图2 2组患者总生存曲线比较
2.3不良反应2组患者不良反应均主要为白细胞减少、血小板减少、贫血、恶心、呕吐、腹泻。2组各不良反应发生率比较差异无统计学意义(P>0.05)。见表2。

表2 2组不良反应比较
3 讨论
胰腺癌恶性程度高、预后差。大约60%的患者在诊断时已出现远处转移,不能行根治性手术,中位总生存时间仅为6~9个月[11-12]。中医药是胰腺癌综合治疗重要辅助手段,有助于增强机体的免疫力,降低放疗、化疗的不良反应,提高生活质量,并有可能延长生存时间[13]。
康莱特注射液主要成分为薏苡仁油,对肺癌、胃癌等多种恶性肿瘤有不错的效果[14-15]。可提高CD3+、CD4+、CD8+、CD4+/CD8+及NKT细胞活性,减少化疗的不良反应,改善患者KPS评分,提高有效率及疾病控制率。姚小健[16]的研究显示替吉奥联合康莱特注射液姑息治疗老年晚期胰腺癌,可改善KPS评分、体质量,控制疼痛。陈艳[17]的研究表明康莱特注射液治疗晚期胰腺癌可提高临床疗效、改善患者的生活质量、降低化疗不良反应。
本研究结果显示,替吉奥胶囊联合康莱特注射液与替吉奥单药比较可延长疾病无进展生存时间(P<0.05);疾病控制率、总生存时间方面有提高的趋势,但差异无统计学意义(P>0.05),这可能与本研究样本量少、单中心、回顾性研究有关。因此还需要进一步行大规模前瞻性随机对照的临床研究。
[1] SIEGEL R,MA J,ZOU Z,et al.Cancer statistics,2014 [J].CA Cancer J Clin, 2014,64(1): 9-29.
[2] CONROY T,DESSEIGNE F,YCHOU M,et al.FOLFIRINOX versus gemcitabine for metastatic pancreatic cancer [J].N Engl J Med,2011,364(19): 1817-1825.
[3] VON HOFF DD,ERVIN T,ARENA FP,et al.Increased survival in pancreatic cancer with nab-paclitaxel plus gemcitabine [J].N Engl J Med,2013,369(18): 1691-1703.
[4] 中国临床肿瘤学会胰腺癌专业委员会.胰腺癌综合诊治中国专家共识(2014 年版) [J].临床肿瘤学杂志,2014,19(4): 358-370.
[5] MORIZANE C,OKUSAKA T,FURUSE J,et al.A phase Ⅱ study of S-1 in gemcitabine refractory metastatic pancreatic cancer [J].Cancer Chemother Pharmacol,2009,63(2): 313-319.
[6] OHKAWA S,OKUSAKA T,ISAYAMA H,et al.Randomised phase Ⅱ trial of S-1 plus oxaliplatinvsS-1 in patients with gemcitabine-refractory pancreatic cancer [J].Br J Cancer, 2015,112(9):1428-1434.
[7] KIM HJ,YUN J,KIM HJ,et al.Phase Ⅱ study of palliative S-1 in combination with cisplatin as second-line chemotherapy for gemcitabine-refractory pancreatic cancer patients [J].Oncol Lett, 2012,3(6):1314-1318.
[8] GE F,XU N,BAI Y,et al.S-1 as monotherapy or in combination with leucovorin as second-line treatment in gemcitabine-refractory advanced pancreatic cancer: a randomized,open-label,multicenter,phase Ⅱ study [J].Oncologist, 2014,19(11): 1133-1134.
[9] 孙燕,石元凯.临床肿瘤内科手册[M].5版.北京; 人民卫生出版社,2007:150-153.
[10]皋文君,刘砚燕,袁长蓉.国际肿瘤化疗药物不良反应评价系统——通用不良反应术语标准4.0版 [J].肿瘤,2012,32(2): 142-144.
[11]JEMAL A,BRAY F,CENTER MM,et al.Global cancer statistics [J].CA Cancer J Clin, 2011,61(2): 69-90.
[12]WITKOWSKI ER,SMITH JK,TSENG JF.Outcomes following resection of pancreatic cancer [J].J Surg Oncol,2013,107(1):97-103.
[13]LI B,GAN R,YANG Q,et al.Chinese Herbal Medicines as an Adjunctive Therapy for Unresectable Pancreatic Cancer: A Systematic Review and Meta-Analysis[J].Evid Based Complement Alternat Med,2015,2015:350730.
[14]秦银忠.康莱特配合放疗对非小细胞肺癌的疗效及患者免疫功能的影响[J].实用癌症杂志,2016,31(4): 578-580.
[15]李冠雄,马任远,李军,等.康莱特联合DP方案对Ⅳ期胃癌的疗效及免疫功能的影响[J].中国药业,2015,24(24): 40-42.
[16]姚小健.替吉奥联合康莱特注射液治疗老年晚期胰腺癌临床观察 [J].肿瘤基础与临床,2015,28(4): 350-352.
[17]陈艳.康莱特注射液联合吉西他滨治疗晚期胰腺癌患者安全性和有效性的系统评价 [J].中医临床研究,2015,7(16): 24-28.
EffectofSecond-lineTreatmentwithS-1andKanglaiteInjectionforPatientswithAdvancedPancreaticCancer
XIAO Peng,BAI Hua,LI Min,LI Ruijun,LIU Guiju,MEI Jiazhuan
(DepartmentofOncology,ZhengzhouPeople’sHospital,Zhengzhou450053,China)
ObjectiveTo evaluated the efficacy and toxicities of kanglaite injection and S-1 in the second-line treatment of patients with pancreatic cancer.MethodsForty-four gemcitabine-refractory patients with advanced pancreatic cancer were divided into two groups.Twenty-one patients in the S-1 group was treated with S-1 alone,and 23 patients in the S-1 and kanglaite group was treated with S-1 and kanglaite injection.The efficacy and toxicities of the two groups were compared.ResultsThe disease control rates were 52.4% and 60.9% in the S-1 group and the S-1 and kanglaite group,respectively (P>0.05).The median progression-free survival was 2.3 months in the S-1 group,and was 3.1 months in the S-1 and kanglaite goup (P<0.05).The median overall survival was months 6.0 in the S-1 group and 6.7 months in the S-1 and kanglaite group (P>0.05).The major toxicities were leukopenia,thrombocytopenia,anemia,nausea,vomiting,diarrhea.ConclusionS-1 and kanglaite injection as second-line treatment is effect and safe in the treatment of advanced pancreatic cancer,and can prolong the progression-free survival of patients with advanced pancreatic cancer.
pancreatic cancer; second-line treatment; S-1; kanglaite injection
肖鹏(1980-),男,硕士,主治医师,主要从事恶性肿瘤的诊断及内科治疗工作。E-mail:zzrmyyxiaopeng@sina.com
梅家转(1966-),男,博士,主治医师,主要从事恶性肿瘤的诊断、内科治疗及生物治疗工作。E-mail:zzrmyymjz@sina.com
10.3969/j.issn.1673-5412.2017.04.005
R735.9;R730.58
A
1673-5412(2017)04-0289-03
2016-06-12)
