免疫检查点抑制剂治疗胃肠道恶性肿瘤最新研究进展
2017-09-08郑磊贞朱雪茹
郑磊贞,朱雪茹
上海交通大学医学院附属新华医院肿瘤科,上海200092
免疫检查点抑制剂治疗胃肠道恶性肿瘤最新研究进展
郑磊贞,朱雪茹
上海交通大学医学院附属新华医院肿瘤科,上海200092

郑磊贞 教授
20世纪90年代初,人类第一个肿瘤相关抗原在黑色素瘤中被发现,使得肿瘤细胞特异性细胞毒性CD8+T淋巴细胞成为癌症治疗新途径[1]。随后,多种免疫治疗手段如白细胞介素-12、基因治疗、树突状细胞等不断出现,然而,这些免疫治疗手段在恶性肿瘤治疗中却未能获得令人满意的疗效。近几年,免疫检查点抑制剂在恶性黑色素瘤和非小细胞肺癌中的应用及其惊人的疗效,使得免疫介导的抗癌治疗战略获得复兴。
1 免疫检查点及其与恶性肿瘤关系
作为细胞免疫的主要效应细胞,T细胞在机体抗肿瘤免疫过程中是核心执行者。而T细胞表面的负性共刺激分子介导的免疫逃逸则是导致恶性肿瘤发生、发展及不良预后的原因之一。T细胞的活化需要两个关键信号:来自抗原递呈细胞表面的主要组织相容性复合体(MHC)-抗原肽与T细胞受体结合的第一信号;由抗原递呈细胞与T细胞表面的共刺激分子相互作用而产生的第二信号[2]。共刺激分子包括正性分子和负性分子,前者产生正性信号,从而促进淋巴细胞增殖、分化及细胞因子的分泌,反之,后者产生负性信号,削弱、限制及终止淋巴细胞的免疫应答。免疫检查点即指免疫系统中这些负性信号通路,其通过调节外周组织中免疫反应的持续性及强度,以避免组织损伤。
免疫检查点通路由配体和受体相互作用而调控,目前已发现的抑制性受体包括CTLA-4、PD-1/PD-L1、淋巴细胞活化基因-3分子(lymphocyte activation gene-3,LAG-3)及T细胞免疫球蛋白粘蛋白-3(T-cell immunoglobulin andmucin-domain-containingmolecule-3,TIM-3)等,其中CTLA-4是第一个应用于临床的T细胞免疫检查点,其次是PD-1/PD-L1[3]。
2 免疫检查点抑制剂
在肿瘤的发生、发展过程中,免疫检查点是产生免疫耐受的主要原因之一。在各种恶性肿瘤中,T细胞表面共刺激分子如CTLA-4、PD-1/PD-L1、LAG-3及TIM-3多异常高表达,诱导肿瘤抗原特异性T细胞失能、凋亡,从而引发免疫逃逸及免疫耐受。目前,研究与应用最广泛的免疫检查点是CTLA-4和PD-1/ PD-L1。最新研究结果表明,免疫检查点抑制剂尤其是伊匹单抗(ipilimumab)、替西木单抗(tremelimumab,CTLA-4抗体)及PD-1和PD-L1抗体(如nivolumab、pembrolizumab)显著增强了肿瘤患者局部免疫反应。
2.1 抗CTLA-4治疗
2.1.1 Tremelimumab Tremelimumab是全人源化的CTLA-4单克隆IgG2抗体,目前已经在黑色素瘤、肝癌等肿瘤中进行评估并显示出一定的抗肿瘤效果。2010年,一项II期临床研究评估了Tremelimumab对晚期胃/食管腺癌疗效[4]。该项研究共纳入18例患者,结果显示,1例部分缓解(PR),4例疾病稳定(SD),中位疾病进展时间(TTP)为2.83个月,中位生存期(OS)为4.83个月。该研究总体效果并不显著,但是获得PR的患者入组时存在肝、肺、胸膜、肾上腺、骨及多处淋巴结的多发转移,接受11程治疗后,OS超过32.7个月。该患者的显著疗效提示,Tremelimumab在某些特殊亚型患者中可以获得显著、持久疗效。
2.1.2 Ipilimumab Ipilimumab是人源化IgG1单克隆抗体,其首先在恶性黑色素瘤、肺癌及前列腺癌临床试验中疗效显著,成为第一个获批上市的免疫检查点抑制剂。一项关于Ipilimumab在不可切除或转移的胃/胃食管交界处癌患者中的多中心II期临床研究(NCT01585987),比较Ipilimumab与最佳支持治疗在一线化疗后患者中疗效。该研究共纳入了143例患者,随机分为试验组(Ipilimumab组)和对照组(支持治疗组)。目前部分试验数据在Clinical Trials.gov已记录(Table1),但具体的试验结果仍未报道。
2.2 抗PD-1治疗PD-1是免疫抑制性受体,主要表达在T细胞、B细胞及NK细胞等表面。该受体与其配体PD-L结合后,抑制T细胞活化、增殖,减少I L-2、IFN-及IL-10的分泌,发挥负性免疫调节作用[5]。
2.2.1 Pembrolizumab Pembrolizumab是高特异性人源化的PD-1单克隆IgG4抗体,在一项大型临床试验(KEYNOTE-001)中[6],对转移性黑色素瘤显示出显著的疗效,总有效率达38%,对非小细胞肺癌也显示出非凡的疗效。随后的各项试验结果均显示,Pembrolizumab在黑色素瘤和非小细胞肺癌中疗效很有前景,遂于2014年FDA批准用于晚期或不可切除对Ipilimumab耐药的黑素素瘤治疗,2015年FDA加速批准Pembrolizumab用于铂类为基础的化疗耐药且PD-L1阳性的晚期非小细胞肺癌治疗。
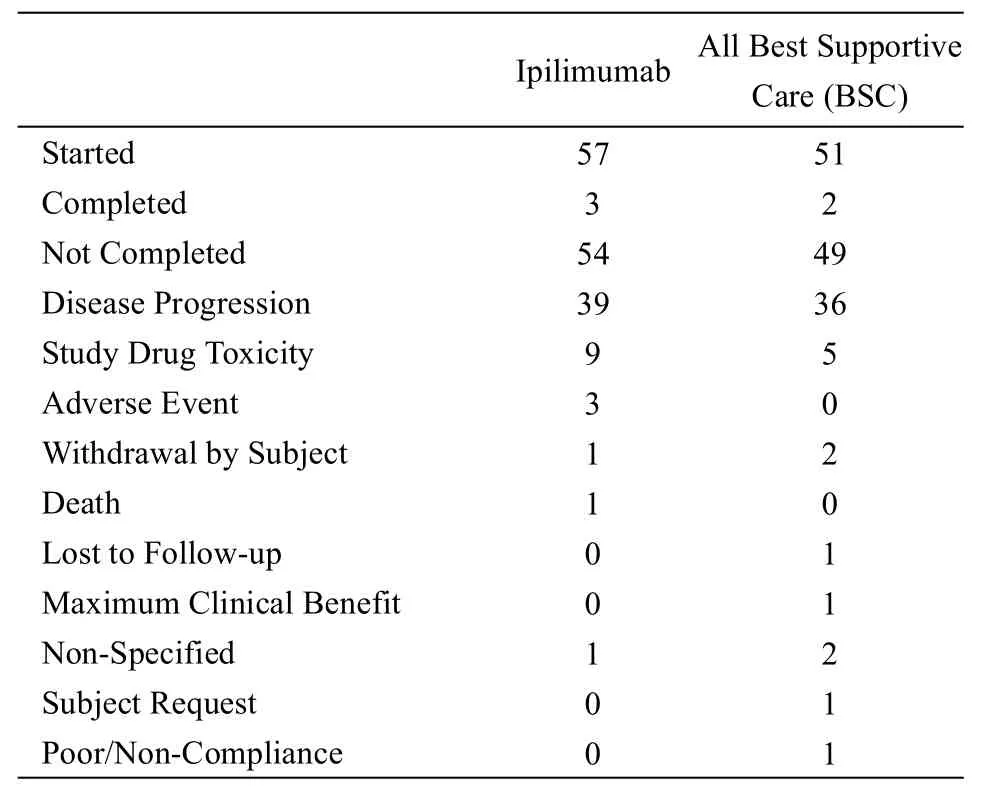
Table1.Theupdated dataof NCT01585987 study.
Le等[7]开展的一项II期临床试验,评估Pembrolizumab的临床疗效。该研究纳入41例转移性腺癌伴或不伴有错配修复基因缺陷(dMMR),其中11例为dMMR结直肠癌(CRC),21例pMMR(错配修复基因表达)CRC,9例dMMR非结直肠癌患者。研究结果提示,dMMR CRC患者免疫相关客观有效率(ORR)达40%,20周免疫相关的疾病无进展生存(PFS)率达78%,而pMMR CRC患者ORR为0%,20周PFS率为11%。伴dMMR非CRC患者ORR为71%,20周PFS率为67%。从该研究我们可以看出,MMR状态可以预测免疫检查点抑制剂Pembrolizumab的临床疗效。2016年1月21-23日ASCO-GI中口头报告了KEYNOTE-028研究[8]中PD-L1阳性食管癌队列研究结果,这是一项Ib期临床试验,旨在评估Pembrolizumab在PD-L1阳性晚期实体瘤中的疗效。该研究共纳入23例PD-L1阳性晚期食管癌患者,每2周接受1次Pembrolizumab 10mg/kg治疗,直至两年或肿瘤进展或不可耐受毒副反应。结果报道是,中位随访时间为7.1个月,不良反应可控,ORR为30%(均为PR),52%患者显示肿瘤缩小。根据目前研究数据,Pembrolizumab在抗肿瘤作用中前景可观。
目前,有关Pembrolizumab的多项研究陆续开展,如KEYNOTE-059研究采用Pembrolizumab单药或者联合化疗治疗晚期胃/胃食管交界处癌的II期临床实验,该项研究志愿者招募工作已结束,预计至2018年10月完成试验,目前尚无相关研究数据报道。III期临床研究(KEYNOTE-061)对比Pembrolizumab与紫杉醇治疗一线PF方案化疗失败或耐药的晚期胃/胃食管交界处腺癌疗效,目前正在志愿者招募中,计划纳入720例。KEYNOTE-180研究用Pembrolizumab单药治疗三线化疗后的晚期/转移的食管癌患者,该II期临床试验计划纳入100例患者,目前正在志愿者招募中。另一项III期临床研究项目(KEYNOTE-181),对比Pembrolizumab和多西他赛/紫杉醇/伊立替康单药治疗一线标准化疗后的晚期食管癌患者疗效,计划纳入600例患者,目前志愿者招募中。在结直肠肿瘤中,Pembrolizumab联合阿扎胞苷治疗化疗难治性转移性结直肠癌疗效的II期临床研究(NCT02260440)志愿者招募已完成,截止2019年11月完成。此外,大量类似研究尚在进行中。
2.2.2 Nivolumab Nivolumab是一种全人源化抗PD-1的IgG4单克隆抗体,其在2014年12月被FDA批准用于Ipilimumab耐药的晚期或不可切除黑色素瘤,2015批准用于铂类为基础化疗耐药的肺癌。2016年1月21-23日ASCO-GI中口头报告了CheckMate研究[9]最新结果,该研究旨在评估Nivolumab单药或联合Ipilimumab治疗晚期或转移性恶性肿瘤安全性及疗效。会议报道了Nivolumab单药治疗晚期胃/胃食管交界处癌患者的初步研究结果。该研究共纳入163例胃/胃食管交界处癌患者,其中Nivolumab单药治疗59例。在这59例病例中,ORR为14%,化疗难治性患者中,6个月生存率49%,12个月生存率36%,药物治疗未出现新的不良反应,毒副作用可耐受。该数据提示,Nivolumab单药治疗晚期胃/胃食管交界处癌安全、有效。
2.2.3 抗PD-L1治疗PD-L1是PD-1配体,广泛表达于活化的T细胞、巨噬细胞、树突状细胞及上皮细胞等,肿瘤可以通过高表达PD-L1而发生免疫逃逸。
2.3 Durvalumab Durvalumab(MEDI4736)是一种IgG1-Kappa类抗PD-L1单克隆抗体,目前该药物在各类肿瘤中疗效尚在评估中。一项有关Durvalumab的Ib/II期临床研究(NCT02340975)旨在对比Durvalumab联合Tremelimumab或单药治疗复发或转移性胃/胃食管交界处腺癌疗效及安全性。目前该项目正在志愿者招募中,计划纳入236例复发或转移性胃/胃食管交界处腺癌患者。有关Durvalumab治疗晚期结直肠癌疗效评估的II期临床研究(NCT02227667)目前也在志愿者招募中。
2.4 Avelumab Avelumab是一个全人源化IgG1抗PD-L1单抗,目前在胃肠肿瘤中,该药物正处于探索阶段。JAVELIN实体瘤Ib期临床试验数据公布,报道治疗晚期胃癌/胃食管交界处癌的安全性及临床活性。共纳入151例确诊胃癌/胃食管交界处癌患者(未选择PD-L1表达状态),分为一线维持治疗组(Mn)和二线治疗组(2L)。初步研究结果提示,Avelumab单药治疗晚期胃癌/胃食管结合部癌安全、有效。该研究是目前抗PD-L1药物治疗胃癌/胃食管结合部癌的最大规模研究[10]。
此外,抗PD-L1检查点药物(如BMS-936559、MPDL3280A等),在实体肿瘤包括胃肠道肿瘤中的疗效及安全性尚处于评估阶段。
3 总结
目前,肿瘤免疫治疗发展如火如荼,各类免疫检查点抑制剂疗效及安全性临床研究陆续开展。部分药物如Tremelimumab、Ipilimumab、Pembrolizumab及Nivolumab在早期临床试验中获得肯定,而确认可以选择免疫检查点抑制剂获益最大人群的生物标记物研究也将成为研究者的一大课题。相信,随着检查点抑制剂在消化道肿瘤中的不断深入研究,将其与化疗、放疗及其它靶向治疗的联合使用可为消化道肿瘤治疗带来突破性进展。
[1]Van Der Bruggen P,Traversari C,Chomez P,.A gene encoding an antigen recognized by cytolytic T lymphocyteson a humanmelanoma[J].Science,1991,254(538):1643-1647.
[2]Janeway CA,Bottom ly K.Signalsand signs for lymphocyte responses[J].Cell,1994,76(2):275-285.
[3]Mellman I,CoukosG,DranoffG.Cancerimmunotherapy comes of age[J].Nature,2011,480(7378):480-489.
[4]Ralph C,Elkord E,BurtDJ,.Modulation of lymphocyte regulation for cancer therapy:a phase II trial of tremelimumab in advanced gastric and esophageal adenocarcinoma[J].Clin Cancer Res,2010,16(5):1662-1672.
[5]Freeman GJ,Long AJ,IwaiY,.Engagementof the PD-1 immunoinhibitory receptorby anovelB7 fam ilymember leads to negative regulation of lymphocyte activation[J].J Exp Med, 2000,192(7):1027-1034.
[6]RobertC,RibasA,Wolchok JD,.Anti-programmed-deathreceptor-1 treatmentw ith pembrolizumab in ipilimumab-refractory advancedmelanoma:a random ised dose-comparison cohort of a phase1 trial[J].Lancet,2014,384(9948):1109-1117.
[7]LeDT,Uram JN,Wang H,.PD-1 blockade in tumorsw ith M ismatch-Repair deficiency[J].N Engl JMed,2015,372 (26):2509-2520.
[8]Toshihiko D,Sap P,Shadia J,.Updated results for the advanced esophageal carcinoma cohort of the phase 1b KEYNOTE-028 study ofpembrolizumab(MK-3475)[J].JClinl Oncol,2016,2016,34(4_suppl):7-7.
[9]LeDT,Bendell JC,Calvo E,.Safety and activity ofnivolumab monotherapy in advanced andmetastatic(A/M)gastric orgastroesophageal junction cancer(GC/GEC):Results from the CheckMate-032 study[J].JournalofClinicalOncology,2016, 34(4S):
[10]Kelly K,Heery CR,PatelMR,.Avelumab(MSB0010718C; anti-PD-L1)in patientsw ithadvanced cancer:Safety data from 1300 patientsenrolled in thephase1b JAVELINSolid Tumor trial [J].Journalof ClinicalOncology,2016,34(15,S):34.
2017-06-22)
郑磊贞,主任医师,医学博士,硕士生导师。现任上海交通大学医学院附属新华医院肿瘤科主任,中国医药教育协会盆腔肿瘤专业委员会副主任委员,上海市抗癌协会癌症康复与姑息治疗专业委员会副主任委员,上海市疾病预防控制中心胃癌防治专业委员会副主任委员,上海市胰腺癌诊治中心副主任委员,CSCO执行委员会理事,上海市抗癌协会理事,上海市医学会肿瘤专业委员会委员,上海市医学会肿瘤靶分子专业委员会委员,上海市化疗质控中心委员等。
(本文编辑:陈培莲)
郑磊贞,zhengleizhen@126.com
