水热法制备二氧化锰及在过氧化氢传感器中的应用
2017-09-06靳福娅余林蓝邦程高孙明郑小颖
靳福娅,余林,蓝邦,2,程高,孙明,郑小颖
(1广东工业大学轻工化工学院,广东 广州 510006;2广东省梅州市质量计量监督检测所,广东 梅州 514072)
水热法制备二氧化锰及在过氧化氢传感器中的应用
靳福娅1,余林1,蓝邦1,2,程高1,孙明1,郑小颖1
(1广东工业大学轻工化工学院,广东 广州 510006;2广东省梅州市质量计量监督检测所,广东 梅州 514072)
以高锰酸钾、硫酸锰、过硫酸钠等为原料,采用水热法合成了一系列二氧化锰(MnO2)催化剂,通过X射线衍射分析(XRD)、扫描电镜(SEM)以及N2吸附-脱附等手段进行了表征。后将一定量的二氧化锰材料与Nafion混合后滴涂于玻碳电极(GCE)表面,构成了一系列新型的过氧化氢传感器。并采用循环伏安法(CV)和计时电流法(I-t)分别对修饰电极进行表征,考察其相应的传感性能。结果表明,海胆状α-MnO2催化剂修饰的玻碳电极对过氧化氢有优异的电催化性能,其灵敏度为26.2μA·L/mmol。H2O2峰电流值在(2×10–6)~(0.14×10–3)mol/L范围内与浓度呈线性关系,最低检出限为0.57×10–6mol/L(S/N=3)。
二氧化锰;水热法;Nafion;过氧化氢;电化学传感器
过氧化氢的检测在医疗诊断、环境检测、食品分析、生物技术等方面有着重要意义,目前的检测方法有分光光度法、滴定分析法、电化学法等,其中电化学法是基于待测物质的电化学性质将待测物化学量转变成电学量进行传感的一种检测技术[1]。具体而言,即通过检测电流、电阻或电位等电信号手段来测定体系中目标物质含量,因其简单便捷、快速高效、稳定准确的特点多被用于研究中。但大多的电化学传感器是基于酶的生物传感器,而酶的稳定性差、对温度湿度pH等外在条件要求严苛,且酶固定化手段繁杂,使得其在应用中往往受限。因此,无酶H2O2传感器成为电化学传感器研究的重要方向。贵金属,如金、银、钯,由于其优越的电催化活性常被用于H2O2的无酶传感中。LU等[2]通过固定金纳米粒子于介孔二氧化硅上并整体覆盖于还原性氧化石墨烯表面构建了一种用于癌症细胞过氧化氢传感检测的新型二维材料。JIA等[3]将小尺寸的钯纳米颗粒均匀分散于螺旋碳纳米纤维上,合成了一种具有高导电性和比表面积的钯/螺旋碳纳米纤维复合材料,在H2O2传感测试中表现出较宽的检测范围。但贵金属昂贵且来源稀缺,并不能大量应用于实际生活中,这促进了过渡金属氧化物对H2O2传感性能的研究。
二氧化锰作为重要的过渡金属氧化物,由于其特殊的物理化学性质,不仅价格低廉、绿色环保,还具有极高的电催化活性。近年来,二氧化锰复合材料在H2O2电化学传感器中的应用备受关注。ZHANG等[4]构建了一种基于MnO2修饰于垂直排列多壁碳纳米管(MnO2/VACNTs)的高灵敏电流型传感器,并能够准确测量出牛奶中的H2O2含量。FENG等[5]采用水热法制备了二氧化锰/石墨烯纳米复合材料,在中性环境中对H2O2的传感表现出良好的重复性、选择性、稳定性和催化活性。然而,同样碍于碳材料的昂贵成本,不同结构与形貌二氧化锰纳米材料的过氧化氢电化学传感研究也显得尤为迫切,已有研究表明,形貌和结构是纳米材料决定电催化活性的重要参数[6]。
本文采取水热法合成了一系列不同形貌的二氧化锰纳米材料,通过X射线衍射(XRD)、扫描电镜(SEM)、N2吸附-脱附等手段对其结构与形貌进行了表征分析,并讨论了MnO2的形貌对于电催化过氧化氢传感性能的活性影响。
1 实验
1.1 催化剂制备
在室温下,称取0.25g高锰酸钾(广州化学试剂厂)、0.11g一水合硫酸锰(广州化学试剂厂)溶于加入15mL蒸馏水的聚四氟乙烯内胆中,持续搅拌30min后将反应釜置于160℃烘箱中反应24h。随后将产物分别用水、乙醇依次洗涤数次,后放于60℃干燥箱中干燥[7]。将干燥后的产物研磨,标记为样品Ⅰ。另取0.27g过硫酸钾、0.17g一水合硫酸锰、0.52g硫酸钾于内胆中,加入15mL蒸馏水搅拌30min,同时加入0.5mL硫酸,将反应釜置于140℃烘箱中反应6h,得到产物标记为样品Ⅱ[8]。取0.47g过硫酸钠与0.34g一水合硫酸锰以同样的方法置于160℃烘箱中反应12h,得到产物标记为样品Ⅲ[7]。
1.2 催化剂的表征
物相分析采用ULTIMA-Ⅲ型X射线衍射仪(日本岛津公司),CuKα射线,扫描速率10°/min,管电压40kV,管电流20mA;表面形貌采用S-3400N(Ⅱ)型扫描电镜(日本日立公司)观测,加速电压为0.3~30kV,工作电压为15kV;比表面积采用ASAP 2380型比表面孔径分析仪(美国Micromeritics公司),样品预先在200℃、N2气氛下处理6h,在–196℃下进行吸附;电分析测试采用德国扎娜(Zahner)电化学工作站。
1.3 MnO2/Nafion的制备
分别称取催化剂1mg,与50μL Nafion 混合后加入0.2mL蒸馏水和0.8mL无水乙醇,超声分散30min后,分别得到 α-MnO2nanowire/Nafion、urchin α-MnO2nanowire/Nafion和 β-MnO2nanorod/Nafion混合溶液。
1.4 修饰电极的制备
玻碳电极(GCE,直径5mm)用氧化铝(直径30nm)抛光后,用蒸馏水洗净,晾干。分别取20μL α-MnO2nanowire/Nafion、urchin α-MnO2nanowire/Nafion和 β-MnO2nanorod/Nafion分散液滴涂于GCE表面,晾干,分别得到 α-MnO2nanowire/Nafion/GCE、urchin α-MnO2nanowire/Nafion/GCE和β-MnO2nanorod/Nafion/GCE修饰电极。另取20μL Nafion溶液滴涂于GCE表面,晾干得到Nafion/GCE修饰电极。
1.5 H2O2传感性能测试
量取200mL磷酸缓冲溶液(pH=7)于电解池中,通入高纯氮气30min,确保除去电解液中的氧气。电化学实验采取三电极体系,修饰电极为工作电极,Ag/AgCl电极和铂片分别作为参比电极和对电极。在室温下,利用循环伏安法研究材料对于H2O2的电传感性能,扫描速率为50mV/s,扫描范围为–1V~0。此外,在–0.8V恒压下利用计时电流法依次向空白溶液中加入不同浓度的H2O2,记录H2O2的响应电流值。
2 结果与讨论
2.1 材料表征
图1为制备得到二氧化锰样品的X射线衍射(XRD)谱图。可以看出,样品Ⅰ与样品Ⅱ的衍射谱图是 α-MnO2晶相(PDF41-0141)的衍射峰,其中样品Ⅰ的特征峰高而尖锐且无杂相峰,说明样品结晶度好。样品Ⅲ则表现出 β-MnO2的晶相谱图(PDF24-0735),其特征峰明显,表明结晶度较好,并且也没有杂相峰。图2(a)~(c)为制得二氧化锰的扫描电镜(SEM)图。从图2可观察到,样品Ⅰ为二氧化锰纳米线,长度约2μm,直径约60nm,且生长较为均匀。样品Ⅱ为三维海胆状二氧化锰,由直径约25nm的纳米管组装而成。样品Ⅲ为二氧化锰短棒,长度约为1μm。
图3为不同形貌二氧化锰的氮气吸附-脱附等温曲线和孔径分布图(内插图)。观察图3(a)~(c)可知,根据IUPAC-吸附等温线[9],不同形貌的二氧化锰样品均为Ⅱ型吸附/脱附等温线,表现出无限制的单层-多层吸附特征。随着P/P0的增大,样品开始发生毛细孔凝聚或者分子层的吸附,吸附量缓慢增加,当吸附压力达到气体的饱和蒸气压时,单层吸附结束,多层吸附开始,吸附量垂直上升。同时,吸附脱附曲线存在明显的H3类型滞后环,在高P/P0处未表现出极限吸附量,表明材料中具有斜孔,这是由于平板状颗粒的堆积所导致的[10]。
表1所示为不同形貌二氧化锰的比表面积与孔径分析结果。可以看出,制得的海胆状三维二氧化锰的比表面积最大,为39.05m2/g。同时,相较于二氧化锰纳米线与纳米棒具有较大的孔体积。由表1可以看出,与二氧化锰纳米线相比,二氧化锰纳米棒具有相对较小的比表面积与孔体积,但其平均孔径约为前者一倍,说明可为催化反应提供更多的活性位。

图2 二氧化锰材料的扫描电镜图
2.2 电化学表征
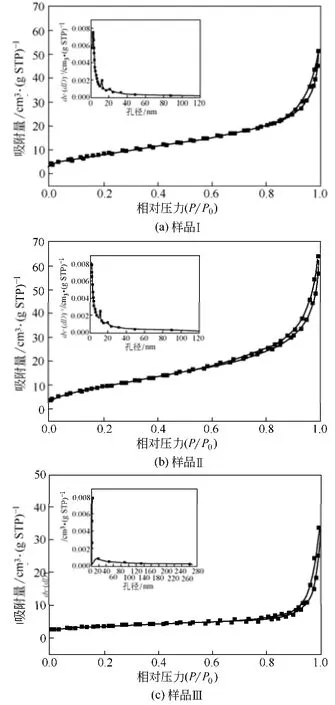
图3 不同形貌二氧化锰的N2吸附脱附曲线

图4 不同修饰电极在N2饱和的PBS(pH 7.0)溶液中的CV图(扫速为50mV/s)

表1 不同形貌二氧化锰的比表面积
图4是不同修饰电极在有无加入1mmol/L H2O2的CV曲线。由图3可知,在Nafion/GCE修饰电极曲线(a,a′)上,H2O2几乎没有响应;而所制得的3种MnO2/Nafion/GCE修饰电极均对H2O2有较好的电流响应,表明二氧化锰材料所修饰的电极对H2O2还原反应有很好的催化效果。观察图3可知,海胆状二氧化锰三维材料表现出最优的电催化活性,其催化峰值电流分别是后者的1.7倍和1.3倍,3种二氧化锰材料对H2O2的电催化作用排序 为:urchin α-MnO2nanowire> β-MnO2> α-MnO2nanowire。此外,二氧化锰对H2O2的电催化作用机理可推测如式(1)、式(2)[11]。

由式(1)可见,二氧化锰可提供的Mn(Ⅳ)活性位点越多,催化反应可吸附的H2O2越多,式(2)反应中电子转移速率越快。已知海胆状的二氧化锰具有三维结构,对比一维结构而言能够提供更多的活性位点,并且具有良好的分散性,较少团聚;其次,海胆状二氧化锰比表面积大,增大了与H2O2分子的接触位点,使其峰电流明显增加;最后,海胆状二氧化锰具有相对更强的导电性[12],促进了电催化反应中的电子转移。因此,海胆状二氧化锰对H2O2有较好的电化学响应。
此外,晶型对电催化活性也具有一定影响。由于α-MnO2具有2×2的孔道结构,较β-MnO2多孔,同时由于其孔道中含有K等离子,其导电性好过β-MnO2,因此理论上,α-MnO2纳米线性能要优于β-MnO2纳米棒。但在电催化反应中,由于α-MnO2纳米线具有折叠墙结构,对H2O2的吸附作用会大大减弱[6]。因此,β-MnO2纳米棒的电催化作用优于α-MnO2纳米线。
图5表明修饰电极在不同浓度的过氧化氢(1mmol/L,2mmol/L,3mmol/L,4mmol/L,5mmol/L)下的CV曲线。可以看出,随着过氧化氢浓度的不同,CV曲线的电流响应值发生了明显的变化。随着过氧化氢浓度的增加,其电流响应值也随之增大,显示出明显的电催化特征。其中,海胆状二氧化锰的电流响应,使其在时间-电流测试中具有更优异的表现,可构建一个高灵敏度的电化学传感器。

图5 修饰电极在 N2饱和的PBS(pH=7)的溶液中,加入不同浓度过氧化氢的CV曲线(扫描速率为50mV/s)

图6 3种修饰电极在N2饱和的PBS(pH 7.0)溶液中以不同扫描速度的CV图
图6为不同扫描速率下修饰电极在–1V~0V电位范围的循环伏安图。可以看出,在10~110mV/s范围内,随着扫描速率的不断增加,还原峰电流随之增加,同时峰电位差(ΔEp)逐渐降低。除此之外,观察图6中各小图可知在不同的扫描速率下,海胆状二氧化锰修饰电极的还原峰电流值与相应扫描速率的平方根(ν1/2)成正比,二氧化锰纳米线与二氧化锰纳米棒修饰电极在PBS溶液中的还原峰电流值也与ν1/2呈线性关系,表明电极反应为明显的扩散控制过程。

图7 3种修饰电极在N2饱和的PBS(pH 7.0)溶液中连续滴加过氧化氢的计时电流相应曲线图
图7为修饰电极对不同浓度H2O2的计时电流响应曲线图。从图7中可以看出,在恒定电压–0.8V下,不断加入一定量的H2O2溶液,响应电流也随之增加,并且在5s内可以达到电流稳定。对于二氧化锰纳米线[图7(a)]而言,当过氧化氢浓度在5×10–4~1.4×10–2mol/L范围内时,其响应电流与过氧化氢浓度呈良好的线性关系,线性回归方程为Ip(μA)=6.1c(mmol/L)+7.3536(R2=0.991),计算可得其检测限为3.31mmol/L(S/N=3)。由图7(b)可知,在H2O2浓度为2×10–6~1.4×10–4mol/L范围内,海胆状二氧化锰修饰电极的时间-电流曲线表明其响应电流与过氧化氢浓度呈线性关系,线性回归方程为Ip(μA)= 26.1519c(mmol/L)+3.81098(R2=0.997),灵敏度为26.2μA/mmol/L,最低检测限为0.57μmol/L(S/N=3)。二氧化锰纳米棒修饰电极的计时电流曲[图7(c)]线表明,H2O2浓度在2×10–6mol/L~1.4×10–4mol/L范 围 内 时 线 性 回 归 方 程 为Ip(μA)=13.2c(mmol/L)+4.9577(R2=0.996),计算得检出限为1.1μmol/L(S/N=3)。

图8 3种修饰电极分别连续7天在加入1mmol/LH2O2的N2-饱和的PBS(pH 7.0)溶液的CV峰电流值
由不同修饰电极的无酶H2O2电化学传感器性能对比(表2)可知,海胆状二氧化锰修饰电极构建的H2O2传感器灵敏度高,具有较低的检测限和较宽的线性范围,表现出良好的H2O2传感性能。
如图8所示,连续7天以相同条件分别制备α-MnO2纳米线/Nafion/GCE(A)、海胆状 α-MnO2纳米线/Nafion/GCE(B)和 β-MnO2纳米棒/Nafion/GCE(C)修饰电极,加入1mmol/ L H2O2检测其峰电流,发现其相对标准偏差分别为3.89%、1.76%、5.34%,说明海胆状二氧化锰修饰电极具有相对较优的重复性。

表2 不同无酶电化学传感器的H2O2性能对比
除此之外,为研究材料对于H2O2传感的选择性,将葡萄糖(glucose)、抗坏血酸(ascorbic acid,AA)、尿酸(uric acid,UA)作为被测体系的干扰物质。图9为α-MnO2纳米线/Nafion/GCE(A)、海胆状 α-MnO2纳米线/Nafion/GCE(B)和 β-MnO2纳米棒/Nafion/GCE(C)修饰电极分别在N2饱和PBS溶液中对H2O2、葡萄糖、AA、UA的计时电流响应曲线。可以看出,相较于对H2O2的响应而言,α-MnO2纳米线对AA有一定的响应,β-MnO2纳米棒对UA有明显响应,而海胆状α-MnO2除对H2O2有明显响应外,对葡萄糖、AA、UA均没有明显的响应。这表明海胆状二氧化锰对葡萄糖、AA、UA具有更优的抗干扰性能,可以构建高效灵敏的H2O2传感器。

图9 修饰电极在N2饱和的PBS(pH7.0)溶液中加入1mmol/LH2O2、0.1mmol/L葡萄糖、0.1mmol/L AA、0.1mmol/L UA的计时电流响应曲线
3 结论
以水热法合成了一系列不同形貌的二氧化锰纳米材料,构建了3种无酶H2O2传感器。结果表明,海胆状二氧化锰由于其三维结构,具有相对较大的比表面积,可为电催化反应提供更多的活性位点;海胆状α-MnO2相较于α-MnO2纳米线和β-MnO2纳米棒对H2O2有相对更优的传感性能,具有较低的最低检测、较宽的检测范围以及良好的选择性和重现性,对于人体内的一些电活性物质如AA、UA等有良好的抗干扰稳定性。
[1] OUNGIPAT W,ALEXANDER W P,KEELY P S. A reagentless amperometric biosensor for hydrogen peroxide determination based on asparagus tissue and ferrocene mediation[J]. Anal. Chim. Acta.,1995,309:35-45.
[2] LU W,LUO Y,CHANG G,et al. Synthesis of functional SiO2-coated graphene oxide nanosheets decorated with Ag nanoparticles for H2O2and glucose detection[J]. Biosensors & Bioelectronics,2011,26(12):4791-4797.
[3] JIA X E,HU G,NITZE F,et al. Synthesis of palladium/helical carbon nanofiber hybrid nanostructures and their application for hydrogen peroxide and glucose detection[J]. Appl. Mater. Interfaces,2013,5:12017-12022.
[4] XU B,YE M L,YU Y X,et al. A highly sensitive hydrogen peroxide amperometric sensor based on MnO2-modified vertically aligned multiwalled carbon nanotubes[J]. Anal. Chim. Acta.,2010,674:20-26.
[5] FENG X M,ZHANG Y,SONG J,et al. MnO2/Graphene nanocomposites for nonenzymatic electrochemical detection of hydrogen peroxide[J]. Electroanalysis,2015,27:353-359.
[6] BABU K J,ZAHOOR A,NAHM K S,et al. The influences of shape and structure of MnO2nanomaterials over the non-enzymatic sensing ability of hydrogen peroxide[J]. Journal of Nanoparticle Research,2014,16(2):1-10.
[7] 陈国荣,陈林峰,蓝邦,等. 二氧化锰的晶型可控合成及其催化燃烧二甲醚研究[J]. 中国粉体技术,2016,22(2):14-17.CHEN G R,CHEN L F,LAN B,et al. Hydrothermal synthesis of MnO2with different crystal phases for catalytic combustion property of dimethyl ether[J]. China Powder Science and Technology,2016,22(2):14-17.
[8] LIN T,YU L,SUN M,et al. Mesoporous α-MnO2microspheres with high specific surface area:controlled synthesis and catalytic activities[J]. Chemical Engineering Journal,2016,286:114-121.
[9] MATTHIAS T,KATSUMI K,ALEXANDER V N,et al.Physisorption of gases,with special reference to the evaluation of surface area and pore size distribution[J]. Pure Appl. Chem.,2015,87(9/10):1051-1069.
[10] 孙明,邢泽峰,刘胜男,等. 一步水热合成 Ag-OMS-2 纳米棒及其催化燃烧性能研究[J]. 天然气化工(C1化学与化工),2013,38(2):11-14.SUN M,XING Z F,LIU S N,et al. One-step hydrothermal synthesis of Ag-OMS-2 nanorods and their catalytic combustion activities[J].Natural Gas Chemical Industry,2013,38(2):11-14.
[11] FENG L,WANG R,SHI Y,et al. Electrochemical study of hydrogen peroxide detection on MnO2micromaterials[J]. International Journal of Electrochemical Science,2016,11(7):5962-5972.
[12] CHINNASAMY R,RAO G M,THANGAVELU R,et al. Synthesis and electrocatalytic properties of manganese dioxide for non-enzymatic hydrogen peroxide sensing[J]. Mater. Sci. Semicond.Process,2015,31:709-714.
[13] FENG X,ZHANG Y,SONG J,et al. MnO2/Graphene nanocomposites for nonenzymatic electrochemical detection of hydrogen peroxide[J]. Electroanalysis,2015,27:353-359.
[14] SLJUKIIC B,COMPTON R G. Manganese dioxide graphite composite electrodes formedviaa low temperature method:detection of hydrogen peroxide,ascorbic acid and nitrite[J]. Electroanalysis,2007,19:1275-1280.
[15] YE D,LI H,LIANG G,et al. A three-dimensional hybrid of MnO2/graphene/carbon nanotubes based sensor for determination of hydrogen-peroxide in milk[J]. Electrochim. Acta.,2013,109:195-200.
[16] ZHANG L,FANG Z,NI Y,et al. Direct electrocatalytic oxidation of hydrogen peroxide based on nafion and microspheres MnO2modified glass carbon electrode[J]. Electrochem. Soc.,2009,4:407-413.
Preparation of MnO2nanomaterials in hydrothermal method and applied in hydrogen peroxide sensing
JIN Fuya1,YU Lin1,LAN Bang1,2,CHENG Gao1,SUN Ming1,ZHENG Xiaoying1
(1School of Chemical Engineering and Light Industry,Guangdong University of Technology,Guangzhou 510006,Guangdong,China;2Guangdong Meizhou Quality & Metrology Supervision and Testing Institution,Meizhou 514072,Guangdong,China)
A series of manganese dioxide,namely urchin α-MnO2,α-MnO2nanowires and β-MnO2nanorods were synthesized using hydrothermal method by changing raw materials such as KMnO4、MnSO4、Na2S2O8,etc. The MnO2materials were characterized by X-ray diffraction(XRD),scanning electron microscope(SEM),and N2adsorption-desorption measurements. A novel hydrogen peroxide(H2O2)sensor was fabricated by coating the mixture of Nafion and nanomaterials on a glassy carbon electrode(GCE). The performances of the modified electrode was investigated using cyclic voltammetry(CV)and chronoamperometry current-time response(I-t). The test results indicated that the urchin α-MnO2nanowires based sensor exhibited the best electro catalytic activity towards the reduction of H2O2with a sensitivity of 26.2μA·L/mmol. And the reduction peak currents of H2O2were linear to their concentrations in the range of 2×10–6mol/L to 0.14×10–3mol/L wih a lowest limit of detection of 0.57×10–6mol/L(S/N=3).
manganese oxide;hydrothermal method;Nafion;hydrogen peroxide(H2O2);electrochemical sensor
O614.7
:A
:1000-6613(2017)09-3380-08
10.16085/j.issn.1000-6613.2017-0157
2017-01-22;修改稿日期:2017-05-15。
国家自然科学基金(21576054)、广东省科技计划(2014A010106030,2016A010104017,2016B020241003)及广东省质监局科技计划(2017ZZ07)项目。
靳福娅(1992—),女,硕士研究生。E-mail:timegoneby@163.com。联系人:余林,教授,主要研究方向为催化新反应、催化新材料、电催化氧还原反应和超级电容器等领域。E-mail:gych@gdut.edu.cn。
