第8版国际抗癌联盟和美国癌症联合委员会胃癌TNM分期系统简介及解读
2017-09-03刘光艺黄镇王子卫
刘光艺 黄镇 王子卫
·专题论坛·
第8版国际抗癌联盟和美国癌症联合委员会胃癌TNM分期系统简介及解读
刘光艺 黄镇 王子卫
目前胃癌的TNM分期已经成为临床胃癌诊疗的首选参考依据。在国际抗癌联盟(UICC)、国际胃癌协会(IGCA)和美国癌症联合委员会(AJCC)的共同协作推动下,通过对全世界范围内胃癌大数据的收集与分析,于2016年10月颁布了第8版胃癌TNM分期系统。第8版TNM分期系统对食管-胃结合部及贲门癌分期标准的选择做出了明确的定义;同时还在单一分期系统的基础上新增了临床TNM分期(cTNM)和新辅助治疗后分期(ypTNM)。此外,新版的分期系统将N3的两个亚组N3a和N3b作为独立组别纳入到分期系统,还对组织学分级进行了一些调整。总的来说,相比第7版胃癌TNM分期系统,新版的分期系统可以指导临床医生更加合理地制定治疗方案,更加科学地评价治疗效果,更加准确地评估预后。然而,随着临床广泛应用和进一步验证,以及新的预测因子的发现,必将会有新的分期系统替代和完善旧的分期系统。
胃癌; TNM分期; 肿瘤分期; 国际抗癌联盟; 美国癌症联合委员会
众所周知,国际抗癌联盟(UICC)和美国癌症联合委员会(AJCC)联合出版的胃癌TNM分期系统已经成为全球范围内胃癌治疗策略选择和预后评估的重要参考依据。自1976年AJCC发布第一版《肿瘤分期手册(CSM)》以来,经过30余年的发展,先后有7版胃癌TNM分期系统为临床医师的诊疗工作提供系统全面的指导。随着2010年第7版胃癌分期系统广泛应用于临床,在6年多的临床应用过程中,该系统的一些不足之处逐步呈现出来,已经不能满足临床诊疗需求。因此,在UICC、国际癌症协会(IGCA)和AJCC的共同协作推动下,于2016年10月联合颁布了第8版胃癌TNM分期系统[1-2]。新推出的第8版胃癌TNM分期系统是基于对全世界范围内胃癌大数据的收集与分析,并在对旧的分期系统进行评价和比较后更新而来。相对于前面几个版本,新分期系统更全面系统,更具国际通用性和代表性。总体而言,第8版TNM分期系统主要变动在以下几个方面[1]:①食管与胃解剖学界线:肿瘤侵犯胃食管交界线,如果肿瘤中心位于胃食管交界线以下2 cm以内,应按照食管癌标准进行分期;肿瘤中心位于胃食管交界线以下2 cm以外,应按照胃癌标准进行分期。贲门癌不涉及胃食管交界线,应该按照胃癌标准进行分期。②病理分期变化:将N3的两个亚组N3a和N3b作为独立组别纳入到分期系统。③新增临床TNM分期(cTNM)。④新增新辅助治疗后分期(ypTNM)。⑤pTNM分期变化:将T4aN2M0和T4bN0M0从ⅢB期调整为ⅢA期。
本文将对以上变更的内容进行具体的介绍、解读和讨论,试图阐明第8版胃癌TNM分期系统的优劣。
一、食管胃结合部原发病灶解剖范围的重新界定
胃食管交界区域(gastroesophageal junction, GEJ)癌的概念由德国胸外科医师Siewert和Stein首先提出[3],并随后得到IGCA和AJCC认可。GEJ线上下5 cm内所有腺癌分为3型:SiewertⅠ型,癌中心在GEJ线上1~5 cm内;Ⅱ型为GEJ线上1 cm和线下2 cm;Ⅲ型为线下2~5 cm内。这个区域的癌分期系统到底是选择食管癌标准还是胃癌标准一直存在争议。在第7版TNM分期系统中,肿瘤中心位于食管-胃交界线以下5 cm以内并且肿瘤侵犯食管胃交界线及以上区域均按照食管癌分期系统进行分期;而肿瘤中心位于食管胃交界线以下5 cm以内,但肿瘤未侵犯食管胃交界线或者则肿瘤中心位于食管胃交界线以下5 cm以外区域则按照胃癌分期系统进行分期。日本的Sano等[4]教授通过对来自全球1 170余例GEJ癌病例中的SiewertⅡ型和Siewert Ⅲ型按照食管癌分期系统(表1)进行分期,结果发现大部分病人被划分到了ⅢC期,同时还发现ⅡA和ⅡB期病人的生存曲线是刚好相反的,即ⅡB期病人预后比ⅡA期病人更好,这显然与临床实际情况不符。来自中山大学陈慧等[5]和南京大学Huang等[6-7]按照AJCC第7版食管腺癌分期标准分组绘制生存曲线发现了与Sano教授一致的结果,研究还发现按照AJCC第7版胃癌分期标准预测EGJ癌病人预后要优于按AJCC第7版食管腺癌分期标准。IGCA在2009年组织收集了总共25 411例SiewertⅡ型和Siewert Ⅲ型GEJ癌行胃癌根治术、并有5年以上随访资料的病例,也证实了SiewertⅡ型和Siewert Ⅲ型GEJ癌按胃癌TNM分期系统进行分期更为合理[4]。
因此,第8版胃癌TNM分期系统重新明确了GEJ癌的分期标准选择。肿瘤侵犯食管-胃交界线,但肿瘤中心位于食管胃交界线以下2cm以外区域或者肿瘤中心位于食管胃交界线以下2 cm以内区域,但肿瘤未侵犯食管胃交界线应按照胃癌TNM分期标准进行分期;如肿瘤中心位于食管胃交界线以下2 cm以内区域,且肿瘤侵犯食管胃交界线应按照食管癌TNM分期标准进行分期,如图1所示。
二、原发肿瘤T分期和组织学分级的变化
原发肿瘤浸润深度一直是UICC和AJCC颁布的TNM分期系统的重要组成部分,原发灶浸润深度是影响胃癌病人预后的重要因素之一。经过多年的临床实践及研究发现第7版的T分期在选择治疗方案和评估预后方面均表现出了前所未有的优越性。因此,第8版胃癌的T分期仅在第7版的基础上进行了细微的调整:将高度不典型增生纳入了原位癌(Tis)的范畴,详见表1。
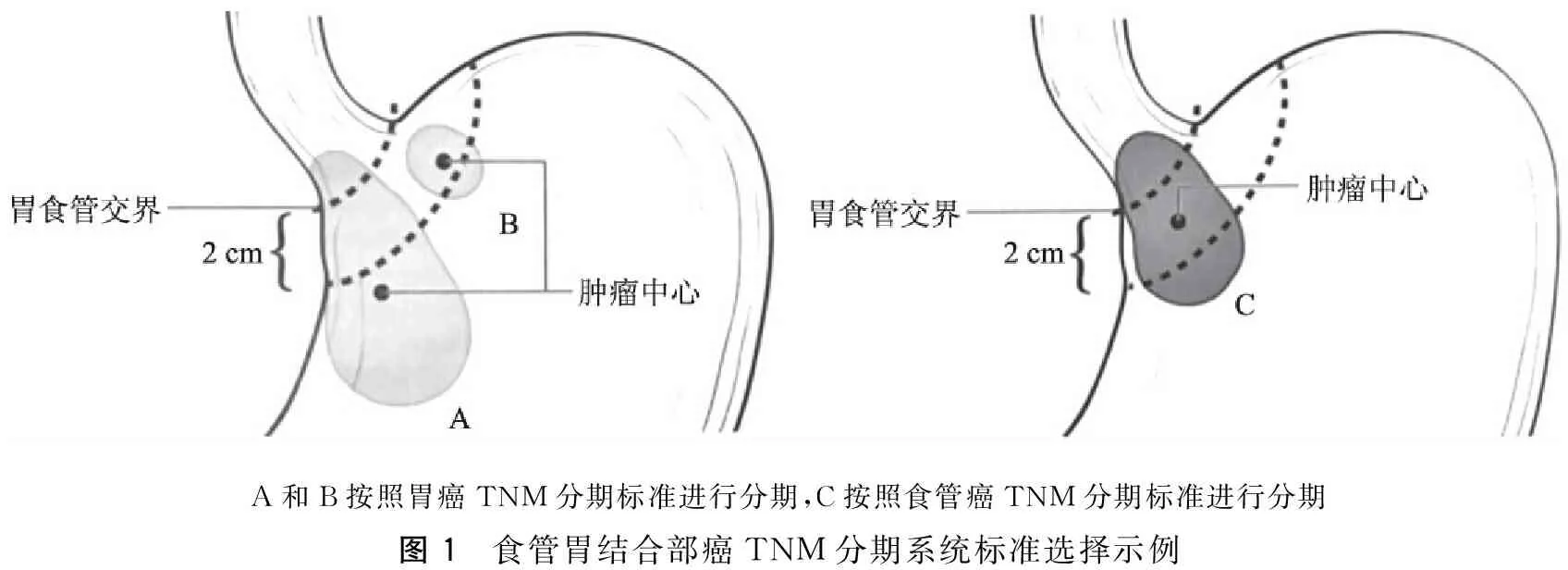
A和B按照胃癌TNM分期标准进行分期,C按照食管癌TNM分期标准进行分期图1 食管胃结合部癌TNM分期系统标准选择示例
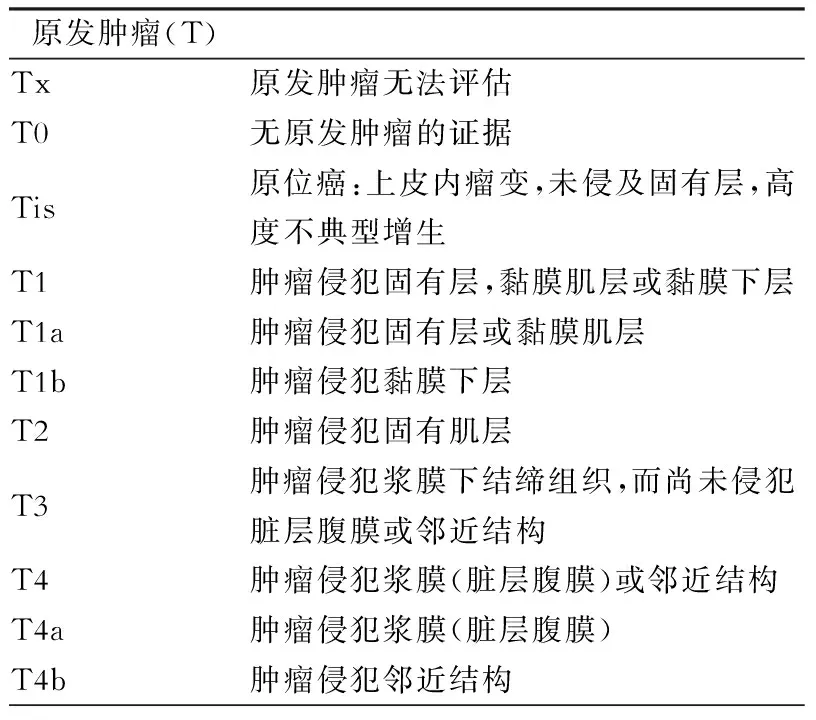
表1 第8版原发肿瘤(T)分期
三、淋巴结分期变化
区域淋巴结N分期本身没有实质性的变化,在第7版中已经将7~15枚和15枚以上区域淋巴结转移分别定义为N3a和N3b。但是在总的TNM分期应用中,第7版仍然将N3a和N3b笼统地归结为N3,而在新一版的分期中,N3a和N3b作为两个独立的亚组参与分期,详见表2。例如在第7版的解剖学分期中,pT4aN3aM0和pT4aN3bM0都按照pT4aN3M0划分为ⅢC期,而在新版中pT4aN3aM0和pT4aN3bM0分别被定义为ⅢB期和ⅢC期。这些总分期的变化说明随着外科手术学和临床病理学技术不断发展,在胃癌根治术中清扫和检获的淋巴结数目越来越多,不断完善的TNM分期为胃癌病人术后进一步治疗及预后判断提供了更加精准的工具。
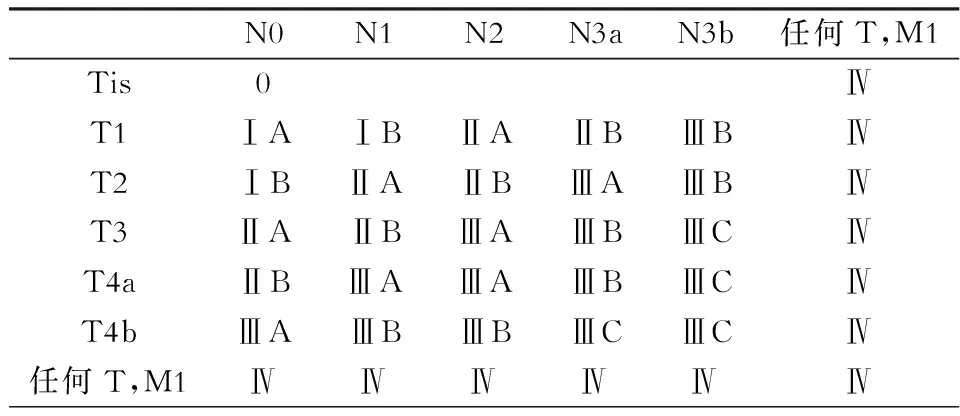
表2 第8版胃癌病理学TNM分期(pTNM)
注:本表参照第8版UICC和AJCC数据编制
此外,多少枚淋巴结应该被检获从而有助于更精准合理的临床分期一直处于争论之中。淋巴结检获数目不足很大程度上会影响N分期,作为TNM分期中十分重要的组成部分,N分期不精准将严重影响病人预后的评估精准性。因此,第8版UICC和AJCC癌症分期指南再次强调检获足够数目淋巴结的重要性,要求病理医师对每一例胃癌根治术标本至少要找到16枚淋巴结,如果为了更加准确评价预后,检获淋巴结数目最好是在30枚以上[8]。
四、新增cTNM分期
第8版TNM分期系统第2个重要更新点是首次提出了胃癌cTNM分期的概念。一般情况下,当病人被确诊定性为胃癌时,临床医生通常会根据相关辅助检查得到一个分期。在确诊胃癌后对胃癌进行临床分期可以为医生制定下一步治疗方案提供指导。在新版TNM分期系统尚未应用于临床之前,临床医生一般都是套用病理学TNM分期标准进行临床TNM分期。实际上,套用分期方式可能会带来很多的问题:一方面,缺乏循证医学支持,有效性尚未得到验证;另一方面,目前不管是超声内镜、CT或者其他辅助检查手段尚不能达到病理学一样精准的T和N分期。简单套用病理学分期可能会出现错误的分期,一定程度上还有可能会误导临床治疗策略的选择。精准的临床分期是制定个体化治疗方案最重要的参考依据,为了满足临床工作的需要,新版的胃癌TNM分期系统新增了胃癌临床分期,详见表3。

表3 第8版新增胃癌临床TNM分期(cTNM)
注:本表参照第8版UICC和AJCC数据编制
在cT分期方面:cT分期和病理学T分期相类似。cT1指肿瘤病灶侵犯黏膜或黏膜下层,影像学方面可以发现内层高强化癌肿与外层稍高强化肌层间可见连续完整的低强化条带;cT2指肿瘤侵犯固有肌层,可以发现中层低强化条带中断消失,外层残余部分稍高强化肌层;cT3指肿瘤穿透浆膜下结缔组织,未侵犯脏层腹膜,可以看到高强化癌肿侵犯胃壁全层,浆膜面光滑或少许短细索条;cT4a指肿瘤侵犯脏层腹膜,但尚未侵犯邻近结构或器官,影像学可以发现浆膜面不规则或结节样形态,周围脂肪间隙密集毛刺或条带状浸润;cT4b指肿瘤侵犯邻近结构或者器官,影像学可以看到肿瘤病灶与邻近脏器结构脂肪间隙消失,指状嵌插或直接浸润为确切侵犯征象[9-12]。IGCA研究委员会发现T4bNxM0的病人预后极差[3],与大多数临床研究结果相一致[5-6]。在第8版TNM分期系统中,超声内镜被认为是判断肿瘤T分期最为理想的检查手段,其效果超过了CT和MRI。但是必须要指出,超声内镜检查结果准确性很大程度上会受到检查者技术水平影响,稳定性不如CT和MRI。
在cN分期方面,分期标准与病理学N分期基本一致。根据淋巴结转移数目分为N0~N3,唯一不同的地方是没有将N3细分为N3a和N3b。另外影像学方面参考征象为:类圆形肿大淋巴结,短径大于1.0 cm[4,13-14]。在cM分期方面,基于影像学检查发现有远处转移则可定义为cM1;除此之外,通过腹腔镜探查证实存在腹膜或其他脏器转移也定义为远处转移阳性。 需要指出的是,胃癌cTNM分期报告内容需涵盖以下几部分:①原发灶:部位(食管胃交界区、胃底、胃体、胃窦、幽门管、大弯、小弯、前壁和后壁),形态(肿块、局限溃疡、浸润溃疡和弥漫溃疡),厚度,密度(黏液腺癌等特异征象),强化特征,黏膜及浆膜面情况,近/远端累及边界位置,与正常胃壁交界情况,与邻近脏器关系;②淋巴结:一般参照日本胃癌学会胃癌处理规约分组报告,报告有明确转移征象的淋巴结数目(或参照N分期的数目范围),最大淋巴结长短径、形态、边界及强化情况;③远处转移:转移灶位置、分布、形态、大小、密度及强化特征,腹膜形态及腹水状况[15-17]。
五、新增ypTNM分期
2011版国家卫计委胃癌诊疗指南推荐:对无远处转移的局部进展期胃癌(T3/4、N+),推荐新辅助化疗。随着新辅助治疗的不断兴起,其临床价值也得到了广泛的认可。对于新辅助治疗后的肿瘤分期,由于缺少合适的分期标准,当前我们使用的仍然是病理分期。为了满足临床所需,AJCC和UICC在制定第8版胃癌TNM分期时新增了ypTNM分期,这是新版分期的又一个重要变化,详见表4。
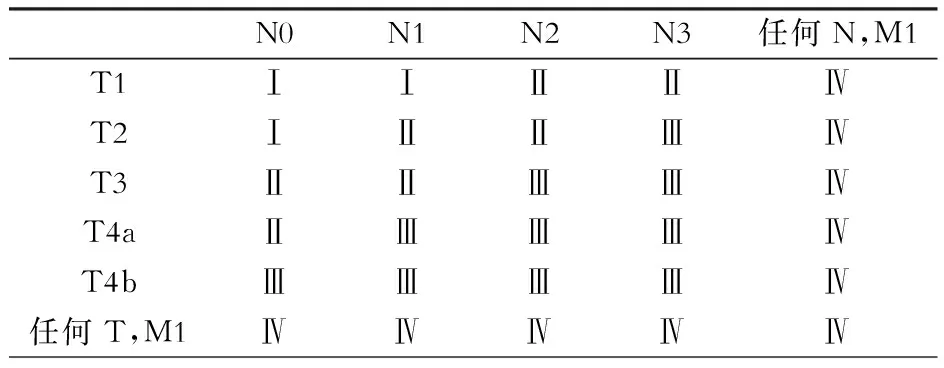
表4 第8版新增胃癌新辅助治疗后TNM分期(ypTNM)
注:本表参照第8版UICC和AJCC数据编制
AJCC还指出:新辅助治疗后的病理标本评估应包括对切除标本的肉眼和显微镜检查。在显微镜下,治疗有效主要体现在炎性组织或纤维化组织代替恶性上皮细胞。对于ypT分期判断主要取决于治疗后残存的病灶处于胃壁的最深层次[18];而ypN分期中对于阳性淋巴结的定义为淋巴结中至少含有一个肿瘤灶。针对于接受新辅助治疗的胃癌病例,术后病检报告应该体现上述两个方面。对于怀疑有远处转移的病例,在ypM分期中应该标记为ypM1[19]。
需要指出的是,由于AJCC对于新辅助治疗后TNM分期纳入研究病例数目比较有限,其适应性及临床应用价值需要时间进行验证。
六、总结
胃癌TNM分期是临床治疗策略选择和判断预后的重要依据,第8版胃癌TNM分期系统已经用于指导临床诊疗工作。与第7版相比,新版分期系统能够更合理指导治疗和反映病人的预后。尤其是对GEJ癌分期的更新,以及新增的cTNM分期和ypTNM分期,使得临床医生能够更加合理地制定治疗策略,更好地评估病人预后。
当然,第8版胃癌分期系统也存在不足之处。据世界卫生组织统计,目前全世界43%以上的胃癌病人来自中国,而贲门癌在中国比较常见,约占30%左右。而UICC和AJCC制定新版分期系统所用的临床病例资料84.8%都来自于日本和韩国,作为患病人数和贲门癌比例均较高的中国人却只占6.4%,研究的结果可能存在偏倚[3]。需要通过更多国家、更为广泛、更具代表的大样本胃癌数据进行分析,进而不断完善和更新。因此,新版胃癌TNM分期的实际价值仍有待于更广泛的临床验证。中国也应该就自身的实际情况,结合新版胃癌分期系统制定更为合理、更适合中国胃癌人群的临床病理学指南。
1 Amin MB,Edge SB,Greene FL,et al.AJCC Cancer Staging Manual. 8th ed. New York: Springer,2016.203-220.
2 Ilhan E,Ureyen O,Meral UM.Ongoing problems concerning 7th TNM staging system and proposals for 8th TNM staging system of gastric cancer.Prz Gastroenterol, 2016,11:223-225.DOI:10.5114/pg.2016.64069.
3 Siewert JR,Stein HJ.Classification of adenocarcinoma of the oesophagogastric junction.Br J Surg,1998,85:1457-1459.DOI:10.1046/j.1365-2168.1999.01197-15.x.
4 Sano T,Coit DG,Kim HH,et al.Proposal of a new stage grouping of gastric cancer for TNM classification: International Gastric Cancer Association staging project.Gastric Cancer,2017,(20):217-225.DOI:10.1007/s 10120-016-0601-9.
5 陈慧,詹俊,于钟,等.食管-胃连接部恶性肿瘤218例临床病理特征和预后分析.中华消化杂志,2015,35:328-332.DOI:10.3760/cma.j.issn.0254-1432.2015.05.010.
6 Huang Q,Shi J,Fan X,et al.Gastric cardiac carcinomas involving the esophagus are more adequately staged as gastriccancers by the 7th edition of the American Joint Commission on Cancer Staging System.Mod Pathol,2011,24:138-146.DOI:10.1038/modpathol.2010.183.
7 Huang Q,Sun Q,Fan XS,et al.Recent advances in proximal gastric carcinoma.J Dig Dis,2016,17:421-432.DOI:10.1111/ 1751-2980.12355.
8 Ajani JA,Bentrem DJ,Besh S,et al.Gastric cancer, version2.2013:featured updates to the NCCN Guidelines.J Natl Compr Canc Netw,2013,11:531-546.
9 Kim JW,Shin SS,Heo SH,et al.Diagnostic performance of 64-section CT using CT gastrography in preoperative T staging of gastric cancer according to 7th edition of AJCC cancer staging manual.Eur Radiol,2012,22:654-662. DOI:10.1007/s00330-011-2283-3.
10Hasegawa S,Yoshikawa T,Shirai J,et al.A prospective validation study to diagnose serosalinvasionand nodal metastases of gastric cancer by multidetector-row CT.Ann Surg Oncol,2013,20:2016-2022.DOI:10.1245/s10434-012- 2817-1.
11Habermann CR,Weiss F,Riecken R,et al.Preoperative staging of gastric adeno-carcinoma: comparison of helical CT and endoscopic US.Radiology,2004,230:465-471. DOI:10.1148/radiol.2302020828.
12Lee SL,Ku YM,Jeon HM,et al.Impact of the cross-sectional location of multi-detector computed tomography scans on prediction of serosalexposurein patients with advanced gastric cancer. Ann Surg Oncol,2017,24:1003-1009.DOI: 10.1245/s10434-016-5670-9.
13Robert MK,Thomas CK.Imaging in assessing lymph node status in gastric cancer.Gastric Cancer,2009,12:6-22. DOI:10.1007/s10120-008-0492-5.
14Seevaratnam R,Cardoso R,McGregor C,et al.How useful is preoperative imaging for tumor, node, metastasis (TNM) staging of gastric cancer? A meta-analysis.Gastric Cancer,2012,15Supp11:3-18.DOI:10.1007/s10120-011-0069-6.
15Kim TU,Kim S,Lee JW,et al.MDCT features in the differentiation of T4a gastric cancer from less-advanced gastric cancer: significance of the hyperattenuating serosa sign.Br J Radiol,2013,86:20130290.DOI:10.1259/bjr.2013 0290.
16Kumano S,Murakami T,Kim T,et al.T staging of gastric cancer:role of multi-detector row CT.Radiology,2005, 237:961-966.DOI:10.1148/radiol.2373041380.
17Markar SR,Karthikesalingam A,Jackson D,et al.Long-term survival after gastrectomy for cancer in randomized, controlled oncological trials: comparison between West and East.Ann Surg Oncol,2013,20:2328-2338.DOI:10.1245/s 10434-012-2862-9.
18Mocellin S,Pasquali S.Diagnostic accuracy of endoscopic ultrasonography (EUS) for the preoperative locoregional staging of primary gastric cancer. Cochrane Database Syst Rev,2015,2:CD009944.DOI:10.1002/14651858.CD009944.pub2.
19Lee YT,Ng EK,Hung LC,et al.Accuracy of endoscopic ultrasonography in diagnosing ascites and predicting peritoneal metastasis in gastric cancer patients.Gut,2005,54:1541-1545.DOI:10.1136/gut.2004.055772.
The 8th edition of the Union for International Cancer Control and the American Joint Committee on Cancer gastric cancer TNM staging system: explanation and elaboration
Liu Guangyi,Huang Zhen,Wang Ziwei.
Department of Gastrointestinal Surgery,the First Affiliated Hospital of Chongqing Medical University,Chongqing 400016,China
Wang Ziwei,Email:wangziwei571@ sina.com
The TNM stage of gastric cancer has become the first reference for clinical diagnosis and treatment of gastric cancer.Through the collection and analysis of data on gastric cancer worldwide,the Union for International Cancer Control (UICC),International Gastric Cancer Association (IGCA) and American Joint Committee on Cancer (AJCC) jointly issued the 8th edition of the gastric cancer TNM staging system,in October 2016.The 8th edition of the TNM staging system has a clear definition of the staging criteria for esophago-gastric junction cancer and cardia cancer,and adds clinical TNM staging (cTNM) and new adjuvant therapy (ypTNM) on the basis of a single stage system.In addition,the new staging system incorporates two subgroups of N3 (N3a and N3b) as independent group into the system,and makes some adjustments to the histological grade.In general,compared with the 7th edition of gastric cancer TNM staging system,the new edition of staging system may guide clinicians more rational treatment,more scientific evaluation of treatment effect,more accurate assessment of the prognosis for gastric cancer patients.However,with the widespread clinical application and further validation,as well as the discovery of new predictors,there will be new staging systems to replace and refine the old staging system.
Gastric cancer; TNM staging; Tumor staging; Union for International Cancer Control (UICC); American Joint Committee of Cancer (AJCC)
400016 重庆,重庆医科大学附属第一医院胃肠外科
王子卫,Email:wangziwei571@sina.com
R735.2
A
10.3969/j.issn.1003-5591.2017.04.002
2017-06-08)
