胃癌根治术后非计划再手术的影响因素分析
2017-09-03刘紫麟谢杰斌鹿飞花霞杨玉芹唐锦何劲松王攀魏寿江王崇树肖江卫
刘紫麟 谢杰斌 鹿飞 花霞 杨玉芹 唐锦 何劲松王攀 魏寿江 王崇树 肖江卫
·论 著·(胃癌专题)
胃癌根治术后非计划再手术的影响因素分析
刘紫麟 谢杰斌 鹿飞 花霞 杨玉芹 唐锦 何劲松王攀 魏寿江 王崇树 肖江卫
目的 探讨胃癌非计划再手术病例的临床特点,总结其临床治疗与预防措施。方法 回顾分析2015年1月至2017年5月川北医学院附属医院胃肠外科15例非计划再手术病人的临床资料,并与同期非再手术组452例病人临床资料进行对比,分析比较两组病例的一般情况、合并基础疾病情况、手术及术后病理相关资料的差异。结果 非计划再次手术发生率为2.5%,死亡率为46.7%;非计划再手术的原因包括十二指肠残端漏、食管空肠吻合口漏、出血、腹腔感染、肠梗阻、切口裂开等。非计划再次手术的发生与术前合并风湿性疾病(P=0.040)、低蛋白血症(P=0.002)、呼吸系统疾病(P=0.016)等基础疾病以及首次手术时间(P=0.045)、美国麻醉医师协会(ASA)分级(P=0.010)、淋巴结转移情况(P=0.015)有关;两组间肿瘤所在的位置、肿瘤直径、浸润深度以及术后TNM分期差异均无统计学意义(均P>0.05)。结论 及时发现并发症并积极处理可降低非计划再次手术的死亡率;针对非计划再次手术风险的充分术前准备、规范的手术操作,预防和减少手术并发症的发生,才能减少胃癌根治术后非计划再次手术的发生。
胃癌; 胃癌根治术; 术后并发症; 非计划再手术
胃癌是我国乃至全世界最常见的恶性肿瘤之一,已成为我国癌症发病率和死亡率的第二位[1-2]。以手术为主的综合治疗,仍然是目前胃癌治疗的主要手段[3]。随着手术器械的改良以及胃肠外科学者对胃癌根治手术理论的完善,伴随胃癌根治手术而来的术后并发症发生率逐渐下降,但仍然是胃肠外科医生不可规避的重大课题[4-6]。及时有效的治疗是降低围手术期病死率的关键,但部分严重的并发症仍需要再次手术干预[5,7]。本文回顾分析2015年1月至2017年5月川北医学院附属医院胃肠外科收治的606例胃癌根治术病人中15例非计划再手术(30 d以内行再次手术干预)病人的临床资料,分析胃癌非计划再手术的影响因素、探讨其临床治疗。现报告如下。
资料与方法
一、一般资料
川北医学院附属医院共收治并行胃癌D2根治术病人606例,其中15例病人因术后发生严重并发症而行非计划再手术干预。15例非计划再手术病人均为全胃切除或远端胃切除术病人。为确保对比的一致性,本研究去除606例病人中139例行近端胃切除、保留胃窦空肠间置双通道术式病人。所有病人术前均行胃镜活检确诊为胃癌,术前常规性胸片、心电图、心脏超声、腹部CT/MRI等辅助检查确认未发现远处转移、可达到手术根治且无绝对手术禁忌。
二、方法
所有病例均由川北医学院附属医院胃肠外科各医疗组完成,所有主刀医生均系有胃肠肿瘤根治术5年以上手术经验者,手术根治原则按照日本胃癌协会《日本胃癌治疗指南,2014》原则行D2或D2+淋巴结清扫[8];肿瘤分期采用国际抗癌联盟(UICC)2010年第7版TNM分期。对比452例行全胃切除或远端胃切除术病人(非再次手术组)与15例非计划再手术病人(再次手术组)术前一般情况及合并基础疾病、手术相关资料、术后病理特征(表1、2),分析非计划再手术病例的临床治疗策略及转归情况,探讨非计划再手术的临床相关因素及预防措施。
病人术前一般情况比较包括性别、年龄、体质量指数(BMI)以及术前血红蛋白;合并基础疾病包括内分泌与代谢性疾病(如需要药物治疗的糖尿病、甲状腺功能亢进、甲状腺功能减退、甲状腺旁腺功能亢进、嗜铬细胞瘤、痛风等)、风湿性疾病(如需要药物治疗的类风湿性关节炎、系统性红斑狼疮、血管炎)、低蛋白血症、心脑血管疾病、呼吸系统疾病(肺部感染、胸腔积液、支气管扩张、慢性阻塞性肺疾病、间质性肺炎等)。
按照前述肿瘤根治原则完成肿瘤切除、淋巴结清扫后,纳入病例中消化道重建方式为Roux-en-Y、Billroth Ⅱ、Billroth Ⅱ+Brawn吻合三种方式之一,具体重建方式描述如下:①Roux-en-Y重建方式,距Treitz韧带12~15 cm处离断空肠,近断端空肠与距Treitz韧带50 cm处空肠行侧侧吻合,远断端空肠与食管行食管空肠端侧吻合;②Billroth Ⅱ方式,距Treitz韧带15 cm处行空肠与残胃后壁侧侧吻合;③Billroth Ⅱ+Brawn吻合方式:距Treitz韧带12 cm处空肠与与距Treitz韧带50 cm处空肠行侧侧吻合,距Treitz韧带15 cm处行空肠与残胃后壁侧侧吻合。
三、统计学方法
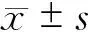
结 果
一、术前一般情况及合并基础疾病情况
再次手术组与非再次手术组比较,两组病例男女性别比例分别为10/5和248/204、平均年龄分别为(61.20±10.35)岁和(62.05±7.47)岁、BMI分别为(22.54±3.71) kg/m2和(21.15±2.63) kg/m2,术前血红蛋白分别为(102.00±31.88) g/L和(113.00±21.32) g/L,一般情况差异无统计学意义;两组病例术前合并的基础疾病中风湿性疾病、低蛋白血症、呼吸系统疾病比较差异有统计学意义,然而,比较术前合并的内分泌与代谢性疾病、心脑血管疾病差异并无统计学意义。(表1)
二、手术及术后病理相关情况比较
与非再次手术组相比,再次手术组病例手术时间略长,分别为(282.67±59.46) min和(253.18±46.70) min,P=0.045,差异有统计学意义。美国麻醉医师协会(ASA)手术病人病情分级比较差异有统计学意义。两组病例胃癌癌肿所在的位置、肿瘤直径、浸润深度以及术后TNM分期比较,差异均无统计学意义,但两组病例淋巴结转移情况比较,差异具有统计学意义。(表2)
三、非计划再手术病例的临床治疗及转归结局
2015年1月至2017年5月,我院胃肠外科606例胃癌根治术病人中,15例病人行非计划再次手术(2.5%),其中7例在术后30 d内死亡,8例恢复良好后出院,具体见表3。15例病人中,全胃切除+D2淋巴结清扫术病人8例,远端胃切除+D2淋巴结清扫术病人7例。非计划再次手术的原因包括十二指肠残端漏6例次、食管空肠吻合口漏3例次、出血5例次、腹腔感染1例次、肠梗阻2例次、切口裂开1例次。再次手术处理方式有修补、缝合止血、肠减压、内镜结扎等,术中常规行腹腔冲洗、置管引流。

表1 再次手术组与非再手术组病例术前一般情况与合并基础疾病情况比较
注:“-”表示统计检验采用Fisher确切概率计算,无特定统计量值。
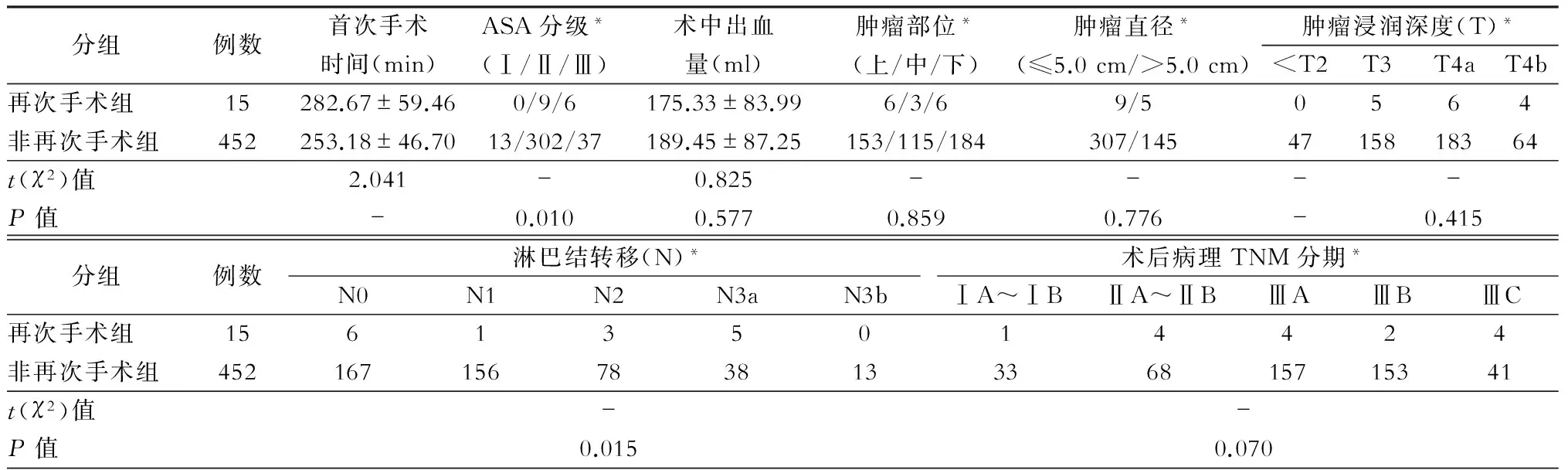
表2 再次手术组与非再次手术组病例手术及术后病理相关情况比较
注:标准*项数据单位为“例”;“-”表示统计检验采用Fisher确切概率计算,无特定统计量值。
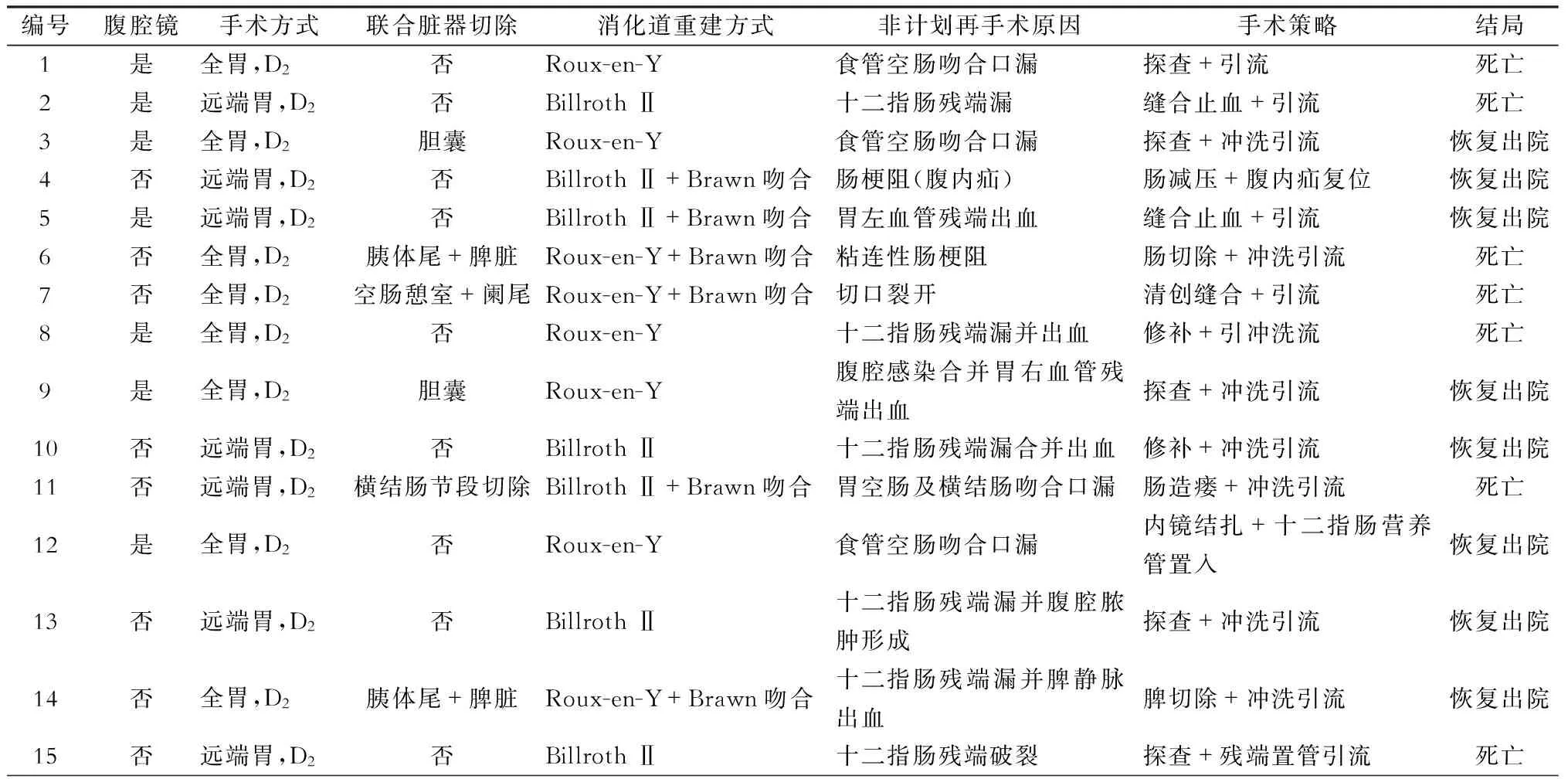
表3 15例非计划再手术病例的临床治疗及转归结局
讨 论
目前,胃癌的治疗仍然是以外科手术治疗为核心的综合治疗[3]。胃癌手术所伴随的并发症尤其是围手术期并发症的防治一直以来都是伴随外科医生职业生涯的重大课题,直接影响病人的康复与远期疗效。
我们的数据显示,胃癌根治术后非计划再次手术率为2.5%,而非计划再次手术病人死亡率为46.7%(7/15)。再次手术组与非再次手术组病例对比,一般情况指标差异并无统计学意义。术前合并需要治疗的风湿性疾病、低蛋白血症、呼吸系统疾病在一定程度上可增加病人的非计划再手术率。有文献报道[7,9-10],合并糖尿病、甲状腺功能亢进等内分泌与代谢性疾病可增加病人术后吻合口漏、切口感染等并发症,部分严重病例仍然需要再次手术干预。我们的数据中并未显示合并内分泌与代谢性疾病在两组比较中差异具有统计学意义,这可能需要更大的数据样本来进一步证实。两组病例术中情况及术后病理学资料比较显示,肿瘤的部位、最大直径、局部浸润深度(T)以及总的TNM分期差异并无统计学意义;首次术前ASA分级、术后的淋巴结转移情况比较,两组差异具有统计学意义。与非再次手术组相比,合并多种基础疾病,必然升高术前的ASA分级,导致相对较大的手术风险,增加围手术期的风险及并发症发生,影响病人的正常康复和远期结局。因此,合并基础疾病及较多的淋巴结转移数量是影响病人术后恢复、增加非计划再次手术风险的重要因素之一。值得注意的是,再次手术组病例术前合并呼吸系统疾病比例明显高于非再次手术组,术后呼吸系统并发症,如胸腔积液、肺部感染者,更是显著高于非再次手术组,这可能是再次手术组病例术后需进入重症监护室行呼吸机辅助治疗、延长住院时间、增加住院费用、增加再次手术组术后死亡率的又一重要原因。
15例非计划再手术病人中,经腹腔镜手术7例,开腹手术8例;手术方式全胃切除+D2淋巴结清扫8例,远端胃大部切除+D2淋巴结清扫7例,本组数据中显示再次手术的发生与是否腹腔镜手术和手术方式没有明确相关性。从我们的资料来看,胃癌根治术后非计划再次手术的主要原因依次为十二指肠残端漏、出血、食管空肠吻合口漏、肠梗阻、腹腔感染、切口裂开,这与文献报道的原因大同小异。另外,文献报道胃癌根治术后再次手术的原因还包括吻合口狭窄、乳糜漏、胰漏、继发性胆囊炎、应激性溃疡大出血、术中其余肠管副损伤所致的迟发性穿孔、切口疝等[4-6,11-12]。
再次手术处理方式以吻合口漏修补、缝合止血、肠减压、内镜结扎为主,术中常规行腹腔冲洗、置管引流对于非计划再次手术的治疗尤其关键。以我们的经验来看,非计划再次手术的治疗主要包括四个环节:①手术术中处理环节。术后早期(24~48 h以内)的出血、吻合口破裂、切口裂开、肠梗阻可以经再次手术缝扎止血、漏口修补、清创缝合、肠排列等处理,但前提是病人具有能够承受再次手术的身体条件,而对于本身合并心脏、呼吸系统等重大基础疾病的病人,严重并发症的发生将可能是致命一击。从表3资料我们可以看出,除确切的出血、梗阻行止血、解除梗阻治疗外,仍然以腹腔冲洗、引流为主。内镜及介入技术的发展为部分出血或微小漏病人提供了保守治疗康复的可能。我们的资料亦有1例食管空肠吻合口漏经内镜夹闭漏口后康复出院的病例。对于术后超过3 d的病例,再次手术时大多因手术区域及肠管的炎性肿胀,漏口无从修补,此时彻底地冲洗和充分地引流决定了再次手术的成败。②术后的针对性药物治疗。对于再次手术的病人,术后的强化抗感染尤为重要。我们的经验是增加肠道菌群移位和呼吸道感染常见菌的提前预防治疗可以一定程度减少感染的发生,同时乌司他丁等稳定细胞膜药物、生长抑素或者奥曲肽等的运用,可减少胃肠道的分泌、减少吻合口压力、减轻炎症反应、防止再出血等发生。 ③强化的营养支持。根据病人的体重及应急情况,准确地计算病人糖、脂肪、蛋白质的需要量,维持正氮平衡;一定晶体与胶体比例可减少术后创面渗出;维持正常的水电解质、血糖水平、酸碱平衡。④确切的护理,包括病人静脉通道以及引流管的护理管理、排痰管理、躯体活动的护理可促进病人的身心恢复、减少其他院内并发症的发生。
因此,及时发现并发症并积极处理可降低非计划再次手术的死亡率;针对再手术风险的充分术前准备、规范精细化的手术操作、良好配合的外科团队以及新技术的开发运用,预防和减少手术并发症的发生,方能从源头上减少胃癌根治术后非计划再次手术的发生。
1 Chen W,Zheng R,Baade PD,et al.Cancer statistics in China,2015.CA Cancer J Clin,2016,66:115-132.DOI: 10.3322/caac.21338.
2 Siegel RL,Miller KD,Jemal A.Cancer Statistics, 2017.CA Cancer J Clin,2017,67:7-30.DOI:10.3322/ caac.21387.
3 Van Cutsem E,Sagaert X,Topal B,et al.Gastric cancer.The Lancet,2016,388:2654-2664.DOI:10. 1016/S0140-6736(16)30354-3.
4 Kubota T,Hiki N,Sano T,et al.Prognostic significance of complications after curative surgery for gastric cancer.Ann Surg Oncol,2014,21:891-898. DOI:10.1245/s10434-013-3384-9.
5 Papenfuss WA,Kukar M,Oxenberg J,et al.Morbidity and mortality associated with gastrectomy for gastric cancer.Ann Surg Oncol,2014,21:3008-3014. DOI:10.1245/s10434-014-3664-z.
6 Li P,Huang CM,Tu RH,et al.Risk factors affecting unplanned reoperation after laparoscopic gastrectomy for gastric cancer: experience from a high-volume center.Surg Endosc,2017.DOI: 10.1007/s00464-017-5423-2.
7 Yi HW,Kim SM,Kim SH,et al.Complications leading reoperation after gastrectomy in patients with gastric cancer: frequency, type, and potential causes.J Gastric Cancer,2013,13:242-246.DOI: 10.5230/jgc.2013.13.4.242.
8 Japanese Gastric Cancer A.Japanese gastric cancer treatment guidelines 2014 (ver. 4).Gastric Cancer, 2017,20:1-19.DOI:10.1007/s10120-016-0622-4.
9 Guevara OA,Rubio-Romero JA,Ruiz-Parra AI. Unplanned reoperations: is emergency surgery a risk factor?A cohort study.J Surg Res,2013,182: 11-16. DOI:10.1016/j.jss.2012.07.060.
10Yu J,Hu J,Huang C,et al.The impact of age and comorbidity on postoperative complications in patients with advanced gastric cancer after laparoscopic D2 gastrectomy:results from the Chinese laparoscropic gastrointestinal surgery study (CLASS) group.Eur J Surg Oncol,2013,39:1144-1149.DOI:10.1016/j.ejso.2013.06.021.
11Hayashi T,Yoshikawa T,Aoyama T,et al.Impact of infectious complications on gastric cancer recurrence.Gastric Cancer,2015,18:368-374.DOI:10. 1007/s10120-014-0361-3.
12Climent M,Hidalgo N,Vidal O,et al.Postoperative complications do not impact on recurrence and survival after curative resection of gastric cancer.Eur J Surg Oncol,2016,42:132-139.DOI: 10.1016/j.ejso. 2015.08.163.
The risk factors and clinical treatment retrospective exploration for unplanned reoperation after gastrectomy in gastric cancer patients
Liu Zilin,Xie Jiebin,Lu Fei,Hua Xia,Yang Yuqin,Tang Jin,He Jingsong,Wang Pan,Wei Shoujiang,Wang Chongshu,Xiao Jiangwei.
Department of Gastrointestinal Surgery,Institute of Hepatobiliary,Pancreas and Intestinal Disease,the Affiliated Hospital of North Sichuan Medical College,Nanchong 637000,China
Xiao Jiangwei,Email:xiaojiangwei@126.com
Objective To investigate the clinical characteristics of gastric cancer patients undergoing unplanned reoperation after gastrectomy and summarize their clinical treatment and preventive measures.Methods The clinical data of 15 patients with unplanned reoperation after gastrectomy,compared with those of 452 patients without reoperation in the same period,were analyzed retrospectively between January 2015 and May 2017 in Department of Gastrointestinal Surgery,the Affiliated Hospital of North Sichuan Medical College.The general clinical characteristics,comorbidities,surgery and postoperative pathology data were compared between the two groups.Results The incidence of unplanned reoperation was 2.5% and its mortality rate was 46.7%.The main causes requiring unplanned reoperation were duodenal stump leakage,esophageal jejunum anastomotic leakage,hemorrhage,abdominal infection,intestinal obstruction and incision dehiscence.Compared to the non-reoperation group,the unplanned reoperation group had a significantly longer operation time (P=0.045),severer ASA grade (P=0.010),more extensive lymph node metastasis (P=0.015) and higher ratio of comorbidities,such as rheumatic disease (P=0.040),hypoalbuminemia (P=0.002),respiratory disease (P=0.016),whereas,there was no significant difference in tumor location,tumor diameter,deep infiltration and postoperative TNM staging (P>0.05).Conclusions It is very important to detect the occurrence of complications timely and deal with them actively to reduce the mortality of unplanned reoperation.Properly preoperative preparation contraposing the risks of unplanned reoperation and standard radical resection are necessary to decrease the morbidity of complications in order to reduce the incidence of unplanned reoperation.
Gastric cancer; Radical gastrectomy; Gastrectomy; Postoperative complications; Unplanned reoperation
四川省教育厅项目(No. 14ZA0192)
637000 四川南充,川北医学院附属医院胃肠外科 川北医学院肝胆胰肠研究所
肖江卫,Email:xiaojiangwei@126.com
R735.2
A
10.3969/j.issn.1003-5591.2017.04.008
2017-06-29)
