放大内镜联合窄带成像在胃部早期肿瘤性病变患者中的应用效果
2017-08-22叶慧玲朱建丽杨上文
叶慧玲,朱建丽,杨上文
(浙江省丽水市中心医院 1.体检中心;2.门诊部;3.消化内科,浙江 丽水 323000)
放大内镜联合窄带成像在胃部早期肿瘤性病变患者中的应用效果
叶慧玲1,朱建丽2,杨上文3
(浙江省丽水市中心医院 1.体检中心;2.门诊部;3.消化内科,浙江 丽水 323000)
目的 探讨放大内镜联合窄带成像(ME-NBI)在胃部早期肿瘤性病变患者中的应用效果。方法选取2013年1月-2016年6月于该院消化内镜中心行内镜检查的151例可疑胃早癌患者为研究对象,所有患者先行普通白光内镜(WLE)检查,然后行ME-NBI检查和靶向活检,重点测量腺管间质距离(以下简称腺间距),根据病理结果分为早癌组[高级别上皮内瘤变(HGIN)、黏膜内癌、黏膜下癌,n =72]和非早癌组[低级别上皮内瘤变(LGIN),n =79]。比较两组的基线资料和ME-NBI征象,采用受试者工作曲线下面积(AUC)来评价其对胃早癌的诊断价值。结果早癌组的边界线、不规则的黏膜微血管、不规则的表面腺管和腺间距升高的发生率明显高于非早癌组,差异有统计学意义(P <0.05)。ME-NBI对胃早癌的AUC为0.947,高于WLE的0.832,具有较高的诊断价值,其灵敏度(Se)、特异度(Sp)、阳性预测值(PPV)、阴性预测值(NPV)和Youden指数分别为97.2%、84.8%、85.4%、97.1%和0.820。腺间距对胃早癌的AUC为0.907,高于传统微血管纹理与表面结构(VS)分型的0.889,且VS分型与腺间距进行联合诊断的AUC达到0.933,其Se、Sp、PPV、NPV和Youden指数分别为95.8%、83.5%、84.1%、95.7%和0.794。结论ME-NBI是胃早癌的重要诊断方法,腺间距具有客观性强、简便易行和可重复性好的优点,能辅助传统VS分型来判断病变性质。
放大内镜;窄带成像;腺管间质距离;胃癌;早期诊断
随着消化内镜技术的迅速发展,近年来在普通白光内镜(white light endoscopy,WLE)的基础上不断涌现出多种新型内镜技术,包括放大内镜(magnifying endoscope,ME)、窄带成像内镜(narrowband imaging,NBI)、色素内镜和共聚焦激光纤维内镜等,这些胃镜精检有助于发现WLE遗漏的早癌病灶[1]。其中,ME可对胃肠道黏膜进行内镜下的放大观察,主要包括黏膜表面的微血管及其他微细结构的形态,帮助判断病灶的性质[2-3];NBI是一种利用了窄波光成像的新型内镜技术,通过符合黏膜组织及血色素光谱特性的窄波光来观察血管和黏膜表面的细微变化,与染色内镜相比,NBI对肿瘤性病变的边界判断更加准确[4-5]。基于以上原理,ME和NBI两种内镜技术可互相补充,两者的结合在临床上越来越常见,更加清晰地观察病灶表面的结构和血管结构,提高食管、胃的早期肿瘤学病变的检出率[6]。但以往研究多为直接观察性研究,缺乏客观指标,主观性较强。本研究通过ME-NBI系统测算疑似为胃肿瘤性病灶与周围正常组织的腺管间质距离(以下简称腺间距),以此来反映微腺管的密度,旨在探讨腺间距对胃早癌的应用价值,为临床提供参考依据。现报道如下:
1 资料与方法
1.1 一般资料
选取2013年1月-2016年6月于我院消化内镜中心行内镜检查的151例可疑胃早癌患者为研究对象。其中,男106例,女45例,年龄41~82岁,平均(63.7±9.0)岁。所有患者均首先行WLE检查发现胃内存在可疑的浅表型肿瘤型病变,然后行MENBI检查,并行靶向活检,结果提示低级别上皮内瘤 变(low grade intraepithelial neoplasia,LGIN)、 高级别上皮内瘤变(high grade intraepithelial neoplasia,HGIN)、黏膜内癌或黏膜下癌。排除存在胃镜检查及活检禁忌证的患者。本研究所有患者均已签署知情同意书,已获得本院医学伦理委员会的批准。
1.2 方法及分组
1.2.1 内镜检查 所有患者均由同一组高年资、经验丰富的胃镜医师进行检查,在行内镜检查前均禁食12 h、禁饮6 h以上,常规完成WLE检查,依次观察食管全段、贲门、胃体、胃窦、幽门和十二指肠,发现黏膜异常病灶后进行重点观察,记录其位置、形态、范围和色泽等,通过注气和吸气来观察局部的病灶硬度。然后行ME-NBI检查,仔细观察、对比其周围正常黏膜与病灶的表面微结构,包括有无边界线、不规则的黏膜微血管和不规则的表面腺管等,并测量腺间距[7-8]:将1个清晰的正常胃部黏膜的腺间距定为1,然后测量其他部位的腺间距,数值为所定义的腺间距的相对值,在同一个视野下测量同一个病变区3个腺间距,算平均值,以此作为该病变区的腺管密度。腺间距值越大,提示该区域单位体积内的腺体数量越多,密度越大,若腺间距>1.2,则视为腺管密度显著升高。对于白色区域显示不清或消失的病变,则以上皮下微血管间的距离代替腺间距。
1.2.2 靶向活检及分组 根据病变的位置、形态、直径及ME-NBI检查结果,并结合微血管纹理与表面结构分型(VS)标准进行靶向活检,将标本送至病理科的1位高年资医师行病理检查,该医师对胃镜结果毫不知情。根据活检结果将所有患者分为早癌组(HGIN、黏膜内癌与黏膜下癌)和非早癌组(LGIN),均行相应的处理,对LGIN患者则根据患者的意愿及镜下表现,让患者选择行内镜黏膜下剥离术(endoscopic submucosa disection,ESD)或定期随访,对早癌患者行ESD或外科手术。全部151例患者的病理结果为LGIN 79例、HGIN 62例、黏膜内癌5例、黏膜下癌5例,分为早癌组(n =72)和非早癌组(n =79)。两组的男性比例和年龄比较差异无统计学意义,见表1。
1.3 统计学方法
所有资料均采用SPSS 19.0统计学软件进行统计分析。计数资料采用χ2检验,计量资料以均数±标准差(±s)表示,比较用t检验。计算WLE、ME-NBI、VS分型等对胃早癌的敏感度(sensitivity,Se)、特异度(specificity,Sp)、阳性预测值(positive predictive value,PPV)、阴性预测值(negative predictive value,NPV)与Youden指数,并绘制其受试者工作曲线(receiver operator characteristic curve,ROC),根据曲线下面积(area under the curve,AUC)评价各指标的诊断价值。P <0.05为差异有统计学意义。
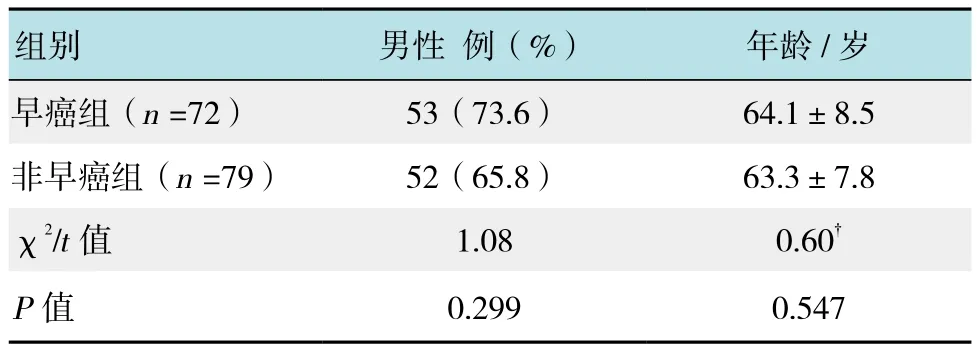
表1 两组患者基线资料Table 1 Comparison of baseline data between the two groups
2 结果
2.1 两组ME-NBI征象比较
结果表明,早癌组的边界线、不规则的黏膜微血管、不规则的表面腺管和腺间距升高的发生率明显高于非早癌组,差异有统计学意义(P <0.05)。见表2。镜下图片见图1。
2.2 WLE和ME-NBI对胃早癌的诊断效果比较
结果表明,WLE和ME-NBI对胃早癌均有一定的诊断效果,其中ME-NBI的AUC为0.947>0.9,具有较高的诊断价值,高于WLE的0.832,其Se、Sp、PPV、NPV和Youden指 数 分 别 为97.2%、84.8%、85.4%、97.1%和0.820,见表3。WLE和ME-NBI对胃早癌的ROC曲线见图2。
2.3 VS分型和腺间距对胃早癌的诊断效果比较
结果表明,VS分型和腺间距对胃早癌均有一定的诊断效果,其中腺间距的AUC=0.907>0.9,具有较高的诊断价值,高于VS分型的0.889。并且,将VS分型与腺间距进行联合诊断时的价值更高,AUC达到0.933,其Se、Sp、PPV、NPV和Youden指数分别为95.8%、83.5%、84.1%、95.7%和0.794,见表4。ROC曲线见图3。

表2 两组ME-NBI征象比较 例(%)Table 2 Comparison of ME-NBI signs between the two groups n(%)

图1 内镜下所见Fig.1 Endoscopic findings
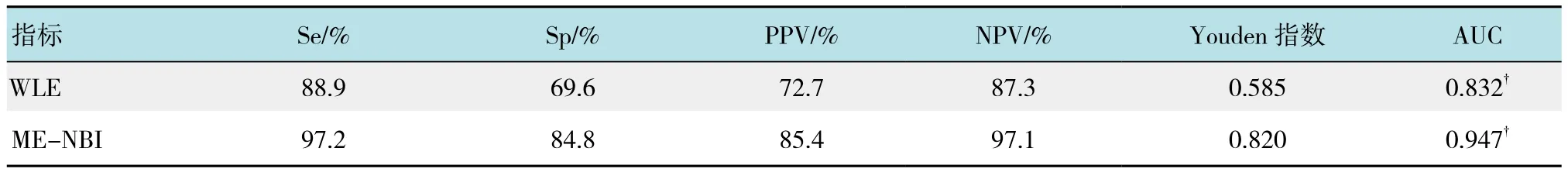
表3 WLE和ME-NBI对胃早癌的诊断效果比较Table 3 Comparison of diagnosis effect of early gastric cancer between WLE and ME-NBI

表4 VS分型和腺间距对胃早癌的诊断效果比较Table 4 Comparison of diagnosis effect of early gastric cancer between VS typing and glandular distance

图2 WLE和ME-NBI对胃早癌的ROC曲线Fig.2 ROC curve of WLE and ME-NBI on early gastric cancer
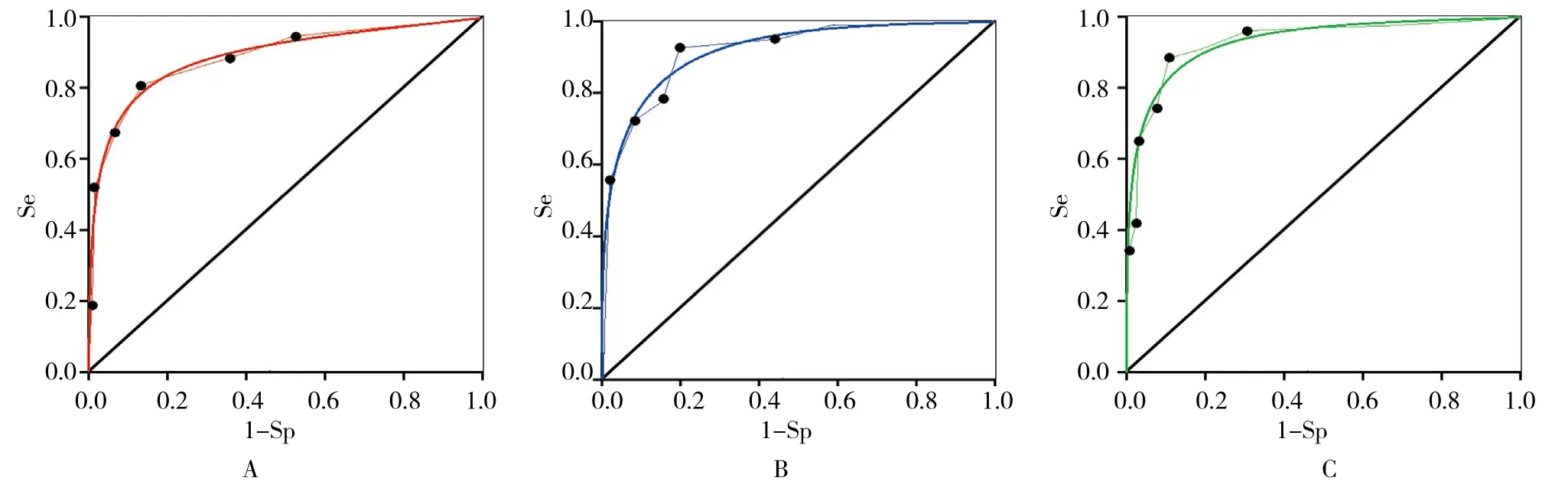
图3 VS分型和腺间距对胃早癌的诊断价值ROC曲线Fig.3 ROC curve of VS typing and glandular distance on early gastric cancer
3 讨论
对于胃早癌患者而言,早期发现并及时进行相应的处理能显著改善其预后,提高其生活质量,这主要依赖于消化内镜技术的发展,能灵敏地判断疑似肿瘤患者的病灶性质,预测其是否为HGIN或早期胃癌。黏膜微血管与组织的增生是胃早癌的主要病理学特征,前者是肿瘤生长、浸润、转移的前提,后者可导致腺体的密集、扭曲、破坏,故仔细观察病灶微血管与腺体的改变有助于判断其性质。与WLE相比,ME-NBI的一大优点就是能将感兴趣区域的消化道黏膜表面结构放大接近100倍,故能更清晰地观察腺体的形态,且通过NBI能重点显示黏膜的微血管,结合其放大功能,有助于评估病灶黏膜微血管的形态[9],故ME-NBI可同时评价消化道黏膜微血管和腺体的增生情况,由此来辅助判断病灶的性质。
以往国内外的多个研究[6,10-13]均报道ME-NBI在诊断胃早癌方面比WLE更加准确、可靠,且能指导靶向活检,有助于提高活检的准确率。2002年,YAO等[14]在国内外首先报道了分化型胃腺癌在MI-NBI下的特征性表现,并提出了早期胃癌的VS分型,该分型主要依据的是胃黏膜的微血管和表面结构的形态以及边界的异常,其认为若病灶存在不规则的黏膜微血管或不规则的表面腺管,且病灶与周围正常组织有边界线,即可诊断为肿瘤性病灶。2011年,郭涛等[15]初步建立了一个ME-NBI诊断早期胃癌的国内标准,其需同时满足黏膜腺管开口形态紊乱不规则或消失、黏膜微血管形态紊乱不规则或毛细血管网消失、病变与周围黏膜分界这三个条件,其认为这些是最为特征性的改变,且ME-NBI对早期胃癌的Se、Sp、PPV和NPV分别为73.7%、99.2%、93.3%和96.3%,准确性明显高于WLE。本研究同样发现早癌组的边界线、不规则的黏膜微血管、不规则的表面腺管的发生率明显高于非早癌组,且ME-NBI对胃早癌的AUC高达0.947,高于WLE的0.832,具有较高的诊断价值,其Se、Sp、PPV、NPV和Youden指数分别为97.2%、84.8%、85.4%、97.1%和0.820。以往的研究对病灶的ME-NBI下表现主要为主观性描述,缺乏一个客观性的指标来辅助判断病灶的腺体或微血管改变。
在浅表平坦型病变里,黏膜微血管常表现为密度增加、增粗、形态不规则,表面腺管则主要表现为萎缩性改变;浅表凹陷型病变的黏膜微血管也表现为密度增加、增粗、形态不规则,有多种形态,如螺丝样、网状等,表面腺管常遭受不同程度的破坏,局部可有密集的腺管,部分显示不清、脱落;隆起型病变的黏膜微血管除了有增粗和扭曲改变外,其形态常表现为环状或网状,聚集在腺管的开口,表面腺管的改变以扭曲、拉伸、开口扩展和间质密集等为主。本研究发现不同形态的胃早癌病灶的黏膜微血管与表面腺管的变化有所差异,但多表现为表面腺管和微血管密集的现象,故采用腺间距这个客观指标通过反应腺管的密度,可在理论上有助于判断病灶的性质。
YAGI等[8]比较了30例早期胃癌ME-NBI下的腺间距与光镜下病理组织中腺间距、腺体深度的关系,发现早期胃癌的腺间距明显升高,腺管的长度与密度均显著增加,形态扭曲。本研究以病灶区域与周围正常组织的腺间距比值来客观反映腺管密度,其值越大提示腺管越密集,从而辅助判断病灶的性质。参考以往文献及我科的临床经验,本研究以1.2为临界值,高于此值提示腺管密度明显升高,结果表明早癌组的腺间距升高率高达86.1%,明显高于非早癌组的46.8%(P <0.05)。本研究还发现腺间距的AUC达到0.907,具有较高的诊断价值,高于传统VS分型的0.889,且如果将VS分型与腺间距进行联合诊断,其AUC可达到0.933,其Se、Sp、PPV、NPV和Youden指数分别为95.8%、83.5%、84.1%、95.7%和0.794,诊断价值更加令人满意。VS分型主要以黏膜微血管和表面结构是否规则来进行判断,其主观性较大,而腺间距是一个相对客观的指标,能重复测量,数次测量后取其平均值能提高其准确度,两者相结合后诊断效能更高。
综上所述,ME-NBI是胃早癌的重要诊断方法,腺间距具有客观性强、简便易行、可重复性好的优点,能辅助传统VS分型来判断病变性质。
[1]徐凯, 徐萍, 陶元生, 等. 胃镜精检在首次胃镜提示胃癌前病变中的应用价值[J]. 中国内镜杂志, 2016, 22(11): 83-87.
[1]XU K, XU P, TAO Y S, et al. Clinical value of intensive endoscopic examination for gastric precancerouslesion diagnosed by first endoscopic examination[J]. China Journal of Endoscopy, 2016,22(11): 83-87. Chinese
[2]YAO K, ANAGNOSTOPOULOS G K, RAGUNATH K. Magnifying endoscopy for diagnosing and delineating early gastric cancer[J].Endoscopy, 2009, 41(5): 462-467.
[3]曹彬, 胡宏艳, 周永清, 等. 放大胃镜对胃黏膜隆起病变定性诊断的临床研究[J]. 中国内镜杂志, 2015, 21(11): 1138-1143.
[3]CAO B, HU H Y, ZHOU Y Q, et al. Clinical research of magnification endoscopy for the qualitative diagnosis of uplift of gastric mucosa lesion[J]. China Journal of Endoscopy, 2015, 21(11): 1138-1143.Chinese
[4]NAGAHAMA T, YAO K, MAKI S, et al. Usefulness of magnifying endoscopy with narrow-band imaging for determining the horizontal extent of early gastric cancer when there is an unclear margin by chromoendoscopy (with video)[J]. Gastrointest Endosc,2011, 74(6): 1259-1267.
[5]WADA M, TAKAHASHI Y, ISEKI C, et al. Plasma fibrinogen,global cognitive function, and cerebral small vessel disease:results of a cross-sectional study in community-dwelling Japanese elderly[J]. Intern Med, 2011, 50(9): 999-1007.
[6]KATO M, KAISE M, YONEZAWA J, et al. Magnifying endoscopy with narrow-band imaging achieves superior accuracy in the differential diagnosis of superficial gastric lesions identified with white-light endoscopy: a prospective study[J]. Gastrointest Endosc,2010,72(3):523-529.
[7]YAO K, NAGAHAMA T, MATSUI T, et al. Detection and characterization of early gastric cancer for curative endoscopic submucosal dissection[J]. Dig Endosc, 2013, 25(Suppl 1): 44-54.
[8]YAGI K, NOZAWA Y, ENDOU S, et al. Diagnosis of early gastric cancer by magnifying endoscopy with nbi from viewpoint of histological imaging: mucosal patterning in terms of white zone visibility and its relationship to histology[J]. Diagn Ther Endosc,2012, 2012: 954809.
[9]牛昊书, 陈海华, 伏亦伟, 等. 窄带成像结合放大内镜技术观察胃表面微血管在早期胃癌诊断中的价值[J]. 胃肠病学和肝病学杂志, 2015, 24(10): 1192-1195.
[9]NIU H S, CHEN H H, FU Y W, et al. Value of magnifying endoscopy with narrow band imaging to observe microvascular architecture for diagnosis of early gastric cancer[J]. Chinese Journal of Gastroenterology and Hepatology, 2015, 24(10): 1192-1195. Chinese
[10]TAO G, XING-HUA L, AI-MING Y, et al. Enhanced magnifying endoscopy for differential diagnosis of superficial gastric lesions identified with white-light endoscopy[J]. Gastric Cancer, 2014,17(1): 122-129.
[11]KAISE M, KATO M, URASHIMA M, et al. Magnifying endoscopy combined with narrow-band imaging for differential diagnosis of superficial depressed gastric lesions[J]. Endoscopy,2009, 41(4): 310-315.
[12]王芳军, 汪娟, 赵可, 等. 放大结合窄带成像在上消化道内镜检查中指导靶向活检的价值[J]. 中华消化内镜杂志, 2014,31(7): 393-397.
[12]WANG F J, WANG J, ZHAO K, et al. The value of magnifying endoscopy combined with narrow-band imaging for targeting biopsy of lesions in upper gastrointestinal tract[J]. Chinese Journal of Digestive Endoscopy, 2014, 31(7): 393-397. Chinese
[13]EZOE Y, MUTO M, HORIMATSU T, et al. Magnifying narrowband imaging versus magnifying white-light imaging for the differential diagnosis of gastric small depressive lesions: a prospective study[J]. Gastrointest Endosc, 2010, 71(3): 477-484.
[14]YAO K, OISHI T, MATSUI T, et al. Novel magnified endoscopic findings of microvascular architecture in intramucosal gastric cancer[J]. Gastrointest Endosc, 2002, 56(2): 279-284.
[15]郭涛, 陆星华, 周炜洵, 等. 放大胃镜结合窄带成像技术在早期胃癌诊断中的应用价值研究[J].中华消化内镜杂志, 2011,28(7): 375-379.
[15]GUO T, LU X H, ZHOU W X, et al. Magnifying endoscopy with narrow-band imaging for early gastric cancer diagnosis[J].Chinese Journal of Digestive Endoscopy, 2011, 28(7): 375-379.Chinese
(吴静 编辑)
Effect of magnifying endoscopy with narrow-band imaging in diagnosis of early gastric neoplastic lesion
Hui-ling Ye1, Jian-li Zhu2, Shang-wen Yang3
(1.Department of Medical Center; 2.Department of Outpatient; 3.Department of Digestive Diseases,Lishui Center Hospital, Lishui, Zhejiang 323000, China)
ObjectiveTo investigate the effect of magnifying endoscopy with narrow-band imaging (MENBI) in diagnosis of early gastric neoplastic lesion.Methods151 patients with suspected gastric cancer underwent endoscopic examination in digestive endoscopy center from January 2013 to June 2016 were enrolled the study. They firstly
conventional white light endoscopy (WLE), then ME-NBI (including intervening part) and targeted biopsy. And all patients were divided into early cancer group (high grade intraepithelial neoplasia, intramucosal carcinoma and submucosal carcinoma, n = 72) and non-early cancer group (low grade intraepithelial neoplasia,n = 79). The area under receiver-operating characteristic curve (AUC) was performed to evaluate prognostic value of each index in early cancer.ResultsThe incidences of the demarcation line, irregular microvascular pattern, irregular microsurface pattern and increasing intervening part in early cancer group were significantly higher than that in the non-early cancer group (P < 0.05). The AUC of ME-NBI for early gastric cancer was 0.947 and higher than 0.832 ofWLE. The sensitivity, specificity, positive predictive value (PPV), negative predictive value (NPV) and Youden index were 97.2%, 84.8%, 85.4%, 97.1% and 0.820, respectively. The AUC of intervening part for early gastric cancer was 0.907 and higher than 0.889 of the traditional VS classification, and AUC, sensitivity, specificity, PPV, NPV and Youden index of VS type combined with intervening part were 0.933, 95.8%, 83.5%, 84.1%, 95.7% and 0.794,respectively.Conclusions ME-NBI is an important method for diagnosis of early gastric cancer, and intervening part has the advantages of strong objectivity, simple and easy to operate, good repeatability, and it could be used to assist traditional VS classification in judging the nature of lesions.
magnifying endoscopy; narrow-band imaging; intervening part; gastric cancer; early diagnosis
R735.2
A
10.3969/j.issn.1007-1989.2017.07.018
1007-1989(2017)07-0085-06
2017-02-13
