硫酸法钛白生产中硫酸与铁粉消耗的分析
2017-07-31邓刚
邓 刚
(广西蓝星大华化工有限责任公司,广西 百色 533011)
硫酸法钛白生产中硫酸与铁粉消耗的分析
邓 刚
(广西蓝星大华化工有限责任公司,广西 百色 533011)
本文对硫酸法生产钛白工艺中酸解的化学反应进行分析,根据钛铁矿的组分,计算硫酸与铁粉的消耗,为评估不同产地的钛铁矿的经济性提供依据。并提出了通过调整工艺,降低硫酸与铁粉消耗的方法。
硫酸法;钛白;酸解;酸钛比
钛铁矿、硫酸、铁粉是硫酸法钛白粉工艺的主要原材料,但硫酸、铁粉不进入终端产品,硫酸以25%和4%的稀废酸,以及FeSO4·7H2O方式排出,企业需花费不菲的代价处理。铁粉与钛铁矿中铁元素一起,转化为FeSO4,60%随废酸处理,40%作为副产品FeSO4·7H2O,以极其低廉的价格销售或倒贴外运。所以节省硫酸与铁粉的使用量,除了降低成本,更大的意义在于减轻企业的环保压力。
硫酸、铁粉的用量与钛铁矿的组分密切相关,在选择新的矿种时,根据钛铁矿的组分,评估生产成本的变化,对企业的经营有着重要的意义。在第一道发生化学反应的“酸解”工序,适当调整工艺参数,有助于减少硫酸与铁粉的消耗。
1 酸解的过程
1.1 钛铁矿的组成
钛铁矿的成分复杂,可将TiO2视作FeO·TiO2的单独组分,其它元素也以氧化物的形式表示。表1是国内常用钛铁矿中占比较高的成分。金红石含量指以金红石晶型构成的TiO2,它无法被硫酸溶解出。TiO2不与硫酸反应;其它元素的氧化物,如V2O5、P2O5等所占的比例均很低,本文暂不讨论。

表1 国内常用钛铁矿成分对比
1.2 酸解的过程
将粉碎的钛铁矿与93%~98%的浓硫酸混合后加入酸解罐,计量加入25%废硫酸作引发液,利用稀释放热引发反应。主反应在160~180℃下持续5~10min,反应产物逐渐凝结形成固相物;熟化1.5~3h,加大量水进行浸取形成钛液,使Ti、Fe等元素的硫酸盐溶解;加入单质铁粉,将钛液中的Fe3+全部还原为Fe2+。由于生产中无法直接分析出Fe3+是否全部被还原,因此铁粉稍过量,少量的Ti4+还原成Ti3+,通过分析Ti3+来确定Fe3+已全部还原。这是因为Fe3+的被还原势高于Ti4+,在Fe3+全部被还原后,才轮到Ti4+被还原。还原结束后,将酸解罐内的钛液放到澄清池交下一个工序处理。
国内普遍采用间歇式酸解,由于涉及高温强酸,反应物是由浆状到固相物的凝固过程,无法使用机械式搅拌,因此在酸解罐内均用压缩空气搅拌。
1.3 主反应化学方程式
硫酸分解钛铁矿的反应一般认为是按以下反应式进行:

实际在热的浓硫酸反应条件下,Ti(SO4)2仅仅是一个过渡的反应,随即发生如下反应:

所以反应物可认为只有TiOSO4,即酸解反应按式(1)进行。
铁的两种主要组成形态FeO、Fe2O3,按下列反应式进行反应:

根据式(1)、(3)、(4),可算出TiO2、FeO、Fe2O3的酸耗比分别为:H2SO4=1.225×TiO2;H2SO4=1.361× FeO;H2SO4=1.838×Fe2O3。FeO是分别分析Fe和Fe2O3后计算的,因此也有一些企业用全铁(Fe%)来表述。
其它金属氧化物与硫酸的反应:

根据以上的化学方程式可得到对应的酸耗比如表2所示。

表2 反应酸耗比
加水浸取后,用铁粉将Fe3+还原Fe2+:

当Fe3+全部还原后,Ti4+开始被还原。
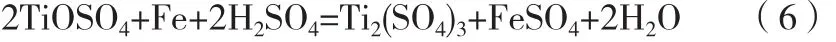
2 影响硫酸消耗量的因素
国内硫酸法厂家的硫酸单耗在3.2~4t·t-1。使用硫酸的只有酸解和漂白两个工序,其中漂白耗酸很少,约0.13t·t-1,其余均为酸解消耗。
综合表2各成分的酸耗比,可得到每t矿理论上的硫酸用量:

TiO2是有效成分,影响硫酸消耗量的是其它非钛元素的氧化物含量。在实际生产中,过量的酸有益于化学方程式(1)向右进行,提高TiO2的酸解率。
钛液中的硫酸以3种形式存在:1)与钛结合的硫酸;2)与其它金属结合的硫酸,称为无效酸;3)过量的硫酸,称为游离酸。目前的分析方法测的是与钛结合的酸与游离酸的总和,称为有效酸。有效酸与钛含量(以TiO2计)的比值称为酸钛比,用F值表示:

F值是重要的技术指标。后续的水解工序要求钛液的F值在1.90左右,比TiO2的酸耗比1.225要高,高出的这部分就是游离酸。用F值1.90替代TiO2的酸耗比,将酸解率95%计入计算式,减去作为引发液的废酸含酸量[取经验值,折合为0.06t·(t矿)-1],修正后得到每t矿所需的浓硫酸量如下:

折算成每t终端产品的单耗:

收率按国内厂家的平均水平87%计。
表3为常见钛铁矿在酸解工序的硫酸单耗,如加上漂白单元的用酸(0.13t·t-1),可得到总的单耗。
[9] 高保彬,钱亚楠,陈立伟,等.瓦斯压力对煤样冲击倾向性影响研究[J].煤炭科学技术,2018,46(10):58-64.
2.2 还原用铁粉单耗
按照方程式(5),可根据Fe2O3换算出所需的铁粉用量为:Fe=0.35×Fe2O3。
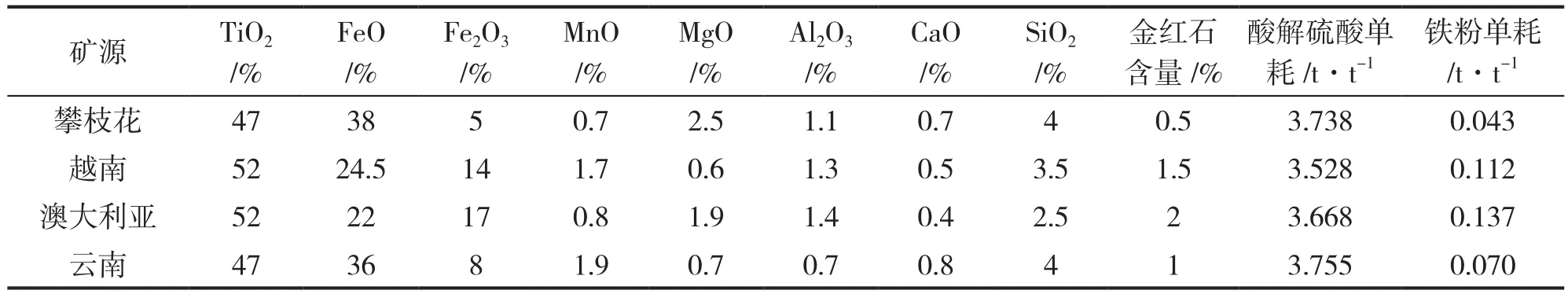
表3 常见钛铁矿在酸解工序的硫酸单耗
3 空气对铁粉消耗量的影响
因为浸取、还原过程的空气搅拌,氧将钛液中的低价态金属离子氧化成高价态,氧化与还原是同时进行的,只是还原的速度大于氧化的速度。因有氧化过程的存在,硫酸与铁粉的消耗量比上文的理论计算值高。
评估氧气对钛液的影响,需考虑其在水中的溶解度。20℃、标准大气压下,氧气密度ρ=1.331g·L-1,空气在水中的溶解度S=18.68mL·L-1,水中的氧气=S×ρ×21%=5.22mg·L-1。如果搅拌非常剧烈,氧气可达到饱和,饱和溶解度是S=9.02mg·L-1。生产中空气流量Q在200~600m3·h-1变化,液面翻腾高度在100~500mm。为便于计算,本文将空气中氧气的溶解度S取平均值为7.12mg·L-1或0.00712kg·m-3。
与还原时Ti4+最后被还原的顺序相反,Ti3+首先被氧化成Ti4+。以国内典型的130m3的酸解罐为例,每批次钛液的体积为85m3,还原结束后Ti3+浓度(以TiO2计)为2g·L-1,总量为85×2=170kg。空气流量Q=400m3·h-1,氧气的溶解度S=0.00712kg·m-3,每h参与反应的氧气量为:

每h被氧化的Ti3+=0.0712×400=28.48kg·h-1,Ti3+浓度下降28.48/85=0.34g·L-1。如需恢复Ti3+至原有的浓度,需补加铁粉。将式(6)与式(7)配平,得到式(8):

所以氧化不仅消耗铁粉,也消耗硫酸,只是不通过浓硫酸补充,而是加入后工序产生的25%的废酸。
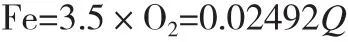
将空气Q=400m3·h-1代入,即得到对应需补充的铁粉量为:Fe=0.02492×400=9.968kg·h-1。需补充的硫酸为:H2SO4=6.125×O2=0.04361Q。
约6h后,Ti3+将消耗殆尽,轮到Fe2+氧化成Fe3+如式(9):将方程式(5)和式(9)配平,得到Fe2+被氧化而需补加的铁粉量:
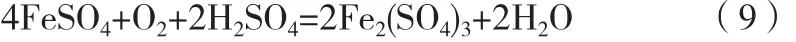
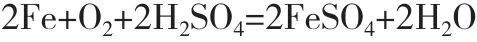
和式(8)一样,其它被氧化的低价态金属离子所对应的需补加的铁粉,只与空气的流量有关。
4 降低硫酸与铁粉单耗的措施
1)将25%的废酸除杂、除盐后浓缩至50%甚至60%,再用于酸解,可将酸耗降至3.3t·t-1,这种方法节省硫酸的幅度大,已有不少厂家采用,但投资大,运营成本高,不在本文讨论之列。
2)钛铁矿中除了钛以外的其它氧化物越低越好,可减少无效酸,但选矿成本大幅上升,抬高矿的价格。企业可根据硫酸、铁粉单价,计算用该钛铁矿的酸、铁粉的单耗,以此综合权衡是否经济。
3)降低主反应中硫酸浓度与酸矿比。
废酸除用于引发主反应外,还起着将反应酸浓调低的作用。因为过高的反应酸浓使反应速度过快,反应不充分,固相物质难浸取。我们可以维持25%废酸加入量不变,减少浓酸量,降低反应酸浓,减少熟化时的空气流量,来提高熟化温度并适当延长熟化时间,弥补因反应酸浓降低带来的酸解率的损失,在浸取前与还原后加入废酸来调节F值。
由于加废酸会稀释钛液中的TiO2,增加了后续工序浓缩的能耗,所以在浸取时可减少水量以提高TiO2浓度。这种后期补偿F值的方法生产的钛液稳定性会下降3%左右。过低的浓硫酸投入量会造成矿粉不能充分润湿而结块,导致局部反应,引起安全事故。
以笔者所在的企业为例,浸取后还原前的钛液F值可低至1.8,还原后再用废酸调至1.9或更高,长期实践表明,未对终端的产品质量造成影响。
4)采购Fe2O3低的铁粉;运输和储存中做好防潮防氧化,避免铁粉表面被氧化。
5)还原时铁粉分多次投放;控制好压缩空气流量,避免氢未来得及反应即逸出。
6)控制三价钛的浓度。Ti3+在水解时不沉淀析出,而是留在钛液中进入废酸,因此过高的浓度是浪费的。Ti3+的浓度在1.5~2.5g·L-1即可确保在水解前没有Fe3+被氧化。
7)避免长时间空气搅拌。
综上所述,铁粉与废酸的补加量与空气流量和时间有关。一个酸解生产周期为10~12h,因此应做好生产调度,合理安排酸解的投料时间,避免物料等待。如确需延后放料,应将空气流量降至维持液面有鼓泡、反应罐底部不堵塞为基准。
5 结论
1)选择非钛杂质少的钛铁矿是节省原材料单耗的捷径,可根据钛铁矿的成分测算生产成本,作为采购决策的依据。
2)通过调整工艺,均衡生产,能在一定程度上减少硫酸、铁粉的单耗。
[1] 张益都.硫酸法钛白粉生产技术创新[M].北京:化学工业出版社,2010:74-87.
[2] 陈朝华,刘长河.钛白粉生产及应用技术[M].北京:化学工业出版社,2006:174-194.
[3] 唐振宁.钛白粉的生产与环境治理[M].北京:化学工业出版社,2000:65-79.
Analysis of Sulfuric Acid and Iron Powder Consumption in Sulfuric Acid Titanium Dioxide Production
DENG Gang
(Guangxi Bluestar Dahua Chemical Co. Ltd., Baise 533011,China)
TQ 134.1+1
B
1671-9905(2017)07-0071-04
2017-04-25
