3例骨髓有核红细胞≥50%髓系肿瘤的诊断*
2017-07-07周丽娜赵鹏陈虎王建中盛宏霞高冬格廖丽张斌
周丽娜,赵鹏,陈虎,王建中,盛宏霞,高冬格,廖丽,张斌
(1.解放军307医院造血干细胞移植科,北京100071;2.北京大学第一医院检验科,北京100034)
·案例分析·
3例骨髓有核红细胞≥50%髓系肿瘤的诊断*
周丽娜1,赵鹏1,陈虎1,王建中2,盛宏霞1,高冬格1,廖丽1,张斌1
(1.解放军307医院造血干细胞移植科,北京100071;2.北京大学第一医院检验科,北京100034)
目的 分析3例髓系肿瘤的临床资料、诊断及预后,理解WHO(2016)中骨髓有核红细胞≥50%的髓系肿瘤的诊断,并初步探讨相关疾病的临床特征及预后。方法 分析3例骨髓有核红细胞≥50%的髓系肿瘤患者初诊时的年龄、病史、症状、体征及实验室检查结果,对比WHO(2016)和WHO(2008)诊断标准并进行诊断,用IPSS-R预后评分系统分析预后。结果 根据WHO(2008)诊断标准,3例均诊断为急性红白血病(AEL);根据WHO(2016)诊断标准,其中2例诊断为MDS伴原始细胞增多-2(MDS-EB-2),1例诊断为急性髓系白血病(AML)伴成熟型。其预后也不同,前2例均为老年男性,骨髓细胞有明显发育异常和复杂的遗传学异常,预后差,而第3例为中年女性,骨髓细胞未见明显发育异常及遗传学异常,预后中等。结论 WHO(2016)分型系统更关注疾病的不同生物学特征,能更好地区分具有不同临床特征及预后的两类疾病,其较WHO(2008)分型系统更具合理性。
髓系肿瘤;骨髓增生异常综合征;急性红白血病;急性髓系白血病(非特指型);非红细胞计数
骨髓有核红细胞≥50%的髓系肿瘤相关疾病很多,包括骨髓增生异常综合征(myelodysplastic syndromes,MDS)、急性髓系白血病(acute myeloid leukemia,AML)[非特指型(not otherwise specified,NOS)]、AML伴MDS相关改变(AML with myelodysplasia-related changes)、治疗相关髓系肿瘤(therapy-related myeloid neoplasms)等。随着诊断技术的发展及新异常的发现,AML和MDS的诊断及其亚型的分类也不断明确和细化,其诊断标准主要经历了4次更新:1976和1982年的法美英分型(French-American-British classification,FAB 分型)[1-2],2001年[3]、2008年[4]、2016年[5]的WHO分型(World Health Organization classification)。WHO(2008)分型与WHO(2016)分型变化较大的是MDS和急性红白血病(acute erythroid leukemia,AEL)的定义和诊断。本研究通过3例骨髓有核红细胞≥50%的髓系肿瘤的诊断来阐释WHO(2016)分型中相关诊断标准的变化。
1 病历资料
1.1 例1 患者,男,80岁,以“腰扭伤、疼痛、活动受限3周”于2016年11月16日入住解放军307医院移植科。入院前3周腰扭伤、疼痛、活动受限,X线提示胸12椎体压缩性骨折;1周前气喘;既往有原发性血小板增多症10年。外院查血示:WBC 1.2×109/L,Hb、PLT均减低(具体不详)。入院查体:体温38.0 ℃,脉搏82次/分钟,呼吸20次/分钟,血压100/60 mmHg。左下腹可见4 cm×5 cm皮肤瘀斑。双肺呼吸音粗,闻及少量干性啰音。胸12椎体压痛(+)、叩痛(+)、活动受限。双下肢肌力正常,左跟腱反射未引出,右跟腱、双侧膝腱反射正常,余未见明显异常。
1.2 例2 患者,男,70岁,头晕1月余,2015年10月18日入院。2015年9月27日无明显诱因头晕,当地查血示:WBC 3.8×109/L,Hb 75 g/L,PLT 48×109/L。既往痛风病史,未予治疗;行肺段切除术,病理示良性病变;胃癌病史,已行手术切除术。查体:贫血貌,双下肢片状充血性皮疹,未突出皮肤表面,余未见明显异常。
1.3 例3 患者,女,35岁,乏力、心慌1月余,既往于2007年行“畸胎瘤”切除术。于2013年5月13日入院,查体:贫血貌,双下肢散在出血点,余未见明显异常。
2 实验室检查
2.1 例1 血常规:WBC 10.86×109/L,ANC(absolute neutrophil count,中性粒细胞绝对计数)7.43×109/L,Hb 64 g/L,PLT 50×109/L。胸部CT:两肺间质性炎症;右肺小结节,考虑良性;双侧胸腔积液,两侧胸膜增厚;冠状动脉、主动脉硬化。腰椎核磁共振成像示:胸腰骶椎椎体及附件、双侧髂骨弥漫性异常,不除外血液病或骨髓病变可能;第3腰椎-第4腰椎、第4腰椎-第5腰椎、第5腰椎-第1骶椎椎间盘突出,腰椎骨质增生,胸12椎体楔形变。C反应蛋白46 mg/L;清蛋白31 g/L、总蛋白50 g/L、凝血酶原时间比值1.38、纤维蛋白原定量4.16 g/L、D二聚体定量554 ng/mL。外周血细胞学检查(计数200个白细胞,图1A、B):白细胞数量不少,原始细胞占5.5%,可见重度核左移;成熟红细胞大小不均,有核红细胞6∶200;血小板散在少见。骨髓细胞学检查(计数500个有核细胞,图1C、D):骨髓增生Ⅱ-Ⅲ级,粒红细胞比值为0.61∶1;粒系占有核细胞33.2%,原始细胞占有核细胞12.4%[非红细胞(non erythroid cells,NEC)计数约占31.3%];红系占有核细胞54.4%,发育异常细胞>10%;巨核细胞(2 cm×1 cm)见500个,单圆、多圆核巨核细胞易见(发育异常细胞约占50%),原始细胞吞噬血细胞(成熟红细胞、有核红细胞等)现象可见。有核红细胞化学染色:铁粒幼红细胞阳性率67%(环形铁粒幼细胞占有核红细胞18%);过碘酸-雪夫反应阳性率12%(图1E、F)。骨髓细胞免疫分型:CD45弱阳性,SS低散射群占有核细胞4.81%,表达HLA-DR、CD34、CD13、CD15、CD117、CD11b,不表达CD2、CD3、CD4、CD5、CD7、CD8、CD10、CD19、CD20、CD22、CD14、CD33、CD64、CD38、CD56、MPO、cCD79a、cCD3,为恶性原始髓系细胞。染色体核型分析(24 h培养G显带):64-68<3n>,XYY,-3,-4,-5,+6,-7,+8,-9,-10,-12,+14,+15,-16,-17,-18,del(18)(p11.1),add(19)(p13.1),+20,i(20)(p10),+21,+22,+mar1,+mar2[cp16]/46,XY,+Y,-5,hsr(6)(p21),-7,+mar2[3]/47,XY,+Y,-5,-7,+mar2,+mar4[1];另见个别结构异常:der(1)t(1;13)(p13,q12),del(2)(p23),del(3)(p11),add(14)(q32),mar3。荧光染色体原位杂交(fluorescence in situ hybridization,FISH)-5/7/8/20/Y染色体数目及缺失检测(计数500个有核细胞):5q-、7q-、-7、+8、-Y为阳性,其他均为阴性。分子生物学检查:WT1/ABL=1.259%;血液肿瘤基因突变筛查(58种基因):JAK2-V617F突变阳性;U2AF1体细胞突变阳性。
2.2 例2 血常规:WBC 2.56×109/L,ANC 1.00×109/L,Hb 80 g/L,PLT 31×109/L。外周血细胞学检查(计数200个白细胞):白细胞数量偏少,原始细胞占11.0%;成熟红细胞大小不均,有核红细胞6∶200;血小板散在可见,大血小板可见。骨髓细胞学检查(计数500个有核细胞):骨髓增生Ⅳ级,局部Ⅲ级,粒红细胞比值为0.44∶1;粒系占有核细胞26.4%,原始细胞占16.2%(NEC计数约占60.4%);红系占有核细胞60.2%,发育异常细胞>10%;巨核细胞(2 cm×2 cm)见61个,单圆、多圆核巨核细胞可见(发育异常细胞<10%)。有核红细胞化学染色:铁粒幼红细胞阳性率89%(环形铁粒幼细胞约占有核红细胞12%);过碘酸-雪夫反应阳性率14%。骨髓细胞免疫分型:CD45弱阳性,SS低散射群占有核细胞8.81%,表达CD13、CD33、CD7、CD34、CD117、HLA-DR、CD38、CD64dim,不表达CD10、CD19、CD20、CD22、CD2、CD3、CD4、CD5、CD7、CD8、CD14、CD15、CD64、CD56、CD11b、cMPO、cCD79a、cCD3,为恶性原始髓系细胞。染色体核型分析(24 h培养G显带):64-66<3n>,XYY,add(3)(p13),+4,-5,-7,+8,+8,-11,-13,+15,-16,-17,-18,-20,-22,+mar1,+mar2[cp14]/46-47,XY,+Y,del(2)(p15),-3,add(3)(p13),-5,+8,-17,-18,+mar1,+mar3×2[cp5]/46,XY[1]。FISH:5q-、+8阳性,其他均为阴性;另提示+5、+Y。分子生物学检查:WT1/ABL=4.67%,41种白血病相关基因检测均为阴性;FLT-3基因ITD和TKD突变检测阴性;NPM1突变检测阴性。
2.3 例3 血常规:WBC 4.91×109/L,ANC 0.60×109/L,Hb 79 g/L,PLT 17×109/L(此后4日内白细胞增高达28.14×109/L);外周血细胞学检查(计数200个白细胞):白细胞数量不少,原始粒细胞占64.5%;成熟红细胞大小不均,有核红细胞56∶200;血小板少见。骨髓细胞学检查(计数500个有核细胞):骨髓增生Ⅰ-Ⅱ级,粒红细胞比值=0.54∶1;粒系占有核细胞33.2%,其中原始粒细胞占31.0%;红系占有核细胞61.4%,未见明显发育异常;巨核细胞(2 cm×2.5 cm)见10个,以颗粒型为主,血小板少见。骨髓细胞免疫分型:28.33%细胞(占全部有核细胞)表达CD7、CD117、HLA-DR、CD34、MPO、CD15dim、CD33、CD13,部分表达CD64,不表达CD11b、CD56、CD19、CD22、cCD3、CD14、CD9、CD10、CD4、CD2,为恶性原始髓系细胞。考虑AML-M6或M1可能性大。染色体核型:46,XX[20]未见异常克隆。FISH:阴性。分子生物学检查:WT1/ABL=0.488%;31种白血病相关基因检测均为阴性;JAK2-V617F突变检测阴性;C-kit(exon8,exon17)突变检测阴性;FLT-3基因ITD和TKD突变检测阴性;NPM1突变检测阴性
3 诊断和治疗
3.1 例1 WHO(2016)诊断标准[5]诊断为MDS伴原始细胞增多-2(MDS with excess blasts-2,MDS-EB-2);WHO(2008)诊断标准[4]诊断为AEL(红系/粒系型,erythroid/myeloid)(原发性血小板增多症转化)。预后评估(revised international prognostic scoring system,IPSS-R[6])预后积分9分,极高危,未治疗中位生存期0.8年,未治疗25%进展为AML时间0.7年。2016年11月19日复查血常规示PLT 23×109/L,2016年11月20日补充血小板(A型单采血小板1单位)。2016年11月21日该患者因肺栓塞、多器官功能障碍综合症出现呼吸、心跳骤停抢救无效死亡。
3.2 例2 WHO(2016)诊断标准[5]诊断为MDS-EB-2;WHO(2008)诊断标准[4]诊断为AEL(红系/粒系型)。预后评估(IPSS-R[6])预后积分9分,极高危,未治疗时中位生存期0.8年,未治疗时25%进展为AML时间0.7年。口服来那度胺,治疗过程中D二聚体定量393 ng/mL,dsDNA弱阳性,抗RO-52抗体阳性(3+),抗核抗体滴度1∶640,符合过敏性紫癜,予抗过敏治疗。患者病情平稳,于2015年10月21日出院,建议定期监测并随诊。
3.3 例3 WHO(2016)诊断标准[5]诊断为AML伴成熟型;WHO(2008)诊断标准)[4]诊断为AEL(红系/粒系型)。预后评估[7]为中危。患者2013年5月17日行IA方案化疗,复查骨髓为达到完全缓解;2013年6月19日行MA方案诱导化疗,血常规恢复后复查骨髓达完全缓解;于2013年8月13日行MA巩固化疗,骨髓抑制发热,予以抗感染治疗后好转;于2013年10月29日行异基因造血干细胞移植术,至2016年仍处于骨髓缓解状态。
4 讨论
2016年,WHO从形态学解释、血细胞减少评估及累加的遗传学信息、分子生物学等方面修订了MDS分类。2016版较2008版MDS的诊断标准主要有4点改变[4-5]。(1)修订了MDS各亚型的名称,以“MDS伴单系、多系发育异常或原始细胞过多”代替“难治性血细胞减少”。(2)重新调整了骨髓有核红细胞≥50%髓系肿瘤的诊断。当骨髓有核红细胞≥50%时,骨髓原始细胞的计算由2008版的占NEC的百分比改成占骨髓全部有核细胞的百分比。因此,修订后AEL大部分归入MDS-EB、AML(NOS)等,仅保留了纯红系白血病。(3)del(5q)外加1个额外的细胞遗传学异常[单体7和del(7q)除外],仍可诊断为孤立性del(5q)。(4)SF3B1突变也应用于MDS伴环形铁粒幼细胞(MDS with ring sideroblasts,MDS-RS)的诊断,若环形铁粒幼细胞≥5%,同时合并SF3B1突变即可诊断为MDS-RS。
前2例患者均为老年男性,以粒系、红系和巨核系减少起病,骨髓有核红细胞≥50%,髓系原始细胞占全部有核细胞的比例<20%,而其NEC计数≥20%,伴多系发育异常及复杂遗传学异常,且患者都合并基础疾病,预后差。其相应的治疗措施有限,2014年MDS诊疗中国专家共识中对此类年龄≥65岁且体能不良患者,多建议选择支持治疗、地西他宾和阿扎胞苷治疗[8]。2例病例根据WHO(2008)诊断标准均符合AEL,而按照WHO(2016)诊断标准则均符合MDS-EB-2。前者属于AML(NOS),其常以原始细胞数量和种类决定其分型,随着细胞遗传学和分子生物学检测方法的不断完善,其中的很多病例被重新定义和分类。后者属于MDS,其以血细胞减少、发育异常和伴细胞遗传学异常为特征。前2例患者同时伴有多系发育异常和复杂的细胞遗传学异常,其预后与例3不同。
例3患者为中年女性,急性起病,白细胞数量不低并在短期内明显增高。骨髓有核红细胞≥50%,骨髓原始细胞占全部有核细胞的≥20%。未见明显遗传学异常,预后中危。及时行异基因造血干细胞移植,目前仍处于缓解状态。根据WHO(2008)诊断标准符合AEL(红系/粒系型),而根据WHO(2016)诊断标准则符合AML伴成熟型。对于AEL(红系/粒系型),其诊断标准中的骨髓有核红细胞≥50%的可重现性较低,即使在不予干预的情况下也无法很好地重复。WHO(2016)将骨髓有核红细胞≥50%且原始髓系细胞占全部有核细胞的比例≥20%的病例归入AML(NOS)中的非急性红白血病型,在AEL中仅保留了纯红系白血病型。
3个病例为骨髓有核红细胞占全部有核细胞≥50%的髓系肿瘤中具有代表性的病例(表1[5,9]),2种疾病有着不同的生物学行为。通过对其临床特征及预后的分析,能更好地掌握相关疾病的诊断和鉴别诊断。例1中原始细胞吞噬血细胞现象罕有报道,其相关的分子生物学异常不明。但符合此特征的疾病发病率极低,能纳入分析的病例数少,希望今后能积累更多相关疾病的信息,以期能更好地理解和鉴别此类疾病。
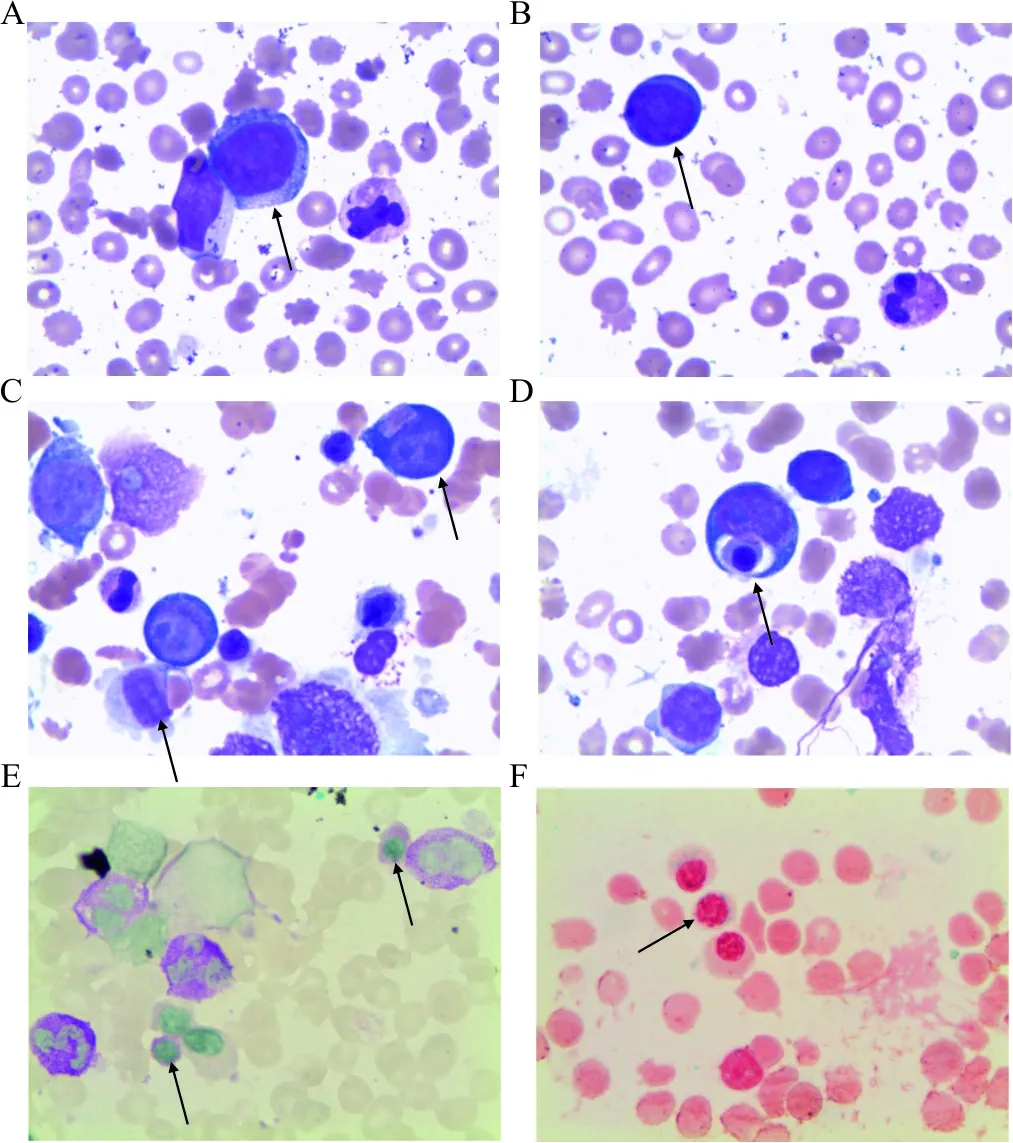
注:A、B为外周血涂片,箭头示原始细胞;C、D为骨髓涂片,箭头示原始细胞吞噬血细胞(有核红细胞、成熟红细胞)(瑞氏-吉姆萨染色);E,箭头示有核红细胞过碘酸-雪夫反应阳性;F,箭头示有核红细胞内铁染色见环形铁粒幼细胞。
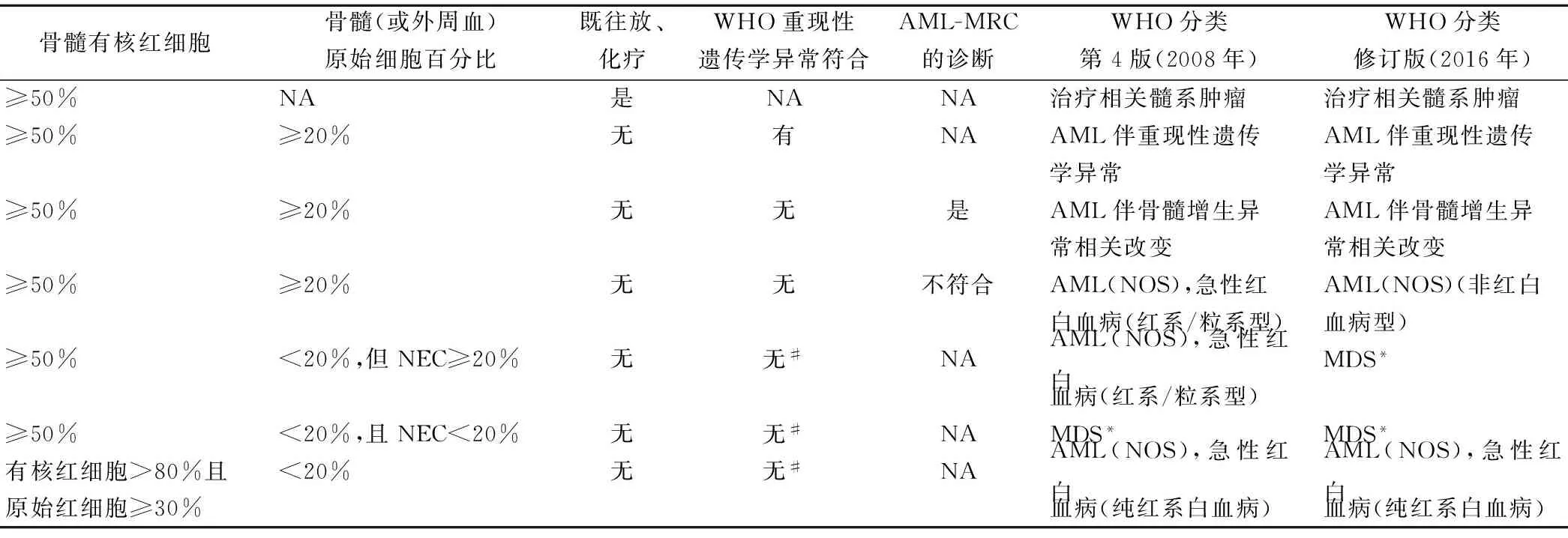
图1 细胞涂片染色结果(×1 000)
注:AML-MRC,急性髓系白血病伴骨髓增生异常相关改变。NA,不适用。#,AML伴t(8;21)(q22;q22.1),RUNX1-RUNX1T1;AML伴inv(16)(p13.1q22)或t(16;16)(p13.1;q22),CBFB-MYH11或APL伴PML-RARA。少数情况下原始细胞<20%,诊断将优先于AML(NOS)或MDS的诊断。*,分类基于髓系原始细胞占骨髓所有有核细胞或外周血白细胞的百分比并符合MDS的其他诊断标准。
[1]Bennett JM, Catovsky D, Daniel MT,etal. Proposal for the classification of the acute leukemia. French-American-British (FAB) Co-operative Group[J]. Br J Haematol, 1976, 33(4): 451-458.
[2]Bennett JM, Catovsky D, Daniel MT,etal. Proposal for the classification of the Myelodysplastic syndromes[J]. Br J Haematol, 1982, 51(2): 189-199.
[3]Elanie SJ, Nancy LH, Harald S,etal. 造血与淋巴组织肿瘤病理学和遗传学[M]. 周小鸽,陈辉树,译.北京:人民卫生出版社, 2006: 59-112.
[4]Vardiman JW, Thiele J, Arber DA,etal. The 2008 revision of the World Health Organization (WHO) classification of myeloid neoplasms and acute leukemia: rationale and important changes[J]. Blood, 2009,114(5):937-951.
[5]Arber DA, Orazi A, Hasserjian R,etal. The 2016 revision to the World Health Organization classification of myeloid neoplasms and acute leukemia[J]. Blood, 2016,127(20): 2391-2405.
[6]Greenberg PL, Tuechler H, Schanz J,etal. Revised international prognostic scoring system for myelodysplastic syndromes[J]. Blood, 2012,120(12):2454-2465.
[7]Margaret RO, Martin ST, Camille NA,etal. NCCN Clinical Practice Guidelines in oncology, Acute Myeloid Leukemia[EB/OL]. V.2. 2016 (2016-06-29)[2016-12-20]. http://www.nccn.org/professionals/physician_gls/f_guidelines.asp.
[8]中华医学会血液学分会. 骨髓增生异常综合征诊断与治疗中国专家共识(2014年版)[J]. 中华血液学杂志, 2014,35(11):1042-1048.
[9]叶向军, 卢兴国. 2016年更新版《WHO造血和淋巴组织肿瘤分类》之髓系肿瘤和急性白血病修订解读[J]. 临床检验杂志,2016,34(9):686-689.
(本文编辑:王海燕)
Diagnosis of myeloid neoplasms for three patients with erythroblast more than 50% of bone marrow nucleated cells
ZHOULi-na1,ZHAOPeng1,CHENHu1,WANGJian-zhong2,SHENGHong-xia1,GAODong-ge1,LIAOLi1,ZHANGBin1
(1.DepartmentofHematopoieticStemCellTransplantation, 307HospitalofPLA,Beijing100071; 2.DepartmentofClinicalLaboratory,PekingUniversityFirstHospital,Beijing100034,China)
Objective To further understand the diagnosis, clinical features and prognosis of myeloid neoplasms with erythroblast more than 50% of bone marrow(BM) nucleated cells in the WHO Classification(2016) by analyzing the clinical data, diagnosis and prognosis of 3 patients with myeloid leukemia. Methods The ages, medical histories, symptoms and signs, and laboratory examinations from 3 patients with myeloid neoplasms whose erythroblast cells were more than 50% of BM nucleated cells when newly diagnosed were collected. Then, they were diagnosed with the WHO Classification criteria(2008) and the WHO Classification criteria(2016), respectively, and their prognosis was evaluated with the revised International Prognostic Scoring System(IPSS-R). Results According to the WHO Classification criteria(2008), all of 3 patients were diagnosed as acute erythroid leukemia(AEL). However, according to the WHO Classification criteria(2016), 2 patients were diagnosed as myelodysplastic syndrome with excess blasts-2(MDS-EB-2), and 1 was diagnosed as acute myeloid leukemia(AML) with maturation. Moreover, their prognostic scores were also different. The former two patients were older men with significant dysplasia and complex genetic abnormalities, and had poor prognosis, while the latter was a middle-aged woman with no obvious dysplasia and genetic abnormalities, and had medium prognosis. Conclusion The WHO Classification(2016) is more reasonable than the WHO Classification(2008), which tends to focus more on the different biological characteristics of diseases, and may better distinguish two types of diseases with different clinical features and prognosis.
myeloid neoplasms; myelodysplastic syndrome; acute erythroid leukemia; acute myeloid leukemia(unspecified); nonerythroid cells count
国家高技术研究发展计划(863计划,2013AA0200103);北京市科技计划(首都临床特色应用研究与成果推广,Z161100000516184)。
周丽娜,1981年生,女,主管技师,主要从事血液病、淋巴瘤诊断及监测工作。
张斌,教授,E-mail: zb307ctc@163.com;王建中,教授,E-mail: jw4ub@sliyun.com。
10.13602/j.cnki.jcls.2017.06.22
R446
A
2016-12-20)
