食品级磷酸氢钙中和剂的选择和优化
2017-06-24寇晓倩赵途李小云
寇晓倩,赵途,李小云
(河北科技大学化学与制药工程学院,河北石家庄050018)
食品级磷酸氢钙中和剂的选择和优化
寇晓倩,赵途,李小云
(河北科技大学化学与制药工程学院,河北石家庄050018)
简要分析了以肌醇渣为原料制备食品级磷酸氢钙的重要性。对现有工艺中和剂的选择和提纯优化进行了具体分析,最终确定以氯化钙和氢氧化钠为复合中和剂。分别选取活性γ-氧化铝和碱改性活性炭对氯化钙和氢氧化钠进行吸附脱氟实验,探讨了不同吸附条件对其脱氟率的影响。用脱氟精制的复合中和剂中和精磷酸,得到符合GB 1889—2004《食品添加剂:磷酸氢钙》要求的食品级磷酸氢钙,氟质量分数为0.004 8%~0.005 0%。较适宜吸附参数:活性γ-氧化铝对氯化钙的脱氟过程,吸附温度为室温、活性γ-氧化铝用量为20 g、吸附时间为50min、氯化钙溶液pH=6、氯化钙浓度为2.7mol/L,最佳脱氟率为93.73%;碱改性活性炭对NaOH的脱氟过程,碱改性活性炭用量为1.0 g、吸附温度为35℃、吸附时间为60min、氢氧化钠浓度为8.75mol/L,最佳脱氟率为72.60%。
食品级磷酸氢钙;氢氧化钠;氯化钙;中和
食品级磷酸氢钙(CaHPO4·2H2O)是一种富含钙、磷两种营养元素的白色结晶性固体粉末,由于其与人体钙磷比相接近,有利于人体充分吸收钙和磷,成为食品行业中补充重要元素钙、磷的优良食品添加剂之一[1-2]。食品级磷酸氢钙主要生产原料为磷矿和脱胶骨块,但因脱胶骨块易携带动物流行病在很多国家都限制使用。中国磷矿多,但品位低,致使制备食品级磷酸氢钙的净化除杂工艺复杂,成本增大。而且中国磷矿这一不可再生资源被大量开采,正在面临日益枯竭的严峻挑战。因此,寻找食品级磷酸氢钙的生产新渠道对于中国民族工业的发展意义重大。肌醇渣是生产肌醇过程产生的副产品,是粉末状固体颗粒,其主要成分为Ca3(PO4)2、CaHPO4、CaSO4、CaO及部分未水解的植酸钙,钙、磷含量丰富,氟、铅、砷等杂质含量低,氟质量分数仅为0.056%,而且肌醇渣年产量高达肌醇产量(3 000 t/a)的9倍以上[3]。因此,选用肌醇渣为原料在减少三废、降低污染、创造价值等方面具有深远意义。目前用肌醇渣生产饲料级磷酸氢钙的报道较多[4-6],而用其生产食品级磷酸氢钙的研究中,除罗祖富[7]、王文娟[8]在影响产品质量和收率的因素方面做了简单介绍外,未见其他详细的研究。通过研究发现,用肌醇渣生产食品级磷酸氢钙是在制备饲料级磷酸氢钙的前提下进一步提纯,对杂质含量的要求更为严格,其中氟的脱除是关键,要严格控制每一个过程中氟的引入,使氟含量符合食品级国家标准。实验的前期阶段,以一定浓度的盐酸酸解肌醇渣产生粗磷酸,对粗磷酸进行初步磷、氟含量检测,发现由于磷氟质量浓度比[ρ(P2O5)/ρ(F)]≥8 500而达到食品级的要求,因此可省去酸解液脱氟的过程,只进行其他杂质的脱除可得到精磷酸,可见中和过程中和剂氟含量的高低对最终产品的质量有绝对的影响。通过查阅文献发现,制备饲料级和食品级磷酸氢钙常选用石灰乳[9-10]或复合中和剂CaCl2-NaOH[7-8]作为中和剂。笔者在前人研究基础上,对中和剂的选择和优化进行了系列研究,并对实验结果进行了详细分析。
1 实验部分
1.1 原料及仪器
原料:精磷酸[盐酸酸解肌醇渣产生粗磷酸通过净化除杂得到精磷酸,ρ(P2O5)/ρ(F)≥8 500,ρ(F)=4.925μg/mL,ρ(P2O5)=0.104 2 g/mL,ρ(Ca2+)= 0.051 24 g/mL];Ca(OH)2、CaCl2、NaOH均为分析纯;细颗粒活性炭;活性γ-Al2O3。
仪器:PHS-25型酸度计,双列四孔恒温水浴锅,PF-1-01氟离子电极,232型参比电极,JJ-1型精密增力电动搅拌器。
1.2 食品级磷酸氢钙生产工艺流程(见图1)
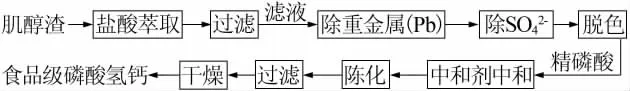
图1 以肌醇酸为原料制备食品级磷酸氢钙工艺流程图
1.3 产品相关标准
GB 1889—2004《食品添加剂:磷酸氢钙》和GB/ T 22549—2008《饲料级:磷酸氢钙》部分指标见表1。

表1 饲料级磷酸氢钙和食品级磷酸氢钙国家标准部分指标
1.4 检测方法
根据GB 1889—2004《食品添加剂:磷酸氢钙》和GB/T 22549—2008《饲料级:磷酸氢钙》,采用氟离子选择性电极法检测氟(F)含量,采用EDTA滴定法检测磷酸氢钙(CaHPO4·2H2O)含量,采用磷钼酸喹啉沉淀法检测磷(P)含量等。
2 实验结果与讨论
2.1 各类中和剂的氟含量检测
采用氟离子选择性电极法分别对Ca(OH)2、CaCl2、NaOH进行氟含量检测,结果见表2。由表2可知,3种分析纯中和剂中Ca(OH)2、CaCl2氟含量较高,而NaOH氟含量较低,可能是因为Ca(OH)2、CaCl2在制备过程中Ca2+更易吸收环境中的氟生成CaF2的结果。

表2 各类中和剂氟含量检测结果
2.2 未处理中和剂进行中和反应
取两组200mL精磷酸于500mL烧杯中,开启搅拌器搅拌。第一组加入石灰乳进行中和反应;第二组先缓慢加入一定浓度的CaCl2溶液26.3mL(CaCl2溶液浓度为2.5mol/L,使磷全部转化为磷酸氢钙理论需要CaCl2溶液26.3mL),再缓慢滴加一定浓度的NaOH溶液(NaOH溶液浓度为6.0mol/L)。严格控制中和终点pH,并考察终点pH对产品中P、CaHPO4·2H2O及F含量的影响。结果见图2。

图2 以未脱氟的石灰乳(a)、Ca(OH)2-CaCl2(b)为中和剂制备磷酸氢钙产品质量
由图2看出,石灰乳中和以及复合中和剂Ca(OH)2-CaCl2中和都是以pH范围为3.0~6.5为中和终点,当中和pH终点为5.0~5.5时,食品级磷酸氢钙中CaHPO4·2H2O、P含量都符合国家标准,且磷收率较高,最高分别达到94.5%和95.1%,而氟含量虽然较低,却远远高于食品级磷酸氢钙国家标准的要求,因此中和剂的选择及脱氟是产品达标与否的关键。考虑到Ca(OH)2微溶于水,加入水后得到乳状的石灰乳,很难将氟杂质脱除干净,而CaCl2和NaOH易溶于水,可以在其溶解后选取合适的吸附剂用简单的吸附法脱氟。
2.3 CaCl2和NaOH脱氟吸附剂的初步选择
实验采用较为常用的脱氟方法吸附法进行脱氟。吸附法因脱氟效果较为稳定、操作简单且价格低廉,是一种处理含氟溶液的重要方法。吸附剂由于具有巨大的比表面积、适宜的孔结构以及优良的孔道结构等,使其具有优良的脱氟能力,而且再生容易,因此被广泛应用。但是,吸附剂种类较多,脱氟效果良莠不齐,因此选取合适的吸附剂十分必要。实验选取活性白土、粉煤灰、活性炭以及活性γ-Al2O3为吸附剂对CaCl2和NaOH两种中和剂进行脱氟实验,比较并确定最佳吸附剂及其实验参数。
以200 mL CaCl2溶液(浓度为2.00 mol/L)和200mLNaOH溶液(浓度为3.00mol/L)为基液,在未对4种脱氟剂进行改性的情况下进行基础脱氟效果比较,脱氟剂用量均为8.000 0 g、脱氟温度为20℃、静态搅拌2.0 h,实验结果见表3。由表3看出,以活性白土为吸附剂进行吸附处理会发生溶胀而不易过滤除去,静置后过滤处理繁琐,以粉煤灰为吸附剂进行吸附处理不但会发生溶胀使得过滤困难,而且因其本身含有少量的氟杂质反而使氟含量增大,因而活性白土和粉煤灰对CaCl2和NaOH的脱氟效果均较差;γ-Al2O3对CaCl2的脱氟效果较优,且过滤处理简单方便;活性炭对NaOH溶液脱氟效果较好。因此CaCl2和NaOH的脱氟过程分别选取γ-Al2O3和活性炭为相应的吸附剂。

表3 不同吸附剂对CaCl2和NaOH的脱氟效果
2.4 活性γ-Al2O3对CaCl2脱氟条件的确定
1)温度的确定。以200mLCaCl2溶液(浓度为2.00mol/L)为基液,投加8.000 0 g吸附剂,搅拌反应90min,考察不同温度条件下活性γ-Al2O3对CaCl2的脱氟率,结果见图3a。由图3a看出脱氟率受温度的影响很小,几乎不变。这可能是因为物理吸附的范德华力随温度的升高而减小,而化学吸附的化学键力随温度的升高而增大,并由物理吸附主导向化学吸附主导的方向转化,物理吸附较快、化学吸附较慢,使得升温过程中化学吸附水平的增大程度与物理吸附水平的减小程度几乎相当。为节省能源消耗、降低工艺成本,选择室温为吸附温度。
2)吸附剂用量的确定。以200mLCaCl2溶液(浓度为2.00mol/L)为基液,投加不同用量的活性γ-Al2O3,在室温下搅拌反应90min,考察不同吸附剂用量条件下活性γ-Al2O3对CaCl2的脱氟率,结果见图3b。由图3b看出,脱氟率随γ-Al2O3用量的增加而逐渐增大。这表明吸附剂用量的增加有利于增大总的吸附面积,增加了活性位点,有利于物理吸附和化学吸附。但是,吸附剂用量过多,会吸收大量的CaCl2液体,造成CaCl2溶液的浪费。而且在γ-Al2O3用量为20 g时吸附效果较佳,继续增大吸附剂用量,脱氟率升高程度不明显。因此,选择γ-Al2O3用量为20 g,在此条件下脱氟率达到89.13%。
3)吸附时间的确定。以200mLCaCl2溶液(浓度为2.00mol/L)为基液,投加20 g活性γ-Al2O3,在室温下搅拌不同的时间,考察不同吸附时间条件下活性γ-Al2O3对CaCl2的脱氟率,结果见图3c。由图3c可知,吸附时间较短时吸附反应不充分,脱氟率较低。在吸附时间为50min时脱氟率达到91.92%。继续延长吸附时间,脱氟率没有明显的变化,吸附反应趋于吸附平衡状态。故吸附时间确定为50min。
4)溶液pH的确定。以200mLCaCl2溶液(浓度为2.00mol/L)为基液,用稀盐酸和稀NaOH溶液调节CaCl2溶液pH至不同的值,在基液中投加20 g活性γ-Al2O3,在室温下搅拌50min,考察不同pH条件下活性γ-Al2O3对CaCl2的脱氟率,结果见图3d。由图3d看出,强酸性和强碱性环境都不利于γ-Al2O3对氟的吸附。这是因为,γ-Al2O3溶于强酸和强碱中,改变了比表面积和孔道结构,而且在强碱性环境中存在大量的OH-,不但会产生大量Ca(OH)2沉淀,而且由于γ-Al2O3对OH-的吸附强度大于对F-的吸附强度,致使脱氟率下降。弱酸环境较适于脱氟,且pH=6时脱氟率最高,达到92.94%。
5)CaCl2浓度的确定。以200mL不同浓度的CaCl2溶液为基液,以稀盐酸调节溶液pH=6,在基液中投加20 g活性γ-Al2O3,在室温下搅拌50min,考察不同CaCl2浓度条件下活性γ-Al2O3对CaCl2的脱氟率,结果见图3e。由图3e可知,活性γ-Al2O3对CaCl2的脱氟率随CaCl2浓度的增大呈驼峰状,可见适当增大CaCl2溶液的浓度可以使溶液中氟浓度相应增大,有利于吸附剂对氟的充分吸附,但CaCl2浓度过大会使脱氟效果降低。最佳的CaCl2浓度为2.7mol/L,在此条件下脱氟率较大为93.73%,最终得到脱氟精制的CaCl2溶液的氟浓度由6.1mmol/L下降到0.37mmol/L。
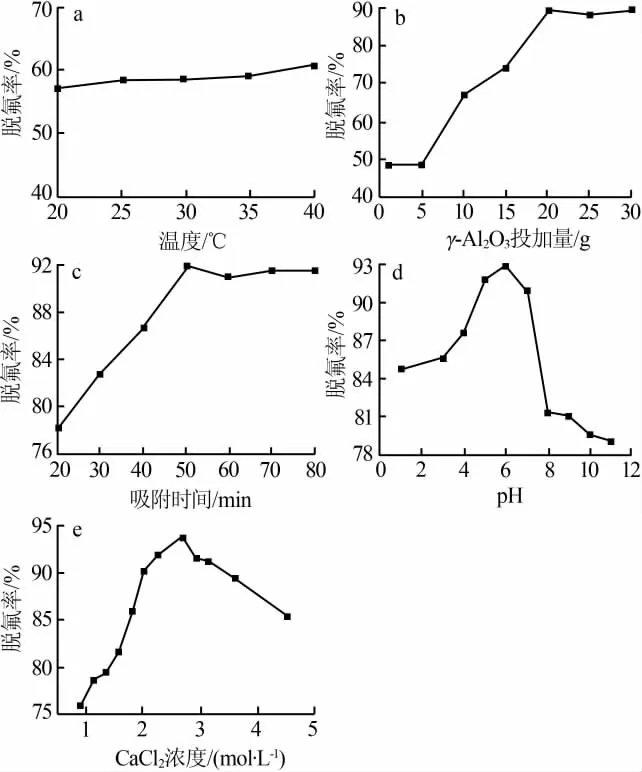
图3 活性γ-Al2O3吸附条件对CaCl2脱氟率的影响
2.5 活性炭对NaOH脱氟条件的确定
1)酸碱改性与未改性活性炭对NaOH脱氟率的影响。酸碱改性活性炭的制备:将细颗粒状活性炭分别在3mol/L的HCl溶液和2mol/L的NaOH溶液中浸渍并搅拌5 h,抽滤,洗至中性,在110℃干燥,冷却,即得到酸改性和碱改性的活性炭。以200mLNaOH溶液(浓度为3.00mol/L)为基液,控制温度为30℃,连续搅拌60min,分别投加不同用量的酸改性、碱改性及未改性的活性炭进行吸附反应,考察不同的活性炭及用量对NaOH的脱氟率,结果见图4a。由图4a可知,各种活性炭对脱氟率的影响由大到小的顺序为碱改性活性炭、酸改性活性炭、未改性活性炭,而且碱改性活性炭用量为1.0 g时有较大的脱氟率为53.88%。故选择碱改性活性炭作为NaOH溶液的脱氟吸附剂,用量为1.0 g。
2)温度的确定。以200mLNaOH溶液(浓度为3.00mol/L)为基液,投加1.0 g碱改性活性炭,连续搅拌60min,考察不同温度条件下碱改性活性炭对NaOH的脱氟率,结果见图4b。由图4b可知,脱氟率随温度的升高先增加后减少。这可能是因为适当地升高温度,NaOH的溶解度随之增加,溶液的黏度减小,分子运动加快,从而使脱氟率增加。但是,温度过高会使活性炭物理吸附能力下降,从而导致脱氟率降低。因此,选择吸附温度为35℃,在此条件下有较好脱氟率为57.55%。
3)吸附时间的确定。以200mLNaOH溶液(浓度为3.00mol/L)为基液,投加1.0 g碱改性活性炭,控制温度为35℃,连续搅拌不同的时间,考察不同吸附时间条件下碱改性活性炭对NaOH的脱氟率,结果见图4c。由图4c看出,随吸附时间的延长,脱氟率出现一个明显的驼峰。这可能是由于,活性炭在吸附前期主要依靠物理吸附,孔道发挥重要作用,所以脱氟率增大;随着时间延长,活性炭表面的活性位点发挥较为重要的作用,OH-会将已经吸附在位点上的F-洗脱下来,从而使脱氟率大幅下降。最佳吸附时间为60min,在此条件下有最大的脱氟率为62.33%。

图4 活性炭吸附条件对NaOH脱氟率的影响
4)NaOH浓度的确定。以200mL不同浓度的NaOH溶液为基液,投加1.0 g碱改性活性炭,控制温度为35℃,连续搅拌60min,考察不同NaOH溶液浓度条件下碱改性活性炭对NaOH的脱氟率,结果见图4d。由图4d看出,脱氟率随NaOH浓度的增加先增加后减少,可见适当增大NaOH浓度有利于脱氟的实现。在NaOH浓度为8.75mol/L条件下脱氟效果较好为72.60%,最终得到脱氟精制的NaOH溶液,其氟浓度由2.0mmol/L下降为0.551mmol/L。
2.6 脱氟精制的CaCl2和NaOH中和精磷酸
取200mL精磷酸于500mL烧杯中,开启搅拌器搅拌,先缓慢加入脱氟精制的CaCl2溶液(浓度为2.7mol/L)25mL(使磷全部转化为磷酸氢钙,理论需要CaCl2溶液24.36mL),再缓慢滴加脱氟精制的NaOH溶液(浓度为8.75mol/L),严格控制中和终点pH,并考察终点pH对产品中P、CaHPO4·2H2O及F含量的影响,结果见图5。由图5看出,中和pH终点为5.0~5.5时,食品级磷酸氢钙中CaHPO4·2H2O、P及F质量分数都符合GB 1889—2004《食品添加剂:磷酸氢钙》及GB/T 22549—2008《饲料级:磷酸氢钙》的要求,分别为99.7%~101.91%、18.2%~18.8%、0.004 8%~0.005 0%,且有最高磷收率为94.8%。

图5 脱氟精制CaCl2和NaOH中和精磷酸制备食品级磷酸氢钙产品质量
3 结论
通过实验得出以下结论:1)CaCl2和NaOH的脱氟过程,分别选取γ-Al2O3和碱改性活性炭为相应的吸附剂;2)活性γ-Al2O3对CaCl2的脱氟过程,在室温、活性γ-Al2O3用量为20 g、吸附时间为50min、CaCl2溶液pH=6、CaCl2浓度为2.7mol/L条件下,脱氟率可达93.73%;3)碱改性活性炭对NaOH的脱氟过程,在碱改性活性炭用量为1.0 g、温度为35℃、吸附时间为60min、NaOH浓度为8.75mol/L条件下,脱氟率为72.60%;4)用脱氟精制的复合中和剂中和精磷酸,得到食品级磷酸氢钙,产品中CaHPO4· 2H2O质量分数为99.70%~101.91%、P质量分数为18.2%~18.8%、F质量分数为0.004 8%~0.005 0%,符合GB 1889—2004《食品添加剂:磷酸氢钙》及GB/T 22549—2008《饲料级:磷酸氢钙》的要求。
[1]刘颖.复合磷酸盐食品添加剂的开发及应用研究[D].贵阳:贵州大学,2008.
[2]陈加甫.国内外磷酸、磷酸盐在食品工业中的应用[J].无机盐工业,1983(8):19-24.
[3]李亚文.肌醇及其相关产品的市场开发研究[J].精细化工,1998,15(5):10-15.
[4]寇晓倩,刘潇,黄娇妹,等.饲料级磷酸氢钙中和工艺探讨[J].无机盐工业,2015,47(9):46-49.
[5]刘潇,寇晓倩,黄娇妹,等.湿法磷酸循环萃取无脱氟工艺研究[J].现代化工,2015,35(3):78-80.
[6]刘潇.盐酸法制备饲料级磷酸氢钙联产氯化铵工艺研究[D].石家庄:河北科技大学,2015.
[7]罗祖富.用肌醇渣生产食品级磷酸氢钙技术[J].农牧产品开发,1997(3):9-10.
[8]王文娟.用肌醇渣生产食品级磷酸氢钙技术[J].适用技术之窗,1997(3):16.
[9]张开诚,丁斌鹰.肌醇滤渣生产磷酸氢钙工艺条件研究[J].武汉食品工业学院学报,1997(3):27-29.
[10]周生飞.利用肌醇渣生产饲料级磷酸氢钙工艺参数的研究及其生物学评价[D].泰安:山东农业大学,2002.
联系方式:1409774461@qq.com
Selection and optim ization of neutralization agent for food grade calcium hydrogen phosphate
Kou Xiaoqian,Zhao Tu,LiXiaoyun
(CollegeofChemistry and Pharmaceutical Engineering,HebeiUniversityofScienceand Technology,Shijiazhuang050018,China)
The importance ofusing the inositol residue as rawmaterial to prepare food grade calcium hydrogen phosphatewas briefly analyzed.In addition,the selection and purification optimization ofneutralizer of the current processwere analyzed in detail,and calcium chloride and sodium hydroxide were ultimately confirmed as the compound neutralizer.Then the active γ-Al2O3and the alkalimodified activated carbon were selected to carry on the adsorption defluoridation experiments respectively.The influences of different adsorption conditions on the defluoridation rate were investigated.Finally,the food grade calcium hydrogen phosphatewith fluorinemass fraction of0.004 8%~0.005 0%,which consistented with the national standard,Food Additive-Calcium Hydrogen Phosphate,GB 1889—2004,was obtained by neutralization reaction between the defluorization refined compound neutralizerand concentrate phosphoric acid.The suitableadsorption parameterswereobtained:the better temperature of the activeγ-Al2O3adsorption defluoridation was room temperature,γ-Al2O3dosagewas 20 g,the adsorption timewas50min,CaCl2solution pH was6,CaCl2concentrationwas2.7mol/L,and thebest removal rateof fluoride was93.73%;The conditionsofadsorption defluoridation ofalkalimodified activated carbon toNaOH were thatalkaliactivated carbonwas1.0 g,temperaturewas35℃,the adsorption timewas60min,NaOH concentrationwas8.75mol/L,and the best defluorization ratewas72.60%.
food grade calcium hydrogen phosphate;sodium hydroxide;calcium chloride;neutralization
TQ126.35
A
1006-4990(2017)06-0040-05
2017-01-19
寇晓倩(1989—),女,硕士,从事食品级添加剂研究。
李小云(1963—),男,教授,从事清洁能源生产。
